摘要
肺移植后可能会发生肺肺泡蛋白质分子,可能是呼吸劣化的原因http:////tlrl307klky.
编辑器:
肺泡蛋白沉积症(Pulmonary alveolar proteinosis, PAP)是一种与肺泡巨噬细胞功能障碍相关的表面活性物质在肺泡腔内积聚的罕见疾病。PAP有三种不同的临床形式:自身免疫性PAP(90%的病例)、继发性PAP和遗传性PAP [1].继发性PAP可能与免疫抑制疾病有关,少数病例与实体器官移植有关[1].事实上,据我们所知,目前只有5例继发于肺移植的症状性PAP病例被报道[2- - - - - -4].
在这里,我们报告了4例肺移植受者的PAP新病例,所有病例的死亡都与PAP发病相关。一名患者在缺乏自身抗体的情况下显示粒细胞-巨噬细胞集落刺激因子(GM-CSF)信号受损,这表明其机制与自身免疫PAP类似。单肺移植受者没有肺受累,也提示肺移植相关的风险增加。
病人一
一名66岁男性具有特发性肺纤维化(IPF)的左侧肺部移植来自一名34岁的男性吸烟者。术后术后课程不平衡,初级接枝功能障碍确定为等级0.在操作后的第72天,急性排斥(A2B0级)[5诊断时未进行补体成分4d (C4d)染色。采用Luminex检测供体特异性抗体(人白细胞抗原DQ7 (HLA-DQ7);平均荧光强度(MFI)=4030),并在术后第101天给予抗胸腺细胞球蛋白,因为组织学证实的急性排斥反应持续存在(A2B0级)[5].随后经支气管活检(术后第134天)显示急性排斥反应完全缓解(A0B0级)。此外,支气管肺泡灌洗液(BALF)分析未显示寄生虫(卡式肺)、真菌学、病毒(采用多重PCR检测)或细菌感染(包括Nocardia.),心脏超声显示左心室功能正常。然而,在类固醇抵抗性急性排斥反应的组织学解决的同时,重复的CT扫描显示从术后第129天起肺混浊呈进行性恶化,仅在移植物中出现“不规则铺装”模式(图1一个).术后第134天经支气管活检的复查(图1 b)和一种新的用周期酸-希夫(PAS)试剂染色的BALF分析(图1 c)导致PAP的诊断。不存在抗(GM-CSF)抗体,使用最近描述的测试研究了基于GM-CSF在流式细胞术中的中性粒细胞上的细胞表面CD11b水平的能力(反映CD11B刺激指数)[6].患者的GM-CSF刺激指数非常低,值为七个,与三个稳定的肺移植接受者的101,55和102的值相比,用作阳性对照(平均稳定肺移植的GM-CSF刺激指数)= 86±26)。Tacrolimus槽水平逐渐变细至5-7 ng·ml−1.患者仍然依赖氧气,在接下来的几个月里,PAP病变持续恶化(ct扫描证实)。他最终于术后516天死于与导管相关细菌感染和肺炎相关的败血症。端粒酶逆转录酶(叔/ /端粒酶RNA组分(, TERC)基因突变已被证明与PAP相关[7],在验尸后的调查中缺席。
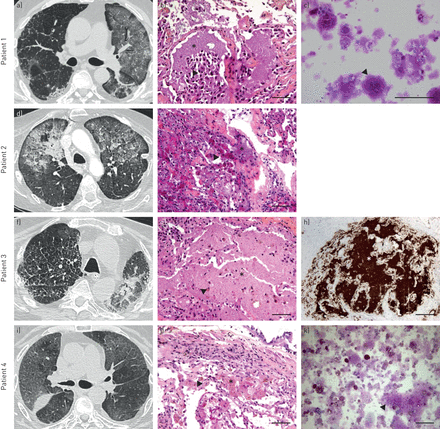
4例肺移植后出现肺泡蛋白沉积(PAP)的患者的图像。图像(a)、(d)、(f)和(i)分别显示患者1、2、3和4的轴位胸部横轴CT (CT)结果。网格叠加在磨砂玻璃的不透明度上,形成一种地理分布的“疯狂铺路”模式(健康区和病态区并列)。图(b)、(e)、(g)和(j)分别为患者1、2、3和4的经支气管肺活检,显示肺泡内无定形嗜酸性颗粒状物质的聚集(*)和大量肺泡巨噬细胞伴细颗粒状棕色细胞浆(箭头)。图(c)和(k)分别为患者1和4的支气管肺泡灌洗液(BALF)染色,显示周期性酸-希夫(PAS)阳性细胞外物质(箭头)。图(h)为患者3的经支气管肺活检,免疫组化染色显示表面活性剂抗体[anti-(表面活性剂蛋白a), anti-(SP-A), 32E12,来自英国剑桥,英国剑桥,具有肺泡内非晶材料(*)的显着强度。当患者3和4患者进行时,观察到正抗(SP-A)染色。秤杆=100μm。
两个病人
一个61岁的女性,具有肺气肿的一名44岁男性吸烟者的双重移植。术后课程与初级接枝功能障碍等级为1年级。在操作后的第33天,胸廓CT扫描显示被认为是非特异性的离散肺泡不透明度。跨渊深的活组织检查显示没有急性排斥(A0B0级)[5,且缺乏供体特异性抗体。重复BALF分析显示铜绿假单胞菌无寄生的支气管定植(卡式肺),Mycological,病毒或细菌(Nocardia.) 感染。从操作后的第75天,呼吸状况随着新的肺不透明度的出现而恶化。在术后第91天,患有在肺CT扫描上看到的静脉肺病灶(图1 d).ct扫描也显示与曲霉病病变相关的“疯狂铺路”模式(图1 d).病人死于与铜绿假单胞菌术后第96天发生肺炎。死后,术后33天复查经支气管活检,最终诊断为PAP (图1 e).
三个病人
一名63岁的男子患有IPF的右侧右侧,来自一名40岁的女性吸烟者的单肺移植。确定后初级接枝功能障碍是3级,延迟呼吸机在操作后的一天20.在操作后第32天进行的跨晶体活组织检查是正常(A0B0级)和供体特异性抗体。在操作后的第42天,在CT-SCAN(专门在肺移植物中并用“疯狂铺设”图案)鉴定了新的肺不透明性(图1 f).BALF表现为巴氏涂片病变特点,支气管定殖粘质沙雷氏菌但没有病毒,寄生(卡式肺),细菌(Nocardia.)或Mycological感染。然而,没有明确地排除没有组织学验证的急性排斥发作,并且没有临床改善给药而是施用类固醇荧光。在没有明确的诊断的情况下,对先前跨越跨越活组织检查,BALF和CT扫描的结果的回顾性分析,然后导致了PAP的诊断(图1 f-1h)。抗(GM-CSF)抗体不存在,开始GM-CSF疗法(250 mg·日−1),由他克莫司转化为环孢霉素。然而,患者病情逐渐恶化,导致呼吸衰竭,最终于术后80天死于败血症。
四个病人
一个65岁的男子,IPF接受了一位27岁女性非吸烟者的双肺移植。初级移植物功能障碍被确定为3级和随后的肠杆菌肝脏肺炎延迟了呼吸机断奶,直到操作后的第16天。从操作后的第90天开始,患者的呼吸状况逐渐恶化,CT扫描显示了“疯狂铺路”模式。横刻度的活组织检查显示在展示Balf时没有细胞急性排斥(A0B0级)葡萄球菌epidermidis没有病毒的殖民化,寄生(卡式肺),细菌(Nocardia.)或Mycological感染。由于检测到供体特异性抗体(HLA-DQ9; MFI = 7598),但虽然C4D染色为阴性[8,考虑抗体介导的排斥反应,患者从术后101天开始进行血浆置换(n=5)。这使得供者特异性抗体MFI (HLA-DQ9;MFI=947),但无呼吸改善。术后第108天给予类固醇丸也没有改善,术后第114天,回顾性复查ct扫描和经支气管活检(术后第97天),再加上BALF的新发现,诊断为PAP (图1我-1k)。抗(GM-CSF)抗体不存在,并且序贯治疗性支气管肺泡灌洗(BALS; n = 4),GM-CSF给药和霉霉酚酸盐酯的撤离导致瞬态改善。从术后第142天,PAP病变数量增加(如CT-SCAN揭示),而逐步呼吸衰竭发生。患者在手术后的第153天从细菌肺炎中死亡。
总结
在我们的单队列肺移植受者中,4年期间发生的继发性PAP表明,在该人群中可能对该并发症认识不足。这种情况可能是由于肺移植后的BALF往往含有微生物、炎症细胞和黏液,很难用它来诊断PAP,或者是肺移植后BALF没有常规系统的PAS染色。在这种情况下,PAS染色的阳性也可以排除肺泡内物质积聚的其他原因,如水肿或纤维蛋白,以及胺碘酮毒性引起的巨噬细胞空泡化的原因。在我们的系列研究中,PAP的组织学诊断通过抗表面活性剂抗体阳性染色(图1 h).通过偏振光检查,无双折射二氧化硅颗粒系统地进行硅蛋白酶排出。在所有患者中,肺癌早期发育的毒药(在第3个,移植后,移植后),致命结果与这种发作相关。在四个案例研究中延迟了诊断,并且仅在特异性重新检查后进行了跨刻度生物检查/ BALF而建立。在AutoImmune和遗传形式的PAP [6,9]已知肺泡巨噬细胞功能障碍被GM-CSF信号障碍的驱动。通过使用最近描述的测试基于GM-CSF的能力在流式细胞术中的中性粒细胞上的细胞表面CD11b水平迅速增加细胞表面CD11b水平的能力,在一名患者中发现了类似的受损的GM-CSF途径。6,9].由于缺乏抗(GM-CSF)抗体而排除了PAP的主要形式(n=3)。单肺移植受者明显缺乏天然肺的受累,这可能表明肺泡巨噬细胞损伤与移植物中特定的致病过程有关;然而,这仍有待确定。此外,免疫抑制疗法的促进作用以前曾在肺或肾移植受者发生的症状性PAP病例中被诱发[2- - - - - -4,10.],包括几乎所有与哺乳动物雷帕霉素靶点抑制剂(mTOR inh)使用相关的病例[4,10.].
在肺移植中,区分PAP和急性排斥反应是很重要的,特别是小叶间隔和小叶间隔增厚是急性排斥反应的特征之一[11.,12.].在我们的患者中,PAP的最初误诊与怀疑或证实的急性排斥反应有关,治疗时增加免疫抑制,可能加重肺泡巨噬细胞功能障碍。最后,我们的病例经常出现随后的肺部感染,这与PAP中报告的抗感染防御效率较低的肺泡巨噬细胞相一致[13.,14.].由于这些诊断上的挑战,医生在尝试提供特殊的治疗时,应该意识到这种罕见的、危及生命的移植后并发症。
披露
补充材料
r . Borieerj - 01369 - 2016 - _borie
M.-P。雷干erj - 01369 - 2016 - _debray
h .发作erj - 01369 - 2016 - _mal
Q.菲律宾ERJ-01369-2016_PHILIPPOT.
g . ThabutERJ-01369-2016_THABUT.
脚注
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com.
- 已收到2016年7月10日。
- 接受2016年12月15日。
- 版权所有©2017