摘要
由于需要在面对内源性和环境挑战的大量暴露时平衡对有效呼吸的要求,对肺部来说,维持一个可持续的防御系统是至关重要的,该防御系统将暴露造成的损害和炎症对脆弱的气体交换表面的有害影响降到最低。因此,上皮细胞和巨噬细胞防御是必不可少的一线和二线保护,防止潜在有害物质在肺部的积累,在体内平衡条件下,这是有效的,而不会引起炎症。尽管上皮细胞和巨噬细胞介导的防御似乎是不同的,但最近的数据表明,它们通过共同依赖气道粘蛋白,特别是聚合粘蛋白MUC5B,而联系在一起。这篇综述强调了我们对连接粘液和巨噬细胞防御的新机制的理解。我们讨论了吞噬作用和粘液中包含的因素对吞噬作用的影响,以及新确定的粘蛋白糖蛋白在直接调节白细胞功能中的作用。糖免疫生物学这一新兴领域的出现为考虑在健康条件下如何维持内稳态以及在疾病中如何恢复内稳态提出了一个新的范式。
摘要
黏蛋白和巨噬细胞协调肺部的第一和第二道天然防线http://ow.ly/s4t7301FLWl
简介
肺的主要功能是气体交换。为此,在正常的潮汐呼吸下,每天有8000 - 12000升的空气通过肺部。气体通过几代传导气道,最终终止于肺泡。肺泡由I型上皮细胞包围,覆盖了95%以上的肺表面。为了能有效地交换氧2和有限公司2I型上皮非常薄,与肺泡毛细血管一起形成的扩散距离<1µm。因此,这些薄表面有复杂的防御机制保护,必须在微粒和病原体到达肺泡壁之前捕获和清除它们,同时防止和/或抑制可能损害脆弱的气体交换结构的潜在炎症反应。这篇综述集中在黏液纤毛梯和肺泡巨噬细胞(AMs)作为宿主在肺部的重要第一和第二防线。
气道组织每天接触约1,000亿吸入颗粒[1].空气中的微粒可来自自然和人为来源,大小和化学成分不同,浓度可因地理和当地环境而异,因此可导致不同的病理反应[2- - - - - -8].大多数吸入物质大到足以影响鼻咽和气管粘膜,它们通过粘液纤毛清除(MCC)近端运输,最终通过咳痰或吞咽排出。其余的沉积在肺周围,被AMs摄取。在正常条件下,颗粒在周围的沉积主要局限于小颗粒(直径<1 μ m)。然而,在颗粒物浓度高的条件下,或在MCC受损的病理环境下,较大的颗粒也可以积聚在肺周围。MCC和AMs的协同作用共同消除肺泡和气道中吸入的微粒,因此形成了强大的外源性清除机制。同时,清除也会清除正常细胞周转或疾病产生的内源性物质。关键的是,尽管AM和MCC的功能通常被认为是不同的,但新出现的数据表明,它们的功能通过生理和生化机制紧密相连。下面我们将分别描述粘液和巨噬细胞,然后讨论它们之间相互作用的新知识。
粘液屏障和粘液纤毛清除
MCC涉及分泌细胞的协调活动,分泌细胞释放聚合粘蛋白糖蛋白,多缘细胞的顶端定位的运动纤毛提供运输和消除手段。纤毛是分子机器,其结构和运动成分高度调控;它们在疾病中的复杂组装、功能和功能障碍在其他地方有综述[9,10].为了这篇综述的目的,我们考虑了运动纤毛的生理作用,并强调了气道中必不可少的黏液纤毛相互作用的关键方面。MCC需要协调调节气道表面液体,以控制分泌粘液的渗透压、粘弹性和由此产生的运输能力[11,12].这种控制是由细胞内的电解质运输机制和细胞外空间渗透物的存在所驱动的。尽管纤毛层和粘液层被认为是独立的实体(“溶胶”和“凝胶”相),但最近的研究表明,这些“层”是一种更连续的糖蛋白水凝胶,这一区别受到了挑战。膜粘蛋白(MUC1, MUC4和MUC16)沿纤毛表面形成水合刷,允许纤毛的自由运动。上面的粘弹性黏液层位于嫁接的纤毛刷上。因此,气道表面水合作用调节纤毛和粘液结构之间的平衡,保持“刷上凝胶”构象,促进有效的运动和MCC [13].
MCC的丧失是呼吸道感染的一个重要原因。例如,MCC受损是感染相关疾病的主要病理生理特征,如原发性纤毛运动障碍(PCD)和囊性纤维化(CF),前者是纤毛运动能力受损或缺失,后者是气道表面脱水导致黏液粘附到气道表面和底层纤毛高渗透性塌陷。对慢性阻塞性肺疾病(COPD)和哮喘的研究结果可能不太重视,它们也显示出显著的MCC损伤[14- - - - - -21].与CF和PCD中黏液和纤毛结构改变的主要作用不同,COPD和哮喘相关的变化是继发于炎症或损伤性刺激,这些刺激会导致纤毛运动障碍和两种主要分泌的粘蛋白MUC5AC和MUC5B的分泌失调[22- - - - - -25].
气道黏蛋白MUC5AC和MUC5B的表达
在健康情况下,MUC5AC和MUC5B都是在肺部产生的。MUC5AC主要存在于整个中央传导气道的表面上皮中,而MUC5B主要存在于中央气道(气管和支气管)的粘膜下腺和外周气道的非纤毛表面上皮细胞中。哮喘患者气道表面和腺上皮MUC5AC水平升高[22,23]和慢性阻塞性肺病[24,26,27].相比之下,MUC5B的水平变化更大。例如,在已经确诊的CF和COPD患者中,痰液中MUC5B水平升高[28,29],主要由气管支气管粘膜下腺提供的中央气道分泌物构成。然而,在早期或临床前慢性阻塞性肺病或强烈过敏性哮喘患者中,MUC5B水平实际上降低,特别是在位于中央和外周气道表面的上皮细胞内MUC5B转录水平降低90%或以上[22- - - - - -24,27].因此,MUC5B的差异抑制可能影响MCC并导致肺病理是合理的。事实上,最近在老鼠身上的研究为这一点提供了机制上的支持。
在小鼠中,缺失Muc5b基因导致严重的上、下气道MCC损伤,并导致致死性自发感染的发展[30.].有趣的是,尽管慢性感染和炎症是主要的结果Muc5b与PCD模型相比,敲除小鼠的病理影响更强。在cilia-defectiveDnaic,Pcdip1,Spef2而且Cby敲除小鼠,尽管MCC严重受损,但没有报道上呼吸道病变是致命的,它们也没有转移到下呼吸道[31- - - - - -33].因此,在肺部的MCC成分中,Muc5b是一种主要的内稳态微生物消除调节剂。此外,在慢性自发性和急性实验性感染中,Muc5ac的产生增加Muc5b基因敲除小鼠。尽管Muc5ac不能完全保护自身,但它可能在延缓感染的影响方面发挥作用[30.].对Muc5ac和Muc5b功能差异的可能解释可能反映了它们在聚合结构、糖基化以及与微生物或抗菌分子相互作用方面的差异。确定Muc5ac和Muc5b的具体和重叠作用仍然是一个急需研究的领域。
粘蛋白表达
MUC5AC / MUC5AC而且MUC5B / MUC5B基因表达水平受内源性和环境因素的调控。对人类MUC5B在美国,单核苷酸多态性已被证明调节表达通过启动子活性的控制[34- - - - - -36].这些基因控制可能影响(或受影响)众多先天和适应性免疫细胞因子信号通路,以及与炎症反应、损伤和组织修复相关的生长因子调节机制。这些在其他地方有广泛的审查[37- - - - - -42].最后,内生因素包括发展性[43- - - - - -46和表观遗传[47- - - - - -49]调节机制,可在肿瘤中黏液蛋白的表达中发挥作用。
粘蛋白聚合
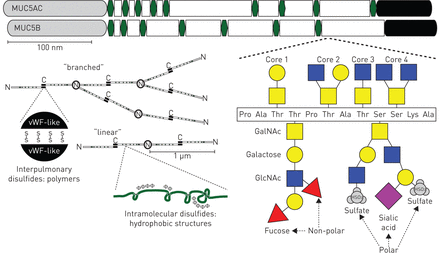
分泌的粘蛋白调节MCC的能力很大程度上取决于它们通过二硫键形成的聚合物结构(图1).与分泌型聚合粘蛋白家族的其他成员一样,Muc5ac和Muc5b由~ 5-6%的半胱氨酸组成(每个分子约250-300个)。它们具有富含半胱氨酸的N端和c端冯氏血友病因子(vWF)型d -样和c端半胱氨酸结二硫键域,这对分子间粘蛋白组装至关重要[51- - - - - -53].另外高度保守的富含半胱氨酸的CysD结构域以不同数量穿插在富含碳水化合物的聚合粘蛋白重复序列中[54- - - - - -56].通过分子内二硫键,CysD结构域被认为可以形成疏水环结构,促进黏液蛋白对齐并调节黏液网格间距[57].此外,每个粘蛋白中至少有100个半胱氨酸存在,这些半胱氨酸是在定义的“结构域”中没有发现的。大多数二硫键被认为在组装过程中在细胞内形成。在细胞外环境中,确实存在的游离半胱氨酸会被氧化并形成额外的交联,从而增加黏液凝胶的弹性模量[50].N端和c端键或cysd的破坏足以“松开”阻塞性粘液。因此,目前的溶粘疗法,如n -乙酰半胱氨酸,以及研究性疗法,都是通过减少二硫化物和降低粘液粘弹性,从而增强粘液运输[58- - - - - -60].目前的一项挑战是确定哪种疗法的剂量既能很好地耐受,又能保持有效防御的益处。
气道中分泌的主要粘蛋白:MUC5AC和MUC5B的高分子结构。MUC5AC和MUC5B(及其同源物)的氨基(N)和羧基(C)端在聚合粘蛋白和血管性血友病因子(vWF,灰色和黑色区域)中进化保守。类vwf结构域参与了c端连接二聚体和n端连接多聚体的共价分子间二硫键组装。多聚物可以以线性或分支结构存在,其大小在1到> ~ 10mda范围内。在类vwf结构域之间是额外的富含半胱氨酸的区域(CysD结构域,绿色六边形),这些区域富含疏水氨基酸(aa)和分子内二硫键。据认为,在健康粘液分泌后,囊状体可调节粘蛋白链的分布和凝胶-孔的大小,但在疾病中,囊状体可被氧化并增加聚合物的尺寸和硬度[50].剩余的粘蛋白载脂蛋白主干大部分富含脯氨酸、丝氨酸和苏氨酸。这个“PTS”区域(白色)是一个不完全重复区域,是o -连锁糖基化的主发位点。丝氨酸和苏氨酸残基上的o键形成Core 1-4结构,定义为在丝氨酸和苏氨酸的羟基上存在n -乙酰半乳糖(GalNAc,黄色方块)键,然后是半乳糖(黄色圆圈)和/或n -乙酰氨基葡萄糖(GlcNAc,蓝色方块)的单个或成对连接。最后,半乳糖和GlcNAc聚糖可以进一步被聚焦物、唾液酸和硫酸盐取代,这些物质可以传递不同的电荷,影响粘液凝胶的水合作用,也可以形成三维结构确认,这对与病原体和宿主细胞凝集素的相互作用至关重要。所示的聚糖结构是可能的连接的例子,不一定代表在特定粘蛋白上发现的那些结构。极性和非极性聚糖可以在每一种核心类型的糖上找到,并且可以沿着相同或不同的分支找到。
粘蛋白糖基化
尽管二硫化物聚合是粘液蛋白分泌的一个重要但未被重视的方面,它们的糖基化可能是更突出的。粘蛋白是由其重糖基化而定义的,特别是在大小不等的富含糖的结构域内(图1).在MUC5AC和MUC5B中,这些区域因富含脯氨酸、苏氨酸和丝氨酸而被称为“PTS”结构域。富含pts的重复序列是o -糖基化的位点,从丝氨酸和苏氨酸残基上的n -乙酰半乳糖胺开始。然后半乳糖和n -乙酰氨基葡萄糖被线性或分支连接和细化,糖可以通过硫酸盐或通过添加末端唾液酸和焦点聚糖进行修饰。粘蛋白聚糖的两个主要作用是吸附水分和参与宿主防御。对于水的吸附,聚糖的变化可以很大程度上影响粘液凝胶的渗透压。例如,唾液酸化末端和硫酸盐末端带强荷电,其大的极性表面积促进水合作用和电负性斥力[11,13].相反,聚焦带更低的电荷和大约50%的低极表面积,这可能促进黏液聚集,增加粘弹性,从而抑制MCC。对于宿主防御,已知粘蛋白聚糖与各种细菌上的糖结合分子相互作用,这些细菌在肺部定植或感染[61- - - - - -67]及胃肠道[68- - - - - -74,在真菌上,如来自烟曲霉属真菌[75],以及呼吸道病毒,例如呼吸道合胞病毒及流感[76,77].这些相互作用是否对宿主或微生物有益,差别很大。然而,由于宿主遗传和环境暴露(如感染或过敏状态),保护是有限的。粘液性质的改变会影响防御能力的减弱(如。通过在MUC5AC/ MUC5AC vs MUC5B/ MUC5B表达水平或PTS结构域糖基化),通常伴有睫状体功能障碍(如。由于纤毛细胞或活动纤毛成分的丧失/缺失)[78- - - - - -91].总之,黏蛋白在黏液凝胶形成和维持中的作用及其结合微生物的能力证明了黏液结合和清除动力学在宿主防御中的协调功能和功能障碍。
综上所述,黏液纤毛屏障作为一种由黏液和纤毛功能调节的防御系统的传统观点,已经通过识别关键因素如Muc5b和解剖黏液纤毛相互作用的复杂生物物理调节而得到了改进。一个直接的挑战是将这些与特定的和必需的分子成分联系起来,以调节它们内在的生物物理功能。此外,新的研究结果介绍了一套新的相互作用,通过粘蛋白调节防御和肺部炎症通过常驻和招募的肺白细胞群。特别是,各种组织中的树突状细胞、嗜酸性粒细胞和巨噬细胞的功能已被证明是由黏蛋白末端聚糖专门调节的。下面我们将重点讨论由细胞外寡糖(包括气道粘蛋白Muc5b)调节的巨噬细胞和嗜酸性粒细胞功能。
巨噬细胞个体发生和清除机制
微粒和微生物会避开第一道防线,即上皮粘液,到达远端肺。在那里,它们必须被第二道防线迅速而有效地清除:吞噬细胞。AMs是肺中主要的吞噬细胞,在健康期间占到空气间隙中白细胞的90% [92- - - - - -95].它们存在于肺泡腔中,也可能存在于气道中。除了清除吸入颗粒物外,它们对清除死亡细胞和维持肺泡内稳态也至关重要。最近的证据表明,AMs起源于胚胎发生时占据胎儿肝脏和卵黄囊的祖细胞[96- - - - - -98].在出生时,这些细胞填充在空气空间中,并迅速成熟为常驻AMs。重要的是,AMs在整个生命过程中自我更新,在没有疾病的情况下,它们不会被循环中的单核细胞取代[99- - - - - -101].在炎症期间,体内的AMs在局部增殖[102].与此同时,循环中的单核细胞迁移到炎症区域,在那里它们成熟为巨噬细胞,称为单核细胞衍生AMs (mdam) [103].因此,炎症AM池包含胚胎和出生后来源的细胞。尽管这两种巨噬细胞亚群都具有吞噬能力,但它们各自在清除外源性微粒和病原体以及清除内源性碎片和细胞方面的作用尚不清楚。有趣的是,随着炎症消退,mdam经历程序性细胞死亡并从肺中移除,留下胚胎来源的驻留AMs以维持肺泡内稳态[103].
在健康期间,住院医疗辅助医生扮演哨兵的角色,不断地调查室内环境中的病原体和吸入的微粒。在大多数情况下,这些药物可以悄无声息地迅速清除,而不会引起可能损伤肺泡气体交换结构的全身炎症反应。事实上,AMs的实验性耗竭导致了夸大的炎症反应[104- - - - - -112],但与此同时AM缺失削弱了控制感染的能力[107,110,113],证明克制的反应更有效和有益。正如下面所讨论的,肺泡环境在调节AM内吞和炎症反应中起着至关重要的作用,它还包含各种各样的分子,可以识别病原体,并通过非炎症性吞噬防御促进清除。
噬菌作用的机制
AMs使用多种机制摄取微粒和病原体,所有这些都涉及内吞作用,在这个过程中,质膜包围目标,内陷,然后捏断形成膜结合的囊泡(在[114,115])。吞噬作用是AMs清除外源性物质的主要内吞过程,它由细胞骨架重排驱动,导致病原体(如细菌或真菌)在膜结合的吞噬体中迅速内化。吞噬体在与核内体和溶酶体连续融合后酸化,溶酶体含有水解酶和活性氧,消化和破坏目标物。AMs与微粒和病原体的初始界面是通过一个吞噬突触发生的,这个吞噬突触是由一系列不同的质膜蛋白形成的,这些质膜蛋白通过它们上的特定部分识别目标,包括微生物和宿主细胞的糖缀合门。这些AM受体启动和/或调节吞噬作用。
噬菌作用的受体
AMs配备了大量的吞噬细胞受体。重要的是,在微生物接触过程中,许多不同的受体家族往往同时被激活。有些受体直接识别吞噬靶标上的特定分子(如。磷脂酰丝氨酸或炎症小体分子),而其他的结合在被调理蛋白包裹的靶上(如。免疫球蛋白、补体成分和表面活性剂材料)。此外,尽管有些(如。Fc受体)直接导致病原体吞噬,其他受体(如。toll样受体(TLRs)通过上调吞噬受体及其下游信号分子的表达,间接促进吞噬作用[116- - - - - -118].在这里,我们讨论了在调理蛋白和气道黏液信号的背景下AMs上的主要受体类别[119- - - - - -125].
免疫球蛋白信号是介导AM吞噬的重要适应性免疫过程。AMs表达高水平的Fcγ受体I (CD64), II (CD32)和III (CD16),识别IgG的Fc区域。在健康人的肺泡衬液中可发现具有生物学意义的IgG浓度[126].为了触发吞噬作用,fc γ-受体与免疫复合体内的多个IgG分子结合。FcγRI是一种高亲和力受体,除了呼吸爆发和微生物杀死也导致吞噬作用。相比之下,FcγRII和FcγRIII也能促进吞噬,但结合亲和力较低。呼吸上皮细胞通过胞吞作用分泌IgA,在近端气道和肺泡的管腔中都很容易检测到IgA [126,127].AMs表达低水平的Fcα ri (CD89)和Fcα/μR,两者结合IgA并驱动吞噬[128].适应性免疫免疫球蛋白功能通过识别碳水化合物抗原、其Fc结构域的N-和o -糖基化以及与具有特异性免疫球蛋白结合结构域的分泌粘蛋白的物理联系与糖聚糖结构相联系[129- - - - - -132].
补体系统通过调节免疫复合物和病原体,增强它们的杀伤和清除,帮助先天宿主防御。健康人的肺泡灌洗液含有经典(C1q, C2, C3, C4)和替代(C3,因子B)通路的成分[133- - - - - -135].经典途径主要通过C1q与抗原-抗体复合物的相互作用激活,但也可以通过C1q直接与细菌、真菌和病毒的膜组分结合而激活[136,137].两种方法对目标的调理都能刺激吞噬作用。AMs表达三种补体受体(CRs), CR1, CR3和CR4。CR1自身不能内化调理颗粒,但可以增强fc介导的吞噬作用。CR3和CR4是具有共同β的异二聚体2整合素链(CD18)与特异性α链配对。CR4含有αX亚基(CD11c),并与C3b和iC3b片段调节的粒子结合。CR3含有一个α毫克ydF4y2Ba链(也称为CD11b)与碳水化合物结合凝集素位点。因此,除了结合C3b和iC3b片段调节的颗粒外,CR3还结合微生物细胞壁含糖成分,包括脂多糖、甘露聚糖、β-葡聚糖等[138,139].虽然CR3似乎能够独立内化调理细菌[140,141],它也与其他受体,包括CR1, CD14, FcγR和FcαRI协同作用[138,142- - - - - -144],以提高颗粒间隙。不足为奇的是,缺乏CR3的小鼠会削弱宿主对革兰氏阴性菌、革兰氏阳性菌和酵母菌的防御能力[145,146].重要的是,来自啮齿类动物的研究表明,CRs的细胞表面表达在驻留AMs上有显著差异与已招募的妇女顾问[103]:体内AMs表达高水平的CD11c/CR4,但CD11b/CR3不表达,而招募的mdam表达高水平的CD11b/CR3,但CD11c/CR4表达低水平。这就提出了一个有趣的假设,AM亚群在控制感染和炎症宿主防御方面具有互补功能。与免疫球蛋白一样,补体成分也存在于气道黏液中,其水平在炎症中上调[147,148].此外,补体成分也增加了气道上皮细胞中Muc5ac的表达[149].
其他类型的碳水化合物凝集素,如c型凝集素,是钙依赖的碳水化合物结合蛋白,包含保守的糖基识别域,参与病原体识别和吞噬作用[150].在肺宿主防御的背景下,两组c型凝集素被很好地识别:肺凝集素(表面活性剂蛋白(SP)-A和SP- d)和病原体结合受体(即甘露糖受体(CD206)和Dectin-1)。SP-A和SP-D是由n端胶原样结构域与c端碳水化合物识别域通过中央铰链区连接而成的高度寡聚单体。通过它们的碳水化合物识别域,SP-A和SP-D可以识别微生物病原体上的糖残基。因此,它们调节革兰氏阴性和革兰氏阳性细菌、分枝杆菌、真菌和病毒,如甲型流感病毒和呼吸道合胞病毒。在AMs上存在许多集集素调节粒子的候选受体,包括C1qRp, SP-R210, CD14和钙网蛋白- cd91复合物(在[151])。除了通过其调理作用增强吞噬作用外,集合素还可以间接促进吞噬作用。例如,SP-A增强清道夫受体A的表达,并可增强fc受体和cr介导的吞噬作用[152- - - - - -154].此外,SP-A和SP-D似乎都能增加细胞表面定位,从而增强甘露糖受体的吞噬功能[155- - - - - -157].甘露糖受体(CD206)在AMs上高度表达,并包含一个细胞外结构域,可以识别甘露糖、n -乙酰葡萄糖胺和焦点聚糖。因此,CD206促进具有不同胞外碳水化合物特征的肺病原体的吞噬,包括肺炎链球菌,肺炎克雷伯菌,结核分枝杆菌,耶氏肺囊虫真菌,比如假丝酵母而且曲霉属真菌[158].CD206参与吞噬的确切机制尚不清楚,很可能需要与共受体的相互作用[159].Dectin-1最初被认为是一种树突细胞特异性受体,但它也在AMs上表达[160].Dectin-1识别真菌细胞壁中的β-葡聚糖[161,162]以及用戊曲辛-3调节的颗粒,戊曲辛-3是一种由单核吞噬细胞对促炎信号作出反应时迅速合成和分泌的蛋白质[163].这些受体共同突出了一组表面分子,与气道表面液体和粘液的外源性和内源性成分相互作用,介导AM吞噬防御。
在具有免疫能力的个体中,感染期间肺部的防御成分如IgG增加,通过识别包括碳水化合物表位在内的多种抗原类型促进病原体清除。事实上,细菌靶点如表面多糖被用于开发有效的肺炎球菌疫苗[164].相反,复发性肺感染和病原体清除障碍在免疫球蛋白缺乏的患者中很常见[165- - - - - -171].此外,在常见的慢性呼吸道疾病,包括哮喘、慢性阻塞性肺病和慢性阻塞性肺纤维化中,有大量文献记载AMs对微生物病原体的清除受损[172- - - - - -175].AM功能障碍与疾病严重程度和加重频率相关[176- - - - - -178].虽然不同疾病的病因不同,但共同的特征包括吞噬细胞受体的表达改变,溶酶体杀伤减少,以及通过诱导周围组织的附带损伤来加重炎症的介质产生增加。AMs中的这些缺陷在从其他部位分离出来的单核吞噬细胞中不存在或减少(如。血)。因此,局部环境的扰动似乎在这些疾病中AM功能的改变中起着主导作用。
气道粘蛋白和肺泡巨噬细胞功能之间的新联系
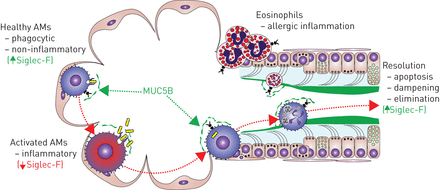
基于独特的解剖定位和高度专用的细胞机制,涉及气道中产生黏液的杯状细胞和肺泡中的吞噬巨噬细胞的规范,它们的功能在外观上是离散的区隔化的。然而,并不是完全有理由将驻留AMs的定位限制在肺泡空间,因为传导气道中的腔内巨噬细胞占大鼠肺中驻留巨噬细胞总数的2-8% [179- - - - - -185].最近的证据表明,即使在牙槽腔室内,被称为无梗肌的肌电辅助细胞的一个亚群也可以进行长距离的交流通过一种钙依赖性信号传导am -肺泡上皮回路,最终抑制免疫功能[186].最近的研究表明,气道黏液与巨噬细胞功能之间确实存在功能联系,这些联系对宿主防御至关重要。在某种程度上,粘液中富含免疫球蛋白和补体成分等分泌因子,这表明粘液是这些防御分子的重要载体。此外,分泌的粘蛋白和固有免疫细胞之间也有直接联系,通过它们在化解炎症时的协同作用,以及粘蛋白上的聚糖和白细胞上的碳水化合物结合凝集素受体(如唾液酸结合免疫球蛋白样凝集素(Siglec’s))之间的物理相互作用。我们认为黏液-白细胞相互作用通过信号和物理清除机制调节稳态、炎症和化解免疫功能(图2).
内稳态和炎症过程中黏液-白细胞的相互作用。在健康肺中,静息泡巨噬细胞(AMs)具有防御性和非炎症性。来自细支气管的MUC5B与肺泡液混合,为MUC5B接触肺泡AMs提供了途径。体内平衡或低剂量刺激引起防御功能,如吞噬作用。在炎症期间,体内的AMs会被激活,这与它们siglecf表面表达的减少有关。此外,白细胞,如单核细胞来源的巨噬细胞(缺乏siglecc - f)或嗜酸性粒细胞(表达siglecc - f)被招募并存活很短一段时间。随着炎症的消退,这些短暂的种群被消除。在小鼠中,解决包括siglecc - f介导的白细胞激活和存活的减少。受损和凋亡细胞随后被muc5b介导的粘液纤毛清除清除。
在小鼠中,肠道黏液蛋白Muc2与树突状细胞上的甘氨酸选择性免疫调节受体相互作用,介导炎症和调节淋巴细胞亚群的发展。在这种情况下,Muc2聚糖结合两种凝集素(Dectin-1和Galectin-3),这两种凝集素与抑制性IgG受体FcγR3协同作用,抑制炎症信号并促进耐受[187].在类似的静脉中,杯状细胞也被证明是将抗原运送到小肠内的单核细胞衍生树突状细胞的重要机制[188].这些活动的结果是形成对外来抗原的耐受性,这些抗原是由摄入的食物颗粒引入的。
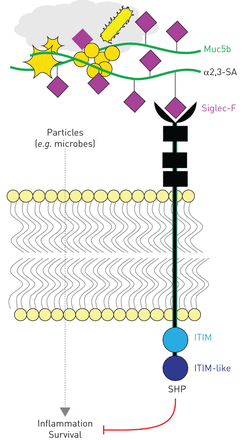
在肺部,白细胞功能的抑制调节似乎是由白细胞激活状态的急性控制介导的。在小鼠中,Muc5b通过其α2,3连接的唾液苷聚糖与siglecc - f结合,siglecc - f是嗜酸性粒细胞和AMs上的一种抑制性SH2结构域含磷酸酶信号免疫受体(图3) [189].在嗜酸性粒细胞上,siglecc - f介导细胞凋亡[190- - - - - -193],从而成为解决过敏性炎症的重要机制。事实上,缺乏siglecc - f或Muc5b唾液化步骤所需的一种特定酶ST3Gal-III的小鼠,无法为siglecc - f制造气道配体,并在2型过敏性炎症肺模型中显示出夸张的选择性肺嗜酸性粒细胞增多[194- - - - - -198].在这种情况下,Muc5b可能有助于MCC对细胞的物理清除,同时防止从小鼠肺清除过程中继续激活和中介物质释放到空气空间。在人类中,siglece - f类似基因siglece -8也能减少嗜酸性粒细胞的存活通过但在小鼠中Muc5b和siglece - f之间观察到的特异性,在人类中Muc5b和siglece -8之间则不那么保守[199- - - - - -201].相反,sigec -9是一种与MUC5B唾液苷结合的亚型,在中性粒细胞、自然杀伤细胞、树突状细胞和单核/巨噬细胞上表达[199].事实上,健康小鼠肺部的固定AMs也表达siglecc - f,但它在细胞表面标记之外的作用尚不清楚。鉴于黏液和巨噬细胞功能障碍在许多肺病理中的关联,随着该领域的发展,确定它们相互作用的性质将具有巨大的兴趣。随着黏蛋白作为重要的防御介质的出现,以及对先天免疫和适应性免疫的糖生物学的重要意义的认识,探究这些问题的努力将涉及既具有挑战性又令人兴奋的实验方法。
推测Muc5b: sigle - f信号转导机制。Muc5b,通过它显示了半乳糖残基上的多价α2,3-唾液酸(SA)键,与siglecc - f的n端凝集素结构域结合,从而驱动免疫受体酪氨酸基抑制基序(ITIM)和ITIM样结构域激活。ITIM信号可能激活Src同源区2域含磷酸酶(SHP)酶,抑制激酶激活的炎症信号,也可能促进细胞凋亡。
结论
肺部的先天防御系统对保持有效的气体交换至关重要。黏蛋白和巨噬细胞作为宿主的第一道和第二道防线,在它们的生理和生理相互作用中发挥着重要作用。这些联系的出现带来了连接上皮免疫规划和先天免疫规划的新挑战的汇合。
脚注
支持声明:W.J. Janssen: NIH HL109517, NIH HL114381;B.S. Bochner: NIH AI72265, NIH HL107151;C.M.埃文斯:NIH HL080396, NIH ES023384, AHA 14GRNT19990040。本文的资助信息已存入公开基金管理人登记处.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 收到了2016年1月17日。
- 接受2016年6月12日。
- 版权所有©ERS 2016