摘要
全身性炎症和合并症对成人哮喘治疗和预后的影响尚不清楚,这也是本研究的目的。
作为Seinäjoki成人哮喘研究(SAAS) 12年随访的一部分,我们测量了170例无慢性阻塞性肺疾病的成人哮喘患者的血清白介素(IL)-6、高敏c反应蛋白(hsCRP)和肺功能,并收集了有关共病和药物治疗的临床信息。
在随访中,54%的患者有IL-6或hsCRP升高提示的全身炎症,58%至少有一种共病,30%至少有两种共病(哮喘相关除外)。与非系统性炎症患者相比,系统性炎症患者接受了更高剂量的吸入皮质类固醇(ICS)治疗,他们的肺功能较低,血液中性粒细胞较高。有≥2个共病的患者哮喘控制试验评分较低,且在调整后的分析中相关性仍然显著。同时伴有全身性炎症和共病的患者哮喘预后最差。多因素回归分析显示,在基线和随访时,IL-6升高、血液中性粒细胞和嗜酸性粒细胞升高以及肺功能较差预测了高ICS剂量。
总之,在患者的成人哮喘,升高IL-6与使用高剂量ICS的关联,而多是发病率与哮喘的恶化症状。
摘要
在成人哮喘发病中,IL-6升高与高ICS剂量和哮喘症状加重的多病相关http://ow.ly/IUtG3010z3v
介绍
在成年期发病的哮喘被认为是哮喘的一种独特的表型。成人发病的哮喘与儿童发病的哮喘有许多不同之处。儿童期发作哮喘的特征是男性占优势,家族性特应性,T-helper 2 (Th2)细胞主要炎症,对糖皮质激素有良好的反应性,预后良好[1,2].相比之下,患者的成人哮喘是最常见的非过敏性的女性,预后差,无哮喘/过敏体质家族史[2- - - - - -5].
哮喘患者往往如过敏性和非过敏性鼻炎,呼吸道感染和胃食管反流条件受到影响。慢性阻塞性肺疾病(COPD)是公认的哮喘经常吸烟的哮喘患者制定一个共同的合并症。此外,成人哮喘患者有合并症,如精神疾病,糖尿病和心血管疾病与普通人群相比,更高的利率,而且往往有一个以上的合并症[6,7].有合并症的哮喘患者有较高的非哮喘相关医疗保健使用,在活动性哮喘患者中最高[6提示哮喘和共病之间存在联系。有一种以上共病的哮喘已被证明会导致与哮喘相关的生活质量下降[8伴随的抑郁症与较差的哮喘控制有关[9,10].
全身性炎症,其特征在于,白介素(IL)-6和C-反应蛋白(CRP)的水平升高,具有哮喘和合并症之间的可能联系。它与疾病,如糖尿病,心血管疾病,全身性风湿疾病和精神障碍除了哮喘相关[11- - - - - -13].尽管肥胖是最著名的低级别全身炎症诱因,但全身炎症的病因比肥胖更广泛:例如,衰老、抑郁、压力和吸烟会加剧全身炎症[7,14- - - - - -16].一个器官的过度炎症也被认为是全身炎症的可能来源[15是一种提示合并症影响哮喘的机制,反之亦然。另一方面,多种疾病的心理应激可能对哮喘等产生负面影响通过与压力有关的全身炎症增加[14].IL-6和/或高敏(hs) CRP升高、中性粒细胞炎症与肺功能恶化或哮喘控制恶化之间的关联此前已被提出[15,16].
成年期哮喘患者通常是超重的中年妇女。因此,我们假设全身炎症和共病在成人发病的患者中很常见,并影响这些患者的哮喘预后和治疗。我们的目的是研究是否共病和全身炎症共同或单独影响哮喘的治疗和结局。
方法
研究设计和患者
目前的研究是Seinäjoki成人哮喘研究(SAAS)的一部分。SAAS是一项前瞻性、单中心(Seinäjoki Central Hospital, Seinäjoki, Finland)的12年随访研究,研究对象为在成年期(≥15岁)确诊的新发哮喘患者。获得机构许可(TU1114和LET),参与者对芬兰坦佩雷大学医院伦理委员会批准的研究方案给予书面知情同意(R12122)。saas研究方案已单独发表[17],包含和排除标准如表S1所示。很快,呼吸内科医师在1999-2002年间根据典型症状诊断出哮喘,并通过客观肺功能测量证实[17].诊断后,患者由自己的治疗医生进行治疗和监测,或在专业护理或初级护理。总队列包括257例患者,203例患者在诊断后随访12年(平均12.2年,范围10.8-13.9年)。随访时,采用结构化问卷对患者哮喘状况及对照、合并症和用药情况进行评估,并测量患者肺功能、血清IL-6和hsCRP。疑似或共存的COPD患者(支气管扩张剂后1秒用力呼气量(FEV)1)/强迫肺活量(FVC) <0.7和>10烟包年)从主要分析中排除(图1)因为主要关注的是不太为人所知的共病的影响。然而,对于一些分析,那些可以被归类为哮喘COPD重叠综合征(ACOS)的患者[18作为单独的组进行比较。
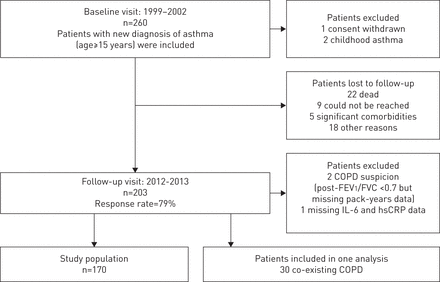
研究流程图。慢性阻塞性肺疾病;钒铁1:1秒用力呼气量;FVC:用力肺活量;CRP:C-反应蛋白。
肺功能、炎症参数和其他临床测量
根据国际建议使用肺活量计测量肺功能[19].更详细的信息可以在网上补充被发现。呼出的一氧化氮的比例(F伊诺)按照美国胸科协会标准[与便携式快速反应的化学发光分析仪测量20.](流速50 mL·s−1;NIOX系统,Aerocrine,索尔纳,瑞典)。静脉血,并测定白细胞分类计数。总免疫球蛋白(Ig)E水平分别通过使用ImmunoCAP(Thermo Scientific的,瑞典乌普萨拉)测量。塞伊奈约基中心医院的实验室试验在认可的实验室(2007:2005和ISO 15189 SFS-EN ISO / IEC 17025)执行。患者完成航空问卷20(AQ20)21]和哮喘控制试验(ACT)。根据全球哮喘倡议(GINA)2010年报告进行哮喘控制评估[22].
合并症
共病的定义和分类是基于以前的研究[23].合并症是自我报告的或基于自我报告的药物治疗。病人记录证实了不清楚的病例。在线补充中列出了作为共病的条件。
系统性炎症
通过ELISA(R&D Systems,美国明尼苏达州明尼阿波利斯市)测定血清IL-6水平,并在罗氏Cobas 8000自动临床化学分析仪(瑞士巴塞尔罗氏诊断公司)上使用颗粒增强免疫比浊法测量hsCRP。检测下限为0.7 pg·mL−1IL-6和0.3 mg·L−1为C反应蛋白测定。Cut-off values used to define systemic inflammation (IL-6 level >1.55 pg·mL−1and/or hsCRP >4.12 mg·L−1)是根据健康受试者的上四分之一[15].
统计分析
连续数据表示为平均值±sd或中位数(四分位数范围)。两组比较采用t检验、Mann-Whitney秩和检验或卡方检验。为了分析两组以上的差异,用Tukey's进行单因素方差分析事后检验、Kruskal-Wallis检验或卡方检验。
当分析ICS剂量的预测因子时,采用多项logistic回归和二元logistic回归预测ACT评分较差。对相关矩阵进行分析,将相关性不强(R<0.7)的解释变量纳入分析。在预测高剂量的模型中,预测因子是基于单因素分析和给出最佳伪r的变量组合来选择的2(Nagelkerke)通过输入方法选择。此外,还采用了正向和反向方法来帮助选择最佳模型。使用SPSS软件22版(IBM SPSS, Chigaco, IL, USA)进行统计分析。p值<0.05为有统计学意义。
后果
有或没有全身性炎症和共病的哮喘患者的结局
我们根据患者是否有共病、全身炎症或两者兼有将患者分为四组。最大的组由全身炎症重叠和至少一种共病的患者组成(38.2%)。合并症和全身炎症的患者年龄越大,体重指数(BMI)越高,吸烟量也越高(表2).结果显示,患者肺功能较差,AQ20评分较高,ACT评分较低,血中性粒细胞(表2).患者全身炎症,但没有使用高剂量ICS的合并症,而具有≥1合并症没有系统性炎症的患者表现出较高的AQ20得分与组同时缺乏比较。
在患者有无全身性炎症性哮喘的成果
到患者的全身性炎症更好地表征哮喘,我们将队列分为两组:1)患者兼有的hsCRP和IL-6(无全身性炎症)的低电平;和2)患者IL-6,C反应蛋白或二者(全身性炎症)的升高的水平。患者全身炎症表明血嗜中性粒细胞的更高的计数,低级肺功能,使用较高剂量ICS和具有较高的AQ20得分并与患者无全身性炎症(相比降低ACT得分表3).即使将所有吸烟者排除在分析之外,全身炎症患者的ICS剂量仍然较高(表S2)。
在整个患者群(N = 170),IL-6和C反应蛋白之间的Spearman相关系数为0.495(P <0.001)。血清IL-6水平呈弱负相关预处理和后支气管扩张肺功能1(%预测)(ρ=−0.218,p=0.006和ρ=−0.244,p=0.001)并与ICS剂量呈正相关(ρ=0.327, p<0.001)。血清IL-6与前(ρ=−0.013,p=0.865)或后支气管扩张剂FEV无相关性1/ FVC(ρ=−0.076,p = 0.325)。
有或没有合并症的哮喘患者的结局
要查看合并症和哮喘结果多发病率的效果,我们把人群分成三组:患者无合并症,有一个合并症与≥2合并症(表4).共病≥2例的患者AQ20和ACT评分较无共病的患者低,血中性粒细胞水平升高,全身炎症升高。有一种或≥2种共病的患者在年龄和使用与哮喘或过敏治疗无关的药物方面存在差异(表4).这些患者的共病情况见表S3。
校正年龄、BMI、背包年和性别后,共病≥2例与较低的act评分(<21)相关(OR 2.477, CI 1.005-6.107;p = 0.049)。除年龄、包年、性别和BMI外,ACT评分与≥2个共病之间的相关性在校正IL-6后仍具有交界性显著性(OR 2.425, CI 0.979-6.005;p=0.056),提示其可能并非主要由IL-6介导。在调整后的分析中,有一种共病或IL-6水平不是不良act评分的预测因素(数据未显示)。治疗过敏或哮喘以外的其他疾病的药物数量与ACT评分之间存在负相关(Spearman ρ=−0.311,p<0.001)。
为了评估哮喘患者的共病数量是否与特定类型的症状相关,我们调查了AQ20和ACT中共病数量与特定问题之间的相关性。在调整分析中,哮喘患者和≥与无合并症的患者相比,2名合并症患者在上楼和做家务时由于胸部问题(AQ20中的Q12和Q13)更经常出现呼吸困难(表5).
同样,在2个以上共病的患者中,哮喘在工作、学校或家庭中得不到同样多的治疗(ACT中Q1) (表5).
对于利息,在患者≥2合并症(无COPD)患者和哮喘ACOS的结果进行比较,我们包括了一个分析的ACOS组。在与ACOS组相比,治疗合并症≥2更频繁的女性和非吸烟者,显示出更好的肺功能,有比性哮喘或过敏相关的药物在使用较多的其他(表4),并有更多的时候任何精神疾病(表S3)。两组表明全身性炎症和升高的嗜中性粒细胞,表示用于ACOS和多的发病率的共同特征,而不ACOS。
ICS高剂量的预测因素
在全身性炎症患者中,ICS治疗哮喘的使用率明显较高。我们进行了多因素logistic回归分析,以找出随访时高ICS剂量(>800 μ g布地奈德当量)的预测因素。预测高剂量ICS的指标为IL-6水平>1.55 pg·mL−1,血中性粒细胞>3.9×109/ L,血嗜酸粒细胞> 0.2×109/五十、 钒铁1/随访和FEV时FVC <0.751诊断时预测小于80%,而更大的哮喘发病年龄(>40岁)是一个临界预测因素(表6).合并症(1或≥2)并不高ICS的预测在多变量模型中剂量和从模型中除去(未示出数据)。介质ICS的预测剂量列于表S4所示。
讨论
我们发现,半数以上的成人哮喘患者有全身性炎症(IL-6水平升高),大多数患者至少有一种合并症和三分之一的几种合并症。IL-6升高与治疗哮喘的ICS剂量增加和与哮喘症状增加相关的多种疾病(除哮喘外的两种或两种以上共病)相关。同时伴有全身炎症和共病的患者哮喘预后最差。
在我们的研究中,半数以上的成人哮喘患者IL-6水平升高,提示全身炎症。由于没有广泛接受的全身性炎症的存在限度,我们的定义是基于健康受试者报告的IL-6和hsCRP的上四分之一[15].我们的研究表明,C反应蛋白是不是挂在哮喘患者的肺部功能,也由以前的研究中提出[15].IL-6与哮喘患者肺功能下降有关[15,24可能是与哮喘预后相关的全身炎症更重要的生物标志物。与既往研究一致,我们发现IL-6升高患者肺功能下降,中性粒细胞升高,IL-6与FEV呈负相关1[15,24].
IL-6是一种多效细胞因子[25由包括炎症细胞和气道上皮细胞在内的多个细胞在损伤或激活时产生。尽管大量证据表明它具有更大的功能作用,但它以前被认为是多种疾病炎症的非特异性标志物。IL-6的升高被认为是老年虚弱的标志,与死亡和发病率风险的增加有关[26].在它可能导致哮喘的各种机制中,最好的特征是它对Th2分化和IL-13产生的刺激作用[27].为了支持这一途径的被操作,在轻度至中度过敏性哮喘年轻的成年人,IL-6和IL-13有相关性[28].IL-6也被报道刺激的Th17分化-β表明IL-6可能会促进转化生长因子(TGF)的存在下的Th17介导的嗜中性粒细胞为主的重度哮喘[27,28].此外,通过活化TGF-β[29],IL-6能够诱导纤维化,气道重塑和后支气管扩张肺功能丧失[28]在我们的全身炎症患者中,升高的血液中性粒细胞支持Th17而不是Th2途径的参与。为了进一步支持,Th17细胞被报道为类固醇耐药[30.],这可以解释IL-6升高患者使用较多ICS剂量的原因。然而,我们不能排除ICS治疗导致我们患者的嗜酸性粒细胞减少而中性粒细胞增加的可能性,正如显示ICS促进中性粒细胞生存的研究所表明的那样[31- - - - - -33].在正常生理情况下,糖皮质激素可减少IL-6的产生,但成人哮喘患者中IL-6的高水平表明糖皮质激素的这种能力可能受到干扰。例如,长期的心理压力已经被证明会降低糖皮质激素抑制IL-6生成的能力[34].
由于患者全身炎症未调整的分析中使用高剂量ICS的,我们构建了一个多变量模型,以高剂量ICS的阐发预测。据我们所知,这是第一次研究,以确定在成人哮喘的随访研究高剂量ICS的预测。我们的研究结果表明,患者的后支气管扩张肺功能1诊断时<80%(大部分未经治疗)的是在诊断12年后使用中至高剂量ICS的患者。为了支持这一观点,在一项后续研究中,低FEV1在确诊后的1年内,预测5.8年后成人哮喘发作更严重[35].此外,在后续的(<0.75)增加的支气管阻塞预测ICS的高剂量。在协议中,患者和无固定气流阻塞最近的聚类分析,患者持续性梗阻往往高ICS的用户[36].此外,血液中炎症标志物升高的患者(嗜酸性粒细胞>0.2×109/ L和中性粒细胞> 3.9×109/L),尽管进行了抗炎治疗,但更有可能使用高剂量ICS,提示更多的类固醇耐药炎症。肥胖以前被认为与类固醇抵抗、高剂量ICS和使用多种控制器有关,但在调整后的分析中,BMI和腰围都不能解释高ICS剂量。IL-6在肥胖受试者中升高,但其功能超出肥胖,与肥胖相比,IL-6可能是影响哮喘治疗和预后的全身炎症和/或代谢变化的更精确标志物。令人惊讶的是,一包年>10并不能预测高剂量ICS的使用。ICS已被证明对吸烟的哮喘患者效果较差[37],这可能导致更倾向于低ICS和长效β的联合治疗2-激动剂而不是高ICS。根据我们的结果,吸烟者经常发生的支气管阻塞比吸烟更能预测高剂量ICS。总之,肺功能和炎症参数(包括升高的IL-6)与高剂量ICS治疗相关。
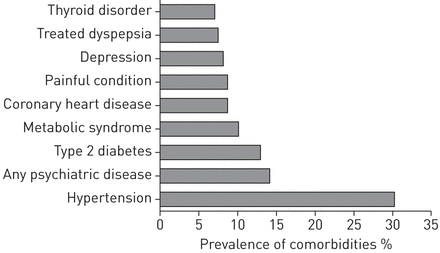
在大多数哮喘研究中,有显著共病的患者被排除在外。SAAS是一项现实生活中的随访研究,其中包括有共病情况的患者。由于没有标准方法可用于测量共病或多发病率,我们使用了大量医疗实践患者评估中使用的标准,以确保广泛的共病条件的测定[23].在该队列中,有明确特征的成人哮喘患者,58%的患者患有一种共病,30%患有几种共病。最普遍的合并症是高血压、任何精神疾病和2型糖尿病。在另一项对全科哮喘患者(年龄40-75岁)的研究中,53%的患者至少有一种共病,≥2种共病的患者占20% [8].另一项研究仅包括成人哮喘患者(平均年龄52岁) 年)发现共病患病率为50.5%,但如。与我们的研究相比,鼻炎和鼻窦炎被列为共病[38].我们的研究与之前的研究一起支持这样的观点,即在成人或迟发性哮喘中共病和多病是常见的,并证实了最近的基于人群的研究[6,39,40],说明在哮喘患者合并症高负担。
我们发现,与无合并症患者相比,至少有两种合并症患者的AQ20和ACT评分较低,表明哮喘症状增加。多种疾病患者的症状增加主要与日常活动中的呼吸困难有关。肥胖已被证明会降低哮喘控制和并发症哮喘[41],但症状多发病率的作用是独立于BMI。根据我们的数据,IL-6可能部分占症状加重,但因为一些合并症的参与,它更可能由多因素的机制解释包括多种介质[中7].其机制可能包括炎症过度以及多种疾病的应激。多病患者表现为血液中性粒细胞升高,但中性粒细胞性气道炎症是否解释了较高的症状仍不清楚。多种疾病的累积也可能导致患者对症状的感知恶化。我们的结果与以人群为基础的研究结果非常一致[6,39,40表明哮喘患者有合并症的情况增加了健康声明和非计划的医疗访问的数量。逻辑上,哮喘伴发疾病已被证明会导致与哮喘相关的生活质量和总体生活质量的降低[8,这在有许多共病的患者中最为明显。在特定的共病中,高血压(在我们的多病组中为72%)与短效β的轻微增加使用有关2激动剂,更频繁的急诊科访问/住院治疗和口服糖皮质激素dispensings哮喘患者[42].我们有合并症的患者平均使用三种药物来治疗他们的合并症,而且仍有可能是多药或某些药物的使用导致了所见的效果,而不是合并症。支持这一观点的是,在韩国老年人群中,在6个月的随访后,更少的共病药物治疗数量,而不是更少的共病,预测哮喘控制改善[43].
鉴于最近对ACOS的关注,我们比较了多病哮喘患者(无ACOS)和有ACOS的患者。与哮喘预后相关的参数的唯一差异是ACOS患者肺功能较差,这与之前的研究一致[44,但是缺乏对哮喘控制和症状的比较。此前也有报道称ACOS中IL-6和痰中性粒细胞水平较高,组间共病指数相似[44].在我们的研究中,ACOS和共病≥2例患者的全身炎症和中性粒细胞水平均同样升高,这可能至少部分地解释了后一组的共病负荷较高,尤其是精神疾病。精神疾病与全身炎症、更糟的哮喘控制和哮喘相关的生活质量有关[9,11].
总之,我们发现,合并症和升高的IL-6例成人哮喘中常见的,并且与哮喘的预后更差有关。无论是IL-6的患者与起源成人发病的哮喘是肥胖,吸烟,压力,哮喘或其他慢性疾病,不是由我们的数据透露,但大量的证据表明,IL-6水平升高有助于多的发展发病率[26],并参与哮喘的病理生理学[27,28].我们的研究结果还表明,IL-6也会使哮喘的治疗复杂化。与无共病的哮喘患者相比,多病哮喘患者更有症状,这一现象被认为是多因素的,而不是仅仅由IL-6介导的。在临床上,IL-6可能有助于识别对ICS治疗反应差的患者,以及识别那些可能受益于生活方式改变作为其治疗计划的一部分的患者,因为锻炼已被证明可以减少全身炎症并改善哮喘的结果[45].此外,抗il -6治疗值得作为一种替代治疗策略进行研究。
确认
艾诺Sepponen(呼吸内科,塞伊奈约基市中心医院,塞伊奈约基,芬兰DEPT)表示感谢,通过这项工作的所有阶段她的帮助。
脚注
编辑评论欧洲呼吸杂志2016;48: 979 - 981。
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:本研究由芬兰防痨协会基金会,Jalmari和Rauha Ahokas基金会,坦佩雷结核病基金会,坦佩雷大学附属医院(芬兰Tampere)的专家责任区的竞技状态研究资金和医学研究基金资助塞伊奈约基的中心医院(塞伊奈约基,芬兰)。本文的资金信息已存入资助者打开注册表.
本研究注册于ClinicalTrials.gov标识号NCT02733016.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 收到了2015年12月28日。
- 接受2016年5月28日。
- 版权©2016人队