摘要
肥胖和哮喘之间的中介途径在很大程度上是未知的。本研究旨在探讨中心性肥胖与儿童哮喘之间的介导途径和最突出的病理机制。
在台湾儿童健康研究中,我们收集了9-13岁儿童的开放队列数据。在2010年至2012年期间,每年对儿童的呼吸结果、特应性疾病、肥胖测量和肺功能进行调查。2012年记录了呼出的一氧化氮浓度。使用广义估计方程和一般线性模型来检查中心性肥胖、可能的介质和哮喘之间的关联。结构方程模型被应用于研究中心性肥胖和哮喘之间的通路。
中心性肥胖(腰臀比)最能准确预测儿童哮喘。活动性哮喘模型中,肺功能、特应性和气道炎症的调解率分别为28.6%、18.1%和5.7%。在终身喘息模型中,肺功能调节的比例为40.2%。在两种模型中,肺功能在三种介质中所占的中介比例最大。
肺功能下降是中心性肥胖相关性哮喘的最重要途径。应应用肺功能筛查对肥胖儿童进行哮喘风险预测。
摘要
肺功能下降是中心性肥胖发展为儿童哮喘最突出的病理途径http://ow.ly/4mJomZ
介绍
肥胖和哮喘是全世界儿童的重要健康问题。最近的两项前瞻性队列荟萃分析报告称,高体重指数(BMI)的儿童患医生诊断的哮喘和突发哮喘的风险增加[1,2]。除了身体质量指数外,其他肥胖指标可能提供更多信息[3.]。米usaad等。(4和我们的团队[5他们都发现,以腰围或腰臀比衡量的中心性肥胖,是儿童哮喘最有用的肥胖指标。虽然可能存在某种“肥胖哮喘”表型[6,7],对于中心性肥胖和哮喘之间关系的病理机制知之甚少。
有几种途径可以解释肥胖和哮喘背后的病理生理学。特应性与哮喘的免疫机制有关,常见于哮喘儿童[8]。两项研究表明,超重儿童患特应性过敏和哮喘的风险增加[9,10],但其他研究报告了相互矛盾的结果[11,12]。最近,F或不等。(3.证明了特应性是肥胖-哮喘关联的重要中介。呼出的一氧化氮分数(F伊诺),可提供气道炎症的定量测量,与儿童过敏性哮喘有关[13]。先前的一项研究声称,超重儿童患有哮喘和高血压F伊诺与正常体重的哮喘患儿相比,高水平哮喘患儿的哮喘控制能力较差F伊诺水平(14]。此外,严重哮喘患儿表现出特应性和增高的双重特征F伊诺(15]。因此,我们认为特应性和气道炎症是中心性肥胖到哮喘发病的中介。
肥胖会降低肺活量[16]并可能随后引起哮喘。一项研究显示,腹部肥胖比BMI更能预测肺功能,提示中心性肥胖对肺扩张受限的重要性[17]。我们之前的研究也表明,中枢性肥胖相关的肺功能下降(以1s用力呼气量(FEV)测量)1)/强迫肺活量(FVC))导致儿童哮喘,但我们没有研究中心肥胖-哮喘联系的其他机制[5]。此外,各种介质在这一环节中的相对作用仍有待澄清。
台湾儿童健康研究(TCHS)是一项涵盖台湾不同地区的全国性人群队列研究,为纵向设计检验我们的假设提供了一个很好的机会。我们继续之前的研究[5],并假设中心性肥胖和儿童哮喘之间的联系可能是由特应性、气道炎症和肺功能不良介导的。我们还评估了每条通路的介导作用,以寻找这一联系背后最突出的病理机制。
方法
数据收集
TCHS是一项多学科的全国性纵向研究,重点关注学童的呼吸健康及其相关因素。我们在之前的研究[5]。它包括两个队列,我们的研究使用了开放队列设计的第二个队列的数据。从2010年到2012年,每年向家长分发相同的问卷,以评估儿童的呼吸健康、特应性疾病和相关混杂因素。2010年至2012年,每年4 - 6月收集家长问卷、儿童肥胖测量和肺功能测试数据。F伊诺在2012年的调查中有记录。所有参与研究的儿童均获得其父母的书面知情同意。研究方案由台湾国立台湾大学医院(台北,台湾)机构审查委员会批准(批准号:200902042R),并遵循赫尔辛基宣言中概述的原则[18]。
测量
结果
我们使用父母问卷来定义活动性哮喘和终生喘息的呼吸结局。以下两个问题用于活动性哮喘:“医生是否曾诊断您的孩子患有哮喘?”和“在过去的12个月里,您的孩子是否有呼吸困难,或者您是否观察到他或她的胸部有喘息或吹口哨的现象?”如果父母对两个问题的回答都是“是”,那么这个孩子就被归类为活动性哮喘病例。关于终生喘息的问题是“你的孩子是否经历过呼吸困难,或者你是否观察到他或她的胸部有喘息或口哨?”父母的问卷回答被用来对基线和随访调查中儿童参与者的呼吸结果进行分类。
肥胖
测量体重时,参与者穿着轻薄的衣服,不穿鞋。使用的电子秤是身体成分分析仪(ioi353;庆山市滋原医院;精度:0.1 kg)。使用壁挂式测高仪(BW-120;台湾永康市永田市)。腰和臀围测量到最接近的1毫米使用柔性胶带。使用Lange卡尺(Beta Technology, Santa Cruz, CA, USA)在双侧三头肌和腓肠肌处测量两份皮褶厚度,最接近0.5 mm。同一位研究者根据我们之前的标准化程序进行了所有测量[5]。将双侧肱三头肌和腓肠肌的平均皮褶相加,得到皮褶总数,体脂率根据先前发表的研究公式计算[19]:
特异反应性
三种特应性疾病,变应性鼻炎,特应性皮炎和特应性结膜炎,被用来代表特应性疾病。采用家长自述问卷来确定医师诊断的三种疾病的终生发生率。父母对基线和随访问卷的回答被用来对儿童参与者的特应性疾病进行分类。
气道炎症
我们使用F伊诺作为嗜酸性气道炎症的替代标志物的测量。2012年的调查使用了NIOX MINO气道炎症监测仪(Aerocrine AB, Solna, Sweden)。测量呼出一氧化氮的标准化程序是根据美国胸科学会和欧洲呼吸学会的建议制定的[188bet官网地址20.]。儿童参与者被要求吸入不含一氧化氮的空气至肺活量,然后以50 mL·s的流速呼气10 s−1。分析后,屏幕上显示出呼出的混合气体中一氧化氮的浓度。
肺功能检查
肺功能测试是根据我们之前的标准化方案进行的[21]。FEV1肺活量计获得FVC数据。FEV1计算/FVC比值。
数据分析
我们首先利用研究人群的分布,根据年龄和性别的百分位数将不同的肥胖测量分为三类(<25%,≥25 - <85%和≥85%)。在整个研究期间,为了检验肥胖测量与呼吸结果(活动性哮喘和终生喘息)之间的关系,我们采用了广义估计方程(GEE)。GEE分析使用一类估计方程,是对重复观测的广义线性模型(GLMs)的扩展[22]。GEE分析中采用的相关矩阵为有效的一阶自回归相关。GEE分析纳入了各种混杂因素,包括年龄、性别、父母教育程度、家庭收入、特应性家族史、孩子是否接受过母乳喂养以及孩子是否接触过母亲吸烟在子宫内。协变量信息缺失的受试者使用缺失指标纳入模型[23]。根据双边估计,统计显著性水平设为5%。
我们进行了一个中介分析来评估是否间接影响通过中介解释了中心性肥胖(腰臀比)和呼吸结果之间的部分关联。结构方程模型(SEM)分析,因为它是同时测试和控制多个路径的好方法[24]。此外,扫描电镜消除了在一个简单的中介模型中单独测试多个相互关联的中介时发生的估计偏差[25]。在扫描电镜中使用潜在变量来减少三次调查中重复测量产生的测量误差。我们假设中心性肥胖到呼吸结果的病理通路是由特应性、气道炎症和肺功能介导的。三项调查的腰臀比数据用于构建潜在变量“中心性肥胖”。2010-2012年调查的呼吸结果采用线性组合。对于每种特应性疾病,我们采用线性组合的方法将三次调查的数据进行组合,然后将三种特应性疾病进行组合,构建潜在变量“特应性”。数据F伊诺中介分析中使用测量值来表示“气道炎症”。FEV数据1/FVC值用于构建潜在变量“肺功能”。FEV1/FVC被选择代表肺功能,因为它与哮喘儿童的肥胖指标相关且升高F伊诺全国性大调查的水平[14]。为了建立模型,中心性肥胖与介质之间以及介质与呼吸结局之间的标准化通路系数必须达到统计学显著性。引导抽签次数设置为500次。对扫描电镜中缺失的数据采用全信息最大似然估计。每个中介的中介百分比计算为间接效应估计值除以模型总效应估计值[3.]。如果<5%,则认为标准化途径系数以及标准化总效应、直接效应和间接效应具有统计学意义。Mplus软件(版本7;使用muthsamn & muthsamn, Los Angeles, CA, USA)进行SEM分析。
为了检验混杂因素的引入是否改变了中心性肥胖与呼吸结局之间介质的显著性,我们进行了GEE和GLM分析。GEE分析用于特异反应和肺功能的介质,而GLM分析用于气道炎症的介质。GEE分析中的特应性定义为父母是否在每次调查中报告了儿童参与者的三种特应性疾病中的任何一种。GEE分析中采用的相关矩阵、调整混杂因素和缺失数据处理同前文。采用SAS软件9.2版(SAS Institute, Cary, NC, USA)进行GEE和GLM分析。根据双边估计,统计显著性水平设为5%。
结果
研究人群包括2010年的2777名四年级学生,2011年的2170名五年级学生,2012年的2311名六年级学生。活动性哮喘患病率由2010年调查的4.8%下降至2012年调查的3.5% (表1)。在为期3年的研究期间,患有终生喘息的儿童比例从14.2%到21.7%不等。在2010年的调查中,40.3%的儿童至少患有三种特应性疾病中的一种。FEV的平均值1/FVC在2010年和2012年调查中分别为90.7%和91.6%。
表2使用GEE显示肥胖测量与呼吸结果之间的关联。BMI百分位数、体脂率和腰臀比在预测活动性哮喘和终生喘息中均显示出显著的剂量-反应关系。在三种肥胖测量中,腰臀比是活动性哮喘的最佳预测指标。对于腰臀比≥85百分位的儿童受试者,活动性哮喘和终生喘息的比值比(95% CI)分别为2.07(1.36-3.15)和1.50(1.18-1.90)。与终生喘息相比,所有肥胖指标与活动性哮喘表现出更好的相关性;最近测量的肥胖指标应该更准确地反映哮喘的现状,而不是过去发生的喘息。
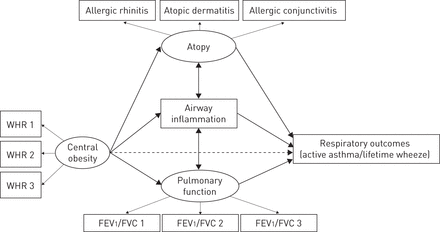
我们使用扫描电镜来研究中心性肥胖(腰臀比)与呼吸结果之间机制的中介途径。表3给出了引入介质时每个路径的标准化路径系数。特应性与气道炎症、气道炎症与肺功能呈正相关。在两种模型中,中心性肥胖与呼吸结果的直接联系都是正的,但并不显著(活动性哮喘模型和终生喘息模型的p值分别为0.06和0.16)。图1扫描电镜结果的图表是在表3。
中心性肥胖与不同介质对呼吸结果通路的结构方程模型。潜在变量被描绘成椭圆形;矩形表示指标和其他测量变量。重要的关系用大箭头表示;不重要的关系用虚线箭头表示。箭头的方向区分了预测者和结果。WHR:腰臀比;FEV1: 1 s用力呼气量;FVC:强制肺活量。
表4在扫描电镜中展示了中枢性肥胖对呼吸结果的标准化总、直接和间接影响。总效应和间接效应通过不同的中介因子在两个模型中均显著(除临界显著性外)通过终身喘息模型气道炎症,p值=0.07)。活动性哮喘模型中,肺功能、特应性和气道炎症的调解率分别为28.6%、18.1%和5.7%。间接影响通过终生喘息模型肺功能为40.2%。在两种模型中,肺功能在三种介质中所占的中介比例最大。
使用GEE和GLM分析的中心性肥胖和介质之间的关联在表5。中心性肥胖与这三种介质呈显著的剂量-反应关系。对于腰臀比≥85百分位的儿童受试者F伊诺2.58 ppb (95% CI 0.11-5.05), FEV1/FVC比对照组低1.41 (95% CI 0.87-1.95)%。使用GEE和GLM分析的介质和呼吸结果之间的关联在表6。所有三种介质均显著预测活动性哮喘和终生喘息。四分位数范围为13 ppbF伊诺FEV占8.69%1/ FVC。对于患有特应性哮喘的儿童,活动性哮喘的优势比(95% CI)为3.77(2.76-5.15)。的四分位数增长F伊诺与儿童表现出活动性哮喘的风险增加1.26(1.13-1.42)倍相关。在肺功能方面,FEV有四分之一的增加1/FVC与活动性哮喘风险降低18(3-31)%相关。
对于使用工作的非结构化相关矩阵的GEE分析,请参阅在线补充表S1, S2和S3。研究结果与《科学》杂志报道的结果相似表2,5和6。对于使用参加所有三次调查的儿童参与者的数据进行的GEE分析,没有任何缺失值,请参阅在线补充表S4, S5和S6。无论我们使用的是完整的数据集(n=1864)还是缺少指标的原始开放队列数据,变量之间的关联都没有太大差异。
讨论
据我们所知,这是第一个讨论中心性肥胖到哮喘通路的中介作用的研究。我们的研究结果表明,特应性、气道炎症和肺功能不良是中枢性肥胖和儿童哮喘之间联系的重要媒介。在这些介质中,肺功能不良是促成这一联系的最突出的病理机制。由于通过体育锻炼改善肺功能比药物治疗逆转特应性和气道炎症更有效且成本更低,因此我们的研究结果对儿童的呼吸健康具有重要意义。
在儿科研究中,较高的BMI值被发现与非特应性哮喘而非特应性哮喘相关[11]。然而,F或不等。(3.认为特应性是肥胖-哮喘关联的重要中介。在我们的研究中,我们调查了三种特应性疾病,以更好地表征“特应性”,肥胖儿童报告了更多的特应性疾病,与其他研究的结果相似[26]。我们的发现与F或不et al。研究并证明特应性显著介导中心性肥胖对哮喘的影响。中心性肥胖可能比BMI提供更多关于特应性疾病的信息。有关肥胖、特应性和哮喘的现有研究之间的差异可能由多种遗传和环境因素来解释[3.]。
F伊诺与嗜酸性而非嗜中性气道炎症高度相关[27]。嗜酸性气道炎症在肥胖-哮喘关联中很重要,因为哮喘患者的粘膜下嗜酸性粒细胞计数与BMI相关[28]。一种针对人白细胞介素(IL)-5的单克隆抗体在促进嗜酸性粒细胞的生存中起着关键作用,与哮喘严重恶化的显著减少有关[29]。旨在减少痰嗜酸性粒细胞计数的治疗策略也减少了哮喘的入院和恶化[30.]。美国一项针对儿童的大型横断面研究表明,肥胖与高血压儿童哮喘控制不良有关F伊诺水平(14]。本研究采用腰臀比,发现气道炎症是中枢性肥胖与哮喘之间的显著中介,但中介作用较小。这可能是因为肥胖相关的全身性炎症不会直接增强气道炎症[31,32]。值得注意的是,在我们的研究中,气道炎症与特应性和肺功能相关(表3和图1),这些发现与其他关于儿童的报告一致[33,34]。我们认为,特应性、气道炎症和肺功能可能协同作用,导致中心性肥胖儿童哮喘症状。
众所周知,肥胖会降低患有或不患有哮喘的受试者的肺功能。在女性哮喘患者中,BMI越高,动态恶性通货膨胀的影响越大[35]。随着年代马和Fredberg(36指出,肥胖通过支气管扩张受损、气道重塑加速和肺生长受损等机制影响肺功能。我们之前的研究也证实了肺功能在中枢性肥胖和哮喘之间的关联中的作用[5]。我们在扫描电镜分析中将呼吸结果与肺功能互换,以测试哮喘是否介导肥胖对肺功能的影响。然而,新模型的适应度信息比我们的原始模型差(在线补充表S7)。因此,我们认为哮喘不太可能是中心性肥胖和肺功能之间的中介。此外,我们的研究首次证明了肺功能在中枢性肥胖和哮喘之间的关联中的中介作用大于特应性和气道炎症。我们的分析还显示,肺功能对终生喘息的影响大于对活动性哮喘的影响。先前的纵向研究已经证明,这可能是因为早期患有喘息或哮喘的儿童在以后的生活中表现出进行性肺功能缺陷[37,38]。在我们的研究中,在2010年的调查中没有终生喘息,但在2012年的调查中回答“是”的参与者与从未有过喘息的人相比,肺功能更差(在线补充表S8)。因此,肺功能对终生喘息的更大影响可能是由于肺功能缺陷持续时间延长所致。我们的研究结果表明,肥胖儿童应该尽早开始体育训练,以减轻肥胖和肺功能的恶化。
关于中枢性肥胖和哮喘之间可能的分子机制,一些研究已经显示出有希望的结果。瘦素是一种由脂肪组织产生的促炎脂肪因子,其水平在肥胖中增加。G的一项研究ul等。(39证实了哮喘患儿血清瘦素浓度与IgE水平呈正相关。在哮喘小鼠模型中,内脏体脂肪的积累通过产生IgE和IL-5来降低过敏致敏性。肥胖也会促进嗜酸性粒细胞引起的过敏性气道炎症。这些发现解释了肥胖在儿童哮喘过敏相关病例中的关键作用[40]。几丁质酶-3样1 (CHI3L1)是一种已知与人类躯干肥胖呈正相关的几丁质酶样蛋白。在肥胖哮喘患者中,发现血清CHI3L1水平与肺功能不良有关[41]。
我们研究的主要优势是重复测量和社区队列的大样本量。大部分数据是连续3年每年收集一次。我们将终生喘息作为主要结果之一,因为“至少一次喘息”在儿童中比哮喘诊断更常见,因此确定了更多肺功能受损的患者[42]。此外,我们在两种不同的统计模型中获得了相似的结果,两种不同的呼吸结果,这使我们的解释更加可靠。
我们的研究受到儿童特应性疾病和呼吸结果的问卷调查的限制;然而,父母们,他们足够成熟,可以提供最准确的回答问卷。我们还使用了关于医生诊断的特应性疾病和客观测量的问题,以避免可能的分类偏差。上的数据F伊诺仅限于2012年的调查。然而,在我们的分析中,气道炎症的影响是显著的,不能忽视。另一个限制是我们在研究中没有评估青春期。然而,我们在GEE模型中使用年龄作为青春期分期的代理,结果对于每个途径都是显著的。
综上所述,与特应性和气道炎症相比,肺功能下降是中心性肥胖到儿童哮喘最突出的病理机制。鉴于肥胖和哮喘的巨大负担,我们的研究结果对疾病预防政策具有重要意义。应对肥胖儿童进行肺功能筛查,以预测哮喘风险。改善肺功能是预防中心性肥胖相关哮喘的最佳策略。
致谢
我们要感谢参与这项研究的孩子和家长。我们也要感谢台湾儿童健康研究小组成员(国立台湾大学公共卫生学院,台北,台湾)协助收集队列数据。
脚注
本文的补充资料来自www.qdcxjkg.com
支持声明:本研究得到台湾国家科学委员会基金#98-2314-B-002-138-MY3和#96-2314-B-006-053的支持。
利益冲突:没有声明。
- 收到了2015年6月18日。
- 接受2016年4月1日。
- 版权所有©ERS 2016