抽象的
Interleukin-1 alpha released by airway epithelial cells may instruct fibroblasts to become pro-inflammatory in COPDhttp:///wly/clyk301tyoj.
The lungs are continuously exposed to inhaled particles and irritants. Tobacco smoking is the leading cause of several airway diseases, including lung cancer, idiopathic pulmonary fibrosis and chronic obstructive pulmonary disease (COPD). In COPD, repeated exposure to cigarette smoke induces chronic inflammation and structural remodelling of the airways, with peribronchial fibrosis and epithelial-to-mesenchymal transition [1],导致(主要是不可逆转的)气道阻塞。因此,对有毒气体的异常气道反应可能是由异常信号传导和上皮,间充质和免疫细胞之间的串扰产生的。
在这个问题中E.uropean Respiratory Journal那O.SEI.等等。[2[通过白细胞介素(IL)-1α,描述上皮细胞信号如何通过白细胞介素(IL)-1α来成纤维细胞。使用人原发性细胞的共培养物(支气管上皮细胞(BECS)和肺成纤维细胞)和人细胞系(MRC5胎儿成纤维细胞和16HBE上皮细胞),该作者表明BECS和成纤维细胞的共同培养诱导热休克的产生蛋白质(HSP)70,IL-8 / CXCL8和IL-1β通过肺成纤维细胞,同时降低α-平滑肌肌动蛋白的表达,转化生长因子(TGF)-β1和细胞外基质蛋白。通过使用BEC(16HBE) - 调节培养基重新携带的这些效果在对照和COPD衍生的细胞之间进行综合,表明可溶性因子的要求。使用中和抗体,作者继续证明CXCL8和HSP70通过共培养系统的成纤维细胞释放与IL-1β和前列腺素E2无关,但依赖于IL-1α。此外,通过暴露于香烟烟雾提取物,在COPD衍生细胞中增强了IL-1α释放。虽然这一点体外模型可能无法完全重新承载体内情况,它为呼吸道上皮细胞和调节间充质细胞提供的信号提供了重要的新见解。
There is accumulating evidence that BECs are key cells in frontline defence that directly signal to immune cells, in particular antigen-presenting cells [3.那4.]。以前的几种作品确定了赋予病原体从事免疫应答的形状[5.]。For instance, BECs exposed toKlebsiella肺炎特别是通过作用于骨髓树突细胞网络来调节局部免疫应答[6.]。R.espiratory syncytial virus-infected BECs regulate CD8+T细胞活化和抗病毒活性,根据“检查点”免疫受体PD-L1的上皮表达的变化[7.]。BECS还调节树突细胞分化和成熟以及对脂多糖的反应性[8.]并抑制T细胞召回普遍航空理体的反应,以确保粘膜稳态和抑制过敏反应[9.]。它还以哮喘显示,BECS可以通过肺部肥大细胞抑制组成型和IgE依赖的组胺释放[10],进一步突出上皮对感应和成型粘膜危险信号传导的核心作用。我们最近表明,来自COPD患者的BEC也将B细胞印记促进促进成熟成产生IGA的血浆细胞,而香烟烟雾部分抵消这种IGA促进效果[11]。This effect was at least partly related to an intrinsic ability of COPD BECs to produce increased amounts of certain cytokines (IL-6 and BAFF; B-cell activating factor) and to induce B-cell expression of TACI (transmembrane activator and CAML interactor). OSEI.等等。[2[还介绍了内在的上皮改变,表明与来自对照的细胞相比,来自COPD患者的BECS在FECS患者中观察到对香烟烟雾提取物的扩增IL-1α反应。
站在环境和宿主组织之间的界面处,先天免疫系统可以通过几种模式识别受体(PRRS)来与病原体相关的分子模式(PAMP),即含量的受体(TLRS),NOD样受体,蛋白质激活的受体和钻机样受体。这些受体的结扎触发了通过释放上皮细胞因子引发的免疫应答,包括IL-6,胸腺基质淋巴促蛋白(TSLP),IL-25和IL-33 [12]。Upstream of these cytokines, the activation of NOD-like receptor family, pyrin domain containing 3 (NLRP3) inflammasome leads to the release of IL-1α, IL-1β and IL-18, acting as pyrogens and T-cell activators. Activated epithelial cells secrete pro-IL-1β that is cleaved by caspase-1 to produce bioactive IL-1β [13.]。尽管最近有证据表明NLRP3炎性在哮喘,COPD和特发性肺纤维化中的参与,及其与IL-1β和NLRP3炎症的密切关系,但IL-1α在呼吸系统中的作用长期被忽视。当发现IL-1组成的两个不同蛋白质组成时,1985年描述了IL-1α[14.]。来自COPD患者的肺样本和暴露于香烟烟雾的小鼠的研究作为COPD的实验模型表达IL-1α的表达增加[15.-17.],其介导小鼠模型中嗜中性粒细胞和树突细胞的积累。然而,IL-1α表达主要是局部归入血吸虫巨噬细胞[17.那18.] and not to epithelial cells. In asthma, Willart.等等。[19.[证明,通过蛋白水解过敏原的上皮激活触发IL-1α的释放,它通过自分泌IL-1受体结扎诱导Pro-Th2细胞因子通过BEC释放,最终促进Th2-偏置的免疫应答。
O.SEI.等等。[2] went one step further by providing evidence of a key role for IL-1α in mediating epithelial signalling to fibroblasts. They showed that IL-1α switches on a differentiation programme in fibroblasts towards an inflammatory phenotype (with increased hsp70 and IL-8/CXCL8, and to some extent IL-6), while abrogating their production of matrix proteins. S乌瓦拉等等。[20最近表明,人肺纤维毒素也在与受损的血液培养后切换炎症成纤维细胞,从而增加其抗IL-1α废除的IL-8 / CXCL8,MCP-1和IL-6的释放或抗-iIL-1RA,但不是抗IL-1β,抗体。通过核因子κB信号传导伴随TLR3的激活来突出纤维毒素的炎症表型。此外,在IL-1α中注意到降低的胶原沉积- / -and IL-1R1- / -博莱霉素暴露后的小鼠。找到oSEI.等等。[2],IE。在IL-1α激活时减少了基质蛋白的合成,挑战IL-1α的这种视图作为平面介质。因此,IL-1α是否参与在COPD中观察到的小导电气道或泛刺激纤维化[21] remains unclear. In cancer, BAE.等等。[22[表明,IL-1α可以通过CCL7,CXCL1和IL-8 / CXCL8趋化因子的分泌增强口腔鳞癌相关的成纤维细胞增殖。
上皮和间充质细胞之间的相互作用在分支形态发生和肺部发育过程中是至关重要的,并且包括在成人肺部的几个方面,包括动态转变状态(上皮 - 间充质和间充质和上皮过渡)和旁静脉调节。在哮喘中,IL-4 / IL-13激活BEC释放TGF-β2,又刺激肌纤维细胞转化和基质蛋白的分泌和血管丝率(例如vascular endothelial growth factor, endothelin-1) [23.],leading to the concept of “epithelial-mesenchymal trophic unit”. This epithelial-mesenchymal signalling pathway should be further explored in chronic airway diseases such as COPD [24.]特别是通过使用由O进行的主要细胞使用多细胞培养模型SEI.等等。[2]。
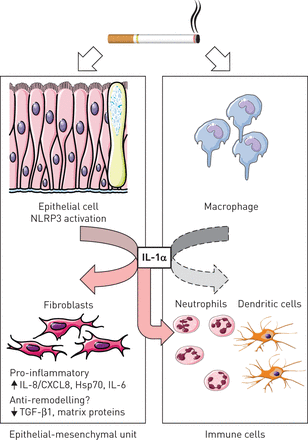
完全是,这项工作说明了通过卷烟烟雾的卷烟烟雾重复支气管上皮损伤(其仍然很大程度上),可能引发慢性炎症组的慢性炎症细胞的改变编程,包括释放IL-1α(figure 1)。然而,这种细胞因子可能通过指示成纤维细胞的促炎炎症编程有助于持续的中性粒细胞的积累,并且仍有待确定在多大程度上,它还有助于改变人类COPD肺的气道中的修复响应和基质沉积。COPD中的额外难度是在不同气道水平的基质周转的相同特征中的同一疾病中的关联,即一些导电气道(虽然其他一些小型气道可能消失)和基质破坏的肺部,或者甚至在肺气肿纤维化表型中相邻的肺泡区之间[25.]。然而,上皮成纤维细胞途径的操纵应该有助于开发新的治疗策略,最近试图靶向COPD中的炎症[26.] might open the way to new biotherapies in severe chronic obstructive lung disease.
脚注
利益冲突:没有宣布。
- R.eceived2016年6月15日。
- 公认2016年6月15日。
- 复制right ©ERS 2016