摘要
计算机断层扫描(CT)是对胸部和肺结构进行成像的选择的模式。在慢性阻塞性肺病(COPD)中,它用于识别肺气肿,支气管壁增厚和气体捕获的关键形态特征。尽管如此,它在调查和管理COPD的地方尚未确定,并且不常规建议。然而,肺癌已经具有重要的临床应用,可以用于诊断伴随病理学并确定哪些严重肺气肿的患者适用于肺粪积减少程序。此外,新的定量分析技术允许客观测量疾病的肺和肺肺表现。这些技术可以对COPD提供重要的见解,并有助于探索条件的异质性和潜在机制。及时,希望这些技术可用于临床试验,以帮助发展疾病特异性治疗,并最终是鉴定将从新的和现有治疗中受益的患者的临床工具。本综述讨论了CT成像在COPD和定量技术中CT成像的当前临床应用,其在分层疾病中的潜在未来作用是最佳结果。
摘要
CT成像在评估COPD中发挥重要态度和迅速发展的作用http://ow.ly/ZREg3
介绍
计算机断层扫描(CT)自20世纪70年代问世以来,已经给医学成像带来了革命性的变化。它能够提供肺和胸部的详细图像,这使得它成为呼吸医学的一种选择的成像方式,它已经成为评估和管理许多肺部疾病患者的重要工具。
在慢性阻塞性肺疾病(COPD)中,CT可以通过对气流限制进行直接促进定义条件的病态变化进行图像[1].依赖肺活量指标来诊断和描述疾病限制了我们对COPD的理解和对该疾病的个体化临床管理。慢性阻塞性肺病是一种复杂的、异质性的疾病,具有不同的临床特征,包括许多不同的表型。临床表型的起源、疾病过程与内型的关联以及个体间异质性的驱动因素尚未得到充分探索,这可能对理解疾病进展和未来对该疾病的管理具有重要意义[2].目前还没有针对慢性阻塞性肺病的有效的疾病改善药物,在其他慢性疾病中也没有看到疗效的改善。除了肺活量测定外,还需要其他工具来帮助解释异质性,并为研究和治疗COPD的方法提供进一步的见解。CT目前在疾病的常规管理和调查中有实际应用,随着新型分析技术的发展,有可能提供关于COPD肺和肺外表现的进一步细节。
CT在当前临床实践中的应用
20世纪70年代以前,组织学和事后剖析需要研究肺的结构变化。CT的引入使胸部可视化和无创评估肺结构成为可能。在COPD中,CT可以识别关键的形态特征,包括肺气肿、支气管壁增厚和气体捕获。这些病理直接导致了气流阻塞,因此,CT有可能为COPD的潜在病理生理变化提供重要的见解。尽管如此,常规CT成像不一定在临床实践中得到广泛应用,其在COPD管理和调查中的地位尚未确立。慢性阻塞性肺疾病全球倡议(GOLD)战略并不定期建议对慢性阻塞性肺疾病进行CT扫描,只建议CT扫描可能有助于鉴别诊断或正在考虑手术选择[3.].一项关于英国呼吸内科医生和外科医生态度的研究强调了这种普遍的矛盾心理,其中只有32%的人认为严重COPD患者有必要进行CT扫描[4.].
CT的使用没有成为COPD的常规有很多原因。其中最重要的一个概念是使用CT不会改变治疗,尽管严格来说并不正确。NETT(国家肺气肿治疗试验)表明,晚期上叶肺气肿和有限的运动能力患者在肺减容量手术后得到改善[5.].在使用支气管内治疗严重肺气肿方面也有相当大的进展和经验,包括线圈、瓣膜、密封剂和气道旁路。在重度异质性肺气肿的正确患者中,这些治疗可导致肺生理和功能能力的显著改善[6.那7.].CT成像还可以识别大疱性疾病,可以接受手术治疗,大疱切除术可以改善健康状况[8.].因此,似乎很清楚,严重COPD的患者需要CT成像来确定哪些患者适用于这些技术。
CT成像也可以发现COPD伴随的肺病理。支气管扩张尤其普遍,研究表明50%的COPD患者有CT证据表明该疾病[9.-11.].当存在时,支气管扩张与更差的气流阻塞有关[11.,加重病情[9.那11.,较高的气道及全身炎症[9.-11.],以及较高的死亡率[9.].COPD也是肺癌的独立危险因素[12.[较高的癌症率与恶化的气流阻塞有关[13.那14.]和肺气肿[15.那16.].纤维化变化也被证明在COPD中是常见的,似乎达到了差的预测[17.].此外,由于过度膨胀和纤维化的相反作用可能使肺生理恢复正常,因此很难诊断。由于这些伴随的病变是常见的,通常与较差的结果相关,并需要改变管理,使用CT成像来发现它们是至关重要的。
对COP在COPD中的常规使用的主要限制是主观的报告,使得难以解释结果并指导管理计划或对疾病进行见解。目标方法已针对关键疾病方面提供数值数据。最初,开发了简单的视觉评分系统,在量化疾病时表现出早期的承诺。这些技术无法检测到微妙的疾病,并且易于内部和interobserver误差,以及对纵向变化不敏感。为了解决这些问题,已经开发了自动定量分析技术,其能够从胸壁和周围结构分段肺部实质和气道。早期软件分析二维轴向切片,但加上CT技术的进步,存在一系列不同的分析软件,允许体积重建(图1).这就提出了定量CT分析可以用来更详细地了解疾病和表型的前景,这篇综述的其余部分将对此进行讨论。
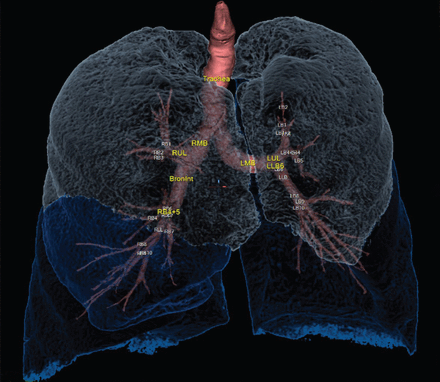
使用Apollo软件(Vida Diageostics Inc.,Coralville,Ia,USA)的支气管树和肺实质的体积计算断层扫描重建。
肺气肿
传统上,肺气肿是一种组织学诊断,定义为终末细支气管远端气腔的异常永久性扩大,并伴有肺泡壁的破坏。在CT上可以发现肺气肿的改变,1978年,Rosenblum等等。[18.]描述了COPD临床诊断患者肺衰减和平均肺密度的区域。
提供关于肺气肿,G的数字数据oddard等等。[19.]开发了一种可视化的肺气肿评分系统,通过估计轴向CT切片上的肺气肿数量,该系统显示出与气流阻塞和组织学标本密切相关[20.-22.].开发了自动化技术以分割肺实质并定量肺气肿。两种主要技术都使用蓄电区由CT上的低衰减区域表示的原理。第一称为CT密度测定法涉及将密度掩模施加到肺实质上并在下面的阈值设定所有体素被假设肺气肿,得到低衰减百分比(%LAA)(图2).最初,使用了−910 HU的阈值,这表明与肺气肿的病理测量有很强的相关性[23.].随后,%laa -950 hu以下(%laa<-950)与微观和宏观肺气肿都有最强的相关性[24.-27.,导致人们普遍采用这一门槛。第二种方法,称为百分位数密度测定法,涉及在衰减分布曲线中选择一个阈值百分位数,它以亨斯菲尔德单位提供密度值,在该单位下,体素的百分比分布。一些不同的阈值在1%和18%之间被使用,并与组织学标本的显微镜下肺气肿密切相关[27.].根据α的一些研究,最常用的阈值是15%1抗胰蛋白酶缺乏症(α1-ATD)[28.-30.].对于这些方法中哪一种是最好的仍然没有明确的共识,即使是现在,不同的研究使用不同的阈值。考虑到肺气肿是一种全有或全无的现象,使用CT密度测量法似乎更直观,它使用一个绝对的界限来量化它。
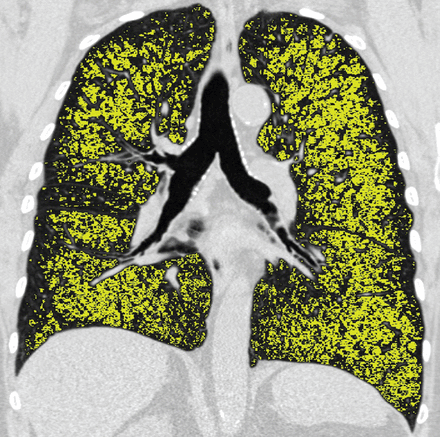
胸部计算断层扫描的冠状重建显示低衰减区域-950胡。
研究证实,CT密度测定显示慢性阻塞性肺病患者的肺气肿水平高于健康吸烟者[31.-34.].也有令人信服的证据表明,CT密度测定与气流阻塞有很强的相关性[10.那32.-41.],对4000多张copd基因研究的CT扫描分析显示,%LAA之间存在很强的负相关<-9501秒用力呼气量(FEV)1),随着GOLD严重程度的恶化,肺气肿加重[33.].CT密度测定法也与气体转移(一氧化碳的肺转移因子)有很强的相关性[10.那35.-40,步行6分钟即可到达[32.那36.那40那42.],BODE(体重指数,梗阻,呼吸困难,运动能力)得分[36.那39.那43.-45.]及身体组成[37.那39.那46.那47.].
这些密度测定技术没有考虑到疾病的分布或不同亚型,这可能具有重要的意义。肺气肿并不以一种统一的方式影响肺,目前还不清楚它如何影响疾病的临床表现。如前所述,在确定哪些患者能从肺减容手术中获益方面,它已被证明是临床重要的[5.].一项小型研究发现,肺中央区和上部区域的LAA %较高[48.].有趣的是,在中部和下部地区,气流限制与LAA的相关性最好,并且发现更均匀的肺气肿与更严重的气流阻塞相关。其他研究表明同质性肺气肿患者的肺功能加速下降[49.]那些具有更多上部区域肺气肿的人[50].随着定量CT分析的进步,可以评估疾病的洛洛叶变异,并发现了裂片之间的肺气肿数量的显着差异[51那52].
基于二次肺叶片内的分布,在组织学研究中描述了三种不同的肺气肿模式:中央管,胰腺和探针肺气肿。CT成像可以可视化这些不同的亚型。使用视觉评分系统的一项研究发现,中心肺气肿是最常见的亚型,但超过一半的肺气肿患者有多个亚型[53].一种被称为基于局部直方图的肺气肿模式的自动化方法,包括将肺划分成小方块,并分析每个方块中存在的肺气肿亚型。这比%LAA更能预测肺功能<-950[54].
这些数据表明CT密度测量和其他方法能够准确量化肺气肿及其与疾病的生理标志物的关系。为了验证CT成像作为疾病的生物标志物,有必要将其与潜在的疾病机制和预后指标进行比较,并跟踪纵向变化。CT密度测量已经发现与COPD患者的死亡率相关[55]和GenKOLS试验的分析[56]发现,%LAA对呼吸和心脏死亡率的预测价值高于GOLD分期。CT上的肺气肿改变也与更高的加重率相关[57-59]及因病情恶化而增加的死亡率[59].
CT成像的一个潜在的重要应用是跟踪肺气肿随时间的变化,并看看它是如何导致功能下降的。直到最近,这些研究大部分是在α患者中进行的1-ATD并表明CT密度测定可以精确地检测肺气肿的进展[60-63],并与肺功能下降有关[29.那60].此外,CT肺密度参数在检测疾病进展方面比传统肺功能更敏感[60因此,已被认为是α治疗效果前瞻性研究的主要终点1-ATD。在COPD中,已经证明CT上肺气肿量较高的患者FEV下降速度增加1[34.那50].CT肺气肿进展也与频繁发作相关[64]和当前的吸烟状态[65].迄今为止最大的纵向研究评估了慢性阻塞性肺病纵向评估以确定预测性替代终点(ECLIPSE)队列的CT扫描[66],发现肺密度和低衰减区逐年递增。然而,受试者之间存在显著差异,这与肺功能没有令人信服的相关性。
在将肺气肿的CT措施与疾病标志物进行比较时,必须考虑我们对这些机制的了解是不精确的。顽育的变化已经与各种基质金属蛋白酶(MMP)有关[31.那67-69]以及痰中中性粒细胞升高[70]和嗜酸性粒细胞[39.那71].许多气道炎性细胞因子,如白细胞介素-8,白酮-B4.和myeloperoxidase,已与肺气肿进展有关[39.那72那73],肺气肿也与血清纤维蛋白原升高有关[74].一些研究将新型生物标志物与肺气肿联系在一起,在ECLIPSE队列中,表面活性剂蛋白D和可溶性RAGE(晚期糖基化终末产物受体)都与肺密度测定的下降有关[66].对细菌定植和肺气肿有点令人着重;但是,B.AFADHEL.等等。[75]没有发现在CT和那些没有的人的患者之间的细菌文化差异。
总之,气体测量相对简单,并且可以用最小的用户干预来执行。CT密度测定与许多生理和临床参数有关。然而,需要进一步的工作来评估肺气肿分布和亚型,并评估肺气肿的纵向变化,以及疾病和疾病机制的结果标志性的关系。
支气管壁测量
气道壁重塑是COPD的一个重要特征,组织学标本证实了整个支气管树的气道壁增厚[76那77].CT分辨率有限,只能直接显示大中型气道。呼吸道的早期测量依赖于人工追踪[78];然而,已经开发了许多自动化的方法。其中之一就是使用“半最大值下的全宽度”原则(图3),使用CT衰减值来通过从气道中心投射光线来识别内部和外部气道壁。这些和其他算法已经精制,并且使用区域越来越多的方法,现在可以生成支气管树的三维重建到第五或第六代气道。可以从这些重建中测量多个气道尺寸,包括支气管壁厚,壁面积,腔面积,总气道区域,壁面积百分比(%WA)和内部周边(P.一世)(图4).一个标准化的参数叫做P.一世10.已经发展出一种预测内周长为10毫米的假设气道壁面积的平方根的方法。
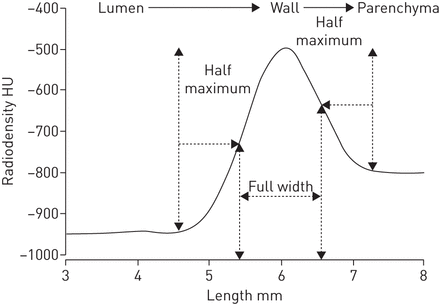
用于确定气道墙尺寸的半最大方法的全宽。
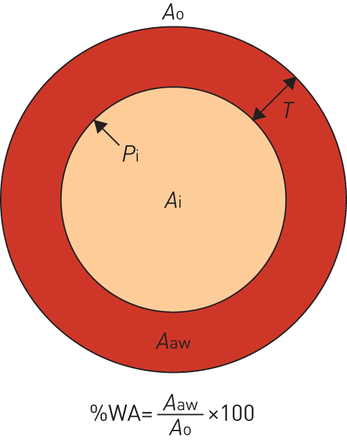
气道壁维度。一种亚历山大-伍尔兹:气道壁面积;T.: 室壁厚度;一种O.:总气道;一种一世:内部区域;P.一世:内部周边;%wa:百分比墙区域。
早期研究发现,CT中CT上增厚的支气管壁的标记增加[46.那79-81].然而,最近的研究表明,呼吸道壁和腔尺寸在COPD中减少,虽然更加成比例地,但导致较大的%WA [33.那79那82].这些差异的原因尚不清楚,尽管后来的研究倾向于对支气管树进行更完整的测量,并在空间上与气道匹配。如果不这样做,在慢性阻塞性肺病患者中,可能会无意中选择更近的气道,因为这些气道壁更厚。这突出了目前测量气道的困难,变量的数量带来了巨大的挑战,显然需要进一步的研究。
考虑到上述限制,测量支气管壁厚度增加与FEV有关1[41.那81那83那84这是更强的远端气道[41.].支气管壁标记还与孔指数形式的功能标记相关[44.那45.],运动能力[32.那36.]及身体组成[46.].尽管这些关联在统计上很重要,但它们中的许多往往是相当弱的。在GenKOLS的研究中,死亡率一般不会随着增加而增加P.一世10.但在严重肺气肿的亚组中,P.一世10.与死亡率有关[56].另一项研究表明,增加的支气管壁尺寸与加剧的死亡率有关[59].据推测,增加的支气管壁厚度是气道炎症的标志,因此可能与慢性支气管炎的症状或频繁的恶化有关。H一个等等。[57[通过表明在频繁的恶化者频繁的情况下,虽然另一项研究未能找到此协会[58].这些指标也显示了慢性支气管炎的症状[84那85].虽然B,但少数研究研究了支气管壁增稠和痰炎症标记物或细菌培养物的CT标记之间的联系AFADHEL.等等。[75并没有发现任何关联。
简单地测量支气管壁厚度的指标可能不足以描述COPD中发生的气道重塑。因此,已经开发了其他方法,其中一种使用峰壁衰减,这是一种可能反映气道壁增厚和密度的标记。这已被证明与FEV呈负相关1[41.那86].
评估气道尺寸随时间变化的工作量很小。一项小型研究观察了一年一次扫描之间的下叶段气道变化,虽然发现了每年的WA %和FEV变化之间的相关性,但没有发现显著差异1衰退 [87].支气管壁厚度的区域性差异尚未得到系统分析。O.哈拉等等。[88]没有发现顶瓣节段支气管和下瓣节段支气管之间的任何差异。
从理论上讲,CT应该是评估大型和中型气道的形态的有用工具。然而,关于这项技术和测量仍有许多不确定性,并且没有明确的证据表明这是COPD中特别有用的工具。
气道疾病
小气道是COPD中气流阻塞的主要原因[77,组织学研究证实上皮上皮化生、杯状细胞增生和支气管周围纤维化。目前还没有测量这种小气道疾病的黄金标准,因此需要更好的方法,在这一领域的大量研究正在进行。CT不能直接成像小气道,因为它们超出了最大分辨率。气体捕获的间接标志可以作为替代标记,定义为呼气后体积没有减少,在呼气CT上被视为低衰减区域。
已经开发了许多量化方法来测量气体捕获,其中最简单的方法包括计算−856 HU以下的体素数量或呼气CT上的平均肺密度(MLD)。这些方法不补偿肺气肿的数量,因此,实际上,将是气体捕获和肺气肿的综合评分。为了纠正这个问题,已经开发了使用成对吸气和呼气扫描的技术,其中包括使用呼气和吸气时MLD的比例。matsuoka等等。[89]开发了一种更复杂的技术,利用吸气和呼气扫描之间的- 856和- 950 HU之间的相对体积变化。这在一项36例患者的研究中得到验证,并发现与肺功能测试的气体捕获标记物有很强的相关性,优于上述其他方法。当将这些技术与单呼吸氮气洗脱技术进行比较时,呼气-吸气MLD比表现最佳[90].一项针对COPDgene受试者的气体捕获的大型试验发现,在严重肺气肿患者中,配对(吸气和呼气)样本比仅使用呼气扫描更能预测肺功能[91].因此,通过配对吸气/呼气扫描来排除肺气肿的CT标记物似乎是合乎逻辑的。
大多数研究气体捕获只是简单地把它与疾病的生理参数联系在一起,而它已经被发现与FEV相关1及其他肺功能参数[31.-33.那36.那38.那92-94],随着黄金地位的恶化[32.那92].很少有研究探讨CT上的气体捕获与疾病的潜在机制之间的联系。我们的研究表明,小气道疾病的CT标记物与许多MMPs (MMP-3、MMP-7、MMP-8、MMP-9、MMP-10和MMP-12)相关,表明这些在COPD小气道重塑中发挥了关键作用[31.].气体积聚在肺部的纵向变化和分布尚不清楚。最近,研究小气道疾病的新型CT方法被开发出来,称为参数响应映射(PRM),它涉及共记录吸气和呼气扫描,以便进行体素逐体素比较(图5)[95].这允许测定肺气肿和功能性小气道疾病,并已被证明对亚组患者有效,这与肺功能检测相关。在copd基因队列中测量的功能性小气道疾病与FEV下降独立相关1较温和患者的情况特别是这种情况[96].这和其他类似的技术提供了表征疾病表型的机会,并且有可能监测疾病状态,因此正在进行大量的研究。
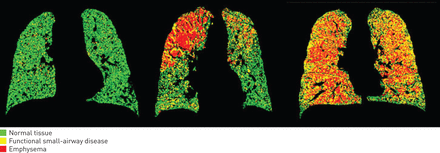
三个人的计算机断层扫描的参数响应映射。摘自[95),并得到出版商的许可。
总之,使用配对的吸气和呼气扫描,CT成像可以有效地测量气体捕获,尽管尚未定义了最佳方法。虽然它确实表现出强大的肺功能措施,所以存在有效问题是关于气道疾病的替代标志性的替代症状。需要进一步的工作,以了解疾病的潜在机制如何与气体捕获以及该参数是否反映随时间随时间的肺功能变化。
其他肺部形态特征
除了以上讨论的肺特征外,已经有了定量分析的努力。一种用于支气管扩张的自动化方法已经开发出来,其中气道内径与相邻血管直径的比例可以被量化[97].这表明支气管扩张的负担随着气流阻塞的增加而增加,并与加重有关。需要进一步的工作来改进和自动化这项技术。
使用CT测量的肺密度也有兴趣作为肺炎症的标志物。目前吸烟者的肺密度增加了增加,而不是从未/出吸烟者[98-100.],并与更大的吸烟历史有关[99那100.和支气管肺泡灌洗的炎症细胞[98].有趣的是,在纵向研究中,吸烟后肺密度减少[100.暗示吸烟导致肺部密度增加,可能是通过肺炎症的增加。这可能证明是在COPD中发生的结构变化之前评估早期肺病的潜在工具。
肺血管成像是一种活跃的研究领域,因为COPD肺血管疾病很好地描述,并且是死亡率的显着预测因子[101.-103.].肺动脉内径以及肺动脉内径与主动脉内径的比值与肺动脉压力的直接测量有关[104.]更高的恶化率[105.].CT上的小型肺血管的横截面积与侵入措施强烈相关[106.].一种自动分割和创建肺部血管的三维模型的技术已经开发出来,允许计算血容量[107.]具有更多肺气肿的受试者血容量较少。需要进一步的工作来证明这一点的临床效用。
肺外表现
COPD具有多种系统性表现形式,胸部的CT能够捕获一些这些信息。COPD中的恶病症和骨骼肌浪费是COPD中的重大问题,体重指数(BMI)与气流梗阻,疾病严重程度和死亡率有关[108.那109.].越来越多的人认识到身体组成的其他标志,如无脂肪质量指数(FFMI),可能更重要,因为它们是骨骼肌功能障碍的更好标志。FFMI已被证明是独立于脂肪量或BMI的死亡率预测因子[110.那111.].CT评估胸肌面积的技术显示COPD患者的肌肉面积明显减少与健康控制,并与GOLD分期相关[112.].这也与疾病的功能标记物有关,包括BODE指数、MRC(医学研究委员会)呼吸困难评分和6MWD [112.].各种脂肪室也可以被评估,包括前胸壁皮下脂肪和腹腔内脂肪,它们已经显示出一些临床相关性。这些方法都是相对粗糙的,仍然需要大量的用户输入。
骨质疏松症在COPD中也很常见[113.骨矿物质密度已被确认与气流阻塞独立相关[114.那115.].椎体衰减值可通过CT测量,并与双能x线骨密度相关[116.],并且还显示了与气流阻塞的关联[117.]及恶化率[118.].
使用CT来定义COPD中的表型
COPD研究的一个主要目的是定义有临床意义的表型,孤立地测量形态变化并没有真正的帮助。需要结合所有这些形态特征的更复杂的分析。一项研究将患者分为三个亚组:A表型有轻微肺气肿,E表型有肺气肿且没有支气管壁增厚,M表型两者都有。一种表型与较高的BMI、出现呼吸困难症状的年龄更大、吸烟暴露的包年更少和肺功能更好有关。A和M的可逆性更强,痰中嗜酸性粒细胞也更高。在另一项研究中,患者被分为以肺气肿为主和以气道为主的两组[57,肺气肿患者FEV较低1,功能受限程度更高,BODE评分较高,BMI较低。Castaldi.等等。[119.]对copd基因队列进行聚类分析,并结合定量CT分析。他们成功地将受试者分成四组,每组都有各自的属性。其他研究也基于CT扫描的肺气肿改变和支气管壁增厚对受试者进行了聚集[120.].这些表型方法的临床应用迄今尚未得到证实。
其他成像方式
尽管CT是提供肺结构图像的首选成像方式,但其主要缺点之一是不能提供功能图像。然而,CT可以与其他成像方式结合,为COPD患者提供功能性数据。正电子发射断层扫描(PET)-CT和单光子计算机断层扫描(SPECT)是结合了放射性同位素和CT成像的核医学扫描,允许功能和分子成像研究与解剖共配准。小分子、多肽或蛋白质由放射原子标记,放射出高能光子,可被PET或SPECT检测到。pet - ct机的,18.F-氟二甲氧氧葡萄糖(FDG)是最常用的放射性标记;它由代谢活性组织溶解,可以用作肺使炎症的标志物。COPD中的摄取显着增加[121.],并与FEV有关1及肺气肿严重程度[121.那122.].通过SPECT,可以用血管或吸入的示踪剂进行灌注和通风成像。
磁共振成像(MRI)是另一种可以提供COPD中肺部功能图像的模态[123.那124.].在使用磁共振对肺部图像进行图像的许多挑战,包括低浓度的质子,多个空气组织界面和相对较差的空间分辨率。直到最近,主要的肺应用是使用对比度增强的成像来评估肺脉管系统。技术的进步,特别是使用氧气增强或超极化的惰性气体来增加信号,允许通风的功能成像,并在COPD中显示通风缺陷[125.].一些研究使功能性MRI与CT上观察到的结构图像组合。一种这样的研究评估了肺部微血管血流量,发现它在COPD中降低,与催眠变化程度有关[126.].另一项研究将MRI测量的通气和灌注缺陷与CT测量的肺气肿和小气道疾病的PRM测量进行了比较。通气缺陷与肺气肿和小气道疾病相关,在气体诱捕区扩散测量值显著升高[127.].磁共振技术仍处于早期发展阶段,但它确实比CT具有优势,因为它可以实现功能性成像,而且更重要的是,它没有辐射。尽管如此,磁共振仍然受到可用性、成本、所需图像分析的复杂性和相对较差的空间分辨率的限制。
未来使用CT在研究和管理中
需要进一步的工作来确认定量CT分析作为疾病的成像生物标志物,这些疾病的成像生物标志物可以实际用于管理COPD患者,并作为一种有用的研究工具,以便在疾病中洞察洞察力。从技术角度来看,CT协议需要标准化为辐射剂量,切片厚度和重建算法可以所有效果分析。用于量化各种形态特征的方法需要优化,尤其是气道测量和气体捕获的情况。可能需要更复杂的工具,这不仅仅是量化结果,而且还考虑了其他特征,包括肺气肿亚型和气道壁衰减。检测肺外部表现的措施也在早期发展中,需要进一步研究来优化这些。
CT分析需要根据预后指标和疾病活动标志物进行评估。迄今为止,纵向研究相对较少,这些研究显示了不同的结果。随着时间的推移,进行跟踪CT变化的研究是至关重要的,以获得疾病进展的准确图像,以及CT成像在捕捉这一点上的有效性。评估可量化的CT疾病标志物和潜在生物疾病活动标志物的研究也相对较少,这些标志物包括炎症标志物、微生物学、蛋白酶和其他生物标志物。我们研究中采用的方法强调了如何通过结合支气管镜采样和CT成像来实现这一点,以证明蛋白酶和COPD小气道疾病之间潜在的重要关联[31.].类似的方法可以用于进一步了解活动性疾病过程和发生在不同肺室和区域的内型,有希望允许新的靶向治疗的发展。
增强CT技术也将增加其在COPD中的应用。一个主要的限制因素是辐射剂量和相关的癌症风险。如果要考虑纵向扫描,减少剂量策略是至关重要的。双能量CT技术正在开发中,可实现肺血管的功能性成像,并将有进一步的应用。其他成像工具也可以增强CT成像,以提供有关疾病活动的更多信息。PET-CT和SPECT是目前的例子,但随着针对COPD关键特征的新型分子探针的发展,它们可能会得到加强。CT也可以与MRI共同注册,结合结构和功能成像。
最重要的问题之一是如何利用CT分析来定义临床重要表型。它不太可能将患者分为肺气肿和气道主要疾病的亚组,对引导治疗方案具有足够的帮助。集群分析和其他统计建模技术可以提供有趣的结果,但更有可能是具有少数实用临床应用的研究工具。CT上的肺气肿和支气管壁增厚已经与增加的死亡率有关[55那56那59,并将这些信息与临床参数相结合,可能有助于增强多维预后工具,如BODE指数。
这项技术可能会对COPD的临床试验和药物发现工作产生重大影响。定量CT已经被用作诊断α级肺气肿进展的指标1-ATD,这可以延长针对气道炎症和小型气道疾病的药物。疾病的异质性导致临床试验设计中的重大挑战。大多数试验包括未选择的患者群体。因此,必须注册大量并持续相当长的时间来识别足够的响应者。提高患者异质性的知识对于优化药物试验至关重要,并且定量CT可能发挥重要作用。潜在的,CT可用于将研究受试者分析成最有可能响应调查药物的表型组。例如,Roflumilast靶向气道炎症,但研究结果一直是强大的。CT可用于定义哪些患者有气道增稠/炎症的证据,并且该主题组可用于任何介入研究。改善研究受试者的分层可能会增加治疗效果并降低响应的可变性,从而增加了开发新的药物的机会。反过来,这将导致CT成像在确定哪些患者可能受益于新型药剂的进一步临床应用。
结论
CT成像在调查COPD的调查中具有重要且迅速发展的作用,可以帮助诊断和提供有关显着伴随疾病的信息,并可用于计划严重疾病的人的介入策略。它还能够以疾病的关键肺平和肺突出表现形象,但挑战是如何利用这些信息的。定量分析显示客观地测量这些疾病特征的承诺,许多人与传统临床和生理标志性的疾病有关。这些技术最初是作为一种重要的研究工具,以了解疾病异质性,并援助我们对COPD关键生物机制的理解。这种理解将有助于最佳的患者选择临床试验,并将这些方法翻译成临床实践可能有助于指导个性化的管理策略和改善结果。
脚注
利益冲突:可以在本文的在线版本旁找到披露www.qdcxjkg.com
- 已收到2016年1月7日。
- 公认2016年3月21日。
- 版权所有©2016















