摘要
最近对肺腺癌的研究建立了与临床相关的基于组织形态学的分类。相比之下,形态学分类器尚未应用于肺鳞癌(SQCC)的常规诊断。然而,基于形态学的特征推定对生存的影响已经提出。
我们分析了541名SQCC患者的队列,这些患者具有完整的临床随访数据,包括形态学特征(角化、肿瘤细胞出芽、肿瘤细胞巢大小、核大小和基质含量)。形态学特征与临床资料和患者预后相关。
角质化,萌芽,基质含量和肿瘤细胞巢尺寸,但不是核大小,与不同的临床病理特征和生存相关。SQCC患者具有角质化,小细胞巢大小,高质量含量高,崭露头角较短,整体存活较短。组合的分级方案由两个最可靠的验证的预后标记组成,IE。萌芽和巢尺寸,导致患者,阶段和性别无关的预测剂,用于总存活,危险比为1.6级肿瘤,与1级肿瘤相比,3级肿瘤的危险比为3.7(P <0.001)。
SQCC的形态学特征对预后有重要影响,并可能构成未来诊断相关的SQCC分级方案的基础。
摘要
肺鳞状细胞癌的形态学特征对生存有重要的预后影响http://ow.ly/St6mM
介绍
众多的国际研究已经验证了肺癌/美国胸科/美国胸部学会研究/欧洲呼吸道学血液血液分类(ADC)的肺癌(ADC)分类的预后价值[188bet官网地址1],甚至进一步的形态学改进可能与ADC中优化预后患者分层有关[2-5.].因此,组织形态学的半定量评估现在是ADC的标准,也是2015年世界卫生组织(WHO)对这些肿瘤分类的支柱[6.].
相比之下,在使用组织形态学作为肺鳞状细胞癌(SQCC)预后指标和根据2004年世卫组织分类分型方面进展甚微[7.]尚未证明是任何临床相关性。
然而,K阿多等.[8.[最近开始解决这个问题,并分析了一系列的485个切除的SQCCs,以确定具体的形态学和细胞学标准。他们证明,在单细胞侵袭、细胞核大和肿瘤出芽活性高的sqcc中,总体生存率显著降低。为了挑战和扩展这一数据集,并为临床相关分级系统铺平道路,我们回顾性分析了一大批手术切除的SQCCs,并对形态学参数进行完整随访,包括K提出的假设预后分层指标阿多等.[8.].
材料和方法
队列
我们的队列包括541例SQCCs,这些患者于2002年至2010年间在Thoraxklinik Heidelberg医院接受了完全切除。楔形切除6例(1.1%),段切除术7例(1.3%),肺叶切除术360例(66.5%),双叶切除术23例(4.3%),全肺切除术145例(26.8%),多伴有系统淋巴结清扫。排除单纯SQCC以外的组织学。所有患者均未接受新辅助放疗和/或化疗。男性442例(81.7%),女性99例(18.3%)。平均年龄64.8岁(范围38.2-82岁)。112例(20.7%)患者接受了辅助化疗,68例(12.6%)患者接受了辅助纵隔放疗。随访期间死亡180例(33.3%),复发162例(29.9%)。在分析终点时,平均随访时间为40.8个月。在分析终点无复发患者的平均随访时间为37.1个月。 The distribution of clinicopathological variables is given in表1.
组织学评价
所有存档的苏木精和伊红染色的切片由两位经验丰富的病理学家(C.K.和A.W.)按照K阿多等.[8.使用奥林巴斯BX51显微镜。根据2015年世卫组织分类,肿瘤分为非角化、角化或基底样SQCC(在线补充图S1) [6.].在显示最广泛的萌芽活动和最大数量的小肿瘤巢穴的区域,评估最小肿瘤巢的肿瘤芽和最小肿瘤巢的大小[8.].
肿瘤出芽被定义为由<5个肿瘤细胞组成的小肿瘤巢(在一个高倍场单独分析(HPF;(×400),在10个hpf中出芽数和总出芽数最多),它们从较大的巢和“芽”“分枝”到邻近的薄壁组织(在线补充图S1)。在应用的显微镜设置下,一个HPF对应的视场直径为0.55 mm (0.24 mm2).
细胞巢是指被肿瘤间质包围的一簇肿瘤细胞。最小侵袭性肿瘤巢的大小进一步划分为大巢(由>15个肿瘤细胞组成)、中间巢(5-15个肿瘤细胞)、小巢(2-4个肿瘤细胞)和单细胞侵袭(在线补充图S1)。最小的肿瘤窝的大小被分为两类:1)整个样本肿瘤区域中最小的肿瘤窝和2)侵袭前最小的肿瘤窝。
肿瘤间质含量分为低(≤肿瘤面积的25%)、中(26-50%)或高(>50%)(在线补充图S1)。为了评估核的直径,肿瘤区域的最大的核被选择。我们使用附近的小淋巴细胞作为参考,分析了至少100个肿瘤细胞的平均核直径。小核被定义为直径小于或等于3个淋巴细胞,中间核相当于直径约为4个淋巴细胞,大核被定义为直径大于4个淋巴细胞。如前所述,通过Ki-67免疫组化评估增殖活性[9.].
结果
sqcc的形态学特征
SQCC(178/541,33%)的三分之一显示角质化,63.7%(344/541)是非抗酸的SQCCs。Basaloid SQCC(18例; 3.3%)罕见(表1).
541例中,185例(34.2%)肿瘤细胞在浸润边缘出芽。在这些病例中,只有22例(4.1%)每个HPF有>5个出芽灶。当对入侵前沿的较大部分(10个HPFs)进行调查时,发现了类似的出芽率(541例中185例,34%)。然而,当评估10个HPFs中出芽病灶的总数,并采用略有不同的15个病灶的切点时,84例(15.5%)属于出芽活性增强的肿瘤(表1).
92例(17.1%)为单细胞浸润。166例(30.9%)的肿瘤细胞巢由<5个肿瘤细胞组成,114例(21%)的肿瘤细胞巢最小为5 - 15个细胞,166例(31%)的肿瘤细胞巢仅由含有> - 15细胞的大肿瘤细胞巢组成。仅考虑侵袭边缘时,单细胞侵袭或小巢(<5个细胞)的SQCC发生率略低(合并34.9%,合并48%;表1).
541个sqcc中有310个(57.3%)具有小核;其余病例分布相当均匀,中等(104,19.2%)和大(127,23.5%)核大小(表1).基质含量低、中、高的分别占152例(31.6%)、156例(32.4%)和173例(36%)。
形态特征的相关性
角质化的存在与肿瘤细胞芽和肿瘤细胞巢的大小显着连接。与角质化和基础形态的SQCC倾向于与非抗胰酶SQCC(在线补充图S2)相比显示出稍高的萌芽频率。与非角质质化和基础群(在线补充图S2)相比,在角蛋白亚组中,在角蛋白亚组中更频繁地常常(在线补充图S2)中的肿瘤更频繁。核尺寸与SQCCS的组织学亚型无关。正如预期的那样,在10HPF中的最大肿瘤细胞芽和10hPFS中的总芽和侵袭性余量的整体肿瘤细胞巢尺寸和肿瘤细胞巢尺寸明显相关。具有小型细胞巢尺寸的SQCCS对更强的萌芽活动具有更高的倾向。此外,具有较高萌芽活性和较小巢尺寸的SQCCs显着更可能具有大核和更高的基质含量(在线补充表S1)。
SQCCs的形态学特征与临床参数的相关性
角化sqcc的患者更年轻(p=0.004;在线补充表S2),与非角质化SQCCs患者相比。未观察到角化与临床病理特征的其他显著关联。
肿瘤细胞芽的存在与原发性肿瘤(Pt)类别呈正相关(P = 0.002),而进一步的临床病理学缔组织并不明显(图1和在线补充表S2)。
细胞巢的大小(总体和浸润边缘)与临床病理变量密切相关。局部淋巴结阳性的晚期肿瘤与局部受限的淋巴结阴性肿瘤相比,其细胞巢更小(图1和在线补充表S2)。还注意到具有高基质含量的节点阳性的结合(在线补充表S2)。核尺寸没有显示与临床病理学参数的关联。

临床参数与形态学的典型关联。局部肿瘤范围(pT:原发性肿瘤)和a)浸润边缘肿瘤细胞出芽以及b)整个肿瘤巢大小之间的关系。淋巴结扩散(pN:区域淋巴结)与c)肿瘤窝整体大小和d)间质含量之间的关系。男朋友:初露头角的焦点;高通滤波器:大功率领域;NS:窝大小。
形态特征与增殖活性的相关性
基底样形态与高增殖活性密切相关(Ki-67: 63%)。增殖活性在非角化(47%)和角化SQCCs (48%;p = 0.021)。我们没有观察到增殖活性与出芽、细胞巢大小或核直径之间的显著相关性。基质含量低的肿瘤中Ki-67增殖指数显著升高(在线补充表S2)。
鳞癌的形态学特征与存活的相关性
与无角化(71.5个月)和基底样方细胞癌(68.8个月)的患者相比,角化方细胞癌患者的总生存期缩短(62.1个月);p = 0.037;表1在线补充图S3)。在纳入年龄、性别和分期的多变量分析中,这种与生存的联系仍然存在(在线补充表S3)。与非角质化的sqcc相比,角质化的sqcc的风险比为1.55 (p=0.011)。组织学类型与无病生存(DFS)的关系不明显。为了阐明basaloid sqcc意外的良好生存率,我们讨论了这是否可能是由于辅助化疗的有利影响。尽管接受辅助化疗的3例基底样细胞癌患者在pT分期较高(pT2a、pT2b、pT4)时仍存活,但未接受辅助化疗的基底样细胞癌患者的生存期与非角质化的基底样细胞癌患者相当(在线补充图S4)。
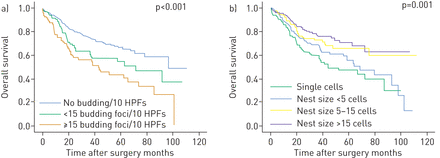
当在一个HPF和10个HPF中评估时,肿瘤细胞出芽对总体生存率有很高的影响。每10个HPFs中出芽灶≥15个的患者平均总生存期为50.2个月,而肿瘤出芽灶<15个的患者平均生存期为63.3个月,肿瘤未显示出芽灶的患者平均生存期为77.0个月(p<0.001;图2和表1).当仅评估一个HPF时,生存相关性具有可比性(在线补充图S5和表1).同样,这种影响与年龄、性别和阶段无关。与10个HPFs中没有肿瘤细胞出芽的患者相比,<15病灶的患者的风险比为1.6,≥15病灶的患者的风险比为2.4 (p<0.001;在线补充表S4)。每10个HPFs的出芽与DFS之间存在边缘性关联(p=0.053;在线补充图S5和表1).在进行可能的多变量分析时,与年龄,性别和阶段无关的对DFS的轻微影响,但危险比仅在≥15次衰退的肿瘤组中仅升高(危险比1.6; P = 0.033),但不是在患有<15个焦点的小组中。
芽面活性和巢大小与鳞状细胞癌存活的关联。患者在边距(每10 HPF)以及B)的肿瘤细胞萌芽,以及B)总肿瘤细胞巢尺寸。HPF:高功率场。
肿瘤细胞巢的大小与总生存率密切相关。总体细胞窝大小较大(>15个细胞)的患者的最长生存时间(平均78.0个月),而随着细胞窝大小的减小,总体生存时间也随之减少(5-15个细胞:77.2个月;<5个细胞:62.1个月;单细胞:53.5个月;p = 0.001;图2和表1).对于侵袭前沿的肿瘤细胞巢大小,可以看到类似的生存相关性(在线补充图S6和表1).两个参数的生存影响与年龄,性和阶段无关。与单细胞侵袭(危险比1)的患者相比,患有5-15件患者的危险比<5细胞的危险比<5细胞的患者的危险比为0.72,其患者进一步降至0.56和0.44或> 15个细胞(p = 0.002;在线补充表S5)。具有DFS的肿瘤细胞巢大小的显着关联并不明显(在线补充图S6和表1).
在我们的队列中,核大小对预后没有影响(表1在线补充图S7)。关于基质含量,与具有低基质含量的肿瘤相比,具有中等和高分子含量的肿瘤具有显着差的整体存活率(P = 0.011);这种效果对DFS不明显(表1在线补充图S7)。
肺鳞癌分级
根据目前的数据,似乎没有一个主要的组织学分类器可以单独用于确定SQCC的肿瘤分级。因此,需要综合各种参数来确定临床相关等级。为此,为了简单起见,我们将重点放在K提出的对生存影响最大的因素上阿多等.[8.]我们可以独立验证(每10 HPF和整体巢大小的肿瘤萌芽)。我们决定将其他参数留出,因为它们是新的(基质含量),冗余(每一个HPF的肿瘤芽,边缘的巢大小)或结果与先前的工作(核大小,组织学亚型)相互冲突。分配芽的分数后(1:没有萌芽/ 10 HPF; 2:<15芽焦点/ 10 HPF; 3:≥15次诱捕灶/ 10 HPF)和巢尺寸(1:> 15个细胞; 2:5-15个细胞; 3:<5细胞; 4:单个细胞)通过总结两个变量来计算每个案例的总分级评分(范围2-7)。原始评分的各自的存活曲线导致离散预后基团的总体存活率特别好(P <0.001;在线补充图S8)。对于DFS,只有7的最大得分为7个,其预后具有异常差的组(在线补充图S8)。在这些数据的基础上,我们定义了2或3分的肿瘤,如良好的分化(1级),分数为4-6的肿瘤,如中等分化(2级)和肿瘤,最大得分为7差异很差(3级)。这导致247级(47%)1例,239(45%)2级病例和43名(8%)分配到3年级(表1).高档肿瘤倾向于更加局部地位;没有注意其他具有临床参数的清晰切割关联(在线补充表S2)。根据我们分级方案的整体存活划分导致预后群体的清除分离(图3和表1).3级也与DFS显着较差的较差;然而,在这方面表现出1级和2年级肿瘤(在线补充图S9和表1).纳入等级,年龄,性别和阶段的多变量存活分析证实了SQCC总体生存率的强烈独立预后影响。与第1级肿瘤相比,2级和3级肿瘤分别具有1.6和3.7的危险比(P <0.001,表2).
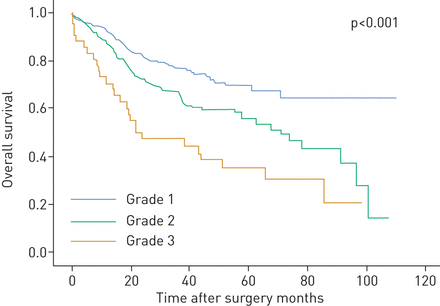
新的鳞状细胞癌肿瘤分级与总生存率的关系。
讨论
我们分析了不同组织特征在大队列的541分切的SQCC队中的预后影响。我们证明角质化,萌芽,单细胞侵袭和更高的基质含量与整体存活率显着更差。在两个最可靠的预测因子中,我们衍生出一种简单的分级方案,具有强烈的独立预后影响。
到目前为止,已经没有建立SQCC的组织形态学特征,其用于预后患者分层的常规诊断。2015年谁分类将SQCC分离成角膜蛋白,非抗炎和无碱肿瘤。不推荐评分[6.].
来自其他肿瘤实体,如结直肠癌[10.],我们知道单细胞侵袭和肿瘤出芽可能与预后不良有关,这一现象最近也被描述为肺SQCC [8.]和ADC [11.].此外,另一项探索性研究为单细胞侵袭对肺SQCC预后的影响提供了证据[12.].同样,肿瘤巢大小也被认为是头颈部SQCC等相关肿瘤实体的预后因素[13.].
到目前为止,通常根据角化程度的降低将鳞癌分为分化良好、中等和低分化肿瘤。然而,在已发表的文献中,有关角化对SQCC患者生存影响的数据有限,到目前为止,还没有明确的证据证明角化对这种肿瘤实体的生存有影响。最近一项485个SQCCs的研究未能提供角化与总生存率预后相关性的证据。本研究没有特别讨论DFS [8.].我们关于角化SQCC的生存结果有些矛盾,因为在我们的队列研究中,角化SQCC的总生存期低于非角化SQCC。这可能部分地解释了我们队列中发现的角化与更小的肿瘤细胞巢大小和更高的出芽频率之间的联系。然而,这一观察结果显然需要在其他大型队列中进一步验证。此外,我们只观察到角化对总生存率的影响,而对DFS没有影响,这也需要验证。
Basaloid SQCC通常被认为是具有受损结果的肿瘤[14.-16.],最近也被描述为具有特定分子背景的肿瘤[17.].在我们的队列中,基底样SQCC的比例是相当小的,但在我们的数据集中,这种肿瘤类型患者更好的总体生存结局是值得注意的。同样,K阿多等.[8.研究还发现,基底样细胞癌患者的5年总生存率略好于非基底样细胞癌患者(69%)与58%)。我们只能推测这些数据差异的原因。切除的基底样鳞癌总体生存率提高的一个解释可能是这些肿瘤对现代辅助化疗有更好的反应,可能是由于它们的高增殖活性。我们在我们的数据集中对这一假设进行了测试,发现接受辅助化疗的基底样细胞癌患者可能会获得特别好的治疗。然而,在我们的亚组群中,患者数量明显太少,无法得出任何明确的结论,这一主题在任何其他研究中都没有被提及。因此,这一假设必须在后续研究中得到验证。
我们可以验证前面描述的[8.细胞巢大小与SQCC总存活率的相关性。当我们观察到巢的大小与肿瘤/基质比率的改变有关时,我们也通过分析肿瘤的整体基质含量来检验这一标准。事实上,将肿瘤分离为低、中、高基质含量提供了一个重要的预后分层,这表明肿瘤/基质比率的评估有进一步的潜力作为预后SQCC分层的附加形态学标准。然而,K阿多等.[8.]不能证明SQCC纤维化程度对预后的影响。
使用四个平均淋巴细胞的近似直径作为根据核直径对肿瘤进行分类的截止点,据报道,大核(直径大于4个淋巴细胞)患者的5年总生存率明显低于小核(直径小于4个淋巴细胞)患者的5年总生存率[8.].然而,在我们的队列中,根据这个建议测量的核直径与患者预后无关。
考虑到目前有关SQCC形态学预后价值的数据,我们决定根据两个可独立验证且与患者预后相关性最好的参数,计算一个简单实用的分级方案。IE。肿瘤细胞出芽和巢的大小。没有成功交叉验证的因素不包括在内。我们从一开始就不把增殖活性作为一个潜在的预测因子,因为我们组之前的一项大型研究坚定地证实,SQCC的预后和增殖之间的关系过于复杂,不能纳入一个实际的分级方案[9.].通过结合两个交叉验证的参数,我们建立了一个简单的分级算法,具有高度的预后。这个评分方案是作为第一个建议。显然,它的临床影响必须在其他国际大型队列中得到验证。此外,必须对组织形态学因素的观察者间差异进行研究,以确保这种分级方法在真实的诊断条件下是可重复的。
我们研究的局限性显然是指其回顾性性质,以及尽管我们的队列研究规模庞大,但在分期分布和治疗方面存在异质性。然而,这也表明拟议的分级方案不仅适用于选定的阶段或特定的临床设置。
总之,我们解决了肺动脉SQCC特异性组织形态学标准的预后相关性,并确认了本实体中肿瘤细胞芽和细胞巢大小的先前提出的阶段无关的预后相关性。在这些数据的基础上,我们建议了第一个基于证据的SQCC临床相关评级计划的提案。我们的数据希望有助于肺动脉SQCC中真正有意义的组织学分级的成功故事,这能够在过去十年中平行巨大的肺部ADC分类的巨大改进。
脚注
编辑评论在:欧元和J2016;47:720-723 [DOI10.1183/13993003.00035 -2016].
本文提供了补充材料www.qdcxjkg.com
利益冲突:可以在本文的在线版本旁找到披露www.qdcxjkg.com
- 已收到2015年6月16日。
- 公认2015年9月18日。
- 版权©2016人队