摘要
肺癌患者原发肿瘤和纵隔淋巴结的准确分期和再分期具有重要意义。对于原发肿瘤,建议进行胸部CT扫描。正电子发射断层显像(PET)应用于治疗意图治疗的患者,以评估转移性疾病。原发性肿瘤的诊断应使用支气管镜或ct引导下经胸穿刺。对于纵隔淋巴结肿大且无远处转移的患者,需要纵隔浸润分期。对于可疑的N2或N3疾病,内镜下穿刺技术,如支气管内超声和经支气管穿刺,食管超声和细针穿刺,或两者结合,优于任何手术分期技术。如发现可疑淋巴结及针吸阴性,应采用纵膈镜或电视胸腔镜进行侵入性手术分期。在中央肿瘤或N1淋巴结,术前浸润分期是有指示的。
诱导治疗后重新恢复仍然是一个有争议的话题。今天,既不是CT,宠物也不是PET / CT扫描足以足以对纵隔节点受累进行最终进一步的治疗决策。仍建议提供提供细胞学信息的侵入性技术。
摘要
肺癌分期中的非侵入性,微创和侵入性技术的作用是什么?http:///wly/lxa6b.
介绍
肺癌是工业化国家恶性疾病患者最常见的死亡原因[1,2].NONSMALL细胞肺癌(NSCLC)占所有肺癌病例的近85%[3.].肺癌患者的正确分期提供了对疾病的局部和近距离的准确信息,指导治疗的选择,并能够估算预后。分期方法包括:成像,如计算机断层扫描(CT),2-DEOXY-2-(18.f)氟 -d-Glucose正电子发射断层扫描(FDG-PET)或集成FDG-PET / CT扫描;基于针对基于针对的活组织检查技术,例如胚胎超声跨旋转针吸附(ebus-tbna)或食管超声针抽吸(eus-na);跨界针吸汗(TBNA)和CT引导的TRANSTHORACIC细针抽吸(TTFNA);最后的手术技术,包括含有含有含有含有含有含有植物学,纵术或视频辅助胸腔镜(VATS)技术。完全切除是潜在治疗的必要因素。虽然在早期的阶段I和II中,手术被接受为主要的治疗方法,但局部晚期阶段和IIIb很少被局部治疗方式固化,例如单独的手术或放射疗法。在这些阶段的各种多重态性协议,包括化疗和放射治疗,导致存活率增加,但在某些亚组中进行了额外的手术[4- - - - - -7].因此,分期程序的重要目标是为多学科决策选择初级手术的候选者,或者在阶段/ IIIB疾病中进行多学科决定。此外,恢复技术是否可以提供关于临床医生的额外问题,其中有关于原发性肿瘤和纵隔节点的预测的信息仍有待解答。
这篇综述的目的是评估和更新无创、微创和有创技术在肺癌分期和再分期中的作用。评估的参数包括敏感性、特异性、假阴性和假阳性率以及准确性。在这份手稿中,欧洲胸外科医师协会(ESTS)、美国胸内科医师协会、国际肺癌研究协会(IASLC)和德国癌症协会的指南和建议被考虑在内。
肺癌分期
原发性肿瘤的诊断(t状态)
Posteroantiorior和横向射线图仍然是胸疾病和初始可用诊断工具的最常见的放射检查,如果肺癌怀疑在大多数国家。可疑的病变或质量,Atelectasis,纵隔或胸腔积液的扩大是促使广泛诊断评估的结果。在涉嫌肺癌的患者中,强烈建议强烈推荐患有对比度的胸部CT扫描,包括肝脏和肾上腺的上部腹部,并强烈推荐[8].CT扫描不仅可以帮助肿瘤诊断,还可以在肿瘤大小和范围内相关,以构建临床评价和肿瘤分期。CT扫描在检测中位于中心位于肿瘤的肿瘤质量方面非常敏感,以及外周肺结核。只有少数研究分析了恶性肿瘤的标准,并报道了成像试验对鉴定恶性孤立结节的高度敏感性,但特异性是可变的,通常差(敏感性,98-100%;特异性,54-93%)[9].由于关于病变的位置的精确信息,必须在侵入性检查作为支气管镜检查或含有支气管镜检查之前进行CT扫描
磁共振成像(MRI)用于肺癌的分段,以便更好地表示肿瘤和胸壁或/和纵隔结构之间的解剖关系,由于软组织更高的对比度。这种有利的效果与宫颈植物通道中没有人工制品,神经疏松症和脊柱沟道等级的效果,MRI是成像的第一选择沟相高级肿瘤,并显示椎体柱的接触或渗透[10.,11.].
FDG-PET成像可以提供有关原发性肿瘤,纵隔节点和任何远离转移的代谢信息。FDG-PET在原发性肿瘤的反射中的重要性是不同的。在肿瘤质量的评估中,可以看到肿瘤和肿瘤之间的差异;对于孤独的肺部病变,肿瘤的大小是重要的。恶性肿瘤的患病率随大小(结节的0-1%<5mm,结节为5-10mm的6-28%,结节的64-82%> 20mm)。FDG-PET用于鉴定恶性孤立病变的敏感性始终如一(80-100%),而特异性跨研究较低,更可变(40%-100%)[9,12.,13.].
支气管镜是最重要的诊断方法,特别是在中心位于中心位于肿瘤中,准确率接近100%[14.].在外周肿瘤中,需要不同附加的活检技术,例如导管,刷子,针或镊子。用于诊断小型肺结核的现代导航技术可以提高诊断准确性[15.,16.].
在一项研究中评估了用于将直接肿瘤侵袭分段为纵隔侵袭(T分期)的食管超声和细针吸入(EUS-FNA)的可靠性。作者报告的假阴性率约为30%,表明不应建议对原发性肿瘤的纵隔侵袭进行这种技术[17.].
在CT引导针活检(TTFNA)的研究中,当活组织检查产生特异性良性或恶性结果时,敏感性和特异性优异(90%)。特别是在小于3cm的病变中,TTFNA导致比支气管镜检查更高的灵敏率[18.].最常见的并发症是气胸,约占病例的10%-30% [19.,20.].
最后,VATS已被用于评估CT扫描描述的T4肿瘤,这意味着可以介绍跨学科多模概念。T4结构的参与可以在38%的患者中发现,并且在6%的恶性胸腔积液中找到。在4%的患者中,未缺点的恶性胸膜调查结果描述了[21.,22.].
淋巴结诊断(n状态)
非小细胞肺癌患者的淋巴结受累程度是最重要的预后因素,并影响不同的治疗策略。临床N1、N2和N3疾病患者是异质性组,预后和生存率不同。在CT扫描上肺门淋巴结肿大(>短轴1cm),且没有纵隔或远处转移的证据时,不推荐评估肺门淋巴结状态,因为这些淋巴结在肺切除术时可以被切除。一个例外是累及多个肺门淋巴结或体积庞大的肺门疾病。相反,这些患者是新辅助治疗的候选者[23.].在IIIA-N2疾病患者的亚组中,诱导化疗与放射疗法和手术合并已被证明是有效的[24.- - - - - -27.].在N3疾病的患者中,一些具有有限数量的患者的研究表明组合化疗后的衰退效果,这意味着选定的患者接受手术的令人鼓舞的结果[28.- - - - - -30.].
aradslc建议在淋巴结地图中实现了几种修改,而与n的前一个地图相比aruke.等.[31.)和M谷和D.resler[32.].首先,定义了节点区域和节点站的差异,并且清楚地描述了节点站的解剖边界[33.].节点区域被描述为包括一个或多个相邻节点站的解剖区域(主动脉区包括亚主动脉和对齐节点站5和6,下部区域是副区和肺韧带站8和9,等等。)。其次,引入了解剖学纵隔中线到左下气管缘的转变(肿瘤纵隔中线),影响Nodal Stations 2R / L和4R / L.这意味着左侧肿瘤,涉及左解剖中间中线(右肿瘤骨髓中线)的预去气管淋巴结或淋巴结的肿瘤患者被归类为N2疾病,而那些左侧肿瘤的病例被归类为N3 [34.].
非侵入性技巧
CT仍然展示了原发性肿瘤以及纵隔节点的主要成像调查。CT扫描准确用于描述节点尺寸(短轴直径> 1厘米),但是节点扩大用于分期的临床相关性是有限的,因为57%的敏感性低,阳性预测值(PPV)仅为56%.此外,淋巴结扩大分期的临床相关性是不令人满意的,因为肿瘤受累也发现高达20%的小节点(负预测值(NPV)为83%)[35.].
FDG-PET的使用提高了肺癌分期的准确性。不同的研究表明,FDG-PET在纵隔分期方面优于CT,其敏感性和NPV分别为85%和93%,与纵隔镜的比率相当。然而,由于炎症过程摄取FDG呈阳性,FDG- pet的特异性和PPV低于纵隔镜和EBUS-TBNA。临床IA期,以治疗为目的,可通过FDG-PET扫描进行纵隔及胸外分期。在临床IB-IIIB阶段,具有治疗意图,强烈推荐FDG-PET扫描[36.].
进一步的技术开发是集成的FDG-PET / CT扫描,其中FDG-PET的高灵敏度和CT扫描的优异形态分辨率和解剖细节描述融合。由于肿瘤与肿瘤与周围的淋巴结与周围纵隔组织和结构之间的区域关系更精确的解剖相关性,有几种研究显示了与单独的FDG-PET相当的集成FDG-PET / CT扫描的诊断准确性增加[37.- - - - - -40].
2007年和2014年,ESTS委员会公布了NSCLC术前淋巴结分部的指导方针。工作组建议,在临床阶段I NSCLC和阴性纵隔FDG-PET图像中,通常可以省略含有含有含有含有含有含有含有含有型血液镜的侵入性分期技术[34.,40].对于疑似N1淋巴结的病例,>3 cm的肿瘤,以及CT扫描或FDG-PET图像上没有疑似淋巴结的中央位置肿瘤,建议采用浸润纵隔分期[40].在30%的N1疾病患者中,CT扫描发现有N2或N3淋巴结[41.].对于肿瘤> 3cm,特别是具有高FDG吸收的腺癌,应考虑用于纵隔节点的进一步侵入性分期技术[42.].最后,病理N2疾病在中枢肿瘤中的患病率高达22%;因此,在本组中,需要使用侵袭性技术进行更准确的淋巴结分期[43.].
微创技术
微创技术或侵入性的非外科技术是基于针的活组织检查技术。TBNA仅在一些中心使用,并且NSCLC中纵隔分期的报告的准确性很大。Holty.等.[44.[表演了荟萃分析,发现TBNA的敏感性主要取决于纵隔转移的患病率。当正确进行时,TBNA对于NSCLC患者鉴定纵隔转移,而且由于低灵敏度和78%和28%的高假阴性率,不能确定TBNA技术作为常规诊断方法在肺癌的阶段。如今,EBUS-TBNA和EUS-NA完全替代TBNA用于肺癌的纵隔分期。
自从不同的社会发表了关于NSCLC分期方法的指南以来,支气管内和食管内超声针吸技术的使用迅速增加[8,36.,40].ebus引导的TBNA主要适用于2R/L、4R/L、7纵隔淋巴结站,以及10、11、12肺门淋巴结站。大多数使用EBUS-TBNA的研究都涉及CT扫描或FDG-PET扫描出现离散淋巴结肿大的患者,中位疾病患病率约为58%。总体中位敏感性为89%(范围46 - 97%),中位NPV为91%(范围60 - 99%)。并非所有的研究都能达到所有淋巴结站的系统方法,但在对N2或N3疾病进行评估后,系统方法和选择性方法之间只有很小的差异被报道[36.,45.,46.].
EUS引导的FNA的产率特别适用于在4L,5和7的后部和下纵隔水平8和9中的评估中的评估。左肾腺体,乳糜泻淋巴结和肝脏也是可能的。此程序需要熟练和经验丰富的调查人员。公布研究的总体流行率为58%,中值敏感性为89%(范围50-100%),中值特异性为100%,中位数NPV分别为86%(范围68-100%)[36.,47.,48.].并发症如出血或感染是罕见的,并且已经报道了超声引导针技术的死亡率。
EBUS-TBNA / EUS-NA的结合使用导致所有纵隔淋巴结的近乎完全评估,除了站5和6例外。中值敏感性和特异性分别为91%和100%,中位数NPV是96%[49.- - - - - -52.].在进一步的随机研究中,如果未发现Nodal受累,则微创内胸腔吸收随后是手术分期,与单独的手术分期进行比较。手术分期组敏感度为79%相对内体造影中的85%和94%在结合的内皮内/手术组中。结合内心识别和手术分期也导致了更少的不必要的胸廓术[51.].
侵入性技巧
由Carlens于1959年推出颈椎综合镜检查,直到2005年的视频辅助含有媒体镜检查(VAM)的分布,并在2005年使用胚胎和内蛀牙过度针吸入技术,这是侵入性完全分期的金标准患有肺癌患者的上纵隔型。纵隔镜检查是在手术室的全身麻醉下和大多数医院作为门诊过程进行。根据IASLC提出的淋巴结地图[33.[左上和下颚站(2R / L和4R / L),可以评估前肱动箱3和子集站7。发病率和死亡率低,平均分别为2%和小于0.1%。根据S的数据发布的数据,宫颈常压检查的中值敏感性为78%,中位数NPV为9267名患者91%ilvestri等.[36.].大约42%-57%的假阴性活组织检查导致了颈椎纵隔镜无法到达的淋巴结站(5、6、7站后方和8、9站)。VAM的优势在于提高了手术视野的可见性。在不损害手术安全性的前提下,提高了该技术的准确性和教学的可能性[53.,54.].额外的优点是透明去除子地淋巴结(站7)和食道的安全可视化[55.].Z阿克卡尔等.[56.]分析了1989年至2011年期间发表的108篇论文报告了常规含有媒体镜检查和VAM;两种程序都没有死亡率和发病率低,尽管可以通过VAM去除更多淋巴结站。准确性或NPV没有差异。
经主动脉弓外侧胸骨上入路的扩展颈纵隔镜检查,首次由Ginsberg.等.[57.[除了宫颈纵像检查术达到的经典上皮气管和子地下淋巴结站之外,还用于评估子系统波动节点节点5和6。中位敏感性为71%,中位数NPV为91%。由于苛刻的技术方法,只有少数宫颈镜片镜检查的机构均经常使用此程序。对于淋巴结站5和6,首先由腔室描述的左前介质介质术提供了对这些站的安全方法。它主要用于左上叶的肿瘤的纵隔分期。该程序需要具有双腔管的全身麻醉,并且在大多数医院用作门诊过程。在操作结束时,可以在肺过度下空后去除胸管。中值敏感性约为71%,NPV为91%,流行率为26%[58.,59.].
除了VAM,一些组通过宫颈方法对纵隔淋巴结切除术的扩展技术。使用视频辅助常存型淋巴结切除术,可以进行一套完全淋巴结切除站2和4个双侧,7和8的淋巴结切除术。转基术扩展纵隔淋巴结切除术(Temla)是一种更自由基的程序,并且通过颈部的小套环切口进行。胸骨猩猩升高,用特殊的牵发器升高,喉部复发性和迷走神经的双侧可视化是可能的。这使得能够完全去除除肺韧带节点(站9)和最远侧下颚节点(站4L)之外的所有纵隔节点站(1,2,3a,3p,4,5,6,7和8)的完全去除。有些作者不仅用这些技术不仅用作分期过程,而且是解剖肺切除前的自由基淋巴结切除术。两种方法的优点是由于移除的节点中的潜在微管状而减少了假阴性结果。在这两种程序中,据报道,高精度为96%至98%和97%和99%的NPV [60.- - - - - -62.].
VATS还可以有助于完成纵隔分期,因为可以评估所有纵隔节点。全身麻醉和双腔管是必要的;在某些情况下,难以到达左下颚骨节点。发病率和死亡率极低:2%和0%。敏感性的中值值为99%,NPV 96%(4%假阴性率)[63.,64.].
肺癌重新衰减
在约50-80%的NSCLC IIIA / IIIB疾病疾病诱导化疗或组合的化学疗法中导致肿瘤反应和涉及N2或N3淋巴结的间隙。在选定的情况下,额外的手术显示令人鼓舞的结果,长期存活[5- - - - - -8,66.].患有原发性肿瘤或持久性纵隔节点的患者与具有经过验证的肺和纵隔下降的人进行了更差的预后[67.- - - - - -69.].重新恢复很重要,因为与单独手术的患者相比,诱导治疗后的切除可能与术后发病率和死亡率增加有关[70,71].重新恢复测试包括CT扫描,FDG-PET或集成的FDG-PET / CT扫描,针脚吸附(EBUS-TBNA或EUS-FNA)的内窥镜方法以及含有常血镜检查的侵入性手术方法,重复纵隔镜检查和VATS。
诊断原发性肿瘤(T-STATUS)
在原发性肿瘤的重新衰退中,大多数涉及CT扫描的研究表明了在分别31%和54%的中位数(范围0-100%)的中位数检测残留癌症的特异性和假阴性率的可变性。单独的化疗后CT扫描的假阴性率高于组合后的化学疗法[72,73].新辅助治疗期间患者的一个重要观察是肺栓塞的渐近过程。我们发现,在扫描CT扫描或灌注扫描期间,在12%的患者中的一种或两种肺部中的部分或完全的节段性失败[74].
大多数宠物研究表明,检测残余肿瘤比CT扫描更好的可靠性[73,75,76]敏感性,特异性,假阴性和隔音率的初级部位的平均值分别为76%,71%,36%和12%。假阴性率在13到100%之间变化,36%的中值率令人失望。根据假阳性率,化疗后患者与化学后疗法后的定量宠物评估没有差异。然而,标准化摄取值(SUV)的变化与原发性肿瘤的病理变化相关。Cerfolio.等.[73描述了最大SUV的变化与切除的肺中非可行性肿瘤细胞的百分比具有线性关系,表明FDG-PET扫描比CT扫描上所示的尺寸的变化更精确的预测器。另外,发现当最大SUV降低80%以上时,患者更可能是一种完整的响应者,而不管细胞类型如何。
支气管镜检查对于重新评估中央气道肿瘤反应和确定局部可操作性是有用的。对于支气管内生长的中央位置肿瘤,建议使用柔性或刚性支气管镜检查并对前瞻性切除边缘进行活检[74].
纵隔节点的诊断(n状态)
通过CT扫描评估纵隔重启可靠性的研究表明,初级分期较低的灵敏度,特异性和精度,表明CT扫描不适用于识别所涉及的纵隔节点的部分或完全响应的患者。与中位假阴性率为31%和假阳性率为34-66%,CT成像在化疗或放化疗后无法预测肿瘤活力[77- - - - - -79].
PET扫描对化疗或放化疗后纵隔淋巴结重建的敏感性低于诱导治疗前,假阴性率较高,在28% ~ 36%之间。这些不良结果的一个潜在原因可能是肿瘤的变化,如周围组织的纤维化和诱导治疗导致的灌注改变[75,76].单独化疗后,患者之间没有差异,并在化学疗法组合后的患者之间存在差异。报告的敏感性为50%-60%,特异性为85-90%。宠物重启的最佳定时建议在感应疗法结束后1个月[79].应该提到的是,最大SUV值取决于本地设备和设置;因此,绝对值不能推断到其他中心。
两项研究报告了使用集成的FDG-PET / CT扫描。由于综合FDG吸收在纵隔中更好的定位,特异性明显增加至93%,假阴性率降至13%[80].来自两种串行PET / CT扫描的SUV最大值,在三次化疗循环之前和之后,允许预测原发性肿瘤和纵隔淋巴结的组织病理应答(分别为73%和89%的特异性)并具有预后值[81].另一项研究发现,在所有病理阶段,重复PET/CT比单独CT更准确[82].由于纵隔节点在可疑残余肿瘤的情况下,25%的假阳性率和20%的假阴性率,需要用于节点分期的侵入性技术[34.].
有限数量的组据报道了它们在感应治疗后评估纵隔节点的针吸入技术的经验。由于N2疾病的普遍性不同,重新变化的内镜eBUS-TBNA和EUS-FNA技术表现出与NPV相对于NPV的结果不同,并且只有每位患者的少数节点站(平均一到两个节点站的选择方法每个病人)。报告的NPV在20%和78%之间变化,表明在负内窥镜针吸汗结果的情况下,应确认侵入性外科纵隔重新恢复[83- - - - - -85].
在一项只有11例患者的研究中,未显像的TBNA导致了0%的假阴性率,这可以解释为患者数量少和选择了一个持续增大的纵隔淋巴结的淋巴结站[86].
重复纵隔镜检查(reMS)作为一种重新治疗方法仅被少数外科医生报道过,并且在新辅助治疗方案被引入局部晚期肺癌治疗之前很少被实施。由于遇到组织粘连,特别是在气管和无名动脉之间,ReMS被认为是技术上的要求。然而,rem在高达98%的病例中是可行的。死亡率几乎为零,发病率非常低(1.9%)。敏感性为29-76%,特异性为100%,准确性为60-93%。PPV和NPV分别达到100%和85%。由于粘连和严重纤维化,初次纵隔镜检查的准确性和敏感性低于报道。摘除或活检淋巴结的数量在发表的系列中有所不同,但明显高于内镜下针吸技术。在重复纵隔镜检查时,由于隐蔽性转移,大多数病例的持续淋巴结疾病存活率较低;因此,对于这样一组不利的患者,手术干预的指征应非常仔细地评估[80,87- - - - - -90].
同一组有两份报告,具有Temla的经验作为恢复技术。在第一项研究中,63名患者中只有七只患者在感应化疗或疗程之前具有先前的纵隔镜检查。敏感性,特异性和准确性分别为95.5%,100%和98.3%;NPV为97.4%,PPV为100%[91].在第二份报告中,与Temla进行了比较了EBUS / EUS针技术。在重新恢复组中,在78名患者的88名患者和Temla中进行内窥镜分期。EBUS或EUS和Temla之间存在显着差异(64.3%和100%; P <0.01)和NPV(82.1%和100%; P <0.01),有利于Temla [92].
最后,L是第一个颈椎常压镜检查作为恢复过程ardinois等.[53.].195例未进行预处理的患者和24例诱导治疗结束后的患者,使用视频辅助入路对纵隔淋巴结进行活检。根据肺切除术时纵隔淋巴结清扫的结果,评估视频纵隔镜检查的准确性。视频纵隔镜检查对未进行预处理的患者的敏感性、特异性和准确性分别为87%、100%和95.6%;在诱导治疗后,这些结果分别为81%,100%和91%。在一项III期(N2)肺癌诱导治疗后再灌注的系统综述中,Candela等.[93比较了手术时的病理结果和重新诊断的方法。虽然重新手术方法通常用于选择或排除患者的手术,但数据显示它们是相当不可靠的。与CT、PET、rem、EBUS或EUS(假阴性率15% ~ 30%)相比,原发纵隔镜检查似乎是重新评估N2期疾病最可靠的方法。
j唯一的VATS研究了纵隔重启的研究Aklitsch.等.[94].在预期的多制度试验中,经过证实证明了载体镜检查中载体镜片镜中的同侧节点的可行性IIIa(N2)NSCLC。共恢复47个视频胸镜检查程序(69%)重新恢复纵隔。在21名患者中,视频胸镜检查未成功(31%)。敏感性为67%,特异性100%和NPV 73%。视频胸腔镜重新恢复受辐射有限,无法到达4R节点站。
第一次登台和重新登台的总结
对于有资格进行治疗的已知或疑似肺癌的患者,建议使用包括肝脏和肾上腺的胸部和上腹部的CT扫描。应使用支气管镜检查或CT引导TTFNA进行原发性肿瘤的诊断。如果可用的话,宠物成像应该用于治疗意图治疗以评估转移性疾病的患者。对于III或IV期疾病的患者,甚至没有任何临床症状,患有III或IV期疾病的患者的头部MRI(或CT扫描)。在纵隔节点和没有远处转移的患者中,建议使用或不增加宠物吸收的侵袭性分期。对于可疑N2或N3疾病,例如EBUS-TBNA,EUS-FNA或这两种方法的组合,内镜针技术优选任何手术分期技术。在使用针吸入技术和可疑节点的负面结果的情况下,应进行使用含有含有含有含有含有含有纵隔或VATS的侵袭性手术分期。在左肺的NSCLC患者中,潜在的治疗治疗,节点5和6的侵入方法通过需要腔室,VATS或延长的颈椎含有宫颈镜检查。暗示远处转移性疾病的成像结果需要进一步评估和组织组织学,仅在治疗意图治疗患者中(无花果。1).
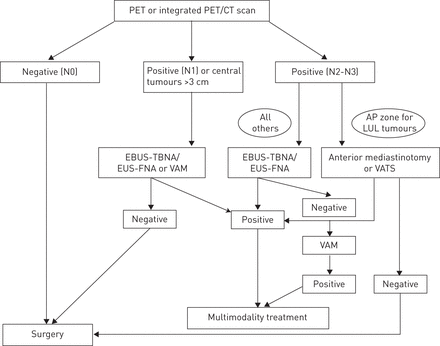
原发性纵隔淋巴结分期算法。PET:正电子发射断层摄影术;CT:计算机断层扫描;AP:主动抑制;LUL:左上叶;EBUS-TBNA:支气管内超声及经支气管针吸;EUS-FNA:食管超声及细针抽吸;VAM:电视纵隔镜检查;VATS:视频辅助胸外科。
关于重新验证的建议难以定义,因为尽管有各种可用技术,但仍据报道高出误报率和30%之间的高假阳性和上限率。在切除后,还在经验丰富的中心中首先在组织病理学标本中鉴定了许多下演患者。胸部和上腹部的CT扫描是预测诱导处理后主要肿瘤的放射线响应的最广泛的方法。然而,CT扫描无法预测完全消除活肿瘤。普遍使用宠物成像或集成的PET / CT扫描,但放射疗法可能导致由于炎症引起的病理摄取;因此,这种方法也没有足够可靠。REMS已被证明在经验丰富的中心安全可行,但由于粘连和纤维化,这种方法在技术上挑战,假负率令人难以置疑高达25%。与EBUS-TBNA和EUS-FNA的经验仍然有限;报告的假阴性率为15%的低于重复载体镜检查。最后,在初始使用针基技术之后,首先宫颈常压镜检查作为恢复技术似乎是评估诱导处理后节点疾病的最有效方法,并选择潜在的手术候选人(无花果。2).
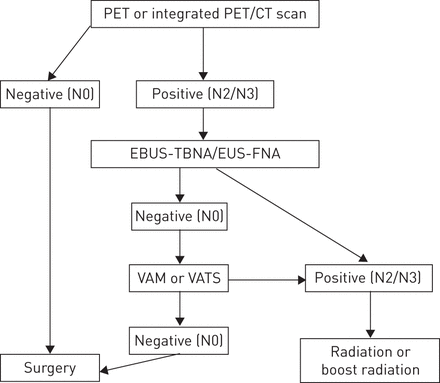
诱导治疗后纵隔淋巴结重建的算法。PET:正电子发射断层摄影术;CT:计算机断层扫描;EBUS-TBNA:支气管内超声及经支气管针吸;EUS-FNA:食管超声及细针抽吸;VAM:电视纵隔镜检查;VATS:视频辅助胸外科。
脚注
本系列的前一篇文章:1号:鲍威尔哈,鲍德温博士。多学科团队管理在胸内肿瘤学中:不仅仅是一个概念?EUR RESPIR J.2014;43: 1776 - 1786。2号:Shlomi D,Ben-Avi R,Balmor Gr,等.肺癌筛查:胸部计算机断层扫描的大规模筛选时间。EUR RESPIR J.2014;44: 217 - 238。第3号:De Ruysscher D,Nakagawa K,Asamura H.手术和非牢房的小尺寸无弹性细胞肺癌。EUR RESPIR J.2014;44: 483 - 494。第4号:Van Schil Pe,Opitz I,Weder W,等.恶性胸膜间皮瘤的多模式治疗:我们今天在哪里?EUR RESPIR J.2014;44:754-764。第5号:Kim L,Tsao MS。肿瘤组织对个性化治疗时代的肺癌管理:什么是足以用于分子测试?EUR RESPIR J.2014;44:1011-1022。第6号:Blum T, Schönfeld N.肺癌患者,肺病医生和姑息治疗:一个发展中的联盟。EUR RESPIR J.2015;45: 211 - 226。第7号:Paesmans M, Grigoriu B, Ocak S等.非劣效性或等效性设计对非小细胞肺癌随机试验的系统定性评价。EUR RESPIR J.2015;45:511-524。8号:Grigoriu B,Berghmans T,Meert A-P。EGFR突变Nonsmall细胞肺癌患者的管理。EUR RESPIR J.2015;45:1132-1141。第9号:Duchemann B,Friboulet L,Besse B. Alk治疗管理+非球体细胞肺癌患者。EUR RESPIR J.2015;46:230-242。
利益冲突:无声明。
- 已收到2014年7月10日。
- 接受2015年4月7日。
- 版权所有©2015















