编辑器:
系统供氧能力受损,特别是在运动过程中,是慢性阻塞性肺疾病(COPD)和心力衰竭合并左室射血分数(HFrEF)降低的关键病理生理特征。不幸的是,COPD和HFrEF经常共存不仅是因为它们的高个体患病率,还因为常见的危险因素,包括吸烟、高龄、氧化应激和全身炎症[1]。
据预计,任何由于COPD和/或HFrEF导致的氧转移速率的降低将对严重依赖于持续氧流的组织特别有害,如中枢神经系统(见[2])。运动脑氧合(Cox)(由近红外光谱非侵入性测定)取决于瞬时供氧率和供氧利用之间的动态平衡[3.]。K.设施等。(4,例如,报道充血性心力衰竭(CHF) HFrEF与运动期间COx明显降低有关。我们的实验室发现,一些晚期COPD患者的运动COx可能受损,即使没有明显的低血氧[5]。此外,具有非侵入性通气(在相同动脉氧含量下的心脏输出的改善对COPD中的COX具有积极作用[6]。这些数据表明,在一些中重度COPD患者中,脑血流减少可能与运动COx受损有关。可以想象,HFrEF的存在会通过添加功能失调的大脑自动调节、低心输出量和低碳酸血症诱导的血管收缩等成分进一步恶化这种情况[4]。然而,HFrEF联合COPD对COx的复合作用及其与运动耐量的关系尚不清楚。为了解决这些问题,我们同时评估了有或没有HFrEF共病的COPD患者在进行性运动期间的COx、全身血流动力学和气体交换。
研究组包括33名男性,患有稳定、非高二氧化碳(静息时动脉二氧化碳压力<45 mmHg)慢性阻塞性肺病、长期吸烟史(>20包-年)、日常呼吸困难(改良医学研究委员会(MRC)评分>2)和中度至重度气流阻塞。COPD+HFrEF组(n=18)患者多普勒超声心动图显示左心室射血分数<40%,并明确诊断为CHF(运动时呼吸困难、颈静脉压升高、心脏肿大、外周水肿和肺气肿),原因是潜在的缺血性心脏病。所有患者均接受标准的当代HFrEF治疗。来自慢性阻塞性肺病诊所的15例患者,无临床、超声心动图和实验室证据的CHF (n=15)与年龄和MRC分级相匹配(表格1)。主要排除标准包括长期动态氧疗、严重肺动脉高压(平均肺动脉压≥40 mm Hg)、贫血(血红蛋白浓度<13 g%)和近期加重(1个月内)。在提供知情同意(经当地医学伦理委员会批准)后,患者接受斜坡递增心肺运动测试,评估动脉化二氧化碳张力(P有限公司2)。从额相Cox(oxohaemoglobin浓度(氧气血红蛋白浓度)中的静静(δ)变化([HBO2]),用近红外光谱(NIRO 200™;浜松光电KK,浜松,日本)和心输出量经胸心脏阻抗(PhysioFlow PF-5™;Manatec Biomedical,巴黎,法国)[7]。根据我们以前的较旧科目和COPD患者的汇总分析5,6], ΔCOx增加<1.10倍和/或任何减少被认为表明生理反应不充分。采用重复测量的单向方差分析来确定组间不同时间点的差异有统计学意义。采用皮尔逊相关分析评估变量之间的相关性。所有检验均采用0.05的统计学显著性。
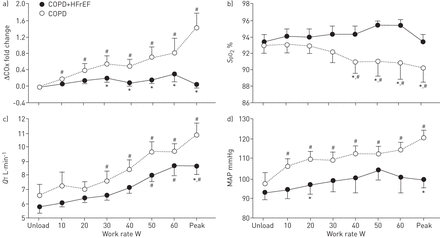
我们发现COPD+HFrEF患者的最大运动能力低于COPD患者。此外,前一组对代谢需求的通气反应增加,这与更大的氧饱和度(图1 b)但下颌和终端下降P有限公司2与慢性阻塞性肺病患者(表格1)。慢阻肺+HFrEF患者在亚极大期血流动力学反应(心输出量和平均动脉压)变迟钝(如图。1C和D.)及最大运动量(表格1)。在COPD+HFrEF组中,ΔCOx随着运动进展的变化也减少了(图1一个)。实际上,ΔCox在15名COPD患者中增加了11名(73.3%),其中15名COPD患者18例COPD + HFREF患者中仍然稳定或甚至减少14例(77.7%)。在平均全身动脉压保持稳定或降低的患者中特别损害ΔCox(P <0.05)。有趣的是,仅在COPD + HFREF组(R = 0.67,P <0.01)中,峰值工作速率与潜水ΔCox(曲线下的面积为40 w)有关(r = 0.67,p <0.01)。
a)前额叶脑氧合(ΔCOx); b)脉搏血氧仪测动脉血氧饱和度(年代阿宝2),c)心输出(问T)和d)平均动脉压(MAP)作为慢性阻塞性肺病(COPD)患者的运动强度的函数,或者没有心力衰竭的患者,其作为合并症的射入部分(HFREF)。数据显示为平均值±se。*:组间比较p<0.05;#:P <0.05对于Intragroup循环的Intragroup比较。
降低动脉氧含量可能是COPD + HFREF中的COX减少的潜在解释,如CHF本身可降低肺弥散容量,加重通气/灌注不匹配,降低混合氧静脉压。然而,我们发现相反的情况,这些患者的动脉氧合保存得比单纯COPD患者更好。较低的P有限公司2脑灌注压受损(由于低平均动脉压和心输出量)是明显的罪魁祸首。事实上,平均动脉压是大脑血流的主要决定因素[8[整个运动试验中是否减少,与COPD + HFREF中的COX相关。平均动脉压的轻微损伤可能降低脑血流量,特别是在存在受损的自动调节和过度交感神经驱动情况下[3.,8]。还有一些证据表明心输出减少可能会损害运动Cox,与平均动脉压有关[8]。所有患者均接受心脏选择性β受体阻滞剂治疗,心率反应减弱是运动心输出量减少的主要机制。这表明药物诱导的运动变时反应减少和低运动COx之间有联系。
这些发现的实际相关性是什么?我们的数据表明HFREF的药理治疗应考虑到前额前皮质对COPD患者的压力灌注障碍特别敏感。运动受损Δcox是心血管疾病患者的独立预后因素,以及脑缺血事件的预测因子[3.]。值得注意的是,当HFREF共存时,中风更频繁在COPD患者中[9]。可想而知,本文报告的COx缺陷也可在其他临床情况下观察到,如急性加重或利尿剂诱导的低血容量血症。ΔCOx的紊乱也可能减少运动输出(中枢疲劳),并有助于早期停止运动[2]。事实上,ΔCOx仅与COPD+HFrEF组的峰值运动能力相关。如果未来的研究建立了因果关系,旨在改善运动期间脑血流的干预措施可能证明对这些患者有用的能源性辅助。
本研究的局限性包括样本量小、COPD严重程度的异质性、无创心排血量测定、缺乏认知和脑血流测量。然而,我们应该认识到,Δ[HbO2]不仅是脑灌注变化的有用指标,还与认知密切相关([10])。COPD+HFrEF组比COPD组出现更少的气流阻塞。因此,我们可能低估了HFrEF对COPD患者脑血流动力学的有害影响。COPD+HFrEF的COx损害是否与单独HFrEF不成比例还有待证实。
总之,本研究提供了新的证据,表明HFrEF共存会损害中重度COPD患者运动时的脑氧合(和脑血流)。有必要进一步研究这是否有助于快速增长的COPD+HFrEF重叠患者群体的运动不耐受及其对预后、治疗和康复的临床意义。
脚注
利益冲突:未申报。
- 收到了2013年5月28日。
- 接受2013年7月7日。
- ©2013人队