文摘
Tiotropium Respimat会增加死亡风险。第一个不伤害。Tiotropium Respimat不应规定在慢性阻塞性肺病http://ow.ly/mzPGL
系统的评论和随机对照试验的荟萃分析药物提供一个高水准的证据通知临床实践,并可以被认为是“黄金标准”来评估治疗的风险/收益(1,2]。三个系统评价和荟萃分析(包括Cochrane综述)的随机安慰剂对照试验tiotropium Respimat,每个使用不同的方法,展示了一个死亡的风险增加50%,它的使用对慢性阻塞性肺病(COPD)患者(3- - - - - -5]。这些分析提供实质性证据表明tiotropium Respimat增加死亡率治疗慢性阻塞性肺病(6,7]。是信息审查每一个系统的评论和问题提出了相关的解释。
2011年,英国医学杂志(BMJ)发表的第一个系统回顾和荟萃分析,包括所有与这些相应平行的组织、随机、安慰剂对照试验tiotropium Respimat治疗慢性阻塞性肺病的报告数据对死亡率和至少30天的时间(3)(表1(8- - - - - -10])。五个试验包括在分析中,两个12周试验和三个12个月的试验,研究6522名参与者。所有五个试验被认为是低风险的偏见。Tiotropium Respimat显著增加全因死亡率的风险,相对风险为1.52 (95% CI 1.06 - -2.16)。对全因死亡率有明显的剂量反应影响,RR 1.46 (95% CI 1.01 - -2.10)和2.15 (95% CI 1.03 - -4.51),分别5-μg和10-μg制剂(图1)。整体估计没有显著改变了敏感性分析使用随机效应模型,限制1年时间的分析三个试验周期,或加入更多的初步数据tiotropium Respimat从一个未发表的研究。社论计算,基于这些数据,预计一个超额死亡每121 5μg患者(COPD)剂量的tiotropium Respimat 12个月(11]。
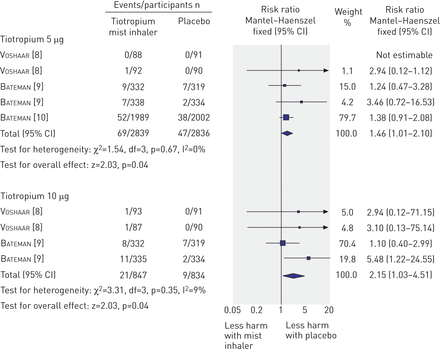
荟萃分析的全因死亡率的风险tiotropium交付的Respimat软雾吸入器(5μg或10μg)出版,随机,安慰剂对照试验的慢性阻塞性肺疾病患者。从[复制和修改3与出版商的许可)。
2012 Cochrane tiotropium回顾包括相同的五个随机安慰剂对照的临床试验tiotropium Respimat,但皮托方法用于集中优势比估计,这可以说是更适合的结合分析罕见的事件,如死亡(4]。Tiotropium Respimat显著增加死亡的风险,或1.47 (95% CI 1.04 - -2.08)。相比之下没有增加死亡率的风险与tiotropium HandiHaler,或0.92 (95% CI 0.80 - -1.05)。
2012年胸腔发表了一篇系统综述直接比较和混合治疗比较随机对照试验的荟萃分析的药物用于治疗慢性阻塞性肺病,提供数据整体或心血管死亡,和在试验持续时间至少6个月5]。直接比较分析,tiotropium Respimat增加死亡的风险与安慰剂相比,或1.49 (95% CI 1.05 - -2.11)。心血管死亡风险更高,在严重的慢性阻塞性肺病患者和更高的剂量。Tiotropium Respimat也增加了死亡的风险与其他常用的吸入治疗慢性阻塞性肺病的相比,包括Tiotropium HandiHaler,或1.65 (95% CI 1.13 - -2.43)、长效β-agonists,或1.63 (95% CI 1.10 - -2.44),和长效β-agonist /吸入激素联合治疗,或1.90 (95% CI 1.28 - -2.86)。
已经有10个重要问题与解释这些系统评价和荟萃分析,它们是基于个人的研究。
的有效性分析
勃林格殷格翰集团提出,tiotropium临床试验项目的赞助商和制造商的tiotropium Respimat和HandiHaler产品,替代死亡风险的估计,不具有统计学意义,可以通过承担多个基于不同死亡率数据集的“敏感性分析”(12,13]。然而,一致的发现风险显著增加的死亡率与tiotropium Respimat三,获得的独立,荟萃分析更可能是有效的。
死亡率的分析
已经提出,分析死亡率是不合理的,因为它不是主要终点的临床试验,因此,应被视为存活率存在(14]。然而,这种观点是有缺陷的(15]。死亡引起的处理显然是一个关键的二次结果与患者和临床医生,有一个强大的先天的原因调查死亡率由于最初的临床试验项目,建议ipratropium溴和tiotropium可能增加死亡的风险16]。死亡率的报告是强制性的(17),死亡率可以可靠地、客观地验证,没有方法论的理由驳回的发现。弱的论点是,选择不同的端点在二级分析可能膨胀I型错误率在一个相对有限的数据集。然而,这个问题适用于多个敏感性分析基于不同数据集的死亡率(12,13),而不是死亡率的主要分析作为独立进行荟萃分析。死亡是一个重要的不利结果,COPD是一种常见的疾病,考虑死亡率的研究是至关重要的在确定这种药物的风险/收益。
全因死亡率和死因别死亡率
的批判,死亡的原因是多样的12]是弱的,因为这是全因死亡率的本质。先前的研究已经表明,分配的死因tiotropium不是简单的在临床试验中,“全因死亡率比死因别死亡率可能是一个更强的端点,因为诊断的不确定性(18]。尽管如此,这两个BMJ和胸腔系统评价发现心血管死亡的风险增加tiotropium Respimat与安慰剂相比,RR 2.05 (95% CI 1.06 - -3.99)3),或1.96 (95% CI 1.07 - -3.60)5),分别。这双重的增加心血管死亡率约占一半的全因死亡率的增加。
不平衡的随机
死亡率的增加的批判tiotropium Respimat可以归因于异常低的死亡率在安慰剂组的这些试验(19),精心设计的有效性,进行了挑战,随机,安慰剂对照试验。系统在所有五个随机临床试验的失败,提供证据基础,是极不可能的。无论是tiotropium Respimat和安慰剂组在所有试验(类似的基线特征表1)有足够的在随机分配隐藏3,4]。
更高的提取率与安慰剂
这种潜在的偏差最小化了审判人员采取了措施以确定所有随机患者的重要地位,即使他们已经停止治疗,从而实现几乎完全捕捉死亡率的结果(3]。例如,在最大的1年期研究的重要地位是已知为≥99%的随机患者死亡的主要分析计划年底治疗期(337天)(10];在其他两个1年的综合分析研究,重要地位以97.7%的随机患者死亡的主要分析计划年底前30天的治疗和随访观察期间(366天)(9,20.]。
包含10μg数据
建议10μg数据不应包括在荟萃分析,因为tiotropium Respimat不是销售在这个剂量(12)与Cochrane手册建议所有治疗手臂的合并到一组(21]。重要的是它提供的证据可能存在剂量-反应关系tiotropium Respimat和死亡率,这进一步支持因果关系。包含数据的高剂量的研究也与肾功能损害患者,因为tiotropium肾排泄和血浆浓度在两个更高的严重肾功能损害(22]。尽管如此,两个荟萃分析,报告上的数据仅5μg准备,都增加了死亡的风险为1.46 (95% CI 1.01 - -2.10)3)(图1)和1.46 (95% CI 1.01 - -2.14)5),分别和5μg剂量也与心血管死亡的风险增加有关,或2.18 (95% CI 1.15 - -4.41)5]。
低估的风险
风险的估计从tiotropium Respimat研究项目很可能低估了实际死亡率的风险在一群没有选择的COPD患者心血管疾病。在这方面,最大的排除标准tiotropium Respimat研究包括最近的历史不稳定心律失常,心肌梗死或心脏衰竭需要住院10),从而明确保证排除患者心血管死亡的风险最高。心血管并发症的重要性确定这种风险中说明了美国食品和药物管理局(FDA)的这项研究中,即使排除这样的高危患者,那些基线心脏病或心脏节律障碍的历史有一个明显的风险增加心脏死亡的5μg tiotropium Respimat, RR 4.03 (95% CI 1.15 - -14.13)和8.61 (95% CI 1.10 - -67.23),分别为(20.]。
微分与tiotropium产品风险
的科克伦(4),胸腔(5]荟萃分析没有报道的影响tiotropium HandiHaler死亡风险,和死亡风险之间的显著差异HandiHaler Respimat吸入器。有人建议,这种差异可能削弱死亡风险的证据tiotropium Respimat [12]。至少有三种可能的解释,可能占微分tiotropium的两个配方的风险。首先,吸入5μg 10μg剂量的tiotropium从Respimat设备可能导致系统性接触tiotropium大于18μg剂量从Handihaler设备。在药代动力学研究中,高两到三倍的峰值和稳态血浆浓度已被证明与相比10μg剂量Respimat 18μg tiotropium HandiHaler剂量,而6 - 35%和5μg剂量浓度更高通过Respimat[那么明显23,24]。
第二个可能性是,tiotropium Respimat研究可能是更有可能包括病人和tiotropium风险增加,尤其是与已知的心脏节律障碍(7]。这个问题已经被证明很难评估,由于排除标准的明显不一致报告赞助商未发表的研究之间的协议,注册协议和公开的出版的手稿tiotropium Respimat研究。此外,COPD人群筛查纳入研究中心可能会有差异,和包罗万象的排除标准,如“病人的疾病,可能使他们处于危险境地,因为研究参与“调查员解释敏感,导致选择偏差可能很难确定事后,使它很难确定哪些患者被排除在外7]。然而,支持这种可能性,数据提交给FDA (25)表明,心脏节律疾病史患者更有可能参加的主要tiotropium Respimat研究[10),比主要tiotropium Handihaler研究[26),(11.8%与6.8%,分别RR 1.72 (1.54 - -1.96))。
第三种可能性是,抗菌剂的反复接触低浓度苯扎氯铵包括一起稳定剂乙二胺tetra-acetic酸(EDTA) tiotropium Respimat,但不是HandiHaler设备,可能导致不良反应(27]。苯扎氯铵支气管收缩的特性,作为支气管收缩的少只有7.4倍强大比组胺受体激动剂(28- - - - - -30.]。此外,暴露于苯扎氯铵是一种公认的引起职业性哮喘的31日- - - - - -33]。安慰剂Respimat管理解决方案包含苯扎氯铵的浓度μg·100毫升−1引起支气管收缩用力呼气量下降在1 s (FEV1从基线)≥15%在COPD患者(4.3%的场合34]。虽然这支气管狭窄与tiotropium纳入预防Respimat解决方案包含苯扎氯铵它显示了急性呼吸道慢性阻塞性肺病(苯扎氯铵的潜在影响34]。重复政府的长期航空公司影响苯扎氯铵和EDTA在COPD并没有被研究过。
生物合理性
在生物学上是有道理的,吸入抗胆碱能药物pro-arrhythmic效果,已与心脏死亡的风险增加(35]。其重要性也建议增加的死亡风险的观察tiotropium Respimat患者存在心脏节律障碍的历史而非冠状动脉疾病(20.]。生物合理性也观察到建议的溴化ipratropium增加心血管疾病的风险,从而表明风险的增加可能代表一个类吸入抗胆碱能药物的效果。这是最初观察到肺部健康调查中,经常使用的溴化ipratropium通过计量剂量吸入器心血管死亡的风险增加,RR 2.57 (95% CI 1.12 - 6.62)36]。Ipratropium溴化也指出增加住院的风险由于心律失常与室上性心动过速的患病率相对较高。随后,系统回顾和荟萃分析的五个试验,包括6155例,报告说,ipratropium溴化的风险增加的主要复合终点心血管死亡、心肌梗死或中风,RR 1.70 (95% CI 1.19 - -2.42)16]。
Generalisability
发现的generalisability临床实践显示,最近的一项研究从荷兰全科医师的数据库(37]。使用tiotropium Respimat增加死亡的风险,风险比为1.27 (95% CI 1.03 - -1.57)与心血管和脑血管死亡的风险最高,人力资源1.56 (95% CI 1.08 - -2.25)。风险存在于患者心血管疾病共存,人力资源1.36 (95% CI 1.07 - -1.73),而不是病人,人力资源1.02 (95% CI 0.61 - -1.71)。这个扩展的死亡率从随机安慰剂对照试验发现现实世界非实验研究提供了证据的一致性影响不同的研究设计。
结论
总之,这三个系统评价和荟萃分析的随机安慰剂对照试验,由独立组调查人员使用不同的方法,提供1级+科学证据进行荟萃分析的随机安慰剂对照试验(低风险的偏见),tiotropium Respimat会增加心血管疾病的风险和全因死亡。提出否则挑战国际公认的循证医学的原则。在缺乏证据的临床效益与tiotropium Respimat相比tiotropium HandiHaler [38),建议可以5μg和10μg准备tiotropium Respimat不应规定治疗慢性阻塞性肺病(6,7]。
脚注
利益冲突:披露可以找到与本文的在线版本www.www.qdcxjkg.com
- 收到了2013年3月7日。
- 接受2013年4月14日。
- ©2013人队















