到编辑:
我们报告患有肺鳞状发育性病变的患者,在计算断层扫描(CT)上看起来是纯地玻璃不透明度(GGO)。
在一个从未吸烟的61岁女性的一名61岁女性的年度健康检查期间,在左下肺中留下了不含15毫米的结节性病变。体检和实验室研究结果不起眼。胸部CT在左肺的下叶中展示了一个偏向的纯GGO结节。结节,测量为15×13mm,位于前置基底段(S8)(无花果。1A)。正电子发射断层摄影扫描显示出病变中没有放射性的积累。用淋巴结取样接受左肺的S8分段切除术。
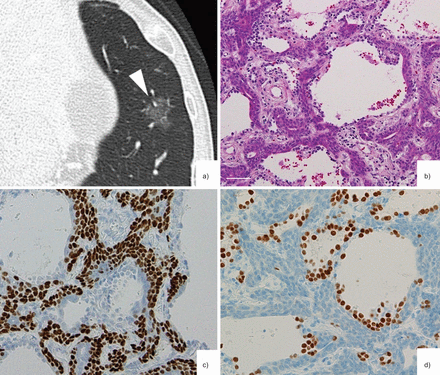
a)胸部计算机断层扫描(CT)显示左肺的前型基底段测量15×13mm的顺利划分的纯地玻璃透明度结节(箭头)。b)多边形细胞沿着肺泡壁存在,但是肺泡结构被保存(氧毒素和eosin; Scale Bar =100μm)。c)P63的免疫组织化学染色。非典型细胞对于p63是阳性的。d)TTF-1的免疫组织化学染色。非典型细胞对于TTF-1是阴性的。上皮细胞,TTF-1的阳性,覆盖了非典型细胞。
组织学检查证明了一种偏向的鳞片生长模式,类似于支气管肺泡癌(BAC),其中非典型电池沿着肺泡壁增长,保留肺泡架构。在检查整个样本的情况下,观察到肺泡结构和空气空间被保存在结节的所有区域中,并且与在CT上观察到的纯GGO相关的组织学外观。它们涉及肺泡壁并连续开发到支气管。在高倍率视图中,具有非典型核的多边形细胞,其在肺泡上皮细胞层和肺泡基底椎板层之间增殖(无花果。1B.)。由不同的细胞内桥梁表现出鳞状分化。通过免疫组织化学染色,非典型细胞对于P63,CK5 / 6和DESMOCOLIN-3为阳性,并且对于TTF-1是阴性的,表明鳞状分化(无花果。1C和D.)。在计数至少1000克癌细胞核后,作为癌细胞中的Ki-67阳性细胞百分比计算的增殖指数为7.9%。基于这些发现,我们被诊断为这种病变作为鳞状发育不良。EGFR.和克拉斯使用先前描述的智能AMP2方法在从手术切除组织中提取的DNA中评价突变[1]。EGFR.和克拉斯未检测到突变。
这种情况显示了CT上的纯GGO。术前,GGO被认为是BAC或非典型腺瘤增生(AAH)。病理学上,多边形电池沿着肺泡壁扩散,显示与BAC或AAH类似的鳞片生长模式。然而,由于细胞内桥的存在,鳞状细胞分化是显而易见的。对于P63和CK5 / 6的TTF-1和阳性染色的负染色的组合支持鳞状细胞分化的诊断[2],[3.]。考虑到这些免疫反应的形态,确认了鳞状发育不良的诊断。
GGO结节最常代表BAC,且较少频繁的其他病变,如AAH,淋巴抑制性疾病或组织肺炎或纤维化[4.]。从未报道过鳞状发育不良的GGO结节。鳞状发育不良通常在中央气道的上皮中发现,这难以放射性地检测,并且被认为是导致鳞状细胞癌(SCC)的枝形病变。相比之下,周围肺中鳞状发育不良的报道很少及其与SCC的相关性未知。
关于SCC,先前讨论了外周病变的发展[5.] - [7.]。在肿瘤的边缘,已经认识到肺Sccs沿着肺泡壁发育。D.ingermans.和M.oii.[5.[通过电子显微镜证明SCC沿着肿瘤周边沿着肺泡隔膜开发的SCC。T.okuda.[6.通过光学显微镜观察确认了类似的发现,并描述了外周SCC亚组,其中癌细胞沿肺泡壁扩散并在基础膜和上皮细胞之间增殖。在k的报告中Obayashi.等。[8.]在大多数肿瘤的大多数部分中观察到沿着肺泡壁的外周SCC发育,显示CT上的混合GGO外观。与这些外周SCC一样,在这种情况下的病变沿着肺泡壁开发,并且在肺泡上皮细胞层和肺泡基底层之间增殖。然而,非典型细胞没有侵入性,导致肿瘤发育不良,而不是癌症的诊断。因此,纯GGO的放射性发现代表了非侵入性病变。这些特征旨在提示肺的外周SCC的前体病变。
与人类相比,毒素暴露后靶向靶肺病变常常发生[9.],[10.]。通过暴露于颗粒材料的高负担(例如滑石,石英或柴油)引起的肺泡区域中产生的肺鳞状细胞型已经描述了[9.]。二恶英和二恶英的化合物摄入也诱导病变,例如支气管元细胞瘤和上皮的鳞状细胞鳞状[10.]。这些鳞状病变被认为是对毒素的常见反应;但是,SCC的发病率低[10.]。在目前的情况下,没有关于暴露于毒素的证据,例如专业暴露于颗粒材料或二恶英污染的食物摄入量;因此,病变的发病机制仍不清楚。
总之,这种极其罕见的案例是肺部外周鳞状发育不良的第一个报告,其作为CT上的纯GGO并沿着肺泡壁开发。
脚注
兴趣表
没有宣布。
- ©2013年