抽象的
耐多药结核病(TB)威胁结核病控制全世界。显微镜观察药物敏感性(MODS)测定法是一种低成本,高性能的TB诊断的快速液体培养和直接异烟肼和利福平药敏试验(DST)的工具。这项研究的目的是探讨了潜在的扩展MODS法快速二线DST,并确定候选药物临界浓度为未来的测试。
根据标准化的MODS协议,对接受二线结核药物治疗的94例结核培养阳性患者的痰标本进行培养,并添加一系列抗菌药物滴定。使用改进的Kaplan-Meier生存曲线分析确定临界浓度。
确定培养基临界浓度(10μg·ml-1)、环丙沙星(1.25 μg·mL-1)、环丝氨酸(40 μg·mL-1)、乙胺丁醇(10 μg·mL .-1),乙酰胺(5μg·mL-1)、卡那霉素(5 μg·mL .-1),对氨基水杨酸(10μg·ml-1)和链霉素(10μg·ml-1). 未确定其他二线药物或吡嗪酰胺的临界点。
在某些二线结核病药物的特定浓度下,这种新的Kaplan–Meier分析清楚地区分了易感或耐药人群。这些候选临界浓度现在应该在一系列流行病学环境中进行测试,以确定直接二线结核病DST和MODS的性能,从而提供潜在的低成本二线结核病DST容量。
超过170万人死于结核病(TB),每年死亡的传染病在世界上领先的原因固化[1].在资源有限的环境中,结核病的影响最大,在这些环境中,穷人遭受的痛苦更大。尽管在实现联合国千年发展目标和遏制结核病伙伴关系确定的目标方面取得了进展,但扩大强大的结核病诊断能力仍然是一项挑战[1那2].
耐药结核病威胁到TB Control [1那2].在全球范围内,耐多药结核病的负担估计有44万例,在58个国家发现了广泛耐药(XDR)结核病[1那2].XDR-TB率的估计是,部分地通过药物敏感性试验(DST)二线结核病药物的可用性的限制。然而,XDR-TB占前苏联和南非,XDR-TB-HIV双重感染的潜在破坏性影响已被证明[耐多药结核病例> 10%2-6.].
XDR-TB的出现是编程失败的间接指示,以充分诊断和治疗MDR-TB [7.].需要在资源限制的设置中可靠且经济有效地执行的快速第二行DST的可用性,以解决这一威胁[8.那9.].非专用显微镜观察药物易感性(MODS)测定,用于液体培养的TB的液体培养检测的高性能诊断技术和MDR-TB的直接DST,具有潜力解决这种需求。在秘鲁发展,MODS已被证明是ISoniazid和利福平DST的快速,可靠,低成本的方法,但研究尚未评估二线药物直接DST的性能[10].另外,在乙胺醇(EMB),链霉素(STM)和吡嗪酰胺(PZA)DST中的数据未能清楚地表明所用药物浓度的高性能[10-12].
对于这三种药物和二线剂直接DST的MOD性能的评估将需要大型前期的多期面研究,将MODS与现有参考标准进行比较,在一系列流行病学环境中。由于MODS是一种直接药物敏感性测试,所以需要使用新鲜的痰样品进行评估,而不是储存菌株的储存菌,具有已知的DST型材。为了设计这样的试验,必须首先为每种药物定义候选临界浓度,这是本研究的主要目标。使用接收器操作曲线(ROC)方法[13]和一种新的Kaplan–Meier生存曲线分析,我们旨在探索每种受试药物的大范围浓度的抑制能力,并确定参考标准中定义为易感或耐药菌株的MODS浓度。因此,可在如上所述的较大试验中前瞻性地评估确定的候选临界浓度。
材料和方法
场的方法
候选人参与者从秘鲁Instituto Nacional de Salud(INS; Lima,Peru)的数据库中确定了纳入的数据库,并选择包含在预定接受特定的MDR疗法,最新的痰培养是阳性和抗性的先前展示了二线剂。同意参与者提供了≥5毫升的痰样品,该样品被转移到Lima的秘书处秘书处Cayetano Heredia(UPCH)实验室,其中储存冷藏和加工,一般在收集24小时内。
实验室方法
痰标本按照MODS方法处理[14[含有七种不同浓度的辣椒霉素(帽),环霉素(CS),胚胎,乙酰胺(ETO),卡那霉素(KM),氨基水杨酸(PAS),PZA和STM,均氨基甲酰胺(C帽),环晶素(CS),甲酰胺(CS),氨基胺(KIM),PZA和STM。痰样品被NaOH-净化污染N- 乙酰 -L.-半胱氨酸法,并在补充的Middlebrook 7H9肉汤(Becton Dickinson, Franklin Lakes, NJ, USA)中重建,如前面所述[15那16].将样品-肉汤混合物移入3个24孔板每孔540 μL。在一系列7孔中加入60 μL预配制的抗生素,以达到预期的井内抗生素浓度范围,第8孔为无药对照。
了在该研究中测试的抗生素浓度范围是基于以前的研究[13那17-24].下列范围进行了测试:CAP和ETO:0.3125-20微克·毫升-1;CIP:0.1567-10微克·毫升-1;EMB、KM、STM: 0.625-40 μg·mL-1;和PZA:12.5-800微克·毫升-1.早期实验表明需要将Cs和PA的上限增加到以下范围:CS:0.3125-20μg·mL-1初期5-320 μg·mL-1;不是:0.1567μg·-10毫升-1最初为0.625-40 μg·mL-1.由于PZA的活性依赖于酸性pH,所以PZA实验最初是在pH 6.8(与所有其他药物一样)和pH 6.0下进行的。然而,结核分枝杆菌在不含药物的孔中的生长通过较低pH值显著削弱。随后PZA实验仅限于pH值6.8。
如前所述,对接种的平板进行培养并检查其生长情况[11那25那26].一旦TB的增长是在一个无毒品以及观察,检查了所有其他的井。在污染或不一致的生长的情况下,原来的样品再次净化和再培养。结核分枝杆菌使用spoligotyping或PCR [确认27].不一致增长被定义为结核分枝杆菌具有更高的药物浓度的生长良好,而不是井显示出没有增长。分离株通过秘鲁国家分枝杆菌参考实验室(INS,LIMA)的比例方法来派遣参考和二线DST。
统计分析
使用Stata9.1®(Statacorp,College Station,TX,USA)和Excel 2003(Microsoft; Microsoft Corp.,Redmond,Wa,USA)进行分析数据。使用比例法作为参考的比例方法计算不同浓度的敏感性和特异性。从该数据构建ROC曲线。使用增加的药物浓度来进行Kaplan-Meier存活分析代替通常的时间变量。每个系列的存活失败事件是样品在所有较低药物浓度下产生阳性培养的重点,但浓度不高。在该点被审查了最高药物浓度的增长系列。从分析中扣留了由于临界浓度不一致或污染而没有遵循这种模式的个体药物浓度系列。通过识别曲线的快速灭菌阶段和曲线的稍后稍后部分之间的接合点,从Kaplan-Meier生存曲线中选择每个药物的临界浓度。未遵循预期模式的曲线通过氨胺涂片状态和比例方法阻力分层。比较ROC和存活分析的结果,以确定最合适的候选临界浓度。
伦理审查
UPCH机构审查委员会(利马)批准了研究方案和知情同意书,秘鲁卫生部利马的国家结核病控制计划也获得了技术批准。
结果
研究人群基线特征
从秘鲁国家结核病控制规划的多药耐多药技术股(UT-MDR)数据库和秘鲁国际结核病研究所确定的115名患者同意参加,并能够提供足够的样本进行检测。其中94例MODS培养阳性,65%也是金胺涂片阳性。按比例法确定的单一样本中耐药的药物数量为3 - 9种,平均每个样本对6种药物耐药(表1);88(94%)样本为耐多药。
一个增长的94个样本结核分枝杆菌对它们进行了822次稀释系列,包括因污染和药物浓度改变而重复稀释。在稀释系列中,25(3%)不包括在生存分析中,因为由于生长不良或污染,它们被认为是不确定的。获得了85个(90.4%)样品中所有9种药物的完整药物滴定系列数据。总共培养了7293个MODS孔,其中54个(0.7%)因污染而无法读取。
ROC曲线
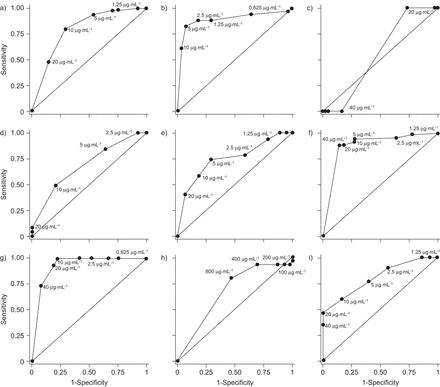
使用比例法的结果作为参考标准,ROC曲线推导出每种药物(图1).对于CIP、KM和PAS,而不是其他药物,在(比例法确定的)耐药检测中,可以确定具有良好敏感性和特异性的单一药物浓度。因此,ROC曲线在确定临界浓度方面的作用有限。
接受器工作特性曲线a)卷曲霉素,b)环丙沙星,c)环丝氨酸,d)乙胺丁醇,e)乙酰胺,f)卡那霉素,g)对氨基水杨酸,h)吡嗪酰胺和i)链霉素。最靠近左上角的曲线表示可能存在的MODS(显微镜观察药敏)药物浓度,对该药物的耐药检测具有较高的敏感性和特异性。
Kaplan-Meier生存曲线
CIP,CS,EMB,KM和PAS的Kaplan-Meier生存曲线(图2)遵循预期的S形曲线,在低药物浓度下几乎没有生长抑制,随后在可能药物敏感的情况下生存概率急剧下降结核分枝杆菌被杀死,结束耐腐蚀,在耐药物能够以更高的药物浓度存活。候选临危药物浓度(表2)直接从这些曲线中取出。Auramine痰涂片状态的分层未显示出任何这些药剂的曲线形状的任何可辨别差异(数据未示出)。
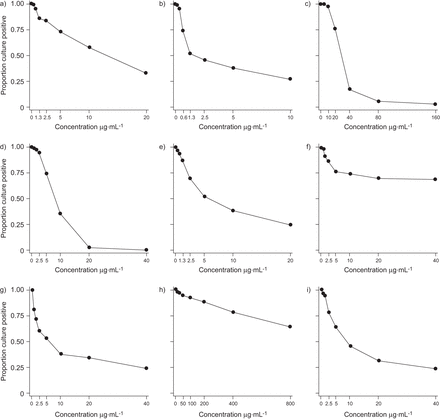
一个)卷曲霉素,b)中的环丙沙星,C)丝氨酸,d)乙胺丁醇,E)ethionamide药物,F)卡那霉素,克)对氨基水杨酸:为培养阳性的在增加药物的浓度存在的比例的Kaplan-Meier存活曲线,h)的吡嗪酰胺和i)链霉素。
相比之下,eTO和STM的Kaplan-Meier生存曲线响应于分别考虑涂片阳性和涂抹阴性样品时的药物浓度增加而响应差分动力学(图3),而涂片阳性样本需要更高的药物浓度来抑制生长(但涂片阳性级别的增加没有增加效应;数据未显示)。所有其他药物均以这种方式分层,但涂片状态未见影响。为这些药物选择的候选临界浓度(表2)由涂片阴性曲线确定,以尽量减少涂片阴性耐药样本的误分类。
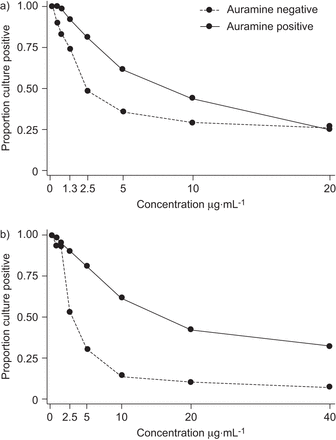
Kaplan-Meier存活曲线由AuRamine涂抹状态分层A)乙醇胺和B)链霉素。
对于CAP,药物浓度与培养阳性概率呈线性关系(图2).亚分析通过比例法分别评估易感或耐药样本,然后根据涂片状况进一步分层,如图所示图4.所有其他药物均按此方式分层,但涂片或耐药状态未见影响。在按比例法指定为易感的样本中,似乎有一个亚群体,该患者队列中约25%的毒株能够抵抗高浓度的CAP (>10 μg·mL)-1在插件)。
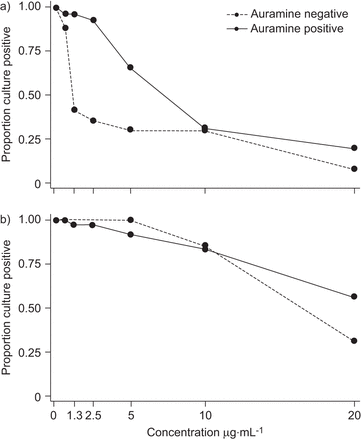
按比例法分为a)敏感菌株或b)耐药菌株,并按涂片情况分层的卷曲霉素样本Kaplan-Meier生存曲线。
PZA的Kaplan-Meier生存曲线显示对药物浓度增加有有限的线性响应。通过涂片状态和/或比例方法进行分层并不能提高区分不同易感性人群的能力。
从这些曲线中得到的候选临界浓度,以及使用这些浓度与本研究中比例方法的MODS的一致性显示在表2.除了EMB、STM和埃托奥,性能差,PZA,候选人的临界浓度可以导出,直接插件的和合二线DST使用方法DST候选人浓度和比例> 75%所有代理测试,并为公里高达89%。
讨论
这些数据表明,目前需要在多种不同流行病学情况下进行前瞻性评估的候选临界浓度,可以在MODS分析中获得大多数二线抗结核药物的临界浓度。结果扩大了MODS的范围,使用以下浓度的其他几种试剂:CAP: 10 μg·mL-1; CIP:1.25μg·mL-1;CS: 40μg·毫升-1;EMB: 10μg·毫升-1;ETO:5微克·毫升-1; KM:5μg·mL-1;PAS:10μg·ml-1STM: 10 μg·mL-1。由于鉴定的耐药菌株数量有限,CS的临界浓度应被视为初步浓度,而PZA的浓度不合适。
这项研究的一个重要的强度为临床痰样品的患者变量曝光历史二线剂和充分表征的DST型材,包括MDR试样的比例很高的可用性。使用临床样品,而不是菌株是直接DST方法和研究(多药耐药的二线药物暴露)的患者组重要的恰恰可能由MODS二线DST是其提供有针对性第一临床组。然而,由于样本显示耐药性相当高的水平,现在还不能确定是否这里描述的临界浓度是相关的较低水平阻力的样本。与展示出一种较低程度的阻力菌株进一步测试将增加在该研究中表现出的结果的普适性。此外,19例谁是在UT-MDR数据库培养阳性被抽样这项研究之前,发现采样培养阴性,可能是由于治疗,谁被报道了6例患者有MDR-TB的UT-MDR数据库被发现没有时的比例方法后来被用于确认电阻图案利福平抗性。现在还不能确定这种差异是否是由于在应变电阻,或实验室变异性的变化。
这些研究数据是及时的,因为在这个时代滚出去利福平耐药的分子检测的有可能是表型二线DST日益增长的需求;这是目前仅限于分枝杆菌生长指示管(MGIT; Becton Dickinson公司)培养和药敏试验,这是昂贵的,基本上只能在国家参比实验室水平。尽管通过的Xpert MTB / RIF,在GeneXpert平台(造父变星,Sunnydale,CA,USA)提供了相当大的希望的未来,更广泛的分子DST用利福平DST补救的暂时困难。然而,许多这些药物(包括异烟肼)的阻力是复杂的,有一个庞大而重要的知识差距,认识负责,每种药物的表型抗性的所有突变,提示分子检测单是不太可能在可预见的未来充分.如果MODS被证明是可靠的喹诺酮类和二线注射剂的DST,它将为寻求管理与利福平和/或异烟肼耐药性鉴定患者越来越多的结核病实验室网络的另一种替代选择。
比例方法定义的对单个二线药物的耐药性从未被证明与临床失败有关,这样的结果数据可能仍然是一个难以实现的目标。比例方法的截止点是通过比较来自没有或广泛治疗的患者与感兴趣的药剂的菌株的增长。比例法还允许某些杆菌在被测试药物存在的情况下突破性生长;如果这些细菌在所有细菌中所占比例小于1%,则该样品将被指定为药物敏感,前提是这些残留的细菌将被其他药物消毒[28那29].mods没有提出这个假设;任何生长都被认为是阳性的,因此抵抗药物。
因为这些缺点在假定的参考标准,用于确定第二行的结核分枝杆菌药敏方法之间的耐药状态和高度可变性[24那30.-34],我们使用改进的生存分析来检查样本中菌株对MODS分析中药物浓度增加的反应。这使我们能够根据细菌对药物浓度的反应,在视觉上区分不同的细菌种群,从而给出临界浓度的上下文,而不是与其他不完善的药物敏感性试验进行潜在缺陷的比较。然而,值得注意的是,即使在区分种群时,临界浓度的选择也取决于观察者的视角。在这项研究中,我们通常选择较低的药物浓度,以确保对药物滴定有中间反应的菌株被认为具有耐药性,从而将无效治疗的风险降至最低。
使用生存分析,我们也能够检查的金胺涂片状态的临界浓度的影响。这是重要的,因为,作为一个直接的测试,也没有在MODS接种量的控制。利福平和异烟肼现在这已经多次被证明是没有重要性,但同样没有为其它代理先前已知的。在这里,金胺状态对CIP的,CS,EMB,KM和PAS,因此对于选择的临界药物浓度不影响生存曲线的整体形状影响不大,因为先前已经证明了利福平和异烟肼DST [11].相对于基因型®MTBDRplus (Hain Lifescience, Nehren, Germany)等分子工具,这可能提供了重要的比较优势,后者迄今只验证用于涂片阳性样本。然而,金胺涂片状态确实对CAP、ETO和STM有影响。对于这些药物,选择的临界浓度主要是基于金胺阴性曲线,以尽量减少耐药菌株因痰标本中分枝杆菌计数低而被误分类的机会。
尽管我们的确定临界浓度的方法不涉及直接比较通过比例法确定的电阻,但两种方法之间通常可以看到高度的协议(表2)这与ROC曲线比较的结果一致(图1).
EMB和STM的MODS和比例法DST结果一致性较差。然而,在检测这些药物时,比例法与较新的DST方法的比较往往显示一致性差,且研究之间的差异很大,这导致了对较新的试验中使用的建议最低抑菌浓度的多次修订[35].已在MGIT960平台的研究表明灵敏度,用于检测由电阻为63-100%EMB的比例的方法所定义,与灵敏度,用于检测的77-100%STM电阻[5.那24那31].类似的结果已被观察到BACTEC 460(Becton Dickinson公司)与敏感性抗性通过的25-91%为EMB比重法和51-95%为STM [限定5.那12那24那31那32].对于Mod的比较EMB和STM具有更可靠的自动化DST系统可能需要进行验证本研究中发现的最小抑制浓度。
PZA DST是有问题的,因为药物在酸性条件下激活,使酸性培养pH值是确定抗性表型的要求[36].作为与其它的培养方法[37那38],生长结核分枝杆菌在MODS中,即使不添加抗真菌药物,酸性条件(pH 6.0)也会抑制培养。当pH值为6.8时,细胞的生长情况要好得多结核分枝杆菌,但添加PZA似乎对区分药物敏感菌株和耐药菌株的作用不大。显然,需要进一步的工作来确定使用MODS作为PZA药敏试验的适当条件。
CS一直是一种困难的药物,用于在其他DST方法中找到临界浓度[17那39].最近一项试图对DSTs进行标准化的研究发现,使用Middlebrook 7H10琼脂或BACTEC 460无法找到CS可接受的临界浓度,比例法检测也不令人满意[39].在这项研究中,发现很少的分离物通过比例方法或MOD标准抵抗Cs,并且没有通过两种方法抵抗的分离物。然而,根据我们的生存曲线分析Cs,两种群体明确区分,其中一个可以受到Cs抑制的一种,尽管高浓度的CS浓度增长。这表明临界浓度为40μg·ml-1可能是一个合理的初步估计,也是进一步评估的起点。
总之,这项工作使用了一种新的生存分析方法来确定二线DST的候选临界浓度结核分枝杆菌使用快速、低成本、直接的DST MODS平台。我们能够使用改良的生存曲线来证明对药物浓度增加的不同反应,我们相信这是一个不偏不倚的耐药性评估。进一步的研究,也许与自动化系统的比较,将有助于:1)确认这里发现的结果;2)确定修改后的MODS培养条件是否允许PZA截止点的识别;3)进一步探索MODS与比例法一致性较差的药剂;4)扩大DST药物储备,包括更广泛的二线药物,如阿米卡星、左氧氟沙星、莫西沙星、利奈唑胺、阿莫西林-克拉维酸、delanamid和TMC207。
在这个耐多药/广泛耐药结核病发病率不断上升的时代,对负担得起、可靠的二线DST指导耐多药治疗的需求变得不可抗拒。目前,表型检测优于基因型检测,因为迄今为止,任何药物都不知道导致基因突变的全谱耐药性。MODS提供了一种高质量、可靠的表型检测的可能性,以一种价格合理、适应性强的形式进行。在具有一系列流行病学特征和药物接触史的不同研究人群中,使用这些临界浓度对二线DST的MODS性能进行前瞻性评估,将确定如何最好地使用这一快速、低成本表型DST工具。
致谢
我们要感谢所有研究志愿者,没有他们的参与,这项工作是不可能完成的。UPCH实地和实验室研究小组(秘鲁大学,秘鲁利马;P.纳瓦罗,V. Huancaré, S. Lopez, R. Limascca, F. Garcia和C. Solis),利马的秘鲁国家分枝杆菌实验室团队(L. Asencios, E. Leo和J. Ramírez)和结核病多药技术联盟(利马卫生部)工作人员(R. Jamanca, A. Crossa和A.M.为了确保研究的顺利进行,他提供了必要的后勤支持。
脚注
支持声明
这项工作从收到的财政支持威康信托基金会(grant 084550/Z/07/Z)董事倡议基金TDR(儿童基金会/开发计划署/世界银行/卫生组织热带病研究和训练特别方案)。S. Fitzwater的资助项目编号为T35AI065385国家过敏和传染病研究所.检察官j·摩尔得到了威康信托基金会.
兴趣表
没有宣布。
- 收到2012年4月10日。
- 公认8月2日,2012年。
- ©2013年