摘要
50多年来,葡萄糖被认为可以穿过肺上皮屏障,由肺上皮细胞运输。然而,直到最近,对这些过程的研究主要集中在它们对肺液量的影响上。在这里,我们考虑了一个新发现的肺葡萄糖转运在维持低气道表面液(ASL)葡萄糖浓度方面的作用,并提出这有助于肺防御感染。
葡萄糖扩散到肌萎缩性侧索硬化症通过细胞旁通路的速率由细胞旁通透性和经上皮葡萄糖梯度决定。葡萄糖在近端气道从ASL中去除通过促进葡萄糖转运蛋白,由细胞内葡萄糖代谢产生的浓度梯度下降。在肺远端,葡萄糖转运通过钠偶联葡萄糖转运蛋白占主导地位。这些过程因物种而异,但普遍保持ASL葡萄糖浓度比血浆低3 - 20倍。
ASL葡萄糖浓度在呼吸道疾病和高血糖时升高。重症监护患者ASL葡萄糖升高与血糖升高相关金黄色葡萄球菌感染。糖尿病患者有或无慢性肺部疾病,呼吸道感染的风险增加。了解肺葡萄糖稳态的机制,可以为控制ASL葡萄糖、预防和治疗肺部感染找到新的治疗靶点。
我们对葡萄糖转运在肺中的作用以及调节葡萄糖在人类肺上皮细胞中的运动的机制的理解远远落后于对肠道和肾脏的理解。自20世纪60年代中期以来,人们已经知道在肺中有能量依赖的钠偶联葡萄糖转运蛋白(SGLT)和能量不依赖的促进性葡萄糖转运蛋白(GLUT)途径来摄取葡萄糖[1],葡萄糖可渗透肺泡上皮屏障[2].然而,该领域的后续研究主要集中在肺SGLT转运作为肺液量调节剂的作用[3.,4],以及饥饿和糖尿病对葡萄糖转运的影响[1,5].直到最近,我们和其他人才开始研究葡萄糖转运作为维持肺腔内营养匮乏环境以限制致病生物生长的重要机制。
气道表面液葡萄糖浓度正常
在肺上皮细胞的液体(气道表面液体;ASL)高于血浆。这与肠道和肾脏的情况相反,后者的腔内葡萄糖浓度经常超过血浆葡萄糖浓度[6,7].在人类中,发现鼻ASL中的葡萄糖浓度<1 mM [8]和平均值±sd下呼吸道0.4±0.2 mM,比通常维持在~ 5 mM的血浆浓度低12.5倍[9].在灌注、液体填充的成年大鼠肺模型中,当灌注葡萄糖为10 mM时,ASL葡萄糖估计为0.5 mM [4].在妊娠122至143天的长期置管绵羊胎儿中,肺液葡萄糖<0.01 mM,血浆葡萄糖< 0.19 mM [3.].在体外在空气-液体界面上生长的抗阻力人肺上皮细胞单层的研究支持了这些在活的有机体内观察。在基底外侧培养基中加入10 mM葡萄糖的永生化人气道细胞(系H441)中,顶端ASL葡萄糖为0.24±0.07 mM [10].在人支气管上皮细胞(HBECs)的原代培养中,在基底外侧培养基中加入16.6±0.4 mM葡萄糖,ASL葡萄糖为2.2±0.5 mM [11].
确定asl葡萄糖浓度的过程
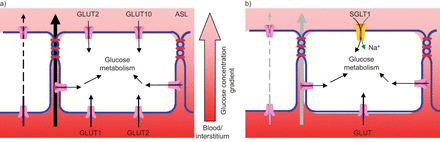
ASL葡萄糖浓度是葡萄糖从血液和间质液通过呼吸道上皮扩散到ASL,并通过上皮葡萄糖运输过程从ASL中去除的净结果。葡萄糖扩散由上皮细胞对葡萄糖的通透性、上皮细胞葡萄糖梯度和表面积决定。葡萄糖的去除是由细胞葡萄糖摄取和代谢决定的(图1) [4,12- - - - - -14].
目前控制气道和远端肺上皮表面液体中葡萄糖浓度的机制模型。a)在气道上皮细胞中,气道表面液(ASL)的葡萄糖浓度是血液和间质液通过呼吸道上皮细胞扩散到ASL的净效应(在较小程度上,是葡萄糖的跨细胞通量),以及葡萄糖被吸收到上皮细胞从ASL中去除。通过根尖膜的葡萄糖摄取由兼性葡萄糖转运蛋白(GLUT)2和GLUT10介导,通过基底膜的葡萄糖摄取由GLUT2和GLUT1介导。b)远端(肺泡)肺上皮细胞中,葡萄糖通过顶端膜摄取通过钠偶联葡萄糖转运蛋白(SGLT)1和基底外侧膜通过身份不明的过剩。
葡萄糖扩散到asl
葡萄糖从血液和间质液进入ASL的运动主要是通过细胞旁途径发生的。早期在活的有机体内研究发现兔呼吸道上皮和猪气管上皮具有通透性l-葡萄糖,葡萄糖的一种异构体,既不被运输也不被代谢。在大鼠肺部,用鱼精蛋白增加细胞旁通透性可增加腔内葡萄糖浓度[15,16].最近的研究表明l-葡萄糖,应用于在空气-液体界面的可渗透过滤器上生长的阻力性人气道上皮细胞单层的基底外侧,以时间和浓度依赖的方式移动到根尖室,与细胞旁扩散一致[10- - - - - -12].此外,顶端的外观l-葡萄糖随经上皮电阻的降低而呈指数增加[10,12].这些发现表明葡萄糖被动地在上皮细胞中扩散通过这一过程受上皮紧密连接对葡萄糖的渗透性和葡萄糖浓度梯度(图1])。
Paracellular通路
上皮细胞之间的紧密连接主要决定上皮细胞的渗透性[17].它们由跨膜蛋白组成,包括连接粘附分子、封闭蛋白(claudin)和闭塞蛋白(occludins),它们通过支架蛋白(如ZO蛋白)与细胞骨架蛋白相互连接。蛋白质成分及其定位有助于形成大小和电荷限制跨细胞扩散途径的不同群体。这些通道可大致分为孔隙型和渗漏型[18- - - - - -22].葡萄糖通过上皮紧密连接屏障的途径目前尚不清楚。
ZO-1、occludin和claudin是决定细胞旁通透性的主要连接蛋白[21,22].克劳丁是紧密结形成的关键,影响紧密结孔隙的路径和电荷选择性。在气道上皮细胞中,claudin- 1,3和5的差异表达改变了上皮对大分子的通透性。cladin -2对阳离子电导率很重要,但对甘露醇的通量没有影响(甘露醇的大小与葡萄糖相似)[23- - - - - -25].occludin的过表达增加了上皮细胞对小亲水分子的通透性,同时减少了离子运动[26].紧密连接通过肺上皮紧密连接调节葡萄糖运动的作用无疑是复杂的。然而,识别限制葡萄糖运动的蛋白质和信号通路可以提供潜在的治疗靶点,以降低ASL中的葡萄糖。
葡萄糖转运在限制asl葡萄糖中的作用
由于葡萄糖能够在气道上皮细胞中扩散,随着时间的推移,ASL葡萄糖可能会与血糖浓度平衡。由于事实并非如此,必须存在其他机制来从ASL中去除葡萄糖和/或限制扩散和跨细胞转运。在下一节中,我们将详述葡萄糖转运在肺上皮中的性质和作用。
葡萄糖转运蛋白
哺乳动物细胞膜上的葡萄糖转运是由促进性GLUTs(由SLC2基因家族编码)或SGLTs (SLC5基因家族)介导的。葡萄糖通过被动扩散沿己糖激酶(HKs)和葡萄糖激酶产生的浓度梯度通过GLUTs移动,葡萄糖激酶磷酸化细胞内葡萄糖。相比之下,sglt介导的转运是由钠和葡萄糖梯度驱动的,因此,可以逆其浓度梯度移动葡萄糖。
人类SLC2家族由14种编码葡萄糖转运蛋白的已知异构体(SLC2A1-14)组成,每种异构体具有不同的组织表达模式、底物(糖)特异性和转运动力学。根据其序列同源性,glut可分为三个不同的类别:I类包括特征良好的转运蛋白GLUT1-4 [28- - - - - -31]和GLUT14 (GLUT3的复制基因)[32];II类包括果糖转运体GLUT5 [33],及GLUT7 [34], glut9 [35]和GLUT11 [36];III类包括最近鉴定的转运体GLUT6 [33], glut8 [37], glut10 [38], glut12 [39]和质子驱动的人肌醇转运蛋白(GLUT13) [40].它们对葡萄糖的亲和性差异很大。GLUT2对葡萄糖的亲和力低于葡萄糖转运蛋白家族的其他成员(米凯利常数(K米)的~ 32毫米非洲爪蟾蜍卵母细胞)[41],而GLUT10的亲和力最高(K米~ 0.3 mM) [42].人类SLC5基因家族由11种亚型(SLC5A1 - 11)组成,其中SLC5A1 (SGLT1) [43]及SLC5A2 (SGLT2) [44]已知编码sglt。
GLUT-和sglt介导的葡萄糖转运在许多组织和细胞类型中都有很好的特征,尽管对它们在肺中的作用知之甚少。由于肺部葡萄糖转运的区域、物种和发育差异,对这一现象的理解非常复杂。
葡萄糖在气道上皮的转运
在人气道上皮(气管、支气管和细支气管)中,GLUTs是主要表达的葡萄糖转运体类型(表1而且2).GLUT10存在于永生的人气道上皮细胞中(H441) [10],并且在人支气管活检的H441的根尖和基底外侧膜以及上皮细胞中均检测到GLUT2蛋白[13].在原代培养的HBECs中,GLUT10存在于根尖膜,但GLUT1蛋白存在于基底外侧膜[11].在H441细胞单分子层中,根皮素(一种谷氨酸介导的转运抑制剂)抑制根尖葡萄糖摄取和增加的出现d-顶端隔室中的葡萄糖[12].在HBEC单层中,2-DOG (GLUT的底物,但不是SGLT的转运物)被带过顶端膜[11].综上所述,这些发现表明通过GLUTs的根尖葡萄糖摄取在维持低ASL葡萄糖浓度中起着重要作用。
由于GLUTs只将葡萄糖沿浓度梯度向下运输,这就提出了GLUTs如何保持低ASL葡萄糖浓度的问题。最近的研究提出了两种机制。首先,进入气道上皮细胞的葡萄糖代谢迅速[12].这将维持较低的细胞内葡萄糖浓度,为基底外侧和根尖膜的葡萄糖摄取提供驱动力。葡萄糖的快速代谢也将被预测限制葡萄糖的跨细胞运动,这可能发生在基底外侧到根尖的葡萄糖浓度梯度。其次,从基底外侧膜和细胞间隙摄取葡萄糖可以改变局部微域的葡萄糖浓度,并降低靠近细胞旁扩散路线的葡萄糖浓度梯度。为了支持这一点,基底外侧根皮素增加了极化H441细胞单分子层顶端室中葡萄糖的出现[12].在这种情况下,结合细胞旁和跨细胞葡萄糖运动将低于细胞葡萄糖摄取,从而产生低ASL葡萄糖浓度[11,12].我们还推测,不同的顶端和基底外侧GLUTs定位可能在调节这些顶端和基底外侧区域的葡萄糖摄取中发挥重要作用。例如,低K米GLUT10的含量较高K米在葡萄糖浓度较低时,GLUT1和GLUT2的s更倾向于从顶端侧摄取葡萄糖。这些结果表明,呼吸道上皮性GLUTs可能是促进呼吸道疾病中ASL葡萄糖耗竭的靶点。此外,可以设想,降低葡萄糖转运蛋白功能的基因突变可能导致气道葡萄糖稳态受损,并导致复发性肺部或上气道感染。
这两种假设都预测气道上皮细胞中的葡萄糖代谢是GLUT转运的关键驱动因素,也是ASL葡萄糖浓度的决定因素。一旦进入细胞,葡萄糖转化为葡萄糖-6-磷酸由HKs催化。由于葡萄糖磷酸化被认为是葡萄糖代谢的限速步骤[62,63]这可能是肺葡萄糖稳态的一个重要过程。HKI、HKII及HKIII已在大鼠肺中发现[52,64],而HKII则存在于人类肺部肿瘤和A549肺泡上皮细胞中[65,66].HK活性如何调节ASL中的葡萄糖摄取、经上皮葡萄糖转运和葡萄糖浓度尚有待探索。然而,可以推测,上调HK活性会增加葡萄糖摄取,降低ASL葡萄糖。已经有兴趣在己糖激酶活性的激活剂和抑制剂治疗糖尿病。这些酶也可能为治疗和预防与ASL葡萄糖升高相关的肺部疾病提供潜在的治疗靶点。
在人气道上皮中,钠偶联葡萄糖转运似乎无助于维持低ASL葡萄糖浓度。在人气道上皮中未检测到SGLT蛋白(表1).在安装于Ussing腔的人气管上皮中,短路电流(我sc)没有因管腔葡萄糖而增加,也没有因根菌素(一种SGLT抑制剂)而降低[11].根尖应用根菌素对葡萄糖摄取或代谢没有一致的影响我sc在人类细胞单层中。使用室内研究比较羊和人气管上皮(来自病变肺)显示根素产生了一个小的减少我sc在绵羊气道中(~ 5%),但在人体组织中无显著影响[67].
虽然GLUTs在气道表面上皮中主导顶端葡萄糖运输,但有一些诱人的证据表明,SGLTs可能存在于粘膜下腺(SMGs)中。在极化培养的浆液型SMG细胞(Calu-3细胞)中,根菌素(200 μM)的加入抑制了20%的基我sc,这可以通过从根尖浴液中去除葡萄糖来模仿[54],与这些细胞中存在的根尖钠偶联葡萄糖转运相一致[68,69].粘膜下腺是否存在sglt在活的有机体内仍有待测试,但鉴于缺乏功能性证据,到目前为止,它们似乎不太可能对气道葡萄糖转运有显著贡献(见前文)。
远端肺上皮细胞葡萄糖转运
在远端肺(肺泡)上皮细胞中,钠偶联葡萄糖转运似乎是根尖葡萄糖从腔内摄取的主要机制。由于尚未在人类远端肺上皮进行研究,因此对这一领域的了解来自动物研究。
已在成年大鼠远端肺上皮中鉴定出SGLT1 mRNA,但未鉴定出SGLT2 mRNA [55,60],以及小鼠和人类的全肺组织[49,56].Bodegaet al。[61]最近在大鼠和绵羊肺的I型和II型肺泡细胞中发现了SGLT蛋白。而在成年兔肺组织中未检测到SGLT1蛋白。在大鼠、兔和羊远端肺中,糖素可抑制SGLTs,从而阻止葡萄糖从管腔中去除[3.,4,70].sglt介导的转运已在新鲜分离的豚鼠肺泡II型(ATII)细胞中得到证实[70].在气道上皮细胞中,与ASL (~ 120 mM)或血浆(~ 140 mM)中的钠浓度相比,细胞内钠浓度较低(~ 23 mM) [71,72].SGLT利用这种钠梯度来推动葡萄糖从ASL(低葡萄糖)摄取到间质和血液(高葡萄糖),而不是其浓度梯度。
相比之下,很少有证据表明腔内谷氨酸介导的远端肺上皮转运。肺灌注的根皮素不抑制家兔葡萄糖或液体的吸收[15,73]或大鼠全肺[4],且胎羊肺很少有腔内2-DOG (GLUT-specific)摄取[3.].然而,根黄素和根黄素均抑制豚鼠肺分离的ATII细胞葡萄糖摄取[70],提示基底外侧膜可能存在GLUTs。
气道和肺泡上皮利用不同的葡萄糖转运机制的观察,导致了对不同肺区域顶端葡萄糖转运作用的推测。气道是抵抗感染的第一道防线,低ASL葡萄糖浓度的产生可能对维持气道无菌至关重要。在发生气体交换的远端肺,钠偶联葡萄糖转运可能是液体重吸收和ASL体积调节的重要驱动因素,产生低ASL葡萄糖浓度是次要的有益影响。肺上皮葡萄糖转运的发育变化也表明这些转运过程在胎儿和成人肺中的作用不同。
肺葡萄糖转运的发育差异
肺葡萄糖转运蛋白表达的发育变化在大鼠肺中表现最好(表2).在胎鼠中,GLUT1 mRNA的表达在妊娠第20天达到最高水平,在出生后第8天降至极低水平[51].妊娠13 ~ 21天的大鼠胎儿免疫组化染色显示,妊娠19天细支气管上皮细胞膜上GLUT12表达微弱,到第21天,GLUT12表达强度增强。与mRNA表达研究一致,GLUT1蛋白在妊娠第19天也在气道中观察到,在第21天强度下降[57].在胎鼠的肺泡上皮中也检测到GLUT1蛋白,尽管到目前为止,尚未在成年大鼠的气道或远端肺中发现GLUT1蛋白[59].SGLT1 mRNA在胎鼠和成年大鼠远端肺中均有表达[55,56].
胎羊从肺腔摄取根素敏感性葡萄糖的最大速率随着胎龄的增加而增加[3.],表明出生时肺sglt表达增加。人类在怀孕后期羊水葡萄糖浓度会下降[74],与肺部葡萄糖重吸收增加相一致。
推测胎儿肺中葡萄糖转运的作用是很有趣的。胎羊肺液中添加葡萄糖[3.]和母体高血糖降低净肺液分泌,可能是通过驱动葡萄糖偶联钠吸收。然而,由于正常胎肺液中葡萄糖浓度很低,除非有妊娠糖尿病,否则这一过程不太可能是肺钠转运的主要决定因素。另一种作用可能是从羊水中清除葡萄糖,这可能具有保存营养和降低感染风险的双重功能。
肺葡萄糖转运的种类和组织差异
人体肺葡萄糖转运的研究在活的有机体内具有挑战性,因此动物和细胞培养模型已被用于探索这一领域。在物种、细胞类型和实验条件之间,转运蛋白的表达和功能存在重要差异,在选择模型时应注意这些差异。
物种的差异
在研究中,大多数物种的成虫主要在气道中表达GLUT转运蛋白,在远端肺上皮中表达SGLT。离体的原代豚鼠ATII上皮细胞对葡萄糖的摄取可被根泡素和根泡素共同降低,表明豚鼠远端肺细胞中不仅存在SGLTs,而且还存在GLUTs [70].相比之下,在成年绵羊中,通过气管上皮的葡萄糖摄取可被根黄素抑制,并需要外部钠,与钠偶联葡萄糖转运一致[75].同样,在离体的马气管中,除了根尖膜(但不是基底外侧膜)外,根素也产生了显著的减少我sc[76].然而,豚鼠和羊/马之间的这些差异更可能反映了实验准备。在完整的上皮细胞中,SGLT主要存在于管腔膜上,但在孤立的细胞中,基底外侧定位的glut也有贡献。
细胞类型
大多数在体外人类气道上皮葡萄糖转运的研究使用了永生化H441细胞或原代培养的HBECs。H441细胞来源于细支气管上皮的乳头状腺癌。在气液界面培养时,这些细胞形成吸收性上皮单层,呈现离子载体转运过程,并具有与人细支气管上皮相似的形态和表型特征[77].H441细胞和HBECs均表达GLUTs,不表达SGLT。然而,GLUT亚型的表达可能存在差异,H441细胞主要表达GLUT2和GLUT10 [10,13]和表达GLUT1和GLUT10的HBECs [11].
实验条件
实验条件在动物和在体外研究可能会影响通道的表达和功能。在动物中,研究远端肺葡萄糖转运需要使用充液肺模型,这可能会改变转运过程。在细胞培养中,非极化的H441细胞表达GLUT4,而在气液界面极化的H441细胞中未检测到GLUT4 [13].
asl葡萄糖浓度升高的影响
那么肺葡萄糖稳态对人类健康和疾病有什么意义呢?临床观察表明,人ASL葡萄糖浓度通常比血浆低~ 12.5倍。然而,当呼吸道疾病和血糖升高时,ASL葡萄糖浓度会升高。健康志愿者无法检测到鼻葡萄糖浓度(<1 mM),但90%的糖尿病患者可检测到(中位数4 mM,四分位数范围2-7 mM) [8].在重症监护中的通气病人,当他们的血糖升高时,更有可能在支气管抽吸液中检测到葡萄糖[7].使用呼气冷凝技术(呼气葡萄糖)估算的ASL葡萄糖浓度在健康志愿者中为0.4±0.2 mM,但在囊性纤维化患者中升高到2.0±1.1 mM,在糖尿病患者中升高到1.2±0.7 mM,在囊性纤维化和糖尿病患者中达到最大值(4.0±2.0 mM) [9].在接受支气管镜检查的患者中,与健康对照组相比,慢性阻塞性肺病(COPD)和慢性严重哮喘患者的支气管肺泡灌洗液(BAL)中葡萄糖水平升高[78,79].这些情况包括压力导致的高血糖,以及I型和II型糖尿病。目前还不清楚这些个体疾病对葡萄糖转运和稳态的任何具体影响。然而,了解这一点可能很重要,特别是随着二型糖尿病在西方人群中越来越普遍。
有直接和间接的证据表明,ASL葡萄糖浓度升高可促进肺部感染。呼吸道病原体金黄色葡萄球菌而且铜绿假单胞菌两者都利用葡萄糖作为生长底物[80].在重症监护室插管和通气的患者,如果支气管吸出物中检测到葡萄糖,则更有可能产生甲氧西林耐药金黄色葡萄球菌从吸入物中分离出来的葡萄糖比没有检测到葡萄糖的葡萄糖[81].糖尿病是鼻定植的诱发因素金黄色葡萄球菌[82].同时患有糖尿病的慢性阻塞性肺病患者比没有糖尿病的患者更易从痰中培养出革兰氏阴性菌[83].慢性阻塞性肺病急性加重期间,入院时血糖浓度的增加与隔离可能性的增加有关金黄色葡萄球菌以及痰中的多种病原体[79].的成长铜绿假单胞菌在高血糖小鼠的肺中发现增加了吗在活的有机体内[11].在囊性纤维化患者中,同时存在糖尿病与感染多种耐药抗生素的风险增加有关铜绿假单胞菌[84].囊性纤维化合并糖尿病患者更易发生肺加重[85],这些人对静脉注射抗生素的反应较弱[86],比没有糖尿病的人多。
未来的问题
虽然有几种机制可以调节整个肺上皮的葡萄糖稳态,但葡萄糖转运无疑在维持ASL中的低葡萄糖浓度,从而限制呼吸道病原体的生长方面起着关键作用。这一新发现的葡萄糖转运的作用提出了一些重要的问题,特别是关于我们对glut介导转运的经典理解。例如,GLUT丰度是否受到ASL葡萄糖浓度变化的调控?为什么SGLT只在远端肺中检测到(SGLT可以逆其浓度梯度运输葡萄糖,这将更有效地降低ASL中的葡萄糖)?此外,在肠道中,sglt被认为具有葡萄糖传感器的重要作用,从而上调glut介导的转运[87].不同的转运蛋白,尤其是GLUT1、GLUT2和GLUT10,在肺葡萄糖稳态中的作用是什么?呼吸系统疾病和糖尿病(特别是II型糖尿病)患者肺部葡萄糖转运是否受损,这是否会导致ASL葡萄糖升高和感染?最后,我们能否以葡萄糖在肺中的转运为目标来改善呼吸道疾病的一些后果?
脚注
权益声明书
没有宣布。
- 收到了2012年3月28日。
- 接受2012年7月19日。
- ©2012人队