摘要
众所周知,慢性阻塞性肺疾病(COPD)是肺癌的重要危险因素。每年约有1%的慢性阻塞性肺病患者罹患肺癌,这可能与吸烟的遗传易感性有关。有毒气体引起的慢性炎症可诱发慢性阻塞性肺病和肺癌。炎症介质可能促进bronchioalveolar干细胞的生长,和激活核factor-κB和信号传感器和转录激活3在肺癌的发展中也起到关键作用的慢性阻塞性肺病。
低剂量计算机断层扫描(LDCT)是一种早期发现肺癌高危患者的有效方法。然而,在初级保健环境中确定哪些患者应该接受肺癌筛查是困难的。在这篇文章中,我们回顾了与COPD相关的肺癌的流行病学和病因学,验证了LDCT肺癌筛查的有效性,并讨论了早期发现COPD对肺癌监测的重要性。
我们建议,为预防这两种疾病,COPD吸烟者筛选应尽早开始,这样他们就可以戒烟,因此,对于一个有效的肺癌筛查计划考生可被识别。
慢性阻塞性肺病(COPD)和肺癌正在迅速增长,成为世界性的健康问题。2008年,世界卫生组织公布了10大死亡原因,慢性阻塞性肺病以328万人(占全部死亡人数的5.8%)居第四位,肺癌以139万人(占2.4%)居第七位[1]。
众所周知,接触有毒气体和微粒,特别是香烟烟雾中的有毒气体和微粒,可诱发这两种疾病。据报道,慢性阻塞性肺病是与吸烟无关的肺癌危险因素[2,3]。多重危险因素干预试验报告,患者的气流受限具有比患者没有气流受限肺癌的显著发病率较高,调整后吸烟(3.02与每1,000 0.43人每年,分别地),并且所述滞后时间为戒烟后对肺癌发展的有益效果可以是只要20年[4]。这表明,与肺功能正常的现在或以前的吸烟者相比,COPD患者更有可能发展为肺癌。虽然这两种主要肺部疾病之间的密切联系一直是人们关注的焦点,但有关其分子途径及其临床相关性的细节在过去十年中才开始得到澄清。
20世纪80年代的肺癌筛查采用了胸部x光片(CXR)和痰液细胞学检查,而这些检查是否能降低死亡率一直没有定论[五]。在2000年代,采用低剂量电脑断层扫描(LDCT)及早发现肺癌,可达到可接受的早期发现阶段,并可提高可切除率[6,7]。然而,死亡率的益处尚未得到证实[7]。
国家肺筛查试验(NLST)的初步结果表明,在接受LDCT筛查的试验参与者中,肺癌死亡人数比接受CXR筛查的受试者少20% [8]。参与者的年龄在55-74岁之间,有现在吸烟者和曾经吸烟者。本研究包括> 53000名受试者,重点研究重度吸烟者,定义为那些吸烟史≥30包年的人。相比之下,慢性阻塞性肺病患者的年龄一般在50-80岁之间,与肺功能正常的重度吸烟者相比,慢性阻塞性肺病患者患肺癌的风险更高[4]。因此,LDCT筛查COPD患者的预期可能通过筛选重度吸烟者实现比检测更高的肺癌的检出率。
本文综述了慢性阻塞性肺病与肺癌的关系,并讨论了早期发现慢性阻塞性肺病对肺癌监测的重要性。
流行病学与肺癌的COPD患者的危险
有几份报告显示慢性阻塞性肺病在肺癌患者中的患病率在8%到50%之间变化[9,10]。肺癌的从COPD产生的年发病率已经被报道为0.8%至1.2%[11-13]。小号killrud等。[11]评估了慢性阻塞性肺病患者的肺癌风险,并进行了相应的病例对照研究,估计慢性阻塞性肺病患者在10年内发生肺癌的累积概率为8.8%,肺功能正常的患者为2.0% (p=0.024)。这表明,肺功能正常的患者中,肺癌发病率仅为0.2%(肺癌发病率是肺功能正常患者的5倍),而肺功能正常的患者肺癌发病率为肺功能正常患者的1%(肺癌发病率为肺功能正常患者的5倍)。最近,德Ťorres等。[14]报道,2507例COPD患者中有215例发展为肺癌(发病率密度为每1000人每年16.7例),中位随访时间为60个月。这一结果表明,在特征明确的慢性阻塞性肺病吸烟者人群中,正在肺诊所就诊的慢性阻塞性肺病患者的肺癌发病率高于以前的报道[11]。
环境和遗传学在肺癌病因基于人群的病例对照研究招募了2100例肺癌患者和2120所控制。这项研究表明,患肺癌的风险与慢性支气管炎(OR 2.0,95%CI 1.5-2.5),肺气肿(OR 1.9,95%CI 1.4-2.8)和慢性阻塞性肺病(OR 2.5,95%CI 2.0-3.1个体中增加的)2]。通过对448,600名终身不吸烟者的20年随访研究,T缸等。[3也有报道称肺癌死亡率与肺气肿(危险率(HR) 1.66, 95% CI 1.06-2.59)和肺气肿合并慢性支气管炎(COPD) (HR 2.44, 95% CI 1.22-4.90)显著相关,但与单独的慢性支气管炎(HR 0.96, 95% CI 0.72-1.28)无关。在这两项研究中,慢性阻塞性肺病的诊断依据是肺气肿或慢性支气管炎的临床症状和患者问卷,而不是肺活量测定法或计算机断层扫描。
COPD的严重程度也会影响肺癌的发病率。首次全国健康和营养检查调查收集了5402名参与者22年的随访数据,结果显示气流阻塞的程度与肺癌发病率呈正相关[15]。在本次调查中的数据的多变量比例风险分析显示,轻度COPD有一个相对更高的风险(HR 1.4,95%CI 0.8-2.6)和中度或重度COPD患肺癌发病率的显著较高的风险与正常的肺功能比(HR 2.8,95%CI 1.8-4.4)。反过来,德Ťorres等。[14据报道,慢性阻塞性肺病全球计划(COPD Global Initiative for Chronic Obstructive lung Disease, GOLD) I期至IV期的肺癌发病率呈逐步下降趋势,IV期(每1000人年9.2例)的发病率不到I期(每1000人年19.9例)的一半。他们推测,一个活跃的和不耐受的免疫系统将作为一个屏障,防止癌症的发展和进展。
因为只有15-20%的吸烟者被认为在他们的一生中会发展成肺癌和/或慢性阻塞性肺病,个人可能对这些疾病有不同的易感性[16]。Cohen[17]是第一个对COPD的遗传流行病学报告。患者的一级亲属患有COPD或肺癌已经为气流受限的风险增加,有无吸烟史。此外,早发性肺癌的一级亲属中有家族史吸烟者无家族史吸烟者相比有肺癌的发展提出了更高的风险随着年龄的增加[18]。这些发现表明,这些疾病与易感基因有关[19]。
肺气肿和气流阻塞(慢性支气管炎)是COPD的两端表型,和广大的COPD患者被发现在中间的某个地方。它仍然是有争议的,其条件,肺气肿或气流阻塞,导致更大的肺癌易感性[20.]。w ^威尔逊等。[21报道说,虽然气流阻塞和肺气肿(与吸烟无关)都是肺癌的预测因素,但肺气肿比小气道阻塞更容易导致肺癌。dËŤorres等。[22结果显示,在计算机断层扫描中发现的肺气肿,而不是气流阻塞,与肺癌发病率的增加有关。结果肺癌筛查的梅奥诊所(美国罗彻斯特MN)从多个逻辑回归模型显示,肺气肿在计算机断层扫描(≥5%)与肺癌的风险增加3.8倍在白种人和风险较高的子组,包括年轻人(< 65岁的年龄,或4.64),重度吸烟者(≥40 pack-yrs,或4.46),和小细胞肺癌(或5.62)[23]。肺气肿是在这些研究中通过计算机断层扫描图像的视觉半定量评分评估。相比之下,男aldonado等。[24]报道,肺气肿的影像学证据,通过自动定量计算机断层扫描分析来评价,不是为肺癌的风险显著(OR 1.042,95%CI 0.816-1.329)和肺气肿严重程度也未患有肺癌(OR 1.57相关联,95%CI 0.73-3.37)。然而,降低的用力呼气量1秒(FEV1)(或1.15,95% CI 1.00-1.32)和FEV1/强迫肺活量(FVC) (OR 1.29, 95% CI 1.02-1.62)是显著的危险因素。ķ以示等。[25也报道了类似的定量计算机断层分析结果。Gierada等。[26据报道,不仅是肺气肿,而且在节段-亚节段水平上的支气管测量,如自动计算机断层分析评估,也与肺癌无关。w ^威尔逊等。[27]报告说,他们的117例肺癌病例对照研究并未显示任何气道阻塞或肺气肿的评估,计算机断层成像图像进行定量分析,与肺癌的风险增加有关的任何证据。因此,肺气肿作为肺癌的危险仍然存在争议,需要进一步澄清。为dhopeshwarkar等。[28]已经假定,通过筛查发现肺癌的研究人群在癌症部位、形态(密度、边界)、大小、组织学、诊断、治疗阶段和生存率方面可能不同于一般的肺癌患者。因此,对这些结果的解释应该谨慎。
有趣的是,非吸烟者中大多数肺癌已经报道在雌[发生29],和男性的10%,女性肺癌的20%被报道为从不吸烟者[30.]。降低FEV1据报道,在从不吸烟的人群中,吸烟会增加患肺癌的风险[3]。Calabro等。[31报告说,预测的FEV仅减少了10%1与肺癌风险增加近三倍有关。他们认为,识别最小的肺功能损伤可能为早期检测和肺癌筛查的试验找到最佳候选。这里提出的证据表明,肺气肿和气道阻塞都是肺癌的独立危险因素,有这些情况的患者应该进行筛选。
COPD合并症和与肺癌
COPD和吸烟诱导全身性炎症的变化,从肺中的局部慢性炎症的结果。COPD患者具有某些合并症,包括冠状动脉疾病,充血性心脏疾病,其它心血管疾病,区域恶性肿瘤(主要是肺癌)和神经疾病[发病率较高32]。他们有3.7慢性合并症的平均水平,而对照1.8合并症[对比32]。美国国家医院出院调查分析了1979年至2001年间超过4700万例医院出院,发现与非慢性阻塞性肺病患者相比,慢性阻塞性肺病患者在肺炎、高血压、心力衰竭、呼吸衰竭和胸部恶性肿瘤方面的年龄调整住院死亡率更高(均p<0.01) [33]。小号在等。[34]总结了关于COPD患者死亡的潜在原因的几个系列。他们报告说,轻度或中度慢性阻塞性肺病患者的主要死亡原因是肺癌和心血管疾病,而在重度慢性阻塞性肺病患者中(<预测FEV的60%)1),呼吸衰竭是主要的原因。这表明,COPD早期检测和所需的肺癌的早期检测和提高生存率的谨慎,定期随访。
肺癌的COPD患者的特性与不COPD不同[35]。患有COPD的吸烟者有开发一种特定的非小细胞肺癌的组织学亚型,鳞状细胞癌[风险较高35-37],虽然已经腺癌的患者中迅速增加被动暴露于香烟烟雾,吸烟者光和女性[22]。德Ťorres等。[14也有报道称,虽然腺癌是仅在黄金期I患者中最常见的组织学类型,但在黄金期II和III患者中最常见的肺癌类型是鳞状细胞癌。近年来新的分子靶向药物,如吉非替尼、厄洛替尼、贝伐珠单抗、克唑替尼等,主要针对腺癌,目前对鳞癌有效的新药物较少。研究单一组织学类型的肺癌与气流阻塞严重程度之间的关系,可能有助于了解慢性阻塞性肺病患者肺癌的病理生物学,并有助于开发新的分子靶向药物,特别是针对鳞癌。
慢性阻塞性肺疾病(COPD)肺癌患者的预后
慢性阻塞性肺病肺癌患者的预后比非慢性阻塞性肺病患者的预后更差,因为癌症治疗不足,肺功能和生活质量较差[10]。我们调查了手术后长期生存在IA期肺癌患者与COPD [38]。COPD患者5年生存率明显低于肺功能正常患者,复发率较高(77.0%)与分别为91.6%;p < 0.0001)。这些结果提示慢性阻塞性肺病患者的肺癌往往是高等级恶性肿瘤,支气管肺泡癌和高分化腺癌的发病率较低。其他研究结果表明,COPD是肺癌肺切除后呼吸衰竭导致呼吸相关并发症的发生和较差的长期生存的重要危险因素[39,40]。大号opez- encuentra等。[41]报道,尽管总生存期为肺癌手术后COPD和非COPD患者相似,在Ⅰ期肺癌患者的生存条件在2个3年在COPD患者比非COPD患者显著恶化。相反,Pompili等。[42报道说,虽然COPD患者与非COPD配对,生活尺度和术后的身体和心理素质比较术后心肺并发症的更高的速率围手术期的变化没有慢性阻塞性肺病和匹配的非COPD之间的差异耐心。因为他们没有报告的长期结果,他们的研究结果对生存的影响尚不清楚。
肺癌的COPD患者可能的共同的致病途径促进发展
几种可能的机制和相关的候选基因已经被提出了从气流阻塞肺癌的进展。可能涉及的易感性的候选基因示于表1。
首先,由吸烟引起的或暴露于有毒物质的气道中积累的环境物质的结果,慢性阻塞性肺病加重功能障碍[粘液纤毛功能障碍61]。粘液纤毛功能障碍被认为主要发生在中央气道。其次,氧化剂和抗氧化剂之间的不平衡会导致DNA的自由基损伤[62]。第三,基因突变和多态性可能影响肺癌发展的加速或抑制。dialyna等。[50]报道谷胱甘肽的遗传无效突变的频率S-转移μ1(GSTM1),其是在烟草反作用组织有害物质的酶,在COPD肺癌患者比健康对照组显著更高。相比之下,基因突变和多态性体内CYP2A6基因表现抑制COPD的癌变及加重[51]。
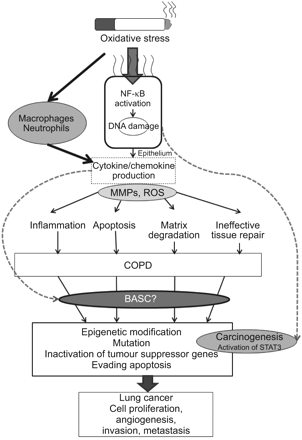
第四,慢性炎症,最近接收到了最多的关注,可导致慢性有丝分裂发生和增加内源性DNA损害的转换的可能性成突变[63]。从气道阻塞引起的慢性炎症在肺癌发展的重要作用,并可能是场效应现象的一个重要组成部分[44,64,65]。COPD包括呼吸道特别的小气道,慢性炎症,和由巨噬细胞的聚集表现,CD4 +和CD8 + T细胞,树突细胞,和嗜中性粒〔66]。有研究显示,下呼吸道的慢性炎症可引致癌变[67-69],而微环境中的炎症介质可促进细支气管肺泡干细胞诱导proneplastic突变、增殖、抵抗凋亡、血管生成、侵袭、转移和分泌免疫抑制因子(图。1)70,71]。
慢性阻塞性肺疾病(COPD)在炎性微环境中发生肺癌的可能机制。氧化应激在香烟烟雾刺激核转录因子(NF) -κB通路在肺上皮细胞和新兵炎症细胞,巨噬细胞和中性粒细胞释放细胞因子和趋化因子。释放的基质金属蛋白酶(MMPs)和活性氧(ROS)诱导炎症、凋亡、基质降解和无效的组织修复,导致空气空间扩大。支气管肺泡干细胞(BASC)可能试图修复和替换受损的肺泡细胞,但在炎症环境中会增强致癌作用。信号转导器和转录3 (STAT3)信号通路激活剂的持续激活也会引起肺部炎症和癌变。
最近提议,核转录因子的激活(NF) -κB可能有至关重要的作用在肺癌的发展慢性阻塞性肺病(72,73]。NF-κB激活增加炎症介质可诱导的COPD,并且还抑制细胞凋亡,诱导细胞增殖的释放,最后加速癌症的发展。NF-κB激活和炎症相关的基因的后续动作可能在COPD和肺癌的核心作用。信号转导和转录因子3(STAT3)的活化剂是具有不同生物学功能的有效转录因子。STAT3信号传导途径的持续激活也诱导在肺肺部炎症和腺癌形成。STAT3和其下游基因可作为生物标志物用于肺腺癌和COPD诊断和预后[45]。肿瘤抑制蛋白p53是炎症的抑制剂一般[74];它的基因,TP53,通常是由香烟烟雾突变,并且可以通过氧化剂活化NF-κB介导的炎症的抑制[73]。
小号undar等。[56]评价的COPD和肺癌的发病表观遗传修饰。他们报告说,氧化应激和炎症反应改变细胞的氧化还原电位,从而导致基因组不稳定,在表观遗传修饰高潮。Epigentic改性剂,其中包括DNA甲基转移酶,组蛋白乙酰转移酶和组蛋白脱乙酰,都参与了“打开和关闭”染色质,并发挥调节基因表达至关重要的作用。
最近的全基因组关联(GWA)在肺癌和慢性阻塞性肺病的研究报告在几个染色体位点和单核苷酸多态性显著协会在这些地区[54,75,76]。GWA研究的结果表明,许多候选基因的慢性阻塞性肺病和肺癌重叠[75]。吸烟引起的肺部炎症被认为是慢性阻塞性肺病的基础,其特征是生长因子和基质金属蛋白酶水平升高。在这种微环境中,已知发生气道上皮癌前转化,可能将COPD与肺癌的发展联系起来[54]。ÿ翁荣南等。[76]认为未来肺癌的遗传流行病学研究可能会大大受益这种重叠的探索通过分表型分型案件和共存COPD控制中受益。
另一个特定的遗传机制参与COPD进展到肺癌的病因学是α1抗胰蛋白酶缺乏症(α1-ATD)等位基因。这些谁α1-与一般人群比较,携带atd的人士患肺癌的风险较高[58,59]。ÿ盎等。[59]报道的模型1585对病例对照和α1-ATD等位基因使用多个逻辑回归分析,发现α1-ATD携带者患肺癌的风险比非携带者高70% (OR 1.7, 95% CI 1.2-2.4)。这表明,α1-ATD等位基因几乎可以成倍肺癌易感性。
慢性阻塞性肺病患者的肺癌预防
肺癌高危人群应作为筛查、监测和预防干预的适当对象。doll和P采访时表示[77提出了一种吸烟的风险预测模型。他们认为,与每天吸烟的数量相比,吸烟时间对肺癌风险的影响更大。慢性阻塞性肺病患者吸烟史多为阳性,其进展与发病年龄、吸烟时间及总吸烟量密切相关。因此,与肺功能正常的吸烟者相比,轻度到中度慢性阻塞性肺病患者在10年内发生肺癌的几率要高出3倍,而重度慢性阻塞性肺病患者在10年内发生肺癌的几率要高出10倍[15],虽然德Ťorres等。[14发现肺功能严重程度与肺癌发病率呈负相关。即使是轻微的慢性阻塞性肺病,肺气肿患者也可能有较高的肺癌风险[14,22],因此患者的慢性阻塞性肺病需要筛选监控肺癌的任何阶段。乙阿赫等。[78]还构建了一个肺癌风险预测模型,通过分析一个大型随机试验(胡萝卜素和维生素a疗效试验)的数据,估计了一个吸烟者(≥20包岁)在10年内被诊断为肺癌的绝对风险。他们报告说,肺癌的风险差异很大,但准确的风险预测可能提供信息,使个人能够决定是否筛查肺癌。小号PITZ等。[79]通过对巴赫模型的进一步发展,建立了基于吸烟状态的肺癌风险预测模型。他们报告说,肺气肿史是目前和以前吸烟者患肺癌的最高风险因素。
最有效的肺癌的预防措施是戒烟。大的纵向研究由Anthonisen等。[80结果显示,在经过14.5年的随访后,33%无症状的COPD轻至中度吸烟者死于肺癌。他们报告说,特殊戒烟干预组的全因死亡率明显低于常规护理组(每1000人年8.83人)与每千人年10.38人;p=0.03),但肺癌组差异无统计学意义。
经常使用的吸入糖皮质激素可降低肺癌与COPD前吸烟者之间的风险[81,82]。然而,长期吸入高剂量糖皮质激素并没有引起吸烟者支气管发育不良或致癌的二级标志物的任何退化[83]并没有减少肺癌的危险性[84]。H棱[85]报道的选择性环氧化酶2抑制剂(塞来考昔罗非考昔或)可以降低肺癌的风险。预防肺癌的其他抗炎剂包括木犀草素[86),生育酚(87和羧基咪唑[88]。他汀类药物最近已经注意到,在肺中重要的抗发炎物质。非随机研究表明,患者的他汀类药物相关的慢性阻塞性肺病心血管和呼吸系统的发病率和死亡率的降低。此外,他汀类药物可改善肺功能下降1减少患肺癌的风险[89,90]。
COPD患者肺癌筛查的重要性
肺癌筛查是一种二线癌症预防方法。肺癌筛查最重要的主要终点是降低肺癌死亡率。美国国家癌症研究所的肺筛查研究发现,在基线时,LDCT队列中20.5%的受试者(1586人中有325人)和CXR队列中9.8%的受试者(1550人中有152人)被诊断为可疑的肺癌。LDCT队列中肺癌确诊检出率为1.9%(1586人中有30人),CXR队列中肺癌确诊检出率为0.45%(1550人中有7人)[91]。在该研究的最终结果报告中,共有1,660名LDCT队列患者和1,658名CXR队列患者被诊断为肺癌,分别为40名(2.4%)患者和20名(1.2%)患者[92]。
日本的研究和美国早期肺癌行动计划(ELCAP)表明,在高危人群中,螺旋ct扫描比CXR扫描更容易发现肺癌[93,94]。小号obue等。[95]报道,对于计算机断层摄影筛查检测肺癌的5年存活率分别为76.2%和初始64.9%和反复筛选分别,。谁被计算机断层摄影在国际ELCAP(I-ELCAP)协议筛选那些患者中,85%的患者的临床I期肺癌,以及所估计的10年存活率为88%[6]。这些研究都显示出非常高的检出率和生存率,并建议计算机断层扫描筛查可能是肺癌的早期发现和治疗手术有益(表2和3)。
乙echtel等。[114]调查了胸部ct对慢性阻塞性肺病患者早期肺癌的检测效果,报告了在88例慢性阻塞性肺病高危患者中发现6例肺癌病例(6.8%)。共有3例I期患者,6例中有3例存活5年。这一检出率高于其他报告的1.2%至1.6%的初始癌症检出率[6,115]。
为了证明肺癌筛查的功效,但是,筛选偏差,诸如交货时间,长度和过度诊断应该解决[116]。因此,随机对照试验更可取。目前,一些国家正在进行几项大型随机对照试验。NLST是最大的多中心、随机对照试验[8]。该试验的独立数据和安全监测委员会宣布,LDCT组的全因死亡率比CXR组低7%,而~ 25%的死亡是由肺癌引起的[111]。有趣的是,在NLST参与者中,有17.4%的人患有慢性阻塞性肺病,7.7%的人患有肺气肿[112]。在NLST结果的辅助分析预计,以澄清与肺癌的发病率这些高风险的健康状况的相关性。
其他最近在早期发现的进步和筛查肺癌已通过审查凡不w ^esteinde和范ķlaveren[117]。他们报告说,光致荧光内镜或自体荧光成像支气管癌的内镜中心气道,检测外周血循环DNA的甲基化基因在等离子体中,测量循环肿瘤提取外来体水平,测定微核糖核酸模式,比较蛋白质分析,检测癌症相关的自身抗体的抗原,呼出的气息分析,在支气管肺泡灌洗液样本中鉴定基于基因组的标记物,以及在痰中鉴定生物标记物是很有前途的候选。
早期发现COPD用于肺癌监测
慢性阻塞性肺病诊断严重不足[118,119和经常被误诊的[120]。小号oriano等。[119]总结下诊断患病率和报告。他们报告说,慢性阻塞性肺病患者的72%〜93%的未确诊。在日本(日本)COPD流行病学研究报告指出,气流受限的患病率(FEV1/FVC <70%)为10.9%,仅有9.4%的气流受限患者曾被诊断为慢性阻塞性肺病[121]。虽然COPD的最终诊断是通过肺活量测定做出的,但在一般实践中,它仅用于30%至50%的新病例[122,123]。
慢性阻塞性肺病在一般人群中的患病率被认为约为1%,而在40岁以上人群中的患病率增加到8%至10% [124]。Fukuchi等。[121据报道,COPD患病率在60岁及以上时急剧增加:50-59岁时5.8%与在60-69岁15.7%,70岁及以上24.7%。
COPD的早期诊断已尝试对高风险患者[125,126]和肺活量测定已被证实在COPD筛查和早期诊断中发挥了重要的作用。乙uffels等。[126]报道,在肺功能检查有呼吸道症状的个体的18%,而在那些没有这些症状的4%,证实气流阻塞。V盎ydF4y2Ba小号chayck等。[125]研究截的情况下发现的有效性患者吸烟史谁是在发生COPD,使用标准化的问卷调查和肺活量测定风险。他们报告说,参与者的18%有气道阻塞,并且当吸烟者基础上呼吸道症状,如慢性咳嗽进行了预选,患者的气道阻塞的百分比那些年龄超过60岁间增加至48%。咳嗽气流阻塞的阳性预测值为27%,而至少两个呼吸道症状,包括咳嗽,呼吸困难或喘息,为29%。在患者所有三个症状,患病率为35%。因此,他们建议,肺功能测试应在慢性咳嗽的吸烟者进行。
这些结果表明,至少,现在或既往吸烟者年龄在60岁以上的老年人,谁具有一定的呼吸道症状,可能是慢性阻塞性肺病的潜在候选人,应由肺功能检查进行筛选。此外,为了防止COPD和肺癌中,根据箭头C的建议alabro等。[31],COPD使用肺功能检查筛选的患者应开始尽可能早地让他们停止吸烟。此外,由于COPD的诊断可能是肺癌筛查的风险分层非常重要,应该使用采用支气管扩张肺功能COPD的标准。
限制对60岁或60岁以上有吸烟史的人进行筛查的问题在于,从不吸烟的人和60岁以下的人不被考虑在内。尽管在过去的几十年里,年轻年龄组的肺癌发病率一直在下降[127],不吸烟的女性人数有上升趋势,但主要是年长女性[128]。范小号chayck等。[125]认为,虽然COPD筛选一般人群是可能的,实现在初级保健机构筛选是相当困难的,并且发现的情况下很可能是一种更合适的方法。因此,与吸烟史和慢性咳嗽年龄小于60岁的年龄情况下应进行对COPD筛选肺功能测试。
另一个问题是,使用固定切断的FEV的70%1/ FVC查明气道阻塞可能导致误判。为了减少老年患者的过度诊断和诊断不足之间的年轻成人患者中,使用的正常FEV与年龄相关的下限1/ FVC已被推荐用于识别气道阻塞[129,130]。然而,使用不同的分界点是困难的,不适合用于筛查普通人群。
一般来说,慢性阻塞性肺病筛查不需要计算机断层扫描。然而,由于没有气流阻塞的肺气肿仍然是肺癌的危险因素,因此LDCT可能对慢性阻塞性肺病患者是必要的。一旦病人在电脑断层上被诊断为肺气肿,他们应该接着电脑断层检查,以及早发现肺癌。
结论
由于COPD和肺癌的死亡率很高,并招致严重的经济负担全世界,早期发现和干预两种疾病是至关重要的。在前者,主动吸烟者肺功能能及早发现慢性阻塞性肺病和帮助选择要包含在肺癌筛查程序与计算机断层扫描的最佳人选。然而,关于疗效,劣势,潜在的危害,和成本效益,选择标准为COPD和肺癌筛查是重要的,要慎重考虑。
脚注
支持声明
这项工作得到了日本教育、文化、体育、科学技术省向Y. Sekine提供的科学研究补助金的支持。
感兴趣的语句
没有宣布。
- 收到了2011年7月23日。
- 公认2011年10月11日。
- ©2012人队