摘要
我们测定了丙酸氟替卡松(FP)加压计量吸入器(Flovent®HFA;葛兰素史克,研究三角公园,NC,美国)管理通过AeroChamber Plus®(Monaghan Medical, Plattsburgh, NY, USA)与面罩和Babyhaler®(葛兰素史克)阀门保持室(VHCs)使用人群药代动力学方法。
1至4岁的哮喘稳定但临床需要吸入性皮质类固醇治疗的儿童接受88 μg FP氢氟烷烃(2×44 μg),每日两次,通过两个装置以开放标签、随机交叉方式给药,每次8天。在每次治疗第8天的12小时给药间隔期间,患者随机分为三种稀疏采样方案中的一种进行采血,以进行药动学分析。确定每个方案的FP血药浓度-时间曲线(AUC)下面积。
17名儿童完成了这项研究。使用带面罩的AeroChamber Plus®FP后的人群平均AUC为97.45 pg·h·mL−1.(95%可信区间85.49–113.32 pg·h·mL−1.)Babyhaler®的浓度为51.55 pg·h·mL−1.(95%可信区间34.45–64.46 pg·h·mL−1.).相对生物利用度(Babyhaler®/AeroChamber Plus®)为0.53(95%可信区间0.30–0.75)。
在两种装置之间观察到肺部生物利用度的临床显著差异。VHC不可互换,因为向肺部输送的药物可能存在差异。可使用群体药代动力学方法确定FP的肺部生物利用度。
对于患有哮喘的幼童(小于5岁)来说,阀门保持室(vhc)是将吸入药物从加压计量吸入器(pMDIs)输送到肺部的关键,并且经常用于难以协调pMDI的驱动和吸入的年龄较大的儿童。然而,药物从VHC输送到肺部可能会增加或减少,这取决于所使用的特定VHC(大小、形状、塑料)对抗静电成分和死腔体积)、药物配方(药物、推进剂和赋形剂)和患者特征(潮气量、平静度)对哭泣和面罩密封)[1.–5.]理想情况下,最相关的肺部给药测量是给药的临床效果,但给药量和反应之间的直接关系几乎不可能测量,因为反应受其他因素的影响,包括哮喘严重程度、基线肺功能、种族/民族、pha哮喘的遗传影响和持续时间[6.].此外,对于大多数吸入药物,无法通过吞咽和从胃肠道吸收的药物活性(口服生物利用度)来测量直接输送到肺部的药物活性不使用活性炭来阻止胃肠道吸收或在肺部使用标记药物的闪烁显像。涉及活性炭或闪烁显像的研究充其量很难在幼儿中进行,并且这种干预在这个年龄组中是不道德的。因此,一种替代方法来确定肺部给药是指测量吸入剂量后的血药浓度。然而,该方法仅适用于口服生物利用度可忽略不计的药物,以确保血液测量仅反映从肺部系统吸收的药物。几项已发表的研究记录了肺部给药的差异通过测量血液水平,将计量吸入器(MDI)连接到不同的VHC,将糖皮质激素(ICS)吸入肺部[7.,8.].
丙酸氟替卡松(FP)是2010年处方最广泛的ICS[9]FP通常与VHC一起用于治疗儿童哮喘。FP的口服生物利用度<1%,因为其几乎完全的首过代谢[10,11]因此,FP吸入给药后的胃肠道和口腔吸收对系统生物利用度无影响[12]因此,吸入剂量FP后的血浆浓度仅代表输送至肺部并从肺部系统吸收的药物(肺部生物利用度)。FP血浆浓度-时间曲线(AUC)下的面积和最大血浆浓度与吸入剂量成正比[13].因此,FP非常适合于通过测量吸入剂量后的血浆浓度来确定VHC的肺输送。
我们在患有哮喘的幼儿中使用群体药代动力学方法来比较FP(Flovent®HFA pMDI;葛兰素史克,美国北卡罗来纳州三角公园研究所)的肺生物利用度通过2个带口罩的vhs: AeroChamber Plus®(莫纳汉医疗,普拉茨堡,纽约,美国)和Babyhaler®(葛兰素史克)。
方法
研究参与者
在随机化开始时,从两个临床点(佛罗里达州杰克逊维尔的Nemours儿童诊所和佛罗里达州Gainesville的佛罗里达大学儿童肺部诊所)招募经医生诊断为哮喘的1至4岁的男性或女性儿童。所有儿童均有症状性哮喘病史,并在筛查来访前12个月内至少经历了两次需要医疗关注和哮喘药物治疗的哮喘症状发作。以下儿童有资格参与:在筛查来访前4周,他们需要接受维持性哮喘药物治疗(包括ICSs),并定期使用该药物;或者,根据他们的疾病过程和当前的治疗指南,应该已经接受ICS治疗(因此,表明临床需要ICS治疗),并计划继续接受该治疗。所有皮质类固醇(局部和吸入)均在随机分组时停用。在研究期间,参与者被允许继续服用处方的非类固醇哮喘药物。以下儿童不符合参与资格:在筛查来访2周内出现未解决的上呼吸道或下呼吸道感染;在前3个月内有肺炎迹象;有其他严重肺部疾病;或需要在筛查前4周内口服皮质类固醇。 Participants were not permitted to take any drug or food that might have inhibited or induced activity of cytochrome P450 3A4 within 2 weeks of dosing (例如红霉素、苯巴比妥和葡萄柚汁)。参与者的父母、监护人或护理者(以下简称“父母”)每天填写日记卡,并记录给药日期和时间、不良事件和伴随用药。每个试验点都获得了机构审查委员会的批准。在研究之前,从每个参与者的父母那里获得了签字并注明日期的书面知情同意书/父母许可。
研究设计
这是一项随机、多剂量、开放标签、双向交叉研究(葛兰素史克方案标识符FAS10002)。每个参与者都进行了筛选访问≤随机分组前30天。在筛查访视时,获得病史,进行包括生命体征在内的体检,并抽取血液进行血液学分析。每名儿童随机接受FP氢氟烷(HFA)pMDI,该pMDI通过面罩或Babyhaler®连接到AeroChamber Plus®上(确定为第1或第2课时)。给儿童两次吸入FP,每次44μg吸入产品,每次间隔30秒,每天两次。在早晨和晚上给药之间至少11小时给药8天(每天总剂量176μg FP)。在研究协调员的指导下,由父母在研究现场给予每种治疗的第一剂。为了确保100%的依从性和稳定状态,研究人员通过让父母和孩子返回诊所或由研究人员到参与者家中观察给药情况来观察每一疗程的最后四次剂量。给药第8天抽取血液进行药代动力学分析。在完成第8天的研究程序后,参与者被转入替代方案。在研究结束时服用最终剂量后,重复进行体检和抽血以进行血液学分析。在第一次治疗的第一次剂量之前或在过渡到替代方案之前,没有对先前吸入的皮质类固醇剂量进行冲洗,因为在研究时使用的所有ICS的半衰期在吸入剂量之后足够短,在进行药物动力学采样时,所有药物都已被清除第8天[14].
根据产品标签使用说明,对父母进行适当准备MDI和VHC的培训,并指示如果孩子感到不安,开始哭泣,或与口罩或保温室搏斗,则应延迟给药,直到孩子平静。
父母在日记卡上记录了研究药物的给药日期和时间。在使用带面罩的AeroChamber Plus®治疗期间,父母被指示让他们的孩子在每次驱动后进行六次潮气呼吸。在使用Babyhaler®治疗期间,孩子在每次驱动后进行5-10次潮气呼吸。一项单独的研究每个中心的协调员在临床研究机构第1和第2课时的第8天给药,以减少参与者之间给药技术的差异。
甚高频设备
带面罩的AeroChamber Plus®和Babyhaler®之间有重要的设计差异。AeroChamber Plus®with Facemask是一款149毫升聚碳酸酯VHC,长度14.9厘米,固定直径4.5厘米,并带有一个集成口罩(Monaghan/Trudell Medical International, London, ON, Canada)。面罩死区范围24.0-46.0 mL,视乎儿童脸上面罩所受的力而定[3.].在VHC和面罩之间有一个单向阀,面罩中有一个呼气阀[15]; 因此,阀门之间没有死区[16].Babyhaler®是一种350毫升的聚碳酸酯VHC,长度为30厘米,带有可拆卸面罩[1.,17].Babyhaler®在低阻进口和出口阀之间有40 mL死区,77-mL面罩死区,总死区为117 mL [1.,15,17].Babyhaler®(面罩和腔室)重190.7 g,而AeroChamber Plus®with Facemask重71.7 g(面罩和腔室)[1.].
在NeMELS儿童诊所,AudioLoop-®带有面罩和Babyhaler®都是根据制造商的说明书首次准备使用的,这两种设备都包括肥皂水洗涤、清水清洗和空气干燥。在佛罗里达大学,这些房间没有清洗,但是28个剂量是Admin。在每一个疗程中都进行了预处理,因此在第8天血液取样之前,两个部位的腔室基本上都进行了预处理。
药代动力学研究设计
根据采用标准群体药代动力学方法的三个采样方案之一,在第1和第2课时的第8天采集血样进行药代动力学分析(表1) [18].参与者被随机分配到三个采样间隔中的一个,如下所示。第1组(n=9):给药前至给药后4小时;第2组(n=7):给药后2.5小时至给药后8小时;第3组(n=2):给药后7.5小时至给药后13小时。第1组、第2组和第3组的取样间隔分别反映了由于吸收和分布、分布和消除以及下一次给药后的消除和吸收而产生的血浆浓度。两个装置的参与者分组分配保持不变。血液取样为p在佛罗里达大学的临床研究单位和沃尔夫逊儿童医院(FL杰克逊维尔)的临床研究中心。两个临床研究设施均为受控环境,每日温度和湿度稳定。参与者居住的两个中心周围的室外天气条件相同。
将五份5毫升的血液样本抽取到锂肝素收集管中,并在冰上储存一周≤采集后2小时,直到可在4°C下离心。通过留置导管(在研究样本采集前丢弃1-mL废样本)或针头棒采集样本。采集血样时允许使用局部麻醉剂(EMLA乳膏;阿斯利康LP,美国德州威尔明顿)。
血浆样本被冷冻并储存在-20°C,直到它们被分析。由于血浆FP(储存在-20°C)的稳定性数据在研究时仅验证了4个月,所以在采集后4个月内对样品进行了分析。血浆FP通过York Bioanalytical Solutions (York, UK)进行分析,采用固相萃取结合液相色谱-串联质谱的有效分析方法,FP检测限为5 pg·mL−1.[19].
药代动力学分析
群体药代动力学模型采用非线性混合效应模型,使用计算机程序NONMEM V版开发[18,20,21].建立了一个具有零级吸收和一级消除的单室模型,其中肺被认为是药物释放进入体循环的FP仓库。对更复杂的模型进行了评估,但没有明显改善拟合性。
由于一些浓度是不可量化的,NONMEM被用来使用最大似然法预测不可量化的浓度[22]此外,在NONMEM中使用IPRED命令计算个体参与者的药代动力学参数。由于样本量较小,因此未评估协变量的影响[23].
通过种群药代动力学模型获得表观清除度(CL/F)和相对生物利用度(F1)。AUC的推导公式如下: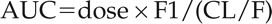
根据对数转换值差0.3134和α=0.05的标准偏差,14名参与者的样本量需要提供90%的功率,使AUC的几何平均值彼此在30%以内,比率的置信区间在0.70–1.43之间[7.]。除要求的14名参与者外,其他参与者被随机分配到两个序列,并分配到第1组药代动力学抽样方案,以便在最有可能达到可测量水平时最大化数据。
结果
研究参与者
在接受筛查的27名儿童中,有20名被随机分配并服用了药物。所有随机的参与者都被纳入研究人群的评估。共有17名儿童完成了研究的两个阶段,来自这些参与者的血浆FP数据被纳入了药代动力学分析。一名参与者完成了两个疗程,但在第2疗程结束时(第8天使用AeroChamber Plus®面罩),静脉通路失败,因此无法获得该疗程的血浆样本。该参与者的第1阶段(Babyhaler®阶段)数据(第2组抽样间隔)被纳入人群药动学分析。两名参与者(分别来自第1阶段和Babyhaler®阶段)在药代动力学取样前因与研究无关的其他原因或不良事件退出了研究。后者在注射88 μg FP HFA MDI后出现导管相关并发症(认为是不良事件)b、 身份证。Babyhaler®导致退出研究。
参与者的平均年龄为2.3岁(表2)。未报告严重不良事件。在7名接受筛查但未随机分组的参与者中,3名撤回同意,3名实验室结果异常,1名失去随访。
平均值±sd17名参与者的潮气量(潮气量确定为7ml·kg−1.×理想体重[2.])为100.3±17.0 mL(范围75.6 ~ 133.0 mL)。
药物动力学
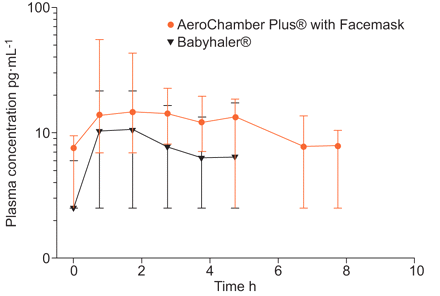
血浆浓度可测量的时间≤使用带面罩的AeroChamber Plus®和≤使用Babyhaler®5小时(图1).总体均值AUC他一直h浓度为51.55pg·h·mL−1.(95%可信区间34.45–64.46 pg·h·mL−1.)使用Babyhaler®和97.45 pg·h·mL−1.(95%可信区间85.49–113.32 pg·h·mL−1.)与AeroChamber Plus®面罩。相对生物利用度(Babyhaler®/AeroChamber Plus®)为0.53 (95% CI 0.30-0.75)。
AeroChamber Plus®with Facemask (Monaghan Medical, Plattsburgh, NY, USA)和Babyhaler®(GlaxoSmithKline, Research Triangle Park, NC, USA)的血浆丙酸氟替卡松(FP)浓度的中位数和95%置信区间的对数标度。给药后较长一段时间内可测量FP浓度通过带面罩的AeroChamber Plus®气室。审查值为2.5 pg·mL−1.当浓度低于检测限时分配,以计算中位数和95%置信区间。
讨论
这项研究的结果表明,学龄前儿童服用FP治疗剂量后的稳态血浆浓度测量可以揭示服用剂量时肺生物利用度的差异通过VHCs不同。这是第一个使用人群药代动力学方法,在交叉设计中直接比较两种不同vhc提供的1 - 4岁儿童ics的肺生物利用度的研究。我们的研究结果证实了之前在儿童和大儿童中进行的研究结果。在这些研究中,当FP交付时,观察到肺生物利用度(以峰值浓度表示)的差异通过不同的车辆健康控制系统[7.,8.].
本研究中观察到的AUCs(Babyhaler®51.55pg·h·mL−1.;含口罩的AeroChamber Plus®97.45 pg·h·mL−1.)低于之前两项针对相似患者群体的研究中观察到的。在一项研究中,88μg FP每日两次或安慰剂通过带面罩的AeroChamber Plus®给药(AUC 151 pg·h·mL)−1.) [24]在第二项研究中通过Babyhaler®检测(AUC 141 pg·h·mL−1.) [25].目前还不清楚为什么在我们的研究中auc较低,但药代动力学方法的差异可能提供了一个解释。在北美和南美的研究与AeroChamber Plus®与面罩[24],每名受试者在给药后30分钟至9小时的规定间隔内收集1至2个样本,在欧洲和澳大利亚进行的Babyhaler®研究中[25],在给药后15分钟至11小时的规定间隔内,每位受试者只采集一个样本。在我们的研究中,使用每种设备从每个参与者身上收集了四个剂量后样本。因此,在我们的研究中,这两种设备在相同的参与者群体中进行了比较,并使用了更频繁的抽样;因此,对变异性有更大的控制。此外,在Babyhaler®研究中[25]FP血浆浓度的检测下限为10pg·mL−1.,而本研究为5 pg·mL−1.. 另一种可能的解释是,由于患者、种族、饮食和其他因素的差异,FP血浆清除率可能存在差异。也就是说,我们的研究参与者的清除率可能较高,因此AUC较低。我们研究中AUC较低的另一个可能解释是给药持续时间:我们研究中为8天,其他两个平行研究中为12周[24,25].W贺兰等[26]提示,在成人中,FP血浆浓度可能在6周时间内积累,但这一观察是否可重复性以及是否适用于幼儿尚不清楚。然而,尽管可能短时间在我们的研究解释了auc越低,相对生物利用度,这不会有任何影响,因为我们使用交叉设计的短时间的顺序每个设备(AeroChamber®第一或Babyhaler®)发生同样的研究。
来自Babyhaler®的下AUC对带面罩的AeroChamber Plus®可能是由于设备特性的不同。Babyhaler®体积较大,死区较大,需要更多的潮气呼吸(大约四到六次呼吸)来清空腔室,而AeroChamber Plus®则需要更多的潮气呼吸(大约两次呼吸)适用于潮气量为180-195毫升的儿童,根据体外研究[15,27].本研究中计算的儿童潮气量范围为76-133毫升[2.],小于该区域使用的潮气量体外模拟研究[15,27]。这表明,与带面罩的AeroChamber Plus®相比,Babyhaler®需要更多的呼吸来排空。Babyhaler®额外呼吸所需的时间增加可能会导致室内药物沉降增加,从而减少可吸入的药物[16].
出于实际和伦理原因,我们没有测量给患者的实际剂量体外使用适合1-4岁儿童的肺部模型进行的研究表明,Babyhaler®和AeroChamber®或AeroChamber Plus®的肺部给药量相似[15,16,27],约为交付剂量的17–24%。然而体外模型可能无法准确反映肺部输送的差异在活的有机体内如我们的研究结果所示。
在Nemours儿童诊所,vhc是根据制造商的说明准备使用的,包括用肥皂水清洗,用清水漂洗和风干。肥皂水不允许在VHC中风干,这是一种已知的减少静电的方法[28,29在佛罗里达大学,这些房间是不用包装就用在包装上的。然而,在这两个地点,在第8天之前,每个VHC都有28个剂量释放到装置中,之前的研究表明,通过10-20次启动VHC以减少静电电荷,沙丁胺醇和布地奈德的肺输送量增加[30,31].在一个体外模型,包括潮汐量、舱室体积、死区体积、阀门不足的影响或VHC的其他泄漏、舱内的气溶胶沉降物和由于直接冲击VHC壁而造成的气溶胶损失。研究发现,起爆对可供吸入的剂量影响最大[15].虽然VHC实际上在第8天之前已经过两次每日给药的预充,但由于Babyhaler®的尺寸较大,可能需要对Babyhaler®进行28次以上的驱动以减少静电电荷;因此,预充不完全可能导致Babyhaler®的AUC较低[16].
面罩密封已被证明是吸入药物量的一个重要决定因素[4.,32–34].然而,没有父母注意到Babyhaler®有任何可能影响药物输送的困难。此外,最后四次剂量由父母在研究协调员在场的情况下给药,第8天剂量由同一研究协调员给每个部位的所有患者给药,以减少患者内和患者间的变异性。研究时FP罐上没有剂量计数器,其他依从性测量(患者报告和称量罐)对于评估依从性不准确[35,36].
血样采集采用群体药代动力学方法。可以使用几种群体药代动力学血样采集设计,但我们选择使用具有混合效应模型的稀疏采样技术,以尽量减少每个参与者所需的血样数量。该方法尤其适用于用于儿科药代动力学研究的ctive[24,25,37,38].在这种设计中,儿童被分配到几个血液取样方案中的一个,这样整个给药间隔都被取样,但每个时间点没有一个儿童接受血液取样。此方法使用聚合总体进行分析,而不是使用来自个体的数据。混合效应建模使用固定效应和随机效应描述数据,以描述主体间的可变性[18,23].在本研究中,由于参与者人数相对较少,协变量的影响没有被评估。一个零级吸收和一级消除的单室模型被发现最适合这些数据。
尽管AeroChamber Plus®的AUC几乎翻了一番对Babyhaler®,FP剂量为176 μg·天−1.(被认为是低剂量)[5.,39]不太可能,除了少数患者[24,25,40–45].随着气道阻塞的改善,肺输送量可能会增加[46,47]由于血清皮质醇的变化是剂量依赖性的,因此可能会产生更大的全身效应[48,49]FP对肺功能的最大影响是在∼3周[50];因此,在治疗的早期就可以看到对血清皮质醇的影响。重要的是,在该剂量(或其他ICS的等效剂量)下使用该药物,血清皮质醇或尿皮质醇排泄量的显著减少似乎不会转化为可观察到的临床副作用(生长率降低或眼部效应)≥1年[40,41]然而,已观察到个体对这些效应的敏感性[25,44,45]此外,为定义全身暴露(皮质醇当量)与生长速度变化之间的关系而开发的药代动力学/药效学模型确定,在本研究中使用的FP剂量下,VHC对生长速度没有影响[38].
我们的研究受到相对较小样本量的限制,无法评估协变量对AUC的影响。最有可能影响结果的协变量是气道阻塞。然而,不能在这么小的儿童中进行肺活量测定,也无法使用振荡法测量气道阻力和电抗标签在我们的网站上;美国只有少数中心有此程序。与哮喘患者相比,健康成人(无气流阻塞)吸入FP的系统生物利用度更高[46,47].然而,我们并不认为这是解释我们观察到的Babyhaler®和带面罩的AeroChamber Plus®之间差异的一个因素。这是一项持续时间短的交叉研究,因此治疗任务之间气道阻塞的变化不太可能会影响药物输送到肺部。
我们的研究结果对幼儿ICS的剂量以及未来的研究有几个重要的影响。从我们的研究和其他使用不同设备的研究中可以清楚地看出,VHC是不可互换的。这项肺生物利用度研究表明,根据所选的VHC,ICS剂量的差异几乎是两倍分娩可能发生在肺部。有人认为分娩的两倍差异与临床相关[51]成人ICSs的剂量-反应关系相对平稳,大多数低剂量患者的反应最大[48]在幼儿中,剂量-反应关系尚未得到很好的描述。因此,如果一名儿童在临床上稳定在低ICS剂量,并切换到VHC,肺输出量降低两倍,哮喘控制可能会恶化。相反,儿童维持中等或高ICS剂量(例如≥352μg·天−1.如果改用VHC,可增加两倍的产出量,则会出现全身不良反应。家长、临床医生和药剂师应接受教育,一旦孩子在特定ICS剂量和VHC组合上稳定下来,就不要交换VHC。此外,VHC的初始处方应包括语言(例如“不得替代”或“医学上必要”),以防止药剂师替代不同的VHC。我们建议,在常规使用特定ICS之前,应评估每个VHC的相对肺生物利用度。
致谢
感谢D.Collins、S.Srebro和L.Sutton(美国北卡罗来纳州三角研究园葛兰素史克)对本手稿的审阅。
脚注
支持声明
本研究得到葛兰素史克公司(美国北卡罗来纳州三角研究园)和美国国立卫生研究院综合临床研究中心M01 RR00082的资助。
感兴趣的语句
有关R.Mehta、R.L.Kunka和L.Hendeles以及研究本身的利益陈述,请访问www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到2010年12月1日。
- 认可的2011年6月15日。
- ©ERS 2012