抽象
肥胖和代谢综合症(MS)经常发生在阻塞性睡眠呼吸暂停综合征(OSAS)。我们假设循环中游离脂肪酸(FFA)的OSAS患者独立肥胖是升高的。这种提升可能有助于MS的在这些患者中发展。
我们研究了119名OSAS患者和119所控制。参与者被招募,并在我们的机构(医院Universitari儿子Dureta,帕尔马,西班牙)的睡眠单元研究并匹配了性别,年龄和身体质量指数(BMI)。MS的发生是通过临床标准进行分析。游离脂肪酸的血清水平,血糖,甘油三酯,胆固醇,高密度脂蛋白胆固醇,天冬氨酸转氨酶,丙氨酸转氨酶,γ谷氨酰,C反应蛋白和8-异前列烷进行了测定。
MS的发生率在OSAS比对照组高(38与21%;P = 0.006)。OSAS患者有较高的游离脂肪酸水平比对照组(平均±SD12.2±4.9与10.5±5.0 mg·dL−1;p = 0.015)。在无MS的受试者中,OSAS患者(OSAS+ MS-)的FFAs水平高于对照组(OSAS- MS-)(11.6±4.7)与10.0±4.4 mg·dL−1;p值= 0.04)。在多重回归模型,调整年龄,性别,BMI和MS的存在下,游离脂肪酸被显著与呼吸暂停/低通气指数(P = 0.04)相关联。
本研究表明,在OSAS中FFAs升高,可能是OSAS代谢并发症的机制之一。
阻塞性睡眠呼吸暂停综合征(Obstructive sleep apnoea syndrome, OSAS)是一种常见的疾病,其定义为反复发作的上气道阻塞和气流停止(apnoeas),通常会导致动脉低氧血症和睡眠中断[1,2]。若干临床特征,诸如肥胖,胰岛素抵抗和代谢综合征(MS)是经常,但不总是,存在于这些患者[3.]。
肥胖与OSAS患者多发性硬化症的发展之间的关系是复杂的,人们对其了解甚少[3.- - - - - -5]。肥胖通常被认为是OSAS和MS的危险因素[4]。然而,肥胖以外的因素似乎在OSAS患者代谢障碍的发展中发挥了重要作用[6,7],包括睡眠片段化和间歇性缺氧。
循环的游离脂肪酸(FFA)主要由脂肪组织的三甘油酯存储释放,并作为生理上重要的能量底物[8]。以前的研究表明,游离脂肪酸的胰岛素抵抗有关MS [发展和各种干扰中起重要作用9,10]。此外,游离脂肪酸也可促进氧化应激,炎症和血管内皮功能障碍[11- - - - - -13]。尽管在病理生理过程游离脂肪酸导致MS的显核心作用,存在没有研究调查OSAS游离脂肪酸和MS之间的关系
在本研究中,我们假设OSAS患者的FFAs升高与肥胖无关,而这种升高可能导致这些患者发生MS。为了验证这一假设,我们比较了它们在OSAS患者(有和没有MS)和匹配的对照组(有和没有MS)中的浓度。
方法
科目和职业道德
在本病例对照研究中,我们纳入了119例OSAS患者和119例对照组。
与会者来自谁参加我们机构的睡眠单位2008年1月至十二月2009年患者和对照组选择的依据OSAS的诊断和相匹配的性别主题招募,年龄(±5岁)和身体质量指数(BMI)(±3千克。米−2)。无其他慢性疾病(慢性阻塞性肺疾病、肝硬化、甲状腺功能障碍、类风湿关节炎、慢性肾功能衰竭和/或精神疾病)。服用低血糖、降血脂药和/或降压药的患者和对照组之间没有差异。没有参与者定期服用抗炎药物。本研究经我院伦理委员会批准,所有参与者在充分了解研究目的和特点后签署同意。
测量和定义
OSAS的诊断是通过全多导睡眠描记术(e系列;包括记录口鼻血流、胸腹运动、心电图、颏下和胫前肌电图、眼电图、脑电图和经皮动脉氧饱和度测量(年代A,O2)。呼吸暂停的定义是>在10秒内没有气流。低氧性被定义为>持续10秒并导致觉醒或氧饱和度降低的任何气流减少。我们认为饱和度降低年代A,O2> 4%。呼吸暂停/低呼吸指数(AHI)定义为每小时睡眠中呼吸暂停和低呼吸次数的总和。病例或对照组状态以AHI阈值≥10个事件·h来定义−1。患者分为三组根据他们的AHI温和(你好10 - 20事件·h−1)、中度(AHI 21-40事件·h−1)和严重OSAS(AHI> 40次事件·H−1)。
白天过度嗜睡是由爱华嗜睡量表主观量化。
根据国家胆固醇教育计划成人治疗小组III临床标准分析MS的发生情况:1)男性腰围≥102 cm,女性腰围≥88 cm;2)空腹血糖≧100mg·dL−1或特定药物治疗的患者;3)甘油三酯≥150毫克·dL的−1或接受特殊治疗的病人;4)高密度脂蛋白胆固醇(HDLc) <40 mg·dL−1男性和< 50 mg·dL−1在女性或特定药物治疗的患者;和5)收缩血压≥130毫米汞柱或舒张压≥85毫米汞柱,或患者特定的药物治疗。MS被诊断如果三个出这五个因素的存在。
禁食过夜后,在08:00和10:00 h的获得静脉血样。血液离心,血清立即分成等份并储存在-80℃直至分析。
葡萄糖,甘油三酯,总胆固醇,HDLC,天冬氨酸转氨酶,丙氨酸转氨酶,γ谷氨酰转移酶(GGT),尿酸和游离脂肪酸,通过在Hitachi模块化分析器标准酶促方法(Roche Diagnostics公司,印第安纳波利斯,IN,USA)测定。C-反应蛋白(CRP)的血浆浓度通过商业化学发光测定法上的IMMULITE 2000分析仪(西门子医疗诊断,NY,USA)进行测定。用的8-异前列烷EIA试剂盒(Cayman Chemicals Company的,安阿伯,MI,USA)测定8-异前列烷。
统计分析
结果表示为%,中值或平均值±SD。使用非配对t-检验(对于任何两个组之间的比较),并使用单因素ANOVA(用于多组比较)进行组装置的比较,随后事后对比在适当的时候。
为了确定睡眠呼吸暂停对游离脂肪酸的效果,我们采用多元回归分析,包括所有科目,研究组,年龄,性别,BMI和AHI作为自变量,游离脂肪酸作为因变量。
该研究供电以检测的2.0毫克的差dL的·−1在游离脂肪酸,假设在健康受试者中的2.0受试者内标准偏差13],显著性水平为5%,幂次为90%,每组20人。
变量之间的相关性采用Spearman等级试验探索。p值<0.05被认为显著。
结果
研究群体的特征总结表格1。在设计上,性别,年龄和体重指数是在患者和对照组类似。
MS的发生率是OSAS组中比对照组(p = 0.006)更高。
代谢和生化指标都在表2。表3和4根据MS的存在或不存在表明这些参数。
与对照受试者相比,OSAS患者表现葡萄糖,GGT,CRP的异常的血浆水平和8-异前列烷(表2)。
OSAS患者血浆FFAs水平明显高于无OSAS受试者(p = 0.015)。MS (OSAS+ MS+)的OSAS患者与MS (OSAS- MS+)对照组的FFAs差异无统计学意义(p = 0.271) (表3)。然而,如果不MS的受试者中,OSAS患者(OSAS + MS-)显示出比对照更高水平的游离脂肪酸的(OSAS- MS-)(P = 0.04)(表4)。
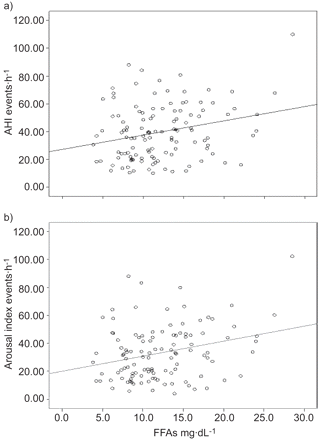
OSAS组FFA水平与AHI显著相关(r = 0.210, p = 0.026;图1一个)和觉醒指数(R = 0.236,P = 0.010;图1 b)。游离脂肪酸也显著相关GGT(R = 0.274,P = 0.003;图2一个),HDLC等水平(r = 0.305,P = 0.001;图2 b)。
游离脂肪酸(FFA)的水平,以及a)呼吸暂停/低通气指数(AHI)之间相关性(r = 0.204,P = 0.026)和b)觉醒指数(在阻塞性睡眠呼吸暂停综合征人口R = 0.210,P = 0.026)研究。
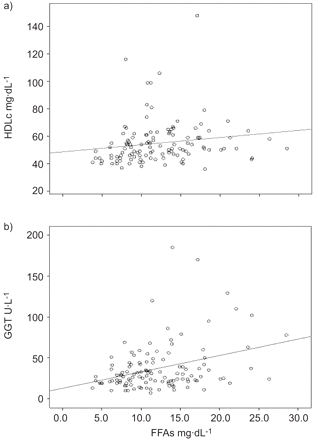
在阻塞性睡眠呼吸暂停综合征人群中,游离脂肪酸(FFA)水平与高密度脂蛋白/胆固醇(HDLc) (r = 0.305, p = 0.001)和g -谷氨酰基转移酶(GGT) (r = 0.274, p = 0.003)的关系。
FFA水平和夜间氧合指数之间的相关性没有达到统计学意义的水平(平均值)年代A,O2r = 0.189 (p = 0.083)和最小值年代A,O2R = 0.139(p值= 0.141))。
在多重回归模型,调整年龄,性别,BMI和MS的存在下,游离脂肪酸被显著与AHI(P = 0.028)相关联。
此外,游离脂肪酸,三组轻度,中度和重度OSAS(ANOVA P = 0.004)和更高的严重OSAS组之间显著不同(13.3±5.2毫克·dL的−1)比在温和的(11.4±4.2 mg·dL−1;P <0.004)和轻度OSAS组(10.5±4.0毫克·dL的−1;P <0.004)。
在没有OSAS MS,FFA水平在严重组较高(12.4±5.0毫克·dL的−1),轻至中度组(11.0±4.1 mg·dL)−1;P <0.01),但游离脂肪酸和AHI之间的相关性分析没有达到统计学显着性(r = 0.154; P = 0.191)。在这一组中,游离脂肪酸也涉及GGT(R = 0.274; P = 0.01),HDLC等相关(r = 0.305; P = 0.037)。
讨论
本研究的优势包括评估FFAs和OSAS之间的关联,以及不受混杂因素潜在影响的MS的存在。
这项研究表明:1)MS的患病率在OSAS患者比科目高于无相似的年龄,性别和BMI的OSAS,这表明OSAS本身是MS的危险因素;2)游离脂肪酸升高OSAS患者;和3)AHI独立地被游离脂肪酸水平相关。这些观察表明,FFA升高可能是参与OSAS患者的代谢并发症的机制之一。
OSAS,肥胖和MS之间的关系是复杂的,还不清楚[3.]。
OSAS患者中MS的患病率高于一般人群[14,15]。然而,这两种OSAS和MS与肥胖,这是用于OSAS的代谢变量的独立影响[重要的混杂因素相关联的5,16]。在我们的研究中,高女士在群患者的患病率比科目没有群相似的年龄,性别和体重指数,表明群本身是一个风险因素的女士女士与心血管事件的风险增加有关,糖尿病和非酒精脂肪肝疾病(17- - - - - -19]。在OSAS患者MS的高患病率提高的可能性,一些与所述MS相关联的并发症的可能归因于OSAS。在这个意义上说,最近的观测显示,阻塞性睡眠呼吸暂停在代谢综合征患者动脉粥样硬化的标志物的增量效应[20]。
对于可能有助于更好地OSAS与MS之间的链路的理解附加的因素搜索是高度期望的。在这项研究中,我们评估是否游离脂肪酸可以在OSAS MS的发展中发挥作用。
在健康受试者实验研究证明,在游离脂肪酸诱导的胰岛素抵抗的海拔[21]。此外,据报道,肥胖受试者中FFAs水平的升高会导致与MS相关的各种障碍的发展,如胰岛素抵抗、高血压、血脂异常等[10,11,22]。
FFA供应在肝脏中增加是用于MS的特性紊乱[发展的初始步骤12]。脂肪酸主要通过甘油三酯的脂解作用从脂肪组织中释放出来[23]。游离脂肪酸的释放由胰岛素作用的调节,并且通过肾上腺素能活性调制[23,24]。FFA浓度在肥胖者[高8]。然而,似乎有限制的个体差异,血浆游离脂肪酸水平与人相似的BMI [之间10]。在我们的研究中,尽管在OSAS组和对照组之间有着相似的人体测量特征,但在OSAS组FFAs含量更高,这表明在这些患者中FFA通量高源于脂肪组织的脂肪分解。
有几种机制支持OSAS和一个不正常的脂肪组织之间的关系,如交感神经活性增高,氧化胁迫或脂肪组织的炎症[25- - - - - -28]。与对照受试者相比,OSAS患者显示炎症和氧化应激的标记物,如CRP和8-异前列烷水平的异常血浆水平。然而,这些差异独立于MS的存在。在我们的研究中,FFA水平在OSAS患者高于无MS比没有MS控制。相比之下,尽管FFA水平OSAS患者高于MS比与MS控制,差异无统计学意义。这可能是在游离脂肪酸水平高变异检测无论是在控制和治疗MS可以解释缺乏意义的。
我们发现游离脂肪酸水平与AHI和觉醒指数之间的相关性显著,这表明睡眠片段化和重复觉醒可能在FFA释放到循环有关。然而,在OSAS这些机制和游离脂肪酸的调控,OSAS之间的中介作用和MS之间的关系需要进一步调查。游离脂肪酸水平在三组重度,中度和轻度OSAS之间的不同。在OSAS患者无MS,FFA水平也高于轻度至中度组高于重度组。我们的研究结果是一致的与林的一项研究et al。(29]。这些作者发现,脂肪细胞脂肪酸结合蛋白水平与阻塞性睡眠呼吸暂停独立地肥胖相关[29]。多重线性回归控制BMI,性别,年龄和MS的存在确认和AHI FFA水平之间的独立相关性。
多项证据支持了OSAS和脂代谢失调之间的独立联系[三十,31]。在我们的研究中,我们观察到的游离脂肪酸,HDLC等之间的关系,这表明游离脂肪酸的肝脏通量增加可能是一个重要因素血脂异常的存在OSAS患者。我们推测,高血浆游离脂肪酸可能是参与OSAS患者的代谢和心血管并发症的机制之一。
限制
一些潜在的混杂因素,如营养状况,身体活动或遗传变异之间的相互作用,并没有考虑到我们的分析。
分析没有对白蛋白进行调整。由于FFAs在血清中与白蛋白结合,这可能会影响结果[32]。
血浆游离脂肪酸的增加导致在健康受试者[内皮功能障碍33]。未来的研究应该研究FFAs的作用,使用技术来评估内皮功能,并评估其对OSAS患者血管床的长期影响。
然而,我们没有测量持续气道正压治疗后的FFAs水平。血浆FFAs水平正常化有望改善胰岛素抵抗和ms的其他特征。我们认为,需要进行包括这些测量在内的未来研究,以确定所有这些观察结果对OSAS患者代谢功能障碍的影响。
结论
这项研究表明,游离脂肪酸在OSAS升高,患者可能在MS的发病机制中起作用OSAS患者。
脚注
支持声明
支持的,部分由丰多科学调查德Sanitarias。
利益声明
无声明。
- 收到了2010年3月30日。
- 接受2010年10月9日。
- ©2011人队