抽象
老化肺癌病人可能在顺铂(CP)肾毒性的风险增加,因为合并症导致加速衰老肾脏的。因此,肾功能的Cp引起的影响无合并症(NC)和高血压加上缺血性心脏疾病(CD)患者或其他人有糖尿病以及缺血性心脏疾病(DMIH)之间进行比较。
在初步研究中,肾小球滤过率(GFR)通过的99m锝标记的二亚乙基硫胺五乙酸间隙测量在38肺癌患者与正常血清肌酸酐浓度([穿心莲])。然后,肾毒性的发生率进行了分析的Cp治疗的回顾性超过第一-第四周期中242名肺癌患者与正常初始[穿心莲]。GFR使用肌酐清除率反复研究。
预处理GFR为57±3毫升·分钟-1·米-2在那些与正常(N = 15)和42±2毫升·分钟-1·米-2在那些与病理性增加(N = 23)[穿心莲]任何时间以下的2-4的Cp周期(P <0.05)。回顾性分析显示,在CD(N = 110)的20.9%,并在DMIH(N = 52)的子组的30.8%,在NC(N = 80)的7.5%开发出的Cp诱导的肾毒性。在进一步的Cp化疗总辍学率,肾毒性是负责在NC的14%,在CD 38%,而在DMIH患者的75%。
我们的老化肺癌患者的主要部分来自合并症导致与Cp肾毒性降低肾性受到影响。
高剂量的顺铂(CP)为基础的联合化疗方案作为非小细胞和小细胞肺癌的一线治疗1。Cp的治疗效果由剂量递增的显著改善。然而,再用Cp高剂量疗法是通过其累积肾毒性限制2。Cp是有毒的肾近端和远端小管3。不同水化(盐水输注)协议中开发的降低肾毒性,并允许剂量递增至治疗水平4。然而,即使有警惕水化,用的Cp治疗的患者中大约三分之一有以下的Cp治疗血液尿素氮水平或在天肾损害的其他证据的暂时升高五。据伯恩斯和福特6,急性肾功能衰竭例住院患者中约20%是由于CP处于肾毒性。德Jongh等。7分析了对400名患者大剂量Cp的肾毒性影响预后的因素与54年的中位年龄和患不同实体肿瘤。肾毒性是(定义为估计的肌酐清除率的≥25%的下降Ç科瑞)在评估期间的任何时间。29%的患者开发的肾毒性,但在41%的患者中观察到上述正常上限血清肌酸酐浓度([穿心莲])的临时升高。他们的多因素分析所选的年龄,女性性别,吸烟,紫杉醇合用和低白蛋白血症肾功能的Cp诱导下降的独立危险因素。
在发达国家,肺癌患者有70岁的年龄中位数8。值得注意的是,肾脏衰老可能是肾毒素更敏感9。老年人口由合并症的影响,例如,高血压以及缺血性心脏疾病(CD)和/或糖尿病以及缺血性心脏疾病(DMIH)。底层和确诊,早期肾损害引起的年龄,CD或糖尿病单独或组合可能是中谁收到降压,vasodilatator或降糖治疗,但都没有的[科瑞]海拔老年患者存在。但是,在老年患者[穿心莲]和尿素的浓度可以仅仅因为降低的肌肉质量和蛋白质摄入的假性,分别。在具有降低的生产肌酸酐和低[穿心莲],异常低的肾小球滤过率(GFR)的条件[穿心莲]之前长时间可能会出现将达到所述参考范围的上限10。增加[穿心莲]将被认为是降低的GFR的至少敏感指示器10。不过,根据肾功能的正常血清指标,年龄CD或DMIH患者可以接受肺癌全剂量的Cp治疗。劳奈-Vacher等。11已经报道了,化疗前的445名肺癌患者〜60%已无法识别,第2阶段的肾脏疾病(GFR 60-89毫升·分钟-1),所估计的C科瑞。
因此,为了确定高剂量的Cp肾毒性的肺癌患者的发生,[穿心莲]的99m锝标记的二亚乙基硫胺五乙酸间隙(99米TC-DPTA)(GFR)和C科瑞(估计GFR; EGFR)之前和Cp的从CD,DMIH还患有或正在从这些潜在的合并症免费(; NC无合并症)患者在用药后进行比较。
材料与方法
研究对象和设计
Semmelweis大学(匈牙利布达佩斯)肺内科的肺肿瘤科每年治疗250-300名非小细胞和小细胞肺癌患者。由于大约30%的患者发生Cp诱导的可逆或持续性尿毒症,为了调查在Cp治疗之前GFR是否已经降低,而[creat]仍然正常,在一项初步的前瞻性研究中,我们通过清除来测量GFR99米TC-DPTA在38阶段IIIB-IV的肺癌患者与正常[穿心莲]调度用于基于CP的化疗。99米TC-DPTA间隙是由同一研究者(L. Duffek)在放射学和塞麦尔维斯大学的肿瘤治疗的系来测量。99米TC-DPTA(IzotópIntézetKFT。,匈牙利,布达佩斯)施用静脉注射的剂量为40个活度。然后患者根据他们的最高后的Cp [穿心莲]任一以下(N = 15)以上(23)所述参考范围的上限(> 106μmol·L分组-1)化疗期间的任何时间(2-4个周期)。Cp以75mg·m的剂量给药-2静脉注射在每个周期。CP输液相距≥21天。
接下来,我们回顾性分析2006年1月至12月间,242例iii期非小细胞或小细胞肺癌患者接受化疗的记录。我们的肿瘤学小组提出了高剂量Cp治疗,除了满足许多其他标准外,Cp仅适用于[creat]和尿素浓度正常且没有任何其他明显症状或肾功能改变迹象的患者。在对242例患者进行初步评估的基础上,根据是否伴有CD和/或DMIH形成了三个主要的亚组。NC亚组无高血压、缺血性心脏病、糖尿病。CD亚组是基于长期的、医学控制的高血压和缺血性心脏病(合并心血管疾病;(n = 110),而DMIH亚组是基于合并存在糖尿病和无高血压的缺血性心脏病(n = 52)。慢性动脉性高血压的诊断是基于病史和抗高血压药物的使用。缺血性心脏病的诊断依据病史、心电图异常和以前使用冠状动脉血管扩张剂、血小板聚集抑制剂或经皮冠状动脉腔内成形术的治疗。没有CD患者遭受了不受控制的高血压、心绞痛、急性心肌梗死或心脏代谢失调,或从任何其他急性或严重的心血管疾病,可能与大剂量化疗禁忌Cp。基于历史被诊断为糖尿病,胰岛素治疗(n = 5)或口头antidiabetetic治疗(n = 47)和空腹血清葡萄糖浓度高于正常水平。所有DMIH患者均未出现无法控制的高血糖或出现糖尿病主要并发症的症状。 Urinary protein test showed opalescence (≥1 g·day-1)在两名患者和轻微乳光(0.5-1.0克·天-1)另外两个患者;大多数具有负(<0.5 G·天-1)的结果。患者随后多次接受联合化疗,均为高剂量Cp (75 mg·m-2静脉注射),并且每个前和最高后的Cp [穿心莲]和尿素浓度值被记录。CP诱导的持续性尿毒症(其指示CP肾毒性)是从进一步的Cp治疗排斥的常见原因。这些患者的数量在三组间比较。临床数据,例如年龄,性别,慢性合并症,血压和肺癌的阶段收集。关于实验室数据,血清葡萄糖,[穿心莲]和尿素浓度进行了分析。[穿心莲]是基于使用来自Dialab(维纳诺伊多夫,奥地利)市售测试改性贾菲两点动力学反应来确定。C科瑞(EGFR)是根据Cockcroft-Gault方程式计算12。这种计算被选中是因为我们的病人的平均年龄<65岁13。
其他的治疗手段和药物
Cp由Teva Hungary(匈牙利布达佩斯)和EBEWE Pharma(奥地利Unterach)提供,剂量为75 mg·m-2。之一的三个附加的化疗剂进行组合给予与CP:吉西他滨(1250毫克·米-2;Eli Lilly公司,敦,荷兰),依托泊苷(3×120毫克·米-2)和紫杉醇(175毫克·米-2;二者施贵宝公司,普林斯顿,NJ,USA)。中性粒细胞减少,用粒细胞集落刺激因子(非格司亭,48个MU; Amgen公司,布雷达,荷兰)处理,严重的血小板减少与血小板输血,和贫血与促红细胞生成素(阿法依伯汀,40000 IU·周-1;杨森Cilag的,Centocor公司,莱顿,荷兰)和/或输血所指示的。需要患者接受镇痛和止吐药物,双膦酸盐,甲泼尼龙等症状药。
水化协议
一个静脉注射500毫升0.9%NaCl中的输注,随后在进一步的500毫升盐水吉西他滨,紫杉醇或依托泊苷。三分之一500毫升盐水输注后的Cp在500mL再次注入。在我们的手中,500毫升的输液通常需要20-30分钟。以下的Cp,第五500mL的盐水灌注(盐水的总体积〜2.5小时内2500毫升)和输液治疗用100mL 20%甘露醇结束(巴克斯特,迪尔菲尔德,IL,USA)静脉注射;甲泼尼龙(40毫克)和各种止吐药物在许多患者也分别给予。
统计分析
数据表示为均值±SEM. 使用GraphPad软件(Graph Pad Prism 5.0;Graph Pad software,Inc.,San Diego,CA,USA)进行统计分析,使用Fisher精确检验、卡方检验和t检验(配对和未配对)。采用单因素或双因素方差分析和Kruskal-Wallis检验对两组以上的患者进行比较。正态分布数据采用方差分析,非高斯分布或非参数值采用Kruskal-Wallis检验。单因素方差分析后,如果发现显著性差异(p<0.05),纽曼-凯尔斯多重比较事后检验用于进一步的分析。后两因素方差分析,使用Bonferroni事后检验。克鲁斯卡尔 - Wallis检验后,邓恩的多重比较事后试验进行。所施加的测试在表中和图例中描述。
结果
在38例肺癌患者中,23例在Cp后病理学上有反应,cret增加(表格1),虽然前处理[穿心莲]值在两组正常。预处理GFR,如通过清除测量99米TC-DPTA,是显著由〜25%,在这些肺癌患者有氮质血症谁回答的Cp治疗周期2-4减少。
为了证实这一点初步观察,进行在242名再用Cp治疗肺癌患者的Cp肾毒性的回顾性分析。其中约三分之二来自如CD或DMIH(主要合并症遭遇表2)。没有差异在性别中,Cp剂量的分布或在接受任何其他化疗剂的患者的比例指出。血压和心脏频率也分别在三个子相似,指示在CD群良好的血压控制。
患者数使得它可以分析4次后继CP之间的循环。第一个CP处理后,[穿心莲]在所有亚组增加,但变化是在子组CD和DMIH比NC(二者p <0.05显著更大;表3). 第二次Cp给药的患者可能少于三个亚组中的第一次,因为Cp肾毒性在许多情况下(见下文)。尽管Cp前[creat]值再次在参考范围内,但第二次Cp输注引起的[creat]增加比第一次大。这一次,DMIH组的血药浓度进入了病理范围,而CD组的血药浓度接近于病理范围,而NC组则不接近。在最初治疗的患者中,只有50%的患者进行了第3个Cp周期。Cp前[creat]再次正常,但Cp后CD和DMIH的值增加到病理范围,而NC亚组没有。大多数在第三次Cp给药后出现偶氮血症的患者在几周后表现出正常化(creat);只有少数在这一阶段退出。第四次大剂量Cp治疗是给那些[creat]值正常的患者,但是同样,CD和DMIH亚组的患者出现了azotaemia,而NC亚组没有观察到(表3)。血清尿素浓度遵循类似的模式为[穿心莲](未示出数据)。
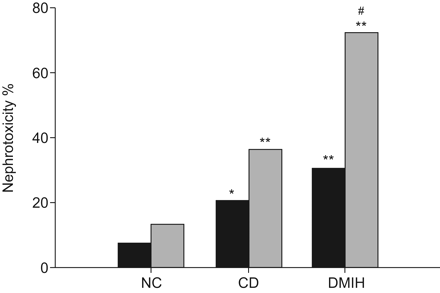
图1显示,的Cp诱导的持续性氮质血症(CP肾毒性)在NC的7.5%显影,CD的20.9%(P <0.05,与NC相比),在DMIH的30.8%(P <0.01,与NC相比)的患者。当检查的肾毒性,从进一步的Cp化疗整体差的贡献,该比例为在NC 14%,在CD 38%(P <0.01,与NC相比),75%在DMIH(P <0.0001与NC和比较p <0.01,CD)患者相比。
肾毒性频率(▪) 肺癌患者接受1-4个周期的大剂量顺铂(Cp)治疗,患有高血压和缺血性心脏病(CD)、糖尿病和缺血性心脏病(DMIH),或没有这些严重的合并症(NC),其肾毒性相关的下降。*:与NC相比p<0.05;**:与NC相比p<0.01;#:P <0.01,与CD(双尾检验差)相比较。
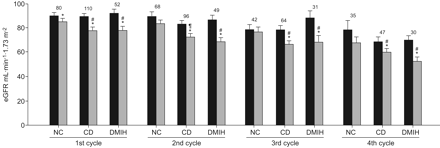
图2证明谁前一日3-4次后,再用Cp保持可治疗的患者的eGFRs。的Cp周期后前的Cp值和适度依次缩小,但仍保持三组在整个第1,第4周期相媲美。这似乎由克罗夫特 - 高尔特方程计算中EGFR是不是在预测CD或DMIH患者肾脏的高脆弱性不够敏感。不过,相对于在CP-天真值,EGFR第四的Cp周期之前,在NC仅约为4%,但16和18%的CD和DMIH组分别减少。总体而言,后的Cp eGFRs随后逆图案相对于[穿心莲]值的。NC患者只在第一个周期后显著eGFR降低的反应,而这两个并存组曾在Cp的所有循环减少的eGFP。统计分析表明,表皮生长因子受体被更在CD和DMIH降低(p <0.05)对NC患者的第二个周期后。
预(▪)和后顺铂(CP)(▓)估计肾小球滤过率在肺癌患者从没有合并症(NC),控制高血压病的高剂量的Cp治疗的第一-第四循环期间(EGFR)的值和缺血性心脏疾病(CD),或控制糖尿病和缺血性心脏疾病(DMIH)。柱上的数字表示的患者人数。*:P <0.05,与预CP(配对t检验)进行比较;¶与NC比较p<0.05(试验后与Bonferroni作双向方差分析);¶:与NC(试验后Bonferroni的双向方差分析)相比无显著性差异。
讨论
本研究表明:1)CD和/或DMIH是肺癌患者中频繁;2)这些合并症增加患者的Cp肾毒性,而那些老人谁是无CD和DMIH是Cp的肾副作用很大的抗拒;3)后茂尿毒症的发展似乎由温和,但显著,减少肾小球滤过率是可预测的,通过计算C作为估计科瑞或测量的99米Tc DPTA许可。尽管已知当GFR已经下降时,肾功能的血清标志物仍在参考范围内10,本观察结果表明,特别是在从CD或DMIH,正常[穿心莲]关于肾功能或朝向高剂量Cp的毒性作用可预测肾耐受状态误导作用的患者。的C估计科瑞可能提供更有价值的信息和更可靠地预测肾毒性的风险。
高龄,CD或糖尿病,特别是它们的组合可能会增加肾脏的灵敏度Cp的上述毒性作用。衰老与肾小球硬化和肾内血管的动脉硬化有关,导致肾功能丧失9。肾血流和肾小球滤过率降低,和许多正常肾小管吸收和分泌能力变钝。席尔瓦9建议老化应被看作是慷慨的备用容量或肾的安全边际损失的侵蚀。管状系统变得能够节约或分泌的NaCl的少14。在老年人中,exsiccation和/或低钠血症变得流行15。在老化肾,数量和小管的体积减小,并且肾间质的体积增加,由于纤维化,这可能与炎症相关联16。肾内动脉硬化在患者年龄10-19,20-39,40-64和> 65岁具有增加的频率注意到17. 关于肾脏老化的生理机制,如肾小球毛细血管高压、肾小球硬化、肾单位数目减少和无缺陷等,已经发现了一些重要的细节18,19。老化诱导提高的反应性氧物质的肾合成20和晚期糖基化终产物21. 衰老的生物标志物,如急性期蛋白,在老年肾脏中积累22。
慢性全身性高血压23和糖尿病24,25加速肾脏的老化。太田等。26表现出较高的脉冲波速度,动脉粥样硬化的标志,在主要肾动脉和从高血压和糖尿病患中年患者的肾间动脉。高血压性肾硬化与对肾小管间质慢性缺血性损伤相关27, Cp肾毒性的主要靶点。除了生理衰老外,长期高血压和糖尿病也会加速肾内动脉硬化18。糖尿病是复杂的,早期肾功能下降24,25。由于所有这些结果,其他原发性肾脏疾病(肾小球肾炎,急性肾功能衰竭和内毒素诱导的血栓形成)的过程中成为加速28,29。因此,氮质血症以下高剂量的Cp行政的发展可以出卖肾脏疾病通过CD或糖尿病引起的底层。
基于这些数据,高剂量Cp对患有CD或DMIH的老年肺癌患者肾毒性的夸大不足为奇。底层DMIH与氮质血症的最大频率高剂量Cp。因为没有一个病人发生急性或慢性肾功能衰竭,或需要肾脏替代治疗,有人可能会问:这是比较严重的肾的副作用Cp如此重要临床,一旦肺癌患者的预期寿命是不利的呢?Cp诱导的尿毒症非常重要,因为:1)在随后的化疗周期中,给予低剂量或不给予Cp;2) cp诱发的肾小球小管失衡导致Mg尿失禁加重2+,钙2+,千+,娜+,氯-和水。上电解质和水动态平衡这些影响可能诱发心律失常,循环性休克和死亡。
有哪些可以改善Cp的实验动物的肾毒性的药物一长串三十。美国食品和药物管理局已批准使用的有机磷汀硫代(Ethyol)在接受CP患者三十,31。癌症患者该组织细胞保护剂的报道疗效不明确32和药物价格昂贵。普遍证明有效的唯一可用的预防措施是通过等渗盐水hyperhydration之前,期间和Cp的输注后4。据我们所知,一直在肺癌患者接受和遵循普遍没有水化协议。关键事件似乎与Cp给药后几乎立即发生(在几个小时内)33. 因此,Cp输液前、中、后应立即采取防护措施33。还没有前瞻性的随机研究,以找出什么是适当的水合周围的Cp输液的老年人与潜在的亚临床肾病34. 生产Cp的公司建议Cp前水合作用足以诱导100-200 mL·h-1(2,400-4,800毫升·天-1)生理盐水利尿的时间由Cp输液,但推荐的体积,速度和时间静脉注射盐水输注之前,期间和之后的Cp似乎不是用于达到上述目的最佳的。虽然盐负荷比水化更重要35盐水利尿的确切定义也没有被详细说明。我们把它定义为排尿〜1%NaCl浓度的尿液。盐水输液,相对于水负荷,只能慢慢再用盐水利尿。的0.9%的NaCl输注(1000毫升)的开始后1个小时的间隔大概为盐水利尿的感应不足。值得注意的是,高尿流量(水利尿)本身并不是对环磷酰胺肾脏保护36;此外,Cp的抗肿瘤功效可能由水负荷被减小36。健康的成年人在西方饮食中摄入常规的盐(约为3克·天)-1)空隙1000-1500毫升尿超过24小时,并其尿NaCl浓度是<0.4%37。基于这些估计,一个健康的成年人的盐水利尿可以是不大于〜50毫升·H-1。老年人和厌食的癌症患者可能确实有显着降低尿排泄的盐水,这可能永远不会被系统地测试。老年人给予高血压或其他常见原因利尿剂可能使这些患者更在他们的化疗(清晨)抵达的时间干燥滤液。Ozols等。38,汤森和哈尼根39施用过程中的Cp给药每天6升的盐水的总体积。德Jongh等。7第一1L的输注0.9%NaCl中,然后的Cp于250mL高渗(3%)的NaCl超过≥3小时,然后再用2升的0.9%NaCl(〜6 1H总计处理时间)。在2006年,在我科(肺病的部,塞梅尔魏斯大学),高剂量的Cp在500mL 0.9%盐水输注(超过约30分钟)的1升的0.9%NaCl(〜1 h)以前在输注后。然后患者接受了进一步1.0-1.5 L的NaCl和之后的Cp 100毫升20%的甘露糖醇。总输液量为约3-4 L和3-4 L.内给予因此,看来我们可能提供较弱的预茂水化,用药更迅速,Cp和,当然,我们从来没有控制尿量或尿钠+浓度(盐水利尿)前的任何时间,期间或的Cp之后施用。甘露醇的管理也一直有些矛盾,因为这剂也可能加重预先存在肾功能不全40。
据哈尼根等。41盐水的输液通过增加重量克分子渗透浓度,而不是浓度,钠的保护肾细胞+或氯-。这些作者已经证明了体外在培养的近端小管细胞Cp的毒性可以通过增加与甘露糖醇,蔗糖,葡萄糖酸钠或NaCl的介质的渗透压相等地防止。CP在低渗介质是有毒的(~220毫渗量·公斤-1),但渗透压高-正常(∼280 mOsm·kg-1)提供了近充分的保护。已经假设,在重量克分子渗透压浓度的变化诱导细胞与核的体积变化,并且在染色质结构随之改变,这降低了的Cp与DNA的访问性。这也被认为有可能是Cp的肾细胞代谢,从而增加其毒性,是通过增加渗透压改变。
2008年,临床药学特殊利益集团对癌症护理欧洲社会预防的Cp肾毒性的制定明确的建议42。建议的基础是:1)GFR或C的估计科瑞使用肾脏疾病的缩写改性饮食或Cockcroft-Gault方程式;2)维护或euvolaemia诱导之前,期间和之后的Cp;3)Cp的缓慢给药;4)维持3-4 L·天-1之后的Cp前一天期间和盐水利尿2-3天;和5)避免利尿剂,包括呋塞米和甘露醇。
总之,在肺癌患者开始大剂量的Cp化疗前,肾毒性的风险应始终基于对EGFR评估42和共存CD或DMIH,因为这些条件,缩小肾脏Cp的耐受性。临床药学特殊利益集团对癌症护理欧洲社会预防的Cp肾毒性的2008年的建议42之前,也应该用生理盐水,中,老年,multimorbid肺癌患者的Cp给药后,随后就补充水分。然而,CD和DMIH患者vigourous输注生理盐水可能会导致容量负荷过重和肺水肿。都需要找出如何有效防止肾毒性的Cp没有心脏负担过重的风险进一步研究。
脚注
对于编辑评论见页760。
支持声明
这项研究得到了匈牙利科学研究基金的资助(OTKA K68758给G.Losonczy,OTKA 68808给I.Horváth)。
利益声明
无声明。
- 收到了2010年4月9日。
- 公认2010年6月29日。
- 版权所有ERS 2011