抽象
促红细胞生成素(EPO)和可溶性EPO受体(sEPOR)被认为在小鼠持续缺氧的通气适应过程中起中心作用。
在这项研究中,我们首次在人类(n = 9)中证明,sEPOR在白天暴露于4天的间歇性缺氧(IH;6 h·天−1,循环2分钟的缺氧和2分钟的复氧;潮末最高氧张力(PET,O-2托尔88,纳迪尔PET,O-245 Torr),从而使EPO浓度上升。我们还确定了这些血液学适应和急性低氧通气反应(AHVR)改变之间的联系强度。
我们观察到sEPOR在第2天达到最低点(-70%),与此同时EPO浓度达到峰值(+50%)。受IH影响后的潮汐量(VT)升高,呼吸频率保持不变,每分钟通气量(V′E)增加。EPO与sEPOR呈负相关(r = -0.261;(p = 0.05),并且在sEPOR和之间VT(R = -0.331; p = 0.02)。EPO呈正相关V′E(R = 0.458; P = 0.001)。
综上所述,IH下调sEPOR可调节随后的EPO反应。此外,IH后AHVR和呼吸模式的改变似乎是由EPO的增加介导的,至少部分是这样。
在人类中,响应于低氧增加促红细胞生成素(EPO)的浓度取决于持续时间和缺氧的严重程度1,短时间暴露于缺氧环境后,EPO的血浆浓度明显升高(高度约4,000 m ~ ~ 84 min)。2,约48小时后达到峰值3.。夜间缺氧(12-14小时·夜)−1)也已经显示出刺激EPO分泌,但EPO浓度的海拔不持续4。阻塞性睡眠呼吸暂停(OSA)患者的间歇性缺氧(IH)与EPO浓度升高的关系并不一致。一些研究报道EPO无系统改变5- - - - - -7,而相比之下,升高的EPO水平,白天坚持,已经报道了OSA患者8。这种差异背后的机制还没有被阐明,但是可以认为,诸如不同程度的OSA严重程度或常常与OSA相关的共病等因素可能发挥了作用。
从临床角度看,EPO已使用了二十年来治疗慢性贫血和同时在预防和/或与肾衰竭相关的贫血的校正通常使用9。最近,对EPO的作用机制广泛的研究导致了潜在的新角色的发现这种蛋白质。基于动物实验中,已经提出了EPO起着通气适应缺氧(VAH)作用和调节呼吸的神经控制10。在野生型小鼠中,全身注射重组人EPO (rhEPO)导致EPO与颈动脉体的EPO受体(EPOR)结合,这被认为增加了缺氧通气反应(HVR)。转基因小鼠的呼吸模式在大脑中过表达EPO10以及那些在大脑和血液中过度表达EPO的人11也被研究过。因此,至少在实验动物中,EPO似乎影响呼吸的中央控制和调节HVR。这个小组最近做了一个实验12在全身水平注射EPO (5000 U rhEPO)后,女性受试者比男性受试者表现出更大的通气增加。然而,对于在持续或间歇性缺氧条件下,特别是在短期缺氧条件下,EPO的内源性分泌的影响,在健康人群中所知甚少。
EPO的作用与它对EPOR的结合有关,EPOR存在于几个解剖部位,包括颈动脉体、前波辛格复合体和孤束核10。的EPOR(sEPOR)的可溶形式,对应于EPOR的胞外域,已在若干组织识别13包括人血浆14。可溶性EPOR与EPOR竞争以绑定EPO,从而限制EPO绑定EPOR的能力15。近日,Soliz等。16证实在小鼠中,在大脑sEPOR的下调,诱导持续缺氧3天(10%氧气2),是必要的,让受戒仪式展开。此外,作者还发现,将sEPOR直接输注于脑内不仅使VAH变得迟钝,而且还下调了EPO和EPOR的脑表达。这与EPO影响呼吸控制的潜在机制是由增加的EPO和减少的sEPOR之间的平衡决定的假设是一致的。
EPO是现在研究关于对在心脏缺血的保护作用的一个重要领域。尽管目前尚不清楚,慢性IH诱导OSA患者的增加EPO,预期的变化是增加在化学敏感性,因此,较大的呼吸不稳定性。本研究是重要的临床意义,因为它显然会理解的关键临床问题,像这样的帮助。
虽然已经有人提出EPO(非生理浓度)控制中央和外周的通气,但没有明确的证据表明sEPOR在血浆中的表达在这个调节回路中是否与在大脑中发挥类似的作用。此外,我们对人类的这种调节回路知之甚少。因此,我们假设,在模拟OSA的4天IH暴露中,健康的受试者会出现血浆sEPOR下调和EPO上调的情况。此外,我们推测ih介导的EPO和sEPOR表达的变化与呼吸模式(潮气量(VT)及呼吸频率(fR))和VAH。
方法
目前的工作是一项更大的研究的一部分,该研究使用了一种模拟中度阻塞性睡眠呼吸暂停患者(但在白天,即。当参与者清醒时)17,18。在这些实验研究中,我们的目的是研究IH对脉管系统(包括心脑血管)和呼吸控制的影响。本研究属于后一类,另一部分涉及氧化应激与HVR的关系。我们小组最近发表了两篇关于IH后心脑血管调节的文章,涉及相同的研究对象和研究方案17和氧化应激在由IH诱导急性低氧通气反应(AHVR)的作用(即。低氧血症和复氧循环)18。
伦理批准
这项关于EPO、sEPOR和呼吸模式的研究是与一项检查人类对IH的脑血管和心血管反应的研究一起进行的17。该议定书得到了卡尔加里大学(加拿大卡尔加里)联合卫生研究伦理委员会的批准,并符合《赫尔辛基宣言》。每个受试者在参与研究前均获得书面知情同意。
主题
九名健康的男性志愿者参与了这项研究。他们的意思是±sd年龄29±5岁,身高173.8±9.5 cm,体重76.2±10.6 kg。平均体重指数为25.1±1.4 kg·m−2。这些志愿者中没有人吸烟,也没有人有心血管、脑血管或呼吸系统疾病史。所有受试者均为卡尔加里(海拔1100米)≥1年的居民。
协议
实验是在我们的实验室中,位于1103米海拔进行的,并且在研究日的平均气压为663±1毫米汞柱。该协议之前已经描述17。简单地说,受试者在13天的时间里,分7天到实验室。前两天(第-4天和第0天)为对照组,在此期间,受试者暴露于假性肠内高压6小时。在接下来的4天(第1-4天),受试者暴露于6小时IH。暴露的最后一天(第8天)后4天,受试者返回实验室进行后续评估。每天的假性IH或IH暴露都是在白天进行的,受试者被告知不要睡觉。在每个实验日(第- 4,0,1 - 4,8天)结束时,进行一个分级低氧试验来评估呼吸模式。这个测试是在第8天的同一时间,在每日暴露假IH或IH结束后约30分钟进行的。
采集血样上天-4,0,1,2,4和8,受试者后〜15分钟离开腔室,以评估EPO的血清浓度和sEPOR的血浆浓度。通气参数(每分钟通气量(V′E),VT,fR和AHVR)的上天-4,0,1,2,3,4和8进行评价。
程序
在网上补充材料中提供呼吸测量的全部细节。
IH暴露
在IH的4天(第1-4天)中,受试者连续暴露于2分钟缺氧循环的6小时(最低点潮末氧张力(PET,O-2)45.0毫米汞柱)和2分钟常氧(峰PET,O-288.0毫米汞柱)。这个协议的进一步细节在别处发表17。
血样分析
血样采集在网上补充材料说明。EPO和sEPOR的血浆浓度的这两种血清浓度用ELISA测定。简言之,使用ELISA试剂盒(R&d系统,明尼阿波利斯,MN,USA)测定EPO浓度,而我们使用稍作修改的版本的方法通过韦斯特法尔描述等。14评估sEPOR。这些方法的详细说明可以在网上补充材料中找到。
统计分析
除人体测量数据,并在网上补充材料中提供的数据,所有的数据都以平均值(95%CI)。不包括在统计分析的两个出54个血样。在一个主题,血液中的数据并没有由于技术上的困难收集1天。在另一个志愿者,sEPOR的浓度在第8天为五个以上的倍高(13.2sd)比平均,并且因此,它被处理为异常值,并从进一步分析中删除。这个数据点被视为基础,它外面落在±对异常值2-sd边界。两个控制天通气和血液的数据,即。第4天和第0天在统计学上没有差异,因此,将这两个基线合并起来进行进一步分析,并在本文的其余部分将其称为“基线”(Bsl)。通气设备的数据(V′E,VT和fR),并使用单向重复测量ANOVA分析血液标志物(EPO和sEPOR)。然后,邓奈特-许试验用于鉴定装置之间显著差异。线性回归分析(与对应的相关系数(r)的)用于分析(血液中标志物(EPO和sEPOR)的变化和通气部件之间的总体关系V′E,VT和fR)。广义线性模型(GLM;与对应的多个相关系数(MR))被用于分析跨研究的天血液标志物的变化和通气部件之间的关系。似然比检验来评估的关系是否显著彼此取决于研究的当天不同。具有自回归相关结构的混合模型回归分析用于描述之间的关系V′E以及在每个时间点根据受试者的EPO水平作为时变协变量进行调整的时间。采用SPSS(16.0版;SPSS Inc.,芝加哥,伊利诺伊州,美国)和SAS(版本9.2;(美国北卡罗来纳州凯里市SAS研究所有限公司)。显著性水平设为p≤0.05。
结果
测量休息
休息换气数据在网上补充表1中进行了概述。
IH暴露对通风元件的影响
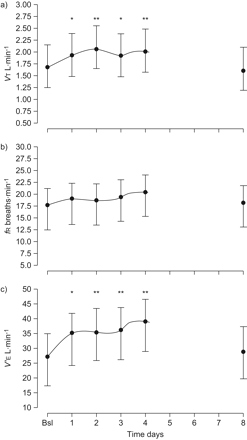
图1说明了在等窒息缺氧时测量的分钟通气成分的变化。我们观察到…的增加VT随着时间的推移(p值= 0.001),1天和4天(+ 20%之间的高原与BSL),接着通过曝光结束时(后4天返回到BSL级别即。第8天)。反过来,fR在整个研究中没有显著变化(p = 0.11)。总体而言,这些变化导致总通气随时间增加(p = 0.004),除第8天外,每个数据点都高于Bsl。类似于VT我们观察到,V′E达到在1天的高原,其在暴露于IH曝光结束之后返回到BSL级别4天,然后期间持续存在。对于AHVR更详细的结果呈现在别处18,并概述在网上补充材料做了简要的。
4天间歇性缺氧时换气的改变。a)潮气量的变化(VT),B)呼吸频率(fR)和c)每分钟通气量(V′E)急性缺氧试验(呼气末氧张力45.0毫米汞柱和呼气末二氧化碳张力1.5毫米汞柱以上静息)中被示出。VT与基线(Bsl)相比,从第1天增加到第4天fR没有改变。作为一个结果,V′E在缺氧过程增加。数据以胡须代表9个参与者95% CI的平均值表示。*:p≤0.05与声波测井;**:P≤0.01与声波测井。
对EPO分泌IH的影响
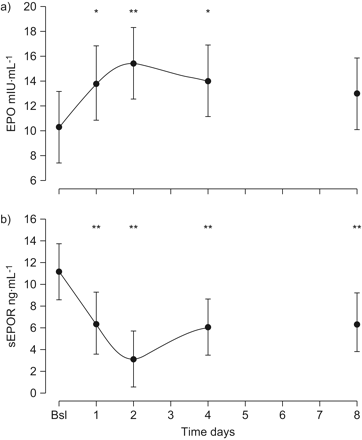
图2一个说明我们的IH模型随着时间的推移刺激了EPO的分泌(p = 0.04)。EPO分泌高峰出现在第2天(+50%)与声波测井;P = 0.003)。在第4天,EPO的刺激仍高于基线水平显著高(+ 36%与声波测井;p = 0.02),此后,EPO浓度在第8天恢复到Bsl值。
血清)促红细胞生成素(EPO)和b)可溶于EPO受体(sEPOR)4天以上间歇性缺氧的。随着时间的推移在EPO和sEPOR的变化被示出。注意在EPO浓度的增加,开始第1天与第2天之后的峰,EPO浓度朝着基线(BSL)水平降低,但仍上相比BSL4天更高。缺氧暴露结束后4天,EPO浓度不从BSL不同。sEPOR暴露于缺氧(第1-4天)期间下降,与上与BSL相比2天最低点。后缺氧恢复4天,sEPOR浓度仍高于BSL低。数据以胡须代表9个参与者95% CI的平均值表示。数据缺失第1天(对于EPO和sEPOR)一个主体和用于在第8天的另一对象(仅sEPOR)。*:p≤0.05与声波测井;**:P≤0.01与声波测井。
IH对血浆sEPOR浓度的影响
在常氧期,sEPOR的浓度与Westphal提出的相似等。14。暴露于IH后,我们观察到第1天开始下降(-43%与声波测井;P = 0.007),与第2天最低点(-70%与声波测井;p < 0.001)。此后,sEPOR浓度在第4天向Bsl回归(-46%)与声波测井;P = 0.002),并保持在所述暴露结束后第4天相同的水平,即。第8天(图2 b)。我们还研究了EPO/sEPOR比值;我们观察到类似于EPO的双相进化,但不显著(p = 0.124;数据未显示)。正如后面所讨论的,我们观察了“反应者”和“无反应者”,这可能至少部分地解释了这个结果。
EPO和sEPOR、通气成分和低氧敏感性之间的关系
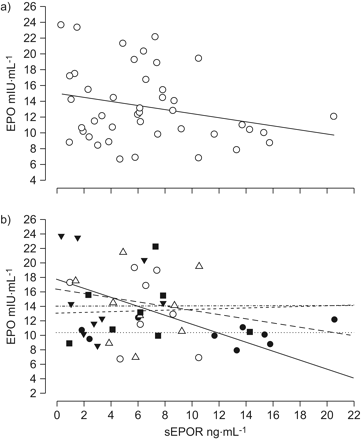
我们观察到sEPOR和EPO之间的整体逆关系(r = 0.26;p = 0.05;图3),同时,根据该模型GLM,EPO和sEPOR之间的关系依赖于研究日,但没有显著性(r = 0.41; P = 0.77;图3 b)。只有在第1天和第2天有相反的关系,在Bsl没有关系,在第4天和第8天。
促红细胞生成素(EPO)和EPO可溶性受体(sEPOR)之间的相关性。a)总相关(r = 0.26; P = 0.05)和b)每日(MR = 0.41; EPO和sEPOR(N = 9)之间p值= 0.77)的关系。的所有单个数据示除了一个主题为其EPO和sEPOR数据失踪1天,另一主题为其sEPOR数据缺少天8.一个)○和 - :所有的数据点。B)•和......:基线;○和 - :每日1次;▾和 - - - 2日;▵和 - · - · - 4日;▪和---:8的一天。
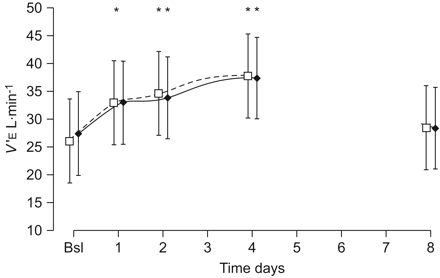
有EPO之间的相对强劲的整体正相关V′E在AHVR测试期间(; P = 0.001; R = 0.46数据未显示)。然而,从混合模型回归分析,由此通风和时间之间的关系是在每个时间点调整EPO的结果,表明EPO对效果非常有限V′E,在AHVR (图4)。这是显而易见的,因为未调整和调整装置是相互接近的。
分钟通气之间关系的混合模型回归分析(V′E)和时间。该图显示了in的变化V′E在整个实验过程中图1(未调整;□)和调整促红细胞生成素(EPO;♦)。第3天没有数据,因为那天没有采集血样。EPO的系统性增加对其改变的影响非常有限V′E。数据以胡须代表9个参与者95% CI的平均值表示。*:p≤0.05与声波测井;**:P≤0.01与车贴语为未调整的车贴语,经调整的车贴语为EPO回归分析。
总的来说,我们也观察到sEPOR的改变与in相关VT(r = 0.33;p = 0.02;数据未显示)。
讨论
主要发现
这项关于健康人类志愿者IH的研究有四个新发现。首先,我们发现V′E由于较高的VT早在IH暴露1天后,持续暴露4天(同时AHVR逐渐升高;请参阅网上的补充资料和18)。其次,我们在人中证明了暴露于IH期间血浆浓度sEPOR降低。第三,我们观察到在sEPOR的减少增加EPO浓度随之而来。最后,EPO和之间观察到适度的强关联V′E之间,以及sEPOR和VT,表明EPO和sEPOR既可以在白天被暴露于IH后观察通气量增加起到一定的作用。
暴露于IH后呼吸模式的改变以及对急性等呼吸器官缺氧的反应
我们观察到的娃的迹象(即。增加VT与变化不大fR;图1)与由长期暴露于持续缺氧(审查介导AHVR变化一致,看19)。然而,暴露于慢性IH,如阻塞性睡眠呼吸暂停患者所经历的,是一个更复杂的范例20.。虽然一些研究已经显示在以急性缺氧与IH通气应答的增加21,其他人没有22,有的已经找到了OSA患者对缺氧的迟钝的通气反应23。在我们的IH模型中,我们观察到VT,V′E和AHVR(见网上补充材料AHVR的结果和概述18参阅更详细的介绍)。这与另一项使用健康受试者OSA模型的研究一致24。塔米西尔等。24使用从我们的一个稍微不同的模式,只要该受试者睡眠过程中暴露和复氧进行15秒,每2分钟(与脱氧的2分钟,并在本研究中2分钟再充氧)。此外,他们的研究对象暴露于IH的≤28天。他们在第4天曝光,因为我们没有没有测量通气适应,但他们提供的长期驯化非常有用的信息。他们实际上观察缺氧敏感性的逐渐上升后,7天和14天曝光24。有许多因素可以解释使用OSA模型得出的结果与以往涉及OSA患者的研究结果之间的差异。例如,有研究认为年龄、病程和疾病严重程度可能与OSA患者AHVR的改变有关20.。在我们的研究中,受试者是健康的年轻男性,没有这种混杂因素。
有趣的是,我们观察到两个增长VT和V′E早在1天之后曝光的,我们没有观察到在暴露于IH以下3天进一步增加。这是最有可能是由于缺氧在本研究中所花的相对较短的总时间。在由塔米西尔研究等。24,很可能他们报告的HVR的增加主要是由于VT。他们的实验对象每天花费更多的时间与6小时IH)更长的一段时间(14或28与4天)提示本研究中存在不完全的VAH。
改建EPO和sEPOR暴露于IH
在本研究中,我们报告暴露于IH的第一天之后增加EPO浓度,对应于中度低氧的3小时。擦汗等。8报告说增加了暴露于IH几年OSA患者血清EPO浓度,而另一些则没有5- - - - - -7。这些发散的结果可以用不同的严重程度在所研究的患者和/或通过混杂常与OSA相关的因素来解释。OSA患者的适应性变化也可能解释这种差异;然而,这一点仍有些投机。
一般的共识是,后2天暴露于慢性缺氧EPO浓度达到峰值3.。我们观察到了类似的模式(即。EPO的第2天)后的峰值,但是这是因为我们的曝光模式的诱导时间较短。不幸的是,我们的数据没有提供底层机制的明显证据。
这是在其中等离子体sEPOR浓度经测量在暴露于IH第一人体研究。我们提供的证据表明,sEPOR被暴露于IH下降。我们的发现与那些Soliz报道一致等。16在小鼠中,尽管不同的低氧暴露模式(较短的时间和严重的缺氧)。鉴于我们观察到一个明显的下降后第1天和最低点第2天,似乎sEPOR的反应是迅速的和非常敏感的缺氧。因此,索利兹报告了下降等。16暴露于缺氧环境3天后,可能低估了这种降低的幅度。第8天,sEPOR浓度仍低于Bsl值。这一观察结果可能与IH后偶尔观察到的AHVR残留增加有关25但这种解释是不符合目前的结果是一致的。因此,响应sEPOR的这个方面值得进一步研究。
另一个有趣的观察是,尽管全球的sEPOR水平在第2天下降到最低点,但个体间的差异很大。事实上,9名受试者中有2名在Bsl和第2天的测量值之间没有任何下降,这两名“无反应者”与其他受试者相比,sEPOR的正常氧基线水平特别低。与EPO相似的是,我们在sEPOR对IH的反应中观察到“反应者”和“无反应者”的分组。与其他仅有的研究相比,我们的研究对象所暴露的缺氧剂量是温和的16我们的研究对象对持续缺氧的反应可能有所不同。值得注意的是,在整个研究过程中,其中一名受试者在通气方面的变化非常有限。
在他们的动物模型中,索利兹等。16提出了EPO在大脑的增加先出现,然后直接刺激通气,而在sEPOR下降后发生并保持增加EPO的可用性。然而,我们的数据不支持这种假设,至少在制度层面,因为我们发现的密切配合EPO和sEPOR反应(但方向相反)分别表现出的峰值和低谷,图案,第2天此外,负的关系,我们EPO和sEPOR之间观察到在1和2天(图3)似乎进一步证实了这一假设,尽管根据全球全球语言监测缺乏意义。因此,在循环血浆中,EPO和sEPOR似乎都与肾脏释放的EPO密切相关9同时发生的循环sEPOR浓度下降,以最大限度地提高EPO的生物利用度。
在促红细胞生成素的改变和IH两者期间的呼吸模式和HVR之间的相互作用
Soliz等。10,11上过表达EPO的小鼠的线工作无论是在脑中只(TG21)10在大脑和血液中(Tg6)11。作者的结论是,中央EPO过表达改变呼吸模式的增加fR,而全身EPO表达调制颈动脉体的响应。这两项研究的结论是,EPO具有刺激通风的能力。然而,最近的一项研究报道EPO注射在人体中的作用12以及它们在男性和女性之间的通气反应观察到大的差别,后者是唯一一个由5000Ù的rhEPO的单次注射正面影响。以Gassmann等。26近日汇集他们以前的研究结果10- - - - - -12并从性别二态性的角度总结了EPO的作用26。Thosee作者提出增加EPO的在脑中的作用不受性别二态性,而血浆EPO增加(单次注射之后,或在它们的转基因小鼠或者线)不诱导性差的研究。在本实验中,研究只雄性和我们的结果与现有文献一致,只要我们没有观察EPO效果清晰V′E(图4)。因此,我们证实,EPO系统的增加对通气的影响非常有限,至少对成年男性是如此。
然而,在血浆EPO浓度持续升高似乎有,只要我们观察到EPO和HVR之间的总体相关性在整个研究的颈动脉体刺激作用(R = 0.475; P = 0.001;数据未示出)。不幸的是,根据最近的文献(见上文),这一观察背后的机制仍不清楚。
由于血清EPO浓度持续升高,我们观察到(图2一个)人们可能会推测EPO最终会穿过血脑屏障,这一机制已经在兔子身上得到了证明27,28。同样,星形胶质细胞29,30.和神经元30.的缺氧性脑的也被证明以释放EPO,既促使更多其中心浓度。总之,这些机制可能最终导致增加EPO的央企,因此获得刺激通风的能力,但我们承认这仍然是投机性的,在这个阶段。
IH期间sEPOR改变和呼吸模式之间的相互作用
由于其对EPO亲和力强,具有sEPOR EPOR竞争以结合对EPO15。其结果是,当暴露于缺氧时,其减少允许更多的促红细胞生成素结合促红细胞生成素,反过来,解释成红细胞16。因此,sEPOR在这一过程中起着中心作用。在目前的研究中,我们报告说,sEPOR在等离子体中实际上是减少暴露在IH。此外,我们观察到sEPOR和之间的联系VT(数据没有显示)。这一结果与最近的小鼠实验结果一致,表明暴露在持续缺氧环境中3天内持续输注sEPOR (10% O2)不仅使sEPOR维持在暴露前的浓度,而且在随后的AHVR测试中消除了通气反应16。然而,我们承认这种关系代表所涉及的参数之一,最有可能的,表演sEPOR和通风中心之间的间接联系。
限制
尽管它的新颖性,我们承认我们的研究有一定的局限性。首先,我们来模拟OSA的IH模式的创新特点是它采用健康受试者往往与OSA相关绎混杂因素。但是,“真正的” OSA和我们正常人OSA的模型之间的主要区别;我们的模型是poikilocapnic缺氧,而OSA涉及高碳酸血症。不幸的是,另一个强大的模型提出塔米西尔等。24面临同样的限制。我们的模型与OSA患者经历的IH的另一个不同之处在于,本研究是在白天进行的,而受试者是醒着的。第二,全球监测机制就日间机制提供了有益的补充资料。然而,尽管有足够高的能力来检测EPO和sEPOR的差异(分别为0.77和>0.95),我们建议,我们适度的样本量可能会限制GLM分析的完整解释。同样,虽然本研究强调了现有文献支持的新机制,但我们观察到的关联并不代表明确的因果关系。例如,EPO和HVR的机制(即。中央与在EPO外周的增加)值得进一步研究。
摘要和结论
综上所述,我们的数据表明,sEPORs在白天暴露于IH时下调。随着sEPOR的减少,我们观察到EPO的增加。我们也证实了IH引发了in的增加V′E通过较高的介VT,而fR不受影响。然而,EPO对二者的影响并不明显V′E或低氧通气反应,但我们提供的是什么sEPOR之间最有可能的间接关系的证据VT。综上所述,这些新的发现为暴露于IH后急性缺氧时sEPOR在增加通气中的作用提供了证据。然而,EPO扮演的角色并不明确。目前的发现证实了最近一次实验的结果12说明全身EPO对HVR的影响不大,尤其是对男性受试者。由于本研究中EPO浓度持续升高,我们不能排除其对VAH有更中心的积极影响,但这方面显然需要进一步的研究。因此,似乎应该从不同的角度来解释Epo在系统一级的增加所产生的影响,而不是从中央一级的相同增加所产生的影响。根据目前的研究结果,驯化过程中所涉及的机制及其相关贡献还需要进一步的研究来充分理解。
最后,本研究中,我们小组在同一志愿者另一个最近发表的研究沿18突出氧化应激在HVR的刺激作用,在描述一起工作以促进VAH两种新的机制。实际上,多重回归分析显示,一起,EPO和氧化应激(8-羟基-29脱氧鸟苷;的8-OHdG)解释40%(即。r2= 0.40;HRV反应p<0.001。HVR此外,这两个变量是重要预测因子(EPOβ= 0.49 (p < 0.001)和8-OHdGβ= 0.39 (p < 0.001),不联系在一起,这表明促红细胞生成素和氧化应激调节HVR独立。这些结果为理解IH如何改变呼吸控制提供了新的潜在的生理机制。此外,目前的研究可能为潜在的未来治疗方法提供重要的途径,因为sEPOR已经被证明有能力废除VAH,因此,可能稳定呼吸。
致谢
我们感谢所有的志愿者为他们的快乐和专门参与这项研究。免疫学试剂(mh2er / 16.5.1)中的溶液麻烦由惠氏研究所(剑桥,MA,USA)提供。
脚注
这篇文章有补充资料www.www.qdcxjkg.com
支持声明
这项研究得到了阿尔伯塔传统医学研究基金会(AHFMR;M.J. Poulin)补助金从亚伯达省的心脏与中风基金会NWT和努勒维特(P.J.汉和M.J.保林),一个新的机会从加拿大创新基金会资助奖(M.J.保林),全职助学金AHFMR和加拿大心脏与中风基金会(ge培养),加拿大卫生研究院的研究(CIHR)加拿大硕士研究生奖学金奖(C.T.C. Duggan),火炬和CIHR战略培训奖学金(明天的研究心血管健康专业人员)(ge福斯特和C.T.C. Duggan),全职霍奇大脑研究所的奖学金(J.V. Brugniaux),该AHFMR(诉Pialoux)和加拿大心脏与中风基金会关注中风计划(J.V. Brugniaux曾帮工诉Pialoux),和一个AHFMR高级医学学者奖(M.J.保林)。
感兴趣的语句
没有宣布。
- 收到了2009年10月3日。
- 接受2010年8月1日。
- ©2011人队