摘要
缺氧和运动被认为是高原肺水肿(high altitude pulmonary edema, HAPE)发生的两个主要因素,但其病理生理机制尚不清楚。因此,我们将32只sd大鼠随机分为常氧休息组、低氧休息组、常氧运动组和低氧运动组。
使用缺氧缺氧模拟4,700米的海拔高度,而运动组成48小时,每4小时休息15-20分钟。在每只动物上进行动脉血液,支气管肺泡灌洗(BAL),肺湿对干重(W / D)比率和组织学测量。
在低氧运动的大鼠中,BAL蛋白和肺W/D比率显著增加,但BAL白三烯B无变化4.和免疫球蛋白M被观察到。在同一组中,肺组织学显示典型的出血性肺水肿和肺泡上皮和毛细血管内皮的破坏,而缺氧或仅诱导轻微内皮和上皮肿胀/破坏。
我们的研究建立了HAPE样症状的组织学和生理学证据之间的直接联系,并且我们证明,在Sprague–Dawley大鼠中,缺氧和劳累可以协同诱导HAPE样症状,而不会诱导肺部炎症。因此,我们提出肺泡上皮和毛细血管内皮应力破坏y在HAPE的发展中起着重要作用。
高空肺水肿(HAPE)是一种可能致命的病症,可能影响迅速向高度提升到高度> 3,000米的非自由化个人1那2.大约2%暴露在高海拔地区的人受到HAPE的严重影响,需要寻求治疗3..然而,在海拔> 4500 m的人群中,亚临床HAPE的发病率可能高达75%4..
缺氧和劳累已被确定为Hape发展中的两个主要因素5.. 然而,触发HAPE发展的确切机制尚不完全清楚。虽然炎症和肺泡液体清除率降低等因素被认为在HAPE病理生理学中很重要6.-9.,肺毛细管应激衰竭,这是由不均匀的缺氧肺血管电压产生的结果10那11,已被建议成为主要煽动机制。实际上,肺毛细血管透气压力增加12-14导致肺泡膜破裂15,使得富含蛋白质的出血性水肿液充斥肺泡腔。霍普金斯et al。16发现在缺氧条件下锻炼人类的压力失败的证据,并透气et al。17研究表明,HAPE患者BAL液中存在红细胞以及蛋白质浓度增加,BAL细胞因子无明显变化。然而,肺毛细血管应力衰竭是否是HAPE发生的主要机制尚不明确,因为无法获得直接证据表明HAPE患者存在毛细血管破裂罗姆人。
因此,需要动物模型来获得肺中毛细血管破裂的直接组织学证据。迄今为止,兔子,绵羊,狗和雪貂已被用来发展Hape动物模型,但结果既不一致也不可重复18-20.大鼠也被用于许多研究,但都需要内毒素激发19,暴露于严重缺氧(236 托尔,9000 m) 或者使用特定的大鼠品系,如麦迪逊品系,该品系对诱导HAPE具有高度敏感性15那21.对猪的一些研究表明,当猪暴露于常压缺氧时,HAPE发病的结果与之一致22,但没有提供令人信服的组织学证据。
在这项研究中,我们假设低氧和运动的结合会导致肺毛细血管的应激性衰竭,并诱发HAPE样症状。为了验证这一假设,我们利用在低氧条件下运动的大鼠建立了HAPE模型。该模型首次允许我们将组织学evi直接联系起来毛细血管破裂与支气管肺泡灌洗(BAL)结果和干湿(W/D)比率的相关性。
材料和方法
动物
选用成年雄性Sprague-Dawley大鼠(复旦大学动物中心,中国上海),体重252 ~ 298 g。实验开始前,将大鼠置于12小时昼夜光照周期2天。所有动物方案均由复旦大学动物保护委员会批准。所有动物实验均按照美国国立卫生研究院(National Institutes of Health)发布的《研究动物使用和护理指南》(Guidelines for the Use and Care of Research Animals)进行23.
实验设计
缺氧环境
低压缺氧室(真空室,华南造船厂,上海,中国)用于产生特定的缺氧条件。简单地说,关闭真空室后,真空室内的空气压力通过与真空室相连的真空逐渐降低。压力降低率设置为20 m·s-1直到它达到相当于4,700米的高度(≈419.97托)的压力。
大鼠在跑步机上运动
训练大鼠以12 m·min的速度在跑步机上行走(DSPT-202, Duan Co., Ltd, China, Hangzhou)-1暴露于缺氧前2天。当大鼠暴露于瓣育低氧缺氧时,它们被迫使用电刺激,在大约12米·min的跑步机上行走-124.
实验组和对照组
每组8只大鼠,各组分别为:常压常压静息(NR)暴露大鼠;大鼠暴露于常压常氧运动(NE);运动性低压缺氧大鼠(HE);以及暴露于低压缺氧(HR)的大鼠。在运动组(低氧或常氧),大鼠步行48小时 h,但允许停车15-20分钟 每4分钟 h、 这样他们就可以获得食物或水。值得注意的是,大鼠在48小时内持续暴露于缺氧 H所有程序均在主室进行,研究者可通过独立控制的前室进入主室,压力设置为470.48 托尔(≈3,800 m)21.当主室压力降至3800 m时,研究者可以进入主室检查大鼠。当研究者完成干预后,将腔室置于419.97 Torr(≈4700 m)的压力下。因此,大鼠大部分时间暴露在模拟海拔4700米的环境中,短暂暴露在3800米的环境中。
动脉血气
在主腔室中进行以下步骤,压力相当于3,800米,用于调查人员安全21.麻醉后(腹腔注射10%水合氯醛3 mg·kg-1;中国上海上海的中国药膏化学试剂有限公司,血液通过直接穿刺和使用肝素的注射器从左心室进行取样来迅速收集。GEM总理3000(仪器实验室,贝福德,MA,美国)立即分析了动脉血液天然气分析的所有血液样本。动脉血液pH值,动脉二氧化碳张力(P.,有限公司2)及动脉血氧压(P.啊,一个2)根据直肠温度进行校正22.
肺组织学
肺在20厘米每小时的压力下充气2o最初然后保持在5 cmh2切开左心房后,用生理盐水灌注肺通过右心室在20-30cmh的压力下2O.当流出血液细胞清除时,肺被灌注10分钟并储存在4%多聚甲醛中,用于光学显微镜或3%戊二醛在4℃下电子显微镜检查。15.5天后,肺被埋入并切片。苏木精和伊红染色切片采用标准程序制备23.基于肺泡水肿,间质水肿,出血,中性粒细胞和巨噬细胞渗透来评分微观肺损伤。血红素和曙红染色切片中肺损伤严重程度的等级如下:没有伤害= 0;25%的领域受伤= 1;50%的领域受伤= 2;75%的领域受伤= 3;并弥漫伤害= 426.所有的组织学样本由两位独立的病理学家按照先前所做的双盲方案进行评分23.电子显微镜成像如前所述15.设定了分级评分,以定量内皮/上皮胁迫失效。该得分由检查部分的每个表面单元观察到的断裂次数组成。
巴尔
将右肺被连接并切片,通过左主支气管将1ml 0.9%的盐水注入左肺。在温和和重复冲洗后2-3倍后取出BAL流体。将总共3ml注入3mL,将BAL流体储存在无菌容器中,通过无菌纱布过滤,以除去粘液和细胞碎片,然后在-80℃下保持在-80℃下进行细胞因子测量22使用Sysmex KX-21(日本神户Sysmex有限公司)计数红细胞和白细胞。使用自动分析仪(日本东京日立有限公司HITACHI-7600)测量总蛋白和白蛋白。使用自动分析仪(日立有限公司HITACHI-7600)通过免疫比浊法测量BAL免疫球蛋白(Ig)M27.BAL白三烯(LT) B4.根据制造商的议定书,由大鼠ELISA套件(Rapidbio Lab,CA,CA)检测到Rate Elisa Kit(Calabasas,CA)。
结果
八只大鼠中有三只暴露于低压低氧运动中,死于27-35.5岁之间 h、 其余三组动物均存活。
动脉血气
我们观察到显著下降P.啊,一个2HE和HR大鼠与NR和NE大鼠比较(表1)⇓;p < 0.01)。P.,有限公司2HE和HR大鼠也因过度通气而降低(表1)⇓;P <0.01和0.05)。pH值显著增加仅在HR大鼠中观察到(表1)⇓;p < 0.05)。基于动脉血气,我们计算了不同组的肺泡-动脉差异(表1)⇓).肺泡-动脉差的计算方法如下:
P.啊,一个2-P.啊,一个2
在哪里P.啊,一个2= (BP -P.H2O.)F一、 O2-P.,有限公司2/ R
P.啊,一个2是肺泡氧气张力;BP是气压;P.H2O.水蒸气部分压力为1atm和37°C;F一、 O2为吸气氧分数;, R为呼吸商,上式设为0.8。与NR、NE和HR组相比,HE组肺泡-动脉差异显著增加,表明肺气体交换效率降低。
肺w / d重量比
肺W/D比值是整体肺水肿严重程度的指标29.HE和HR大鼠肺W/D重量比显著高于对照组(NR)大鼠(表1)⇑;P <0.01和0.05)。HE组的W / D比显着高于NE组(P <0.01)。NE和NR组之间的肺W / D重量比没有显着差异。
巴尔
BAL蛋白是肺泡毛细血管膜通透性变化的指标30..与NE和对照组NR大鼠相比,HE和HR大鼠BAL总蛋白浓度显著升高(表1)⇑;p < 0.01)。HE和HR大鼠BAL中的白蛋白浓度也明显高于NE和NR大鼠(表1)⇑;分别为p<0.01和0.05)。尽管HE和HR大鼠的总蛋白和白蛋白均增加,但两组之间没有显著差异。与NE和NR大鼠相比,HE和HR大鼠BAL中的红细胞和白细胞计数显著增加(表1) 1.⇑;P <0.01和0.05)。HE大鼠红细胞计数显著高于HR大鼠(p<0.05)。基于Schoeneet al。6.世卫组织观察到BAL-IgM和LTB水平升高4.在人类受试者中,我们进行了Bal IgM和LTB4.测量。四组之间没有显着差异(表1⇑)巴尔先生4.数据表明,炎症可能不会参与我们的Hape模型的早期阶段。然而,BAL蛋白质测量以及细胞计数表明缺氧暴露增加肺泡 - 毛细血管渗透性,而运动协同扩大缺氧引起的阻挡损伤。
大体外观和光学显微镜
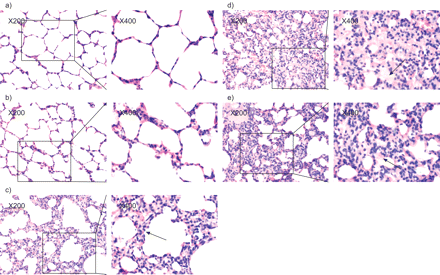
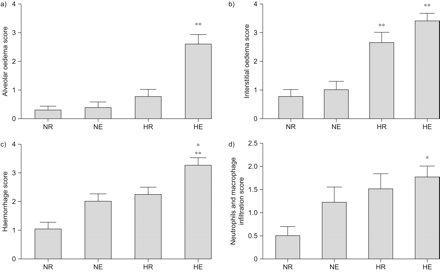
HE组3只死亡大鼠鼻口出血,提示严重肺水肿。五分之三的HE幸存者和八分之一的HR大鼠表现出不同程度的肺出血。与NR大鼠相比(图1a)⇓), HE未存活者肺泡内肺泡水肿液明显增多,肺间质肿胀/增厚,红细胞增多(图1d⇓)他在老鼠中幸存下来(图。 1e⇓).HR大鼠中的肺组织学显示肺泡空间中显着增厚的肺泡隔膜和少量红细胞,但没有明显的肺泡水肿(图1C⇓),表明缺氧本身不会诱发HAPE样症状。在NE大鼠中,间质中的红细胞仅略有增加,但肺泡和间质水肿无明显增加(图。 1b⇓).图2提供了组织学发现的摘要⇓.与其他三组相比,He组的肺泡水肿评分显着增加(图2A⇓)与NR组相比,HE组和HR组间质水肿评分均显著增加(图。 2b⇓;p < 0.01)。与NE和NR组相比,HE组的出血评分显著升高(图2c)⇓;分别为p<0.05和0.01)。与对照(NR)组相比,HE组中性粒细胞和巨噬细胞浸润增加(图。 二维⇓;p < 0.05)。综上所述,形态学分析显示,与单纯缺氧和运动相比,联合缺氧和运动可导致更严重的肺泡-毛细血管屏障破坏。在HE大鼠中观察到的严重屏障破坏以典型的肺泡出血和水肿为特征。
苏木精伊红染色肺组织。a)静息时暴露于常压常氧状态下的大鼠。b)运动后常压常氧大鼠肺泡间隔稍增厚,间质红细胞较少。c)在休息时暴露于低压缺氧的大鼠。箭头示间质性肺水肿。d)暴露于低氧运动(HE)大鼠的非幸存者。箭头示肺泡水肿伴红细胞。切片表现为弥漫性间质水肿。e) HE组幸存者。箭头示肺泡水肿伴红细胞。 The slice presents a diffuse interstitial oedema. Two magnifications (×200 and ×400) of the same slice are displayed for each group.
肺损伤的组织学评分。a)肺泡水肿评分。**:运动性低气压缺氧(HE)大鼠p<0.01与暴露于休息(HR)的低次次缺氧的大鼠,暴露于常规(Ne)和暴露于疗程(NR)的正常常见氧毒性的大鼠的大鼠。b)卧间水肿得分。**:HE和HR组P <0.01与NE组和NR组。c)出血评分。*:HE组p<0.05与NE组;**:HE组p<0.01与NR组。d)中性粒细胞和巨噬细胞浸润评分。*: HE组p<0.05与NR组。每组N = 8。数据以平均值±表示SEM..
电子显微镜
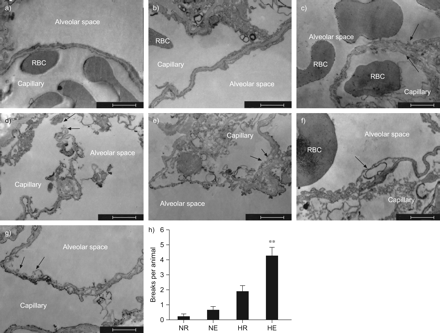
电镜显示详细的超微结构变化。图3a显示正常(NR组)上皮和内皮屏障⇓在HE大鼠中,血气屏障完全破裂(图3d),包括内皮层破裂(图3d)。 3e⇓)上皮肿胀(图。 3f⇓)和上皮的破坏(图3G⇓)与对照大鼠相比(图3A⇓)和NE大鼠(图3B⇓)上皮细胞受到不均匀的影响,有肿胀或破裂的迹象(图。 3f⇓g)和肺泡中的红细胞提示肺泡上皮细胞被破坏和剥落,有利于肺泡浸润。在HR大鼠中,轻微的内皮和上皮肿胀以及肺泡间隙的少量红细胞表明类似于人类亚临床HAPE的情况(图3c⇓)电子显微镜损伤评分显示,缺氧或单独运动仅轻微增加内皮细胞和上皮细胞肿胀/破坏,而缺氧和运动一起显著诱导内皮细胞和上皮细胞破坏(图。 3g⇓).
电子显微镜调查结果。a)对照组(大鼠暴露于ressobaric armoxia(nr))。毛细管中血气屏障和红细胞(RBCS)的连续性。秤杆=1μm。b)用运动(NE)暴露于正常常见常见氧化的大鼠。血液 - 气体屏障的连续性和毛细管中的RBC。秤杆=1μm。c)在休息(HR)下暴露于瓣育低氧缺氧的大鼠。内皮层和上皮衬里(箭头)和毛细管和肺泡中的RBC肿胀。秤杆=2μm。 d) Rats exposed to hypobaric hypoxia with exercise (HE). Complete rupture of the blood–gas barrier including epithelium, endothelium and basement membrane (arrows). Scale bar = 1 μm. e) HE group. Disruption of endothelial layer (arrows). Scale bar = 2 μm. f) HE group. Swelling of epithelial lining (arrow) and RBCs in the alveolar space. Scale bar = 2 μm. g) HE group. Disruption of epithelial lining (arrows). Scale bar = 1 μm. h) Summary of electron microscopy findings. The results are averaged numbers (±SEM.)每片表面单位观察到的肺泡毛细血管破裂。对每只大鼠进行了三片切片分析。**: HE组p<0.01与HR,NE和NR组。硝酸镧用作示踪剂,以突出肺泡壁。
讨论
缺氧和运动被认为是HAPE发生的两个主要因素,我们假设HE大鼠会出现HAPE样症状。因此,我们建立了缺氧条件下运动诱发HAPE的大鼠动物模型。
我们的结果表明,HE大鼠出现了典型的HAPE样症状,这是由生理学和组织学分析确定的,如肺泡-动脉差异增加(表1) 1.⇑),增加了水灰比(表 1.⇑),增加了BAL总蛋白/白蛋白含量(表1)⇑),肺内皮细胞和上皮细胞肿胀/破裂和肺泡泛红/出血(图 1.⇑, 2⇑和3⇑).据我们所知,这项研究首次表明,缺氧和运动协同诱导斯普拉格-道利大鼠hape样症状。确实,尽管在缺氧或运动暴露的大鼠中BAL总蛋白和白蛋白浓度显著增加,但在同时暴露于缺氧和运动的大鼠中,BAL总蛋白和白蛋白浓度的增加更高(表1)⇑),提示内皮/上皮通透性恶化31.-33..此外,详细的电镜分析显示,缺氧或运动仅引起轻微的肺泡上皮和毛细血管内皮肿胀/破坏,而联合缺氧和运动显著增加内皮/上皮肿胀和破坏。HE大鼠BAL中红细胞计数的升高强调了缺氧和用力联合对肺泡毛细血管膜的破坏。在我们的模型中,HR大鼠表现出与人类亚临床HAPE相对应的中间特征/症状。事实上,间质水肿得分,球白蛋白浓度、球红细胞内容和W / D比率与NR和NE组相比升高但这些参数仍低于他组和alveolar-arterial差异并不意味着肺气体交换的一个改变。
使用该模型,我们还首次显示了应力失效的组织学证据与其他测量数据(如W/D比、BAL分析和动脉血气)之间的直接联系。确实,毛细血管破裂与水肿评分、W/D比值、BAL白蛋白浓度和肺泡-动脉差异呈正相关(表2)⇓).这些明确的相关性强烈建议压力衰竭在我们模型中的类似Hape样症状的发展中发挥着重要作用。
另一个被认为在HAPE发病机制中发挥作用的因素是炎症6..因此,我们测量了IgM和LTB4.落下帷幕。然而,四组间两种LTB均无显著差异4.和IgM。在我们的动物模型中,没有炎症迹象的远端肺病变表明炎症在hape样症状的发展中起次要作用17.此外,尽管HE组中性粒细胞和巨噬细胞浸润评分较高,但在其他实验组(HR和NE大鼠)中也升高,且与水肿评分、毛细血管破裂或W/D比值均无显著相关性(表2)⇑).
减少肺泡液清除率(AFC)也被认为有助于HAPE的发展7.-9..实际上,在肺泡泛滥的情况下,通过允许肺泡流体去除,肺泡流体清除率构成第一防御,已知通过上皮的活性纵向传输的机制。由于缺氧介导的肺泡上皮钠通道的功能/表达抑制7.那9.,AFC可能会在我们的模型中受到影响。然而,关于HE组中观察到的肺损伤,我们不认为AFC降低触发了我们模型中HAPE的形成。AFC目前正在我们的动物模型中进行研究。
然而,我们的模型确实存在一些局限性。事实上,由于我们的实验环境中测量的复杂性,我们无法测量肺动脉压,并且运动强度可能无法转换为在人类中观察到的运动水平。
因此,我们提出,通过劳累加重缺氧性肺血管收缩会导致远端肺结构的应激性衰竭,促进肺泡泛红,伴有富含蛋白质和出血性水肿。
综上所述,我们的暴露于低压缺氧的运动大鼠模型能够在没有内毒素引发、严重缺氧或使用特殊菌株的情况下诱发HAPE样症状。我们的HAPE模型与肺部炎症无关。BAL中白蛋白浓度升高以及W/D比升高与肺水肿之间的相关性内皮/上皮肿胀/破坏提示肺泡毛细血管屏障应力破坏在HAPE的发生中起主要作用。
支持声明
上海市领先学科项目(项目编号:B115);国家自然科学基金项目(30871131);国家211工程项目(211XK20;所有的中国)。
兴趣表
没有人申报。
致谢
感谢刘敏(上海交通大学,上海,中国)的文献检索支持,Yu z(复旦大学上海医学院,上海)的电子显微镜技术支持,Xu z(复旦大学上海医学院)的组织学支持,Zhang H.和Zhu W.(上海海军医学研究所)使用低压缺氧舱。我们还要感谢M. Howard(加州大学,旧金山,加州,美国)对科学写作的支持。
脚注
对于编辑评论,请参阅第470页。
- 收到了2009年1月5日。
- 公认2009年8月26日。
- ©ERS期刊有限公司