文摘
只有一小部分的吸烟者患慢性阻塞性肺疾病(COPD),表明遗传易感性的重要角色。瘦素受体(LEPR)存在于人类的肺组织,可能在COPD发病机制中发挥作用。目前的研究调查了基因变异之间的关系LEPR基因和COPD肺功能下降。
总的来说,429年欧洲美国人随机选择从国家心肺和血液研究所肺部健康研究。36单核苷酸多态性(snp)LEPR基因分型使用Illumina公司吗TMGoldenGate平台(Broad研究所,剑桥,妈,美国)。年平均用力呼气量下降1 s %预计时间埋葬期间使用线性回归计算。线性回归模型也被调整了潜在的混杂因素。此外,在活的有机体内受体基因的表达与免疫组织化学评估肺从smoke-exposed天生的老鼠。
我们识别重要的之间的关联(p < 0.05)和21个snp肺功能下降。单体型分析证实其中的几个协会与单个标记。免疫组织化学结果在小鼠近交品种支持潜在LEPR在COPD发病机制中的作用。
我们确定了基因变异LEPR基因显著相关的肺功能下降的人口吸烟与慢性阻塞性肺病。我们的结果支持的角色LEPR作为一个小说慢性阻塞性肺病的候选基因。
慢性阻塞性肺疾病(COPD)是第四大死因在美国和全世界第五大死因,及其普遍预计将增加在未来几十年1,2。绝大多数COPD是由环境因素引起的。在美国,这种接触主要是吸烟(CS);然而,只有15%的吸烟者发展慢性阻塞性肺病。这表明遗传易感性的重要角色。
除了在肥胖(抑制食欲),瘦素已被证明有多个其他功能,包括交感神经活动增加,维持生殖功能,免疫力,血管生成,保持正常的呼吸功能的肥胖和细胞增殖的气管上皮细胞和肺的增长3。调整后的肥胖,瘦素通路与炎症标记物以及多个有关炎症条件,包括心血管疾病4,5。其潜在作用在COPD患者系统性炎症反应明显瘦素与其他相关的炎症标记物6- - - - - -8。瘦素可以直接刺激巨噬细胞的吞噬活动,提高endotoxin-induced生产肿瘤坏死factor-α、白介素6 (IL)和白介素,通常细胞因子参与了COPD发病机理9- - - - - -12。相反,缺乏瘦素及其受体可能使患者免疫缺陷和感染10。血清中瘦素水平升高在急性加重的慢性阻塞性肺病,也一直在与肺部细菌感染有关,而与慢性阻塞性肺病急性加重,肺功能下降有关7,13- - - - - -15。瘦素对多种影响通过其瘦素受体(LEPR),位于人类染色体1奔跑。产生LEPR在几个或者拼接形式分享细胞外和跨膜域但不同细胞质残留16,具有广泛的组织分布,包括肺组织17。
我们测试的基因变异之间的联系LEPR基因和肺功能下降的一个子集多中心国家心脏,肺和血液研究所(NHLBI)支持肺部健康研究(lh)队列。此外,潜在LEPR在COPD发病机理中的作用进一步评估smoke-exposed AKR / J小鼠,显示标记领空扩大的组织学和形态学标准18。决定居民LEPR是否不同局部肺细胞的情况下,模拟人类的慢性阻塞性肺病,我们对小鼠进行免疫组织化学肺部分来自AKR CS / J小鼠暴露于4个月与室内空气控制。
识别途径和新颖的分子靶点,修改临床病程发展预防策略和新的治疗方法的基础。
方法
主题
受试者参与当前的研究包括了429年欧洲的美国人(EA)随机选择的4287名参与者进行的多中心的NHLBI-supported lh的DNA。肺功能测定每年超过5年,根据美国胸科学会指南使用相同的肺活量计,软件,程序和阅读中心人员19,20.。肺量测定法测试的质量由技术人员进行集中监控在整个测试和比较的基线呼吸量测定法显示良好的再现性很小的意思是短期措施自身内在的变化在1 s (FEV用力呼气量1)21。肺功能的数据年度访问1年访问5用于当前分析和已被证明有很好的线性符合先前的lh分析19,22。受试者不到三年肺功能测量被排除在分析(n = 15)。
单核苷酸多态性选择和基因分型
单核苷酸多态性(SNPs)表示LEPR基因选择从Goldenpath (genome.ucsc.edu)和/或国家生物技术信息中心(NCBI;www.ncbi.nlm.nih.gov;美国马里兰州贝塞斯达)。标准包括:1)单核苷酸多态性近似inter-SNP距离尽可能接近5 kb当时可用的dbSNP建造124 (NCBI);2)表示的单核苷酸多态性在启动子、编码和3′翻译;3)单核苷酸多态性与可接受的设计分数据Illumina公司分析设计工具Illumina公司基因分型TMGoldenGate平台(Broad研究所,剑桥,妈,美国)。优先选择snp包括:1)监管和编码单核苷酸多态性;2)高度多态的单核苷酸多态性,最好是次要的等位基因频率≥10%;3)验证单核苷酸多态性;和4)内含子/外显子的snp边界。36LEPR人类染色体snp跨越228294个基点1奔跑的平均inter-SNP距离6.53 kb(范围1.9 -14 kb)列于表1⇓。
统计分析
年平均肺功能下降(post-bronchodilator FEV1%预测)是计算线性回归斜率时间埋葬研究期间。线性回归模型被用来调整潜在的混杂因素,包括基线特征、吸烟史(pack-yrs),年龄,性别,FEV1% pred和气道反应性(AR)。基于“增大化现实”技术的计算作为一个定量测量,利用两点斜率22。除了调整基线特征,1)体重指数(BMI)的变化,计算线性回归斜率和2)吸烟状态在5年,定义为“连续抽烟”,“间歇吸烟者”和“持续的懒人”,也分析。
向前和向后选择被用来开发一个吝啬的模型。回归的残差中基因加性模型和最常见的纯合子基因型为每个SNP作为参考类别。吸烟和遗传效应的交互项测试使用叮铃声(美国波士顿)23,而定量测试交互。每一个SNP位点均为哈迪温伯格平衡。所有分析StataSE,版本8.0(美国占据集团,大学城,TX)和叮铃声23。
个人单体型分析使用叮铃声。成对连锁不平衡(LD)基于D′统计测量使用Haploview (Broad研究所)24。LD块定义使用默认的算法25。滑动窗口的两到四个相邻的单核苷酸多态性被用来测试协会。单体型估计计算使用阶段(美国西雅图,华盛顿州)假设没有重组26。
小鼠模型
10周大AKR / J小鼠暴露于CS 5 h·天−1,5天·周−1为6个月。曝光是由燃烧2 r4f参考香烟(列克星敦市肯塔基大学,烟草研究所,肯塔基州,美国),使用一个天井吸烟机(爱尔兰人企业,林地、钙、美国)。每个香烟抽2 s,每分钟总共八个泡芙,流速为1.05 L·分钟−1提供一个标准的35厘米3。烟雾机调整产生的混合物(89%)和侧流烟烟主流烟(11%)。烟室每天监测了总悬浮颗粒物和一氧化碳浓度为90毫克·m−3和350 ppm。Air-exposed控制老鼠被安置在一个过滤的空气环境。
免疫组织化学
从smoke-exposed 5-μm paraformaldehyde-fixed,石蜡包埋组织部分和室内空气控制AKR / J小鼠deparaffinised和水化乙醇系列。部分被封锁与3%正常血清非特异性结合从鸡肉和主要抗体孵育1 h在室温下。孵化后与主抗体在一夜之间在4°C,幻灯片和PBS Tween-20洗,孵化为30分钟在室温下用一个适当的生物素化的二次抗体和发展利用3、3′-diaminobenzidine衬底和chromagen Dako(英国斯托克波特)。抗原检索使用柠檬酸缓冲执行了30分钟。抗体被用于以下浓度:LEPR, ObR(山羊多克隆,我很快,1:10 0;美国圣克鲁斯生物技术、圣克鲁斯,AZ),驴抗体二级抗体(sc2020 1:400,圣克鲁斯生物技术)。
结果
临床特点的主题展示在表2⇓。没有统计的差异之间的基线特征(n = 414)包括在最终的分析与排除因为超过两个数据点在肺功能失踪(n = 15日数据未显示)。分布的基线特征和肺功能测量也类似的完整的lh组这个子集被选中(n = 5887,数据未显示)。年龄,基线肺功能,基于“增大化现实”技术、吸烟状态在5年,独立和体重指数的变化与肺功能下降,并被包含在最终的回归分析。没有明显吸烟状态之间的相互作用在5和LEPR多态性。
Single-marker分析
所有36LEPR单核苷酸多态性在哈迪温伯格平衡。所有两点测试结果之间的联系LEPR标记和FEV1% pred下降展示在表3⇓。我们发现的证据明显的21单核苷酸多态性之间的关联LEPR基因和FEV1% pred下降,跨越的长度基因内含子2的5′末端。最重要的微小等位基因单核苷酸多态性与衰减肺功能下降有关。特别感兴趣的,每个功能标记rs1137100 G等位基因,在第4外显子,它创建了一个赖氨酸精氨酸氨基酸变化与·年0.33%−1衰减FEV的年度亏损1% pred。
单体型分析
考虑大多数基因snp的集群在六LD块与高水平的LD snp之间也观察到在不同的块,一个系统的滑动窗口方法实现,考虑到windows的两到四个snp /窗口开始第一个(5′)标记,在基因和工作,一次一个标记。单体型测试显示多个协会在三个特定区域重叠信号与上面描述的snp的结果。协会25个单显示强于单个SNP的结果(图2所示⇓)。其中最引人注目的5′末端的地区LEPR(区域1)和单体型GCCT (rs7531867、rs1805096 rs1892535和rs6691346),显示一个强大的协会与肺功能下降(p = 0.003)和包括coding-synonymous SNP, rs1805096。此外,一个3-SNP和两个4-SNP窗口区域2中单生成rs10443259 rs10889562(内含子2到5)最密切相关的肺功能下降(p = 0.002),并包含功能性rs1137100标志,如前所述。
成对连锁不平衡(LD)的主题是强大的LD表示为红色方块,无意义的LD的蓝色方块,白色方块很少或根本没有LD。LD街区被确定为指出。
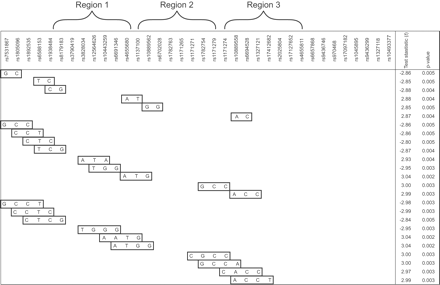
单(n = 25)显示协会大于单核苷酸多态性的结果。
的验证LEPR作为一个纯系小鼠慢性阻塞性肺病的候选基因表型
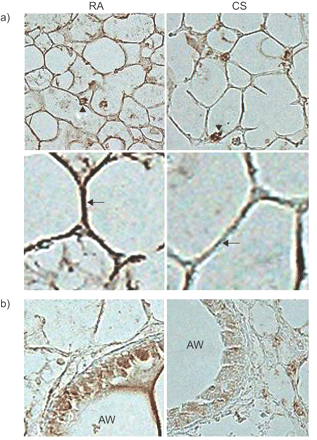
AKR / J小鼠,特征明显近交品系,暴露于4个月的CS不仅展览领空扩大还开发气道增厚和炎症,是非常让人想起慢性阻塞性肺病18。我们检查是否CS暴露改变LEPR表达式在肺部的压力。使用免疫组织化学,我们观察到LEPR在巨噬细胞表达明显,航空公司和房间的领空隔间air-exposed AKR / J小鼠。然而,在烟雾暴露,降低染色的领空和气道壁(图3所示⇓)。这些发现符合LEPR表达差别CS-induced对这些CS-exposed上皮车厢的老鼠。
降低瘦素受体表达的肺实质AKR / J小鼠暴露于香烟烟雾的4个月(CS)或室内空气。代表图像的最低三个老鼠每条件。一)减少瘦素受体的免疫组织化学染色(布朗)smoke-exposed小鼠肺泡壁的使用多克隆抗体对ObR和avidin-biotin-peroxidase复杂的方法。箭头表示保存瘦素受体染色后肺泡巨噬细胞的CS曝光。箭头显示了空域墙染色smoke-exposed老鼠。b)降低瘦素受体表达也明显在smoke-exposed小鼠气道上皮细胞。类风湿性关节炎:室内空气暴露;亚历山大-伍尔兹:气道腔。
讨论
我们确定了21的snpLEPR与肺功能相关基因明显EA人口下降与慢性阻塞性肺病和单体型分析SNP分析结果的支持。协会信号观察到在这些snp可能代表两个或三个基因的信号。此外,肺的LEPR架构的潜在作用和慢性阻塞性肺病表型是由一个AKR / J小鼠模型显示下降LEPR表达在气道壁和上皮烟雾暴露。我们的结果确定LEPR作为一个小说慢性阻塞性肺病的候选基因。
据我们所知,没有先前的研究调查了角色的遗传多态性LEPR基因和慢性阻塞性肺病或其相关的表型。我们研究的表型是肺功能的下降速度而不是慢性阻塞性肺病本身。的基本原理是,肺功能下降的速度是一个比一个更精确的表现型横断面测量肺功能需要定义慢性阻塞性肺病,并可能作为一种基因同质的表型。我们确定了21的snpLEPR基因明显与EA的人口有COPD的肺功能下降。最引人注目的地区之一的5′末端LEPR(区域1),其中包括受体的胞内域的一部分16并可能导致不同的信号强度。大多数变体中确定LEPR与肺功能下降的衰减,有关,值得注意的是,产生的SNP rs1137100 G变体,它编码一个氨基酸替换LEPR在细胞外的领域27·0.33%年−1衰减在FEV的损失1% pred。气流阻塞,发生在慢性阻塞性肺病是由小气道疾病,肺实质破坏和增加航空公司发展几十年来的响应能力28。因此,随着时间的推移,这些基因变异可能产生实质性影响疾病进展。40岁的时期,一个人G等位基因的纯合子rs1137100 FEV1% pred相比高出26.4%,主要的等位基因的纯合子。鉴于小等位基因频率为0.26,如在我们的群体中,我们可以推断7%的人口为小等位基因纯合子(GG), 38%是杂合子(AG)和55%为主要的等位基因纯合子(AA)。甚至为吸烟状态调整后,这种基因变体可以解释轻度和中度或中度和严重慢性阻塞性肺病在当前全球倡议对慢性阻塞性肺疾病(黄金)标准29日。
缺乏特征明显的COPD受试者与肺功能纵向数据的唯一性与lh加我们的人口,但是限制复制这些结果的机会。但是,发现多个重要的单个基因的snp减少虚假的结果的可能性由于多个测试,但它也可能是部分原因是高度的LD在这个基因。此外,当使用一个错误发现率为0.2,6个单核苷酸多态性与肺功能下降仍将统计上显著相关(p < 0.006),在目前的研究。先前的研究显示的遗传变异LEPR与标记相关的炎症,包括c反应蛋白(CRP)和纤维蛋白原水平,贷款支持的假设瘦素途径的生理影响炎症特征。具体地说,小rs1805096位点等位基因(T)是降低纤维蛋白原水平、CRP和il - 6水平的一项研究健康的东亚峰会30.。降低CRP和il - 6水平与减毒有关lh组肺功能下降31日。有趣的是,小等位基因(T)的编码SNP rs1805096率也降低肺功能在我们的研究中(0.295%·年下降−1;p = 0.007)。因此,我们假设一个潜在机制的疾病修饰效果LEPR基因可能通过介导的炎症机制。认为瘦素可能函数作为免疫调节细胞因子越来越接受。瘦素之间的关系在慢性阻塞性肺病和肌肉萎缩和恶病质32;和瘦素的存在中度COPD患者诱导痰液及其协会与其他炎症标记物33表明瘦素可能参与到当地的炎症反应在慢性阻塞性肺病。
纯系小鼠或豚鼠受到慢性CS接触已被证明是无价的CS-induced实质肺部疾病的模型34,35。此外,使用复杂的人类疾病的动物模型,解析中确定候选基因广泛的基因或基因组调查是一个标准的方法初始路径验证,特别是如果其他人口不能用于复制和治疗目标是一个表面上的目标36,37。我们注意到减少染色在空域墙和气道上皮车厢,但保留在AKR / J smoke-exposed小鼠巨噬细胞表达。这是与布鲁诺的结果一致et al。13发现瘦素及其受体的表达减少吸烟者和学科与轻微到严重慢性阻塞性肺病与健康不吸烟的科目。因此,降低瘦素受体表达(收购或基因)可能是一个重要的诱发因素CS-induced肺病。
总之,目前的研究是第一个报告之间的关联LEPR多态性和慢性阻塞性肺病。我们的研究结果支持瘦素的作用途径,尤其是LEPR在慢性阻塞性肺病和肺功能下降。具体来说,个人选定的微小等位基因多态性较低容易肺功能和慢性阻塞性肺病恶化的损失。苏格兰民族党和单体型测试点的三个集群信号突出两个潜在位点之间的连锁不平衡考虑这些信号:功能性SNP rs137100和同义SNP rs1805096编码。虽然这两个snp不互相LD (D′= 0.45, R2= 0.125),单的意义,包括每个SNP邻国LD块重叠,使它有点难以区分这两个信号。有必要复制我们的发现在其他人群;然而,我们的研究结果确定LEPR作为一种新颖的目标在慢性阻塞性肺病和肺功能损失。
支持声明
这项研究得到了国家心肺和血液研究所(拨款HL076322 HL066583 HL010342;美国马里兰州贝塞斯达)和美国国家老龄化研究所(AG21057;贝塞斯达)。本研究也支持部分由校内研究项目,国家人类基因组研究所和美国国立卫生研究院(贝塞斯达,医学博士,美国)。基因分型服务提供的约翰霍普金斯大学(美国马里兰州巴尔的摩)根据美国联邦政府合同号n01 NHLBI -高压- 48195。kc巴恩斯的部分支持由玛丽贝丽尔补丁特恩布尔学者计划(巴尔的摩,医学博士,美国)。
感兴趣的语句
没有宣布。
确认
我们要感谢:p .太极,m·坎贝尔A.L.斯科特,A.E. Jedlicka号明茨(疟疾研究所基因阵列的核心设施,约翰霍普金斯大学,巴尔的摩,医学博士,美国);自动跟踪斯科特,k .晨练Ashworth r和c波姆(遗传疾病研究中心研究所,约翰霍普金斯大学);和h . Voelker k .泛内尔(lh数据协调中心,明尼苏达大学,明尼阿波利斯,MN,美国)。
主要调查人员和高级职员的临床和协调中心,国家心肺和血液研究所(贝塞斯达,医学博士,美国)如下。医学博士Altose(首席研究员)和C.D. deiz(项目协调员):哦,克利夫兰凯斯西储大学美国。硕士Eichenhorn(首席研究员),kj布莱登(项目协调员)和R.L. Jentons(项目协调员):亨利福特医院,底特律,美国小姐。R.A.明智(首席研究员)、C.S.兰德(首席研究员)和·席勒(项目协调员):巴尔的摩约翰斯·霍普金斯大学医学院的医学博士,美国。P.D. Scanlon(首席研究员)通用卡洛(项目协调员)K.S. Mieras和交通线沃尔特:美国梅奥诊所,MN,罗彻斯特。A.S. Buist博士(首席研究员),L.R.约翰逊(lh肺功能协调员)和V.J.圆粒金刚石(项目协调员):俄勒冈健康科学大学,或者美国的波特兰。厕所贝利(首席研究员)和第2杰拉尔德(项目协调员):伯明翰阿拉巴马大学,伯明翰,半岛,美国。D.P. Tashkin(首席研究员)和I.P。祖尼加(项目协调员):加州大学洛杉矶,加州,美国。天然橡胶Anthonisen(首席研究员,指导委员会主席),j . Manfreda(首席研究员),r。穆雷(首席研究员),南卡罗莱纳州Rempel-Rossum(项目协调员):曼尼托巴大学、温尼伯,加拿大的MB。J.E. Connett(首席研究员),P.L. Enright, P.G. Lindgren p·奥哈拉(lh干预协调员),硕士双刃短剑和热处理Voelker:明尼苏达大学协调中心,明尼阿波利斯,MN,美国。.罗杰斯(首席研究员)和主机Pusateri(项目协调员):美国宾夕法尼亚州匹兹堡市匹兹堡大学。右眼Kanner(首席研究员)和通用Villegas(项目协调员):犹他大学,美国犹他盐湖城。党卫军赫德(肺部疾病的前主管部门),摩根大通(J.P. Kiley(前项目官员和董事的肺部疾病),g . Weinmann(前项目官员、董事、气道生物学和疾病项目,DLD),贝拉吴(流行病学与临床应用):国家心脏,肺和血液研究所的工作人员,贝塞斯达,医学博士,美国。
- 收到了2008年8月5日。
- 接受2008年12月19日。
- ©人期刊有限公司