摘要
哮喘和慢性阻塞性肺疾病的慢性炎症驱动气道的病理性结构重构。使用噻托溴铵,乙酰胆碱最近被确认在持续过敏性哮喘豚鼠模型的气道平滑肌重塑中发挥主要调节作用。本研究的目的是调查气道重塑的其他方面,并比较噻托溴铵与糖皮质类固醇布地奈德的有效性。
对卵白蛋白敏感的豚鼠用雾化的卵白蛋白挑战12周。
卵白蛋白诱导气道平滑肌增厚,气管平滑肌高度收缩,肺收缩蛋白(平滑肌肌球蛋白)含量增加,粘液腺肥大,黏液蛋白5亚型A和C (MUC5AC)阳性杯状细胞数量增加,嗜酸性粒细胞增多。此前有报道称噻托溴铵治疗可抑制气道平滑肌增厚和收缩蛋白表达,并可防止气管过度收缩。本研究表明噻托溴铵还能完全防止过敏原诱导的黏腺肥大,并部分减少muc5ac阳性杯状细胞数量的增加和嗜酸性粒细胞浸润。布地奈德治疗还可防止气道平滑肌增厚、收缩蛋白表达、气管收缩力和黏腺肥大,并部分减少muc5ac阳性杯状细胞数量和嗜酸性粒细胞增多。
这项研究表明,噻托溴铵和布地奈德在抑制气道重塑的几个方面同样有效,进一步证明噻托溴铵的有益作用可能超过支气管扩张。
乙酰胆碱是气道中主要的副交感神经递质,也是一种自分泌或旁分泌激素,由非神经元来源分泌,包括气道上皮细胞和炎症细胞1- - - - - -4.在呼吸系统中,乙酰胆碱通常与诱导气道平滑肌收缩和粘液分泌有关5;这两种作用都是由毒蕈碱受体介导的,其中毒蕈碱M主要参与其中3.受体亚型6- - - - - -9.阻塞性呼吸道疾病,包括哮喘和慢性阻塞性肺疾病,副交感神经活动增加2.因此,毒蕈碱受体拮抗剂,如短效异丙托溴铵和长效噻托溴铵,是这些疾病的常用支气管扩张剂,特别是在慢性阻塞性肺疾病中,迷走神经张力似乎是气道阻塞的主要可逆成分10.
最近的证据表明,乙酰胆碱在呼吸系统中的功能作用不仅仅是诱导气道平滑肌收缩和粘液分泌。在体外研究表明,长期刺激毒蕈碱受体可增强气道平滑肌收缩蛋白的表达、促有丝分裂信号和细胞增殖1,11,12.此外,毒蕈碱受体刺激可诱导原代培养肺成纤维细胞增殖13,并触发促炎介质的释放,包括白三烯B4从气道平滑肌和气道上皮细胞和炎症细胞14- - - - - -17.乙酰胆碱的促炎作用可能在炎症性气道疾病中增强3.慢性阻塞性肺疾病患者中性粒细胞表达和功能增加18.此外,在之前的一项研究中发现,在反复过敏原挑战的豚鼠中,气道平滑肌质量、收缩力和收缩蛋白表达均有所增加,而长效毒蕈碱受体拮抗剂噻托溴铵治疗后,气道平滑肌重塑的这些特征(部分或完全)均有所降低19.这表明,作用于毒蕈碱受体的乙酰胆碱可能在哮喘和慢性阻塞性肺病的病理生理和发病机制中发挥了比目前认识到的更大的作用2.
除气道平滑肌外,抗胆碱能药物对过敏原诱导的气道重塑的潜在抗重塑作用迄今尚未报道。此外,没有研究直接比较噻托溴铵的抗重塑效果与其他治疗策略。因此,本研究的目的是比较溴化噻托溴铵与本体酸糖皮质类固醇布地奈德的疗效,并研究这两种治疗策略对气道重塑各个方面的影响,包括气道平滑肌重塑、细胞外基质沉积和粘液生成细胞的诱导。
材料与方法
动物
体外繁殖的无特异性病原体雄性Dunkin-Hartley豚鼠(Harlan, Heathfield, UK),体重250-300克,使用Al(OH)对卵白蛋白(OVA)敏感。3.作为辅助。4周后进行实验。本研究中描述的所有方案都得到了格罗宁根大学动物实验委员会(格罗宁根大学,格罗宁根,荷兰)的批准。
如前所述,在有意识和无约束的情况下,通过吸入OVA (Sigma, St Louis, MO, USA)或生理盐水的雾化溶液进行刺激20..当观察到呼吸窘迫的第一个迹象时,停止吸入过敏原。不需要抗组胺药物来预防过敏性休克。
研究设计
每周向豚鼠注射一次OVA或盐水,连续12周,以诱导之前所述的气道重塑19,21.对于噻托溴铵治疗,动物接受雾化剂量的溴化噻托溴铵(Boehringer Ingelheim, Ingelheim, Germany)盐水(0.1 mM溶液;每次灌盐水或OVA前30分钟。对于布地奈德治疗,动物接受布地奈德的雾化剂量(由格罗宁根大学H.W. Frijlink提供)悬浮在生理盐水中,添加1%吐温80 (1 mM悬浮液;每次挑战前24小时和1小时。治疗组如下:ova致敏/盐挑战组(n = 9);ova致敏/ ova挑战(n = 10);ova致敏/盐挑战/噻托溴铵处理(n = 8);ova致敏/ ova挑战/噻托溴铵治疗(n = 7);ova致敏/盐胁迫/布地奈德治疗(n = 9); and OVA-sensitised/OVA-challenged/budesonide-treated (n = 7). For all of the tiotropium-treated animals and for some of the OVA-sensitised/saline-challenged (n = 5) and OVA-sensitised/OVA-challenged (n = 6) animals, lung material stored from a previous study19用于组织学分析。对于ova致敏/盐挑战和ova致敏/ ova挑战的动物,将先前储存的和新获得的肺材料生成的数据合并起来,生成单个ova致敏/盐挑战对照组和单个ova致敏/ ova挑战对照组。在12周的挑战方案中,每周监测豚鼠体重;治疗组之间没有发现体重增加的差异。
组织收购
豚鼠在最后一次给药24 h后,采用实验性震荡法处死,然后快速放血。肺部立即被切除并保存在冰上以便进一步处理。将气管取出并转移到含有5%二氧化碳/95%氧气的37°C的Krebs-Henseleit溶液中,组成如下(mM): NaCl 117.5;氯化钾5.6;MgSO41.18;CaCl22.5;不2阿宝41.28;NaHCO3.25.0;葡萄糖5.5,(pH值7.4)。
组织化学
采用左右肺叶主支气管横截面进行形态计量学分析;这些切片被染色,以便识别其各种成分。平滑肌采用免疫组化染色法检测平滑肌特异性肌球蛋白重链(SM-MHC;新标记,Fremont, CA, USA),细胞外基质采用马松三色染色,黏液产生细胞采用定期酸-希夫(PAS)染色或免疫组化染色,黏液蛋白5亚型A和C (MUC5AC;Neomarkers)。用于MUC5AC免疫组化的抗体此前已被证明与豚鼠MUC5AC有交叉反应22.用辣根过氧化物酶连接的二抗和二氨基联苯胺检测一抗。在苏木精和伊红染色的肺切片中发现嗜酸性粒细胞。切片内的气道进行数码摄影,并细分为软骨性和非软骨性。所有免疫组化测量均采用数字量化软件进行23.
西方的分析
如前所述制备肺匀浆19.蛋白质裂解物用十二烷基硫酸钠-聚丙烯酰胺凝胶电泳分离,然后用标准免疫印迹技术。抗体用增强化学发光法观察(Pierce, Rockford, IL, USA)。对斑点照片进行密度分析(TotallabTM;非线性动力学,纽卡斯尔,英国)。
等距张力测量
如前所述,进行了等距浓度实验19.简单地说,气管是不含浆液结缔组织的。单开环剥去上皮的制剂被安装在含有Krebs-Henseleit溶液的器官浴中进行等长记录,温度为37°C,饱和5%二氧化碳/95%氧气。平衡后调整静息张力至0.5 g;然后使用20和40毫米氯化钾进行预收缩。在洗脱和另一个30分钟的平衡期后,用甲胆碱构建累积浓度-响应曲线。
数据分析
所有数据均以平均值±表示扫描电镜.除非另有说明,平均数之间的统计差异采用单因素方差分析计算,然后采用Newman-Keuls多重比较检验。在p值<0.05时,平均值之间的差异被认为是显著的。
结果
气道平滑肌
既往研究发现,反复吸入过敏原可增加气道平滑肌质量、肺收缩蛋白表达和气管平滑肌收缩力,提示气道平滑肌重构19.用噻托溴铵治疗可部分或完全防止这些变化。因为噻托溴铵对气道平滑肌重塑影响的数据已经发表19,这些数据汇总于表1⇓.
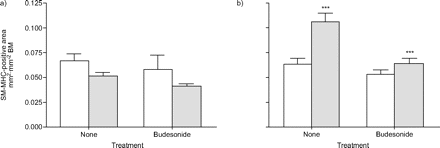
为了研究布地奈德治疗的效果,计划进行了相同类型的实验。与前一篇报道相似,反复挑战OVA增加了非软骨气道的气道平滑肌质量,而大型软骨气道的气道平滑肌质量没有变化(图1)⇓).使用SM-MHC抗体定量气道平滑肌质量,这是收缩气道平滑肌表型的严格标记24.与盐胁迫对照组相比,在重复过敏原暴露后,sm - mhc阳性面积增加66±15% (p<0.001)。布地奈德治疗完全阻止了这种增加(图1)⇓).布地奈德在减少平滑肌增厚方面比噻托溴铵更有效,噻托溴铵部分阻止sm - mhc阳性区域增加76%,如先前报道的(表1)⇑)19.
反复过敏原刺激和布地奈德治疗对豚鼠肺气道平滑肌质量的影响:a)软骨气道(基底膜(BM)长度1.82±0.08 mm);b)非软骨气道(BM长度0.74±0.02 mm)。在平滑肌特异性肌球蛋白重链(SM-MHC)染色的肺切片中发现气道,并对SM-MHC阳性区域进行形态计量学分析。□:生理盐水;░:卵清蛋白。数据以平均值±表示扫描电镜。每只动物分析每种分类的6至8个气道(动物数量详见研究设计部分)。* * *: p < 0.001与生理盐水的挑战。
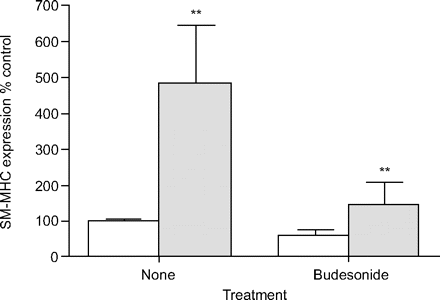
根据这些意见,并与前一份报告一致19Western分析显示,ova挑战动物肺SM-MHC表达显著增加4.8±0.7倍(图2)⇓).正如观察到的气道平滑肌厚度,这种增加几乎完全逆转布地奈德治疗。布地奈德没有显著减少盐胁迫动物的SM-MHC阳性面积和肺SM-MHC表达。如先前报道的,布地奈德对ova挑战动物肺SM-MHC表达的影响比噻托溴铵的抑制作用更明显,噻托溴铵部分减少了过敏原诱导的升高,降低了38%(表1)⇑)19.
重复过敏原刺激和布地奈德治疗对豚鼠肺平滑肌特异性肌球蛋白重链(SM-MHC)表达的影响。用Western blotting分析肺组织匀浆中SM-MHC和β-actin(负荷对照)的表达。SM-MHC的平均表达归一化为β-肌动蛋白,未处理的盐胁迫动物(对照组)的表达设为100%。□:生理盐水;░:卵清蛋白。数据以平均值±表示扫描电镜.* *: p < 0.01与生理盐水的挑战。
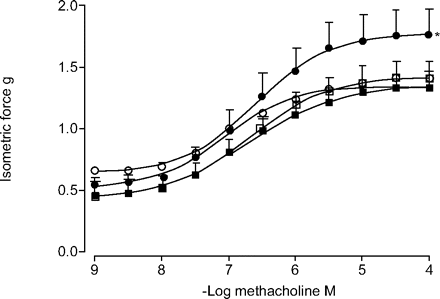
此外,与盐胁迫动物相比,反复暴露于OVA使气管平滑肌的收缩力增加了32±1%(图3)⇓).虽然布地奈德单独治疗与盐水处理的动物相比没有效果,但它完全扭转了ova引起的收缩力增加(图3)⇓).噻托溴铵治疗也完全逆转了ova引起的气管收缩力的增加,并有额外的有益效果,因为它减少了最大收缩,即使是在盐胁迫的动物中(表1)⇑)19.总的来说,这些结果表明布地奈德和噻托溴铵都能有效减少豚鼠过敏原诱导的气道平滑肌重塑。
重复过敏原刺激的效果(〇和□:生理盐水;•和▪卵白蛋白)和布地奈德治疗(〇和•:不治疗;■和▪布地奈德治疗)气管收缩能力。测定了豚鼠气管环中甲胆碱的剂量-反应关系,并拟合为四参数s型方程。数据以平均值±表示扫描电镜.每只动物分析三个气管环(动物数量详见研究设计部分)。*: p < 0.05与盐水挑战和与卵白蛋白/布地奈德。
细胞外基质
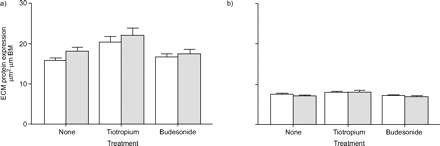
在哮喘和COPD患者的气道中观察到异常的细胞外基质沉积25,26.因此,我们进行了旨在量化豚鼠气道壁内细胞外基质沉积的实验。用马松三色染色法测定的细胞外基质水平,在OVA和盐胁迫的动物中,无论是在软骨或非软骨气道中,都没有差异。噻托溴铵和布地奈德治疗对气道壁基质沉积也没有影响(图4)⇓).
重复过敏原刺激和噻托溴铵或布地奈德治疗对豚鼠肺细胞外基质(ECM)蛋白表达的影响:a)软骨;b)非软骨气道。在马松三色染色的肺切片中发现ECM,并对马松阳性区域进行形态学分析。□:生理盐水;░:卵清蛋白。BM:基膜。数据以平均值±表示扫描电镜。每只动物分析每种分类的4到6个气道(动物数量详见研究设计部分)。
食用细胞
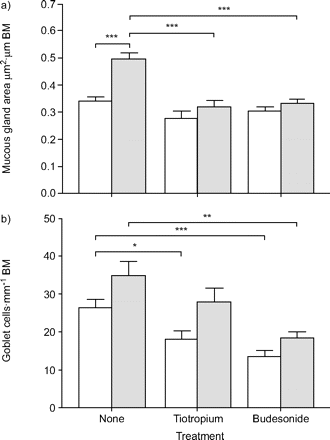
粘液分泌过多是一种病理特征,在哮喘和慢性阻塞性肺病中都可见,它对气流限制有显著影响27,28.这些患者粘液分泌过多,并伴有黏液腺肥大和杯状细胞增生27,28.因此,采用PAS染色对肺切片中黏液产生细胞进行量化。气道上皮和粘膜下粘液腺内的杯状细胞染色呈阳性。粘液腺和杯状细胞主要存在于软骨气道;因此,在这些实验中只评估了软骨气道。反复暴露于OVA可使粘液腺面积显著增加45±7%。尽管溴化噻托溴铵和布地奈德对盐胁迫的动物没有效果,但两种治疗方法都完全防止了过敏原诱导的黏腺肥大(图5a⇓).重复暴露过敏原也有诱导豚鼠杯状细胞总数增加的趋势;然而,这种差异没有达到显著性(p = 0.06)。有趣的是,布地奈德治疗部分减少了杯状细胞总数,与后续的过敏原挑战无关;溴化噻托溴铵还能减少盐胁迫动物的杯状细胞数量(图5b)⇓).
重复过敏原刺激和噻托溴铵或布地奈德治疗对:a)黏腺面积的影响;b)肺内软骨气道杯状细胞总数。在定期酸-希夫(PAS)染色的肺切片中发现粘液产生细胞。对于粘膜下黏膜腺,对pas阳性区域进行形态计量学分析;杯状细胞数,计数PAS染色阳性的上皮细胞。□:生理盐水;░:卵清蛋白。BM:基膜。数据以平均值±表示扫描电镜。每只动物分析4到8个气道(动物数量详见研究设计部分)。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。
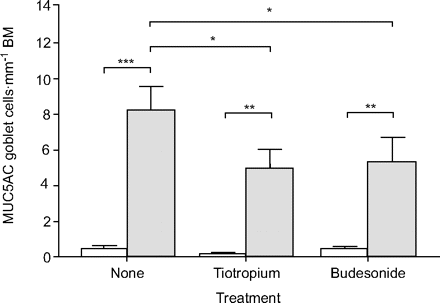
OVA对杯状细胞增生的影响相对较小,这可能与豚鼠呼吸道中存在大量杯状细胞有关,甚至在对照盐胁迫动物中也是如此,这可能掩盖了过敏原的进一步诱导。因此,更多的实验是针对气道上皮中MUC5AC染色的定量。MUC5AC在培养的粘液分化过程中高度表达29据报道,尽管杯状细胞存在,但在对照组大鼠的气道中几乎检测不到30..基于这些研究,我们假设在测量气道上皮内的粘液分化时,MUC5AC比PAS染色更敏感。事实上,组织化学表明,在盐胁迫的豚鼠气道中几乎没有MUC5AC的表达,而这种糖蛋白在ova胁迫的动物中高度诱导(图6)⇓).布地奈德和噻托溴铵治疗没有改变盐胁迫动物的MUC5AC阳性杯状细胞数量,但部分减少了OVA对MUC5AC的诱导(图6b)⇓).总的来说,这些数据表明布地奈德和噻托溴铵在减少过敏原诱导的气道粘液生成细胞重塑方面同样有效。
重复过敏原刺激和噻托溴铵或布地奈德治疗对肺内软骨气道粘液蛋白5亚型A和C (MUC5AC)阳性杯状细胞数量的影响。muc5ac阳性细胞经免疫组化鉴定。□:生理盐水;░:卵清蛋白。BM:基膜。数据以平均值±表示扫描电镜。对每个气道进行2 - 4个气道分析(动物数量详见研究设计部分)。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。
气道嗜酸性粒细胞
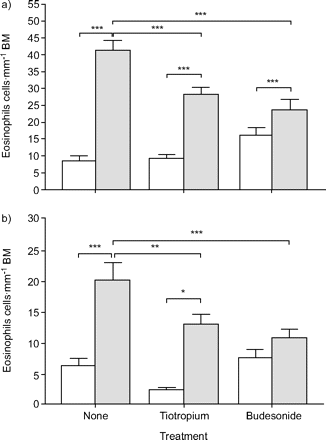
OVA挑战诱导的嗜酸性粒细胞主要流入粘膜下(图7)⇓)和软骨气道的外膜隔室,比较气道平滑肌(表2⇓).非软骨气道也得到了类似的结果。噻托溴铵对盐刺激动物气道嗜酸性粒细胞数量无影响,但对ova刺激动物软骨和非软骨气道粘膜下隔室嗜酸性粒细胞数量有部分抑制作用;布地奈德治疗也有类似的效果(图7)⇓).噻托溴铵和布地奈德对两种气道分类的平滑肌和外膜隔室嗜酸性粒细胞的抑制作用相当(表2)⇓).
重复过敏原刺激和噻托溴铵或布地奈德治疗对粘膜下隔室嗜酸性粒细胞增多的影响:a)软骨;b)非软骨豚鼠气道。用苏木精-伊红染色法鉴定嗜酸性粒细胞。□:生理盐水;░:卵清蛋白。BM:基膜。数据以平均值±表示扫描电镜。每只动物分析每种分类的5到6个气道(动物数量详见研究设计部分)。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。
讨论
结合之前的研究19本研究结果表明,长效抗胆碱能剂噻托溴铵可预防过敏原诱导豚鼠气道重塑的几个方面,包括气道平滑肌增厚、肺收缩蛋白表达增加、气管平滑肌高收缩、黏腺肥大、杯状细胞MUC5AC表达和气道嗜酸性粒细胞增多。总的来说,似乎内源性乙酰胆碱作用于毒蕈碱受体,在过敏性气道疾病的慢性病理中起着广泛的作用,而针对这些作用的抗胆碱能药物在哮喘相关病理生理学的治疗中具有一定的前景。
目前的结果还表明,噻托溴铵的抗重塑作用与布地奈德非常相似。为了对这些药物进行比较,表1总结了以前和目前研究中报道的效果⇑.显然,溴化噻托溴铵和本体酸布地奈德都能有效防止过敏原挑战豚鼠的气道平滑肌重塑,尽管存在一些微小的差异。尽管在缺乏详细剂量-反应关系的情况下,定量比较这两种药物的潜力有限,但在本研究中使用的噻托溴铵和布地奈德的浓度下,布地奈德治疗似乎在防止非软骨气道平滑肌增厚方面更有效;此外,布地奈德治疗消除了收缩蛋白积累的增加,而噻托溴铵的抑制作用是部分的。相反,噻托溴铵降低气管平滑肌收缩力的程度比布地奈德更大。这些药物对粘液腺肥大和MUC5AC表达的影响具有可比性。总的来说,数据表明布地奈德和噻托溴铵在防止过敏原诱导的气道重塑方面同样有效。然而,目前还不清楚噻托溴铵是否也能有效逆转既定的气道结构变化。皮质类固醇氟替卡松可有效防止棕色挪威大鼠气道重塑,但不能充分逆转同一动物模型中已建立的气道结构变化31.这种差异可能解释了为什么糖皮质激素通常不能完全有效地逆转人类哮喘患者的气道结构变化32.显然,为了研究噻托溴铵对已建立的气道重塑的潜在影响,未来的研究是有必要的。
重复过敏原刺激对气道平滑肌重塑的影响取决于气道的大小。在小的非软骨气道中可见气道平滑肌增厚,而在大的软骨气道中未见。尽管如此,气管平滑肌收缩力增加,这表明该模型中的气道平滑肌重塑的特征是气道生成依赖的气道平滑肌增厚和表型成熟的组合。过敏原诱导的肺SM-MHC表达变化支持这一论点,因为非软骨气道平滑肌增加了约65%,不足以解释肺平滑肌球蛋白总增加约4倍。这说明每个平滑肌细胞中SM-MHC的表达一定增加了,从而解释了相似平滑肌质量下气管的高度收缩。
本研究的结果为杯状细胞在应对过敏原挑战时调节黏液腺肥大和MUC5AC表达的机制提供了重要的新见解。目前的发现,这些病理可被噻托溴铵预防,提示毒蕈碱受体在粘液生成细胞的重塑中具有重要的调节作用。这是第一个证明黏腺重塑和MUC5AC表达对过敏原的反应是由内源性乙酰胆碱调节的研究。噻托溴铵对健康气道黏膜腺和MUC5AC表达无影响,提示乙酰胆碱诱导的病理生理重塑与气道炎症的存在有关。这得到了使用消炎药布地奈德的结果的支持,它们产生了惊人相似的效果。此外,噻托溴铵可以防止过敏原挑战动物的气道嗜酸性粒细胞增多。据报道,乙酰胆碱可能促进气道结构细胞释放趋化因子和细胞因子,如气道上皮细胞和气道平滑肌14- - - - - -16,以吸引炎症细胞进入气道,并在功能上与这些细胞释放的生长因子或细胞因子相互作用,诱导结构靶细胞的直接重塑效应,类似于气道平滑肌重塑所观察到的效果2,11.虽然在结膜杯状细胞中已报道过毒蕈碱受体激活表皮生长因子受体33目前,尚无详细的分子研究研究毒蕈碱受体在气道黏腺增生和肥大中的作用。为了阐明支持毒蕈碱受体反应的细胞内信号机制,未来的分子和细胞研究是需要的。
噻托溴铵对粘膜腺和气道平滑肌的抗重塑作用最为明显。两者都受迷走神经支配,特别是在近端气道,并表达毒蕈碱受体2.此外,噻托溴铵还可部分抑制MUC5AC通过气道杯状细胞的表达,并有减少盐水和ova挑战动物杯状细胞数量的趋势。包括杯状细胞在内的气道上皮细胞的神经支配因物种而异34;然而,已知这些细胞表达乙酰胆碱合成酶胆碱乙酰转移酶,排泄乙酰胆碱和乙酰胆碱本身的转运分子35- - - - - -38.目前尚不清楚参与过敏原诱导的气道上皮粘膜分化的乙酰胆碱来源是神经元还是非神经元。然而,在体外而且体外证实毒蕈碱受体对肺成纤维细胞增殖影响的研究13还有气道炎症15- - - - - -18目前观察到噻托溴铵减少气道嗜酸性粒细胞增多,这提高了气道中非神经元乙酰胆碱可能是哮喘和COPD气道重塑的决定因素的真正可能性;未来的研究将明确指出这一领域。
在软骨或非软骨气道中,反复的过敏原刺激未引起气道壁内三色马松染色的可测变化。然而,由于毒蕈碱受体介导人肺成纤维细胞增殖13,该受体系统可能在一定程度上调节了患者气道壁内基质的生成。因此,抗胆碱能药物对气道壁内细胞外基质沉积的潜在影响需要进一步研究。
目前的结果与布地奈德证实较早在活的有机体内而且在体外证明糖皮质激素对气道平滑肌增厚有预防作用的研究结果39.解释糖皮质激素对气道平滑肌的抗增殖作用的机制尚未完全阐明,但似乎与抑制细胞周期调节蛋白cyclin D1和刺激细胞周期抑制蛋白p21有关Waf1 / Cip139- - - - - -41.此外,本研究还对糖皮质激素的作用提供了一些新的见解,如布地奈德可有效防止气管平滑肌收缩蛋白的表达和过度收缩。这表明糖皮质激素治疗阻止气道平滑肌表型成熟在活的有机体内这与最近用培养的人气道平滑肌细胞进行的研究相吻合,表明糖皮质激素抑制收缩蛋白的积累42.糖皮质激素靶向的机制尚未被研究在体外并需要调查。
布地奈德在本模型中阻止黏液生成细胞的重塑。布地奈德对过敏原诱导的小鼠杯状细胞增生有抑制作用43.虽然布地奈德减少了豚鼠杯状细胞的数量,但这种影响似乎与后续的过敏原挑战无关。噻托溴铵也能减少盐胁迫动物杯状细胞的数量。即使在盐胁迫条件下,豚鼠也能表达大量杯状细胞;显然,基础杯状细胞的数量可以通过靶向糖皮质激素和毒蕈碱受体来调节,提示组成性趋化因子/细胞因子和乙酰胆碱的释放参与了维持豚鼠杯状细胞的数量。布地奈德还能抑制过敏原诱导的muc5ac阳性杯状细胞和黏腺面积的增加。因为气道炎症是黏液高分泌的关键44,布地奈德的抑制作用可能不是完全出乎意料的。此外,糖皮质激素对粘蛋白基因表达的直接影响也有报道在体外45.结合使用噻托溴铵获得的结果,这些数据表明糖皮质激素和抗胆碱能药物都可能有效地防止过敏性呼吸道疾病中粘液生成细胞的重塑。
总之,本研究的结果表明噻托溴铵有效地防止反复过敏原挑战豚鼠气道重塑的多重特征。这表明乙酰胆碱通过毒蕈碱受体在过敏性气道疾病的病理生理学中起着重要的调节作用。噻托溴铵的抗重塑效果与糖皮质类固醇布地奈德相当。因此,噻托溴铵等抗胆碱能药物的有益治疗作用可能超过其支气管扩张作用,并可能减轻慢性呼吸道疾病患者的气道重塑和肺功能下降。
- 收到了2007年1月13日。
- 接受2007年5月18日。
- ©ERS期刊有限公司