抽象的
这篇综述的目的是讨论在慢性炎症条件下,如变应性疾病中发生的趋化因子表达的调控方面的最新进展。重点将放在当前的数据上,这些数据表明转录后调节在趋化因子基因调节中发挥的作用比以前认识到的更大。特别是,越来越多的数据表明,在这种情况下,控制mRNA稳定性的机制可能与决定或维持趋化因子基因表达水平的增加有关。这些调控途径可能是新型抗炎策略的重要靶点。
系列“信令和转录调节炎症和免疫细胞:重要性肺生物学和疾病”
通过K.F.编辑Chung和I.M.阿德科克
本系列中的1号
背景
自20世纪80年代以来,研究了趋化因子的小型分泌蛋白质的超家族,稳步发展成为自己的研究世界。现在明确确定这些分子在人类生物学中许多稳态和病理过程中起着核心作用。主要是趋化因子造成免疫系统对炎症性侮辱的方式,通过协调在先天和适应性炎症反应的不同阶段期间白细胞的募集,激活和归巢1.易于设想如何改变趋化因子表达或功能可能导致炎症反应的持久性超出其原始目的,因此为建立慢性炎症而产生关键致病事件2.
鉴于炎症在过敏性气道疾病,特别是支气管哮喘发病机制中的核心作用,驱动趋化因子表达和功能的分子途径现在被视为抗炎策略发展的主要一线候选。然而,每一项研究的突破都揭示了趋化因子网络的复杂性的新水平,因此,为靶向治疗的识别和设计增加了新的挑战。
在过去的几年里,越来越多的数据表明转录后调控在决定趋化因子表达水平中起着重要的作用。特别是,控制mRNA稳定性的机制似乎在决定炎症反应中趋化因子基因表达的时间和水平方面起着至关重要的作用。虽然关于趋化因子翻译调控的数据仍然缺乏,但关于RNA转换和翻译如何整合的知识有所增加3.那4.在不久的将来,可能会在这一领域产生新的见解,并进一步扩大对可能通过治疗干预靶向的促炎机制的识别。
趋化因子:过敏性气道炎症中的多任务分子
趋化因子最初被鉴定为白细胞贩运的调节因素5..随后,人们发现这些分子也参与了炎症过程的其他方面,如纤维化、组织重塑和血管生成6..趋化因子的多种动作和功能现在被认为在不同的条件下发挥了重要作用,例如血管,肿瘤,传染病和过敏性疾病,以及参与移植排斥和自身免疫疾病的免疫病理学2.
到目前为止,已经鉴定并克隆了>40个趋化因子和bbb20个趋化因子受体7..The chemokine superfamily is divided into four branches, based upon the number and spacing of conserved cysteine residues present in their amino acid sequence (table 1⇓)。这些亚属可称为CC(或β),CXC(或α),C(或γ)和CX3.C.缺失或插入的前两个出的四个保守的半胱氨酸之间的氨基酸的存在下分别表征CC和CXC家族。的C(或γ)亚家族包括淋巴细胞,其中只有两个半胱氨酸是保守的。CXXXC趋是CX的唯一成员3.C亚家族,它是唯一膜结合的趋化因子,因为它具有与CC样结构域连接的跨膜域通过粘蛋白丰富的长区域。
已经在各种人慢性炎症疾病中鉴定了炎性部位内炎症部位中相对特异性的趋化因子子表的上调表达,以及炎症的动物模型。这种表达模式与不同炎症细胞类型的选择性募集相关9..在诸如哮喘的过敏性疾病的情况下,其特征在于嗜酸性粒细胞,T-辅助(TH)2淋巴细胞和嗜碱性粒细胞的抑制液,增加了几种CCC趋化因子的表达增加,例如CCL2(单核细胞化学蛋白(MCP)-1),CCL13(MCP-4),CCL5(调节在激活,正常T细胞表达和分泌),CCL11(Eotaxin-1),CCl24(Eotaxin-2),CCl26(Eotaxin-3),CCl17(胸腺和活化调节的趋化因子)和CCL22(单核细胞衍生的趋化因子)牢固建立6.那10..特别地,在气道中CCl11的表达与嗜酸性渗透性的存在强烈相关11.-14..目前认为,在慢性哮喘中,趋化因子的作用是连接Th2淋巴细胞的激活和嗜酸性粒细胞、嗜碱性粒细胞和额外的Th2淋巴细胞向组织募集6.那9..事实上,抗原激活的CD4+ Th2细胞可产生白细胞介素(IL)-4和IL-13,这些细胞可与促炎细胞因子(如IL-1和肿瘤坏死因子(TNF)-α)协同作用,并刺激上皮细胞、内皮细胞和组织巨噬细胞中嗜酸性粒细胞、嗜碱性粒细胞和Th2特异性CC趋化因子的产生8..通过相应的趋化因子受体的齐心化表达,募集嗜酸性粒细胞和嗜碱性粒细胞被募集到组织中并由这些趋化因子激活,这一事件导致过敏性疾病的公知病态标志15..此外,Th2细胞特异性趋化因子,CCL17和CCL22进一步扩增CD4 + TH2细胞的募集,因此产生了自维持促炎环6.那9.那10..IL-13过表达的动物模型以及某些趋化因子敲除确认了Th2衍生的细胞因子和嗜酸性趋化因子(例如Eotaxins)的相互依存,在建立肺炎反应中8..这些有吸引力的模型可以为测试过敏性炎症的各种药理抑制剂提供基础16..
可以诱导广泛的趋化因子在体外通过不同类型的白细胞或驻留细胞中的促炎刺激,例如肥大细胞,树突细胞,成纤维细胞,上皮细胞,内皮细胞和平滑肌细胞10..然而,来自动物模型和人类受试者的气道标本的检查揭示了趋化因子的细胞来源更窄的光谱,这表明在调节趋化因子生产的复杂机制的存在体内,在体内平衡和疾病状态中控制适当的白细胞运输。随着炎症反应的发生,参与这些调节机制的不同途径可能被改变,因此,在确定慢性炎症疾病(如哮喘)中趋化因子的异常表达方面发挥着关键作用。
基因表达在炎症和过敏转录后调控的日益重要的作用
基因表达的转录后调节是一种强大的自适应机制,其响应于各种细胞扰动,例如应激,增殖或免疫激活17.. 已知该机制在调节早期反应基因表达的时间和数量方面至关重要,它与基因转录紧密协调并在磷酸化介导的信号事件的共同控制下发挥作用18..转录后调控的基因表达的关键作用已经凸显在最近的基因阵列研究,其中的应激诱导的基因〜50%被发现在mRNA稳定性的水平主要调节19..在不稳定的mRNA的半衰期变化二维的范围往往是四倍波动20.尽管看起来幅度不大,但这个幅度的改变已经被证明会导致稳定状态下mRNA水平的1000倍以上的差异,而这反过来又会导致蛋白质生产的巨大变化20.
mRNA分子,如运输,亚细胞定位,稳定性和翻译的生命周期的多个阶段,都依赖于顺式调控元件的分散在整个分子中存在21那22.在这些序列中,MRNA的3'-未转过来的区域(UTR)内存在的富含亚甲酸酯 - 脲酸酯的元素(ARE)代表了最守恒,富裕的RNA基序组,其显示为调节截然不同的转录物子集23-25.该组序列是非常异质的,包括Auuua五聚体和富含富有的延伸,可以以不同的组合聚集在一起。是序列最初在三个课程中松散地分类:I和II类包含Auuua Pentamers,无论是分散(I类)还是聚集为非阿凡(Uuauuuuau / Au / A; II级),与U-Rich的地区相关联,但是在III类转录物中,Auuua五聚体根本不存在25.最近,已经建立了一种含有的mRNA分子数据库26基于Auuua Motif的重复,将Ares重新分配为五组27.为了合并这两种分类,AREs随后根据3 ' -UTR内这些要素的数量和结构重新组合(表2)⇓)17..最终,由于多个和不同域的组合,ARE获得其功能。最近的研究强调了非甘露糖的重要性,例如U拉伸,而不是Auuua五聚体,作为通过特异性调节RNA结合蛋白识别结合位点所必需的次级mRNA结构的关键元素28.第一次确立了ARE的功能角色在体外通过在嵌合记者mRNA的稳定性从粒细胞巨噬细胞集落的3'-UTR亚克隆ARE-含有序列的报道基因构建体刺激因子(GM-CSF),和检查的降低29.该方法已广泛应用于对信号传导的研究和涉及的RNA结合因子介导的衰减18.那30.除了MRNA营业额之外,还通过不同的信令途径参与翻译的调节,如TNF-α,IL-2和IL-3所示3.那31.然而,待介导的mRNA营业额和翻译之间的特定相互关系尚未完全未被揭露17..AREs在控制mRNA稳定性和翻译中的关键作用已得到证实体内在遗传改变的靶向的小鼠模型中是缺失(Δare):在TNF-α基因中的是区域的消融导致TNF-α的产生增加,这被发现是由TNF速率的降低引起的-αmRNA衰减和翻译抑制损失32.
最近,已经建立了一种含有的mRNA分子数据库26那27.这个基因库编码参与不同生物过程,例如细胞周期,细胞活化,肿瘤发生和应激反应,并且许多这些蛋白质的蛋白质牵涉几种疾病状态。在免疫和炎症的许多关键基因,如IL-2,IL-3,IL-4,IL-5,和GM-CSF,其的mRNA显示的ARE,表达的确是调节转录后并且在这些之中,趋化因子基因正在越来越多地确定33.基因的生物相关性发现含有和战神调节27指出这些RNA序列是免疫中基因表达的中心顺式调控元件,并进一步表明针对are介导调控途径的治疗干预的潜在影响。
mRNA更新,这一点还没有完全阐明,依赖于形成信使核糖核蛋白(MRNP)络合物,其中,所述的mRNA结合到ARE结合蛋白是相关的控制的机制。一旦结合,这些因素可以加速或,反过来减缓脱腺苷依赖性mRNA降解通过影响衰变过程的多个步骤,包括RNA转录物的可接近性特异性mRNA降解复合物17.那34-37.
最近已经克隆和功能表征了几种具有结合蛋白质,并且它们在转录后基因表达组织中被涌现为关键调节分子23那38.这些因子参与了mRNA生命周期的几个关键步骤,如成熟mRNA的核输出和亚细胞定位,以及mRNA衰变和转译的速率,并位于越来越被识别的信号通路的下游,如下所述。are结合蛋白通常与其他调控蛋白和RNA识别基序联合作用,以实现完整的调控功能30那37那39.
越来越多的证据表明,有含有蛋白质的表达和/或功能的改变以及控制它们的信号传导途径可能在人类疾病中起作用32那40-44..然而,在人类炎症和过敏过程中,mRNA的转换和翻译的改变还有待深入研究,因为这些机制和它们使用的途径是作为抗炎治疗的靶点。
在急性炎症反应的终止之后,早期反应基因的表达,例如原癌,生长因子,细胞因子和趋化因子,在生理学上恢复到低水平或保持沉默,同时通过转录抑制,同时通过介导的mRNA加速衰变和翻译沉默17.那18..这些快速关闭的转录后机制的失败与癌症和其他疾病密切相关45.-47..归因于控制炎症和免疫力的mRNA果实的相关性18.那48.允许的假设是,在炎症和过敏性疾病,炎症性转录物(趋化因子包括)的适当和及时的mRNA降解的改变可能导致他们的异常稳定,最终导致炎性蛋白质生产的一种慢性增加。这一观点也被获得的一些证据支持体内:小鼠携带缺失的TNF-α基因ARE体现了关节和肠,这强烈相似浸润存在于人类类风湿性关节炎和克罗恩氏病中,分别内的早期炎症反应。这些突变型小鼠也显示TNF-α的高循环水平,从在速度降低导致TNF-α的mRNA降解和从翻译抑制的损失32.有趣的是,在缺乏Tristetraprolin(TTP)的小鼠中发现了TNF-αmRNA衰减率的非常相似的炎症反应和改变,其与TNF-α3'-UTR结合的含有结合蛋白质并促进其快速衰减49..
此外,最近的数据表明,调控mRNA稳定性是一种重要的、新颖的机制,可以决定Th1/Th2细胞因子的差异表达。巴特勒等.50.报道称,在Th2偏置的小鼠菌株DBA / 2中,与在Th1-中发现的细胞因子水平相比,增加IL-4和IL-13 mRNA的稳定性稳定性地占这些细胞因子的表达增加。偏置C56BL / 6菌株。
趋化因素表达后转录调节:今天的观点
在体外对趋化因子转录后调控的研究日益揭示这一机制在决定趋化因子表达中的影响。在不同的细胞类型中,已经发现了广泛的刺激,以触发几种趋化因子的mRNA周转变化(表3)⇓),具体如下:促炎和免疫调节细胞因子,如TNF-α,IL-1,IL-4,干扰素(IFN)-γ和IL-1031那51.-60.;与缺氧相似的相关信号61.那62.;传染性药剂,如病毒63.那64.或细菌衍生的产物,如脂多糖(LPS)或甲酰-甲硫酰-亮基-苯丙氨酸(FMLP)65.那66.;等刺激,诸如一氧化氮67.和活化的蛋白C.68..重要的是,转录后调节机制也正在成为重要的糖皮质激素,主要的治疗药物类过敏性疾病的能力,抑制趋化因子的表达33那69..值得注意的是,在极化炎症反应中选择性地表达的T细胞衍生的产品可以利用转录后途径对趋化因子基因表达施加相反的影响。例如,在人单核细胞中,IFN-γ通过增加mRNA稳定性来推动CXCL8的表达56.,而在相同的细胞类型中,IL-4通过降低其mRNA的半衰期来下调CXCL8表达54..
可用在体外趋化因子mRNA转换的研究大多使用转录抑制剂,放线霉素D.根据该方案,用诱导刺激治疗细胞以实现感兴趣的基因的稳态mRNA水平,然后没有收获总mRNA在攻击时期的结束时进一步处理,或以各种时间间隔分离,但在与放线菌素D孵育后的各种时间间隔。这种实验方法提供了快速有效的转录封锁,并产生了关于半的变化的大型和有价值的数据体系 -各种细胞刺激方案之后的趋化因素RNA转录物的寿命。然而,由于其细胞毒性和对某些MRNA的稳定性的潜在直接影响,这种方法具有关键的限制81..因此,需要不同的方法来验证用放素霉素D获得的结果。更详细地研究了更新的研究组研究了调节分子水平的趋化因子mRNA周转的机制。这些研究中的大多数使用转录脉冲策略81.,一种允许在分离中研究mRNA衰减的方法,并识别调节该过程的区域。该实验方案采用脉络膜构建体的瞬时转染,其中3'-UTR或其他更具体的调节序列(即。感兴趣的基因的富含序列在报告基因中插入瞬时诱导的启动子的报告基因中,例如C-FOS血清诱导或四环素(TET) - 推解的启动子体系。通过改变培养基中的血清或滴度的量来实现报告器mRNA转录的瞬态爆发。报告者的转录活动的终止模拟转录抑制剂的效果,而不会扰动除转染的构建体中发生的任何转录过程。调节序列的插入影响报告器mRNA的衰减速率,并允许确定该序列的稳定性潜力。通过删除或突变的插入序列的修改可用于揭示该过程中涉及的钥匙结构区域。此外,还可以通过共转染信号分子的组成型活性或显性负形式,使用该系统研究指导这些方法的信令途径的参与51..
CXCL8的转录后调控:为趋化因子mRNA更新的分子机制研究的模型
多种,异质性AREs存在于几个趋化因子转录本的3 ' - utr中,如CXCL1, CXCL2和CXCL3(生长相关癌基因(GRO)-α, GRO-β和GRO-γ)27, CXCL882.,ccl2.83.巨噬细胞炎症蛋白(MIP)-1α84., CCL1185.和CCL20(MIP-3α)。然而,尽管CCL5和CCL13的3′-UTR中缺乏ARE86.,在糖皮质激素(GCs)孵育后,气道上皮细胞中CCL13 mRNA的衰变加速80,而CCL5 mRNA的稳定性与呼吸道合胞病毒攻击后增加63.,指向其他RNA基序参与这些转录物的mRNA成交量的调节。
如前所述,关于AREs和这些转录本中其他RNA基元的功能、与之结合的因子的身份以及调控趋化因子mRNA稳定性和/或翻译的信号通路,我们知之甚少。迄今为止,以CXCL8为模型获得了这方面的大量数据,大量研究已经确定了转录后控制的几个机制72.那87..
成熟的CXCL8转录本显示一个长3 ' - utr,包含多个有时聚集的AUUUA基序,在a -和u -富序列延伸的背景下。CXCL8表达的主要特征是在炎症细胞因子、病原体或应激对细胞刺激的反应中,mRNA和蛋白水平的快速、广泛变化。这种趋化因子在稳态条件下的许多细胞类型中几乎检测不到,但根据细胞刺激的类型,它可以上调100倍。IL-1β或TNF-α诱导CXCL8 mRNA的半衰期较长73.那88.,表明MRNA稳定在刺激刺激的稳态mRNA水平强度增加中的潜在作用。霍夫曼等.87.基于他们的研究以及来自多个研究小组的数据,提出了一个模型,即特定刺激下CXCL8的产生程度是由以下至少三种调控机制组合而成:1)转录抑制释放基因启动子;2) NF -κ b -和应激活化蛋白激酶/c-Jun n端激酶(SAPK/JNK)介导的转录激活途径;3)通过p38丝裂原活化蛋白激酶(MAPK)途径(也称为SAPK2)稳定mRNA。总的来说,是霍夫曼的研究等.86.表明,这些机制的相对贡献随着细胞的激活状态和激活刺激的性质而变化。简而言之,转录镇压,与IL-8 mRNA的快速营业额一起占未刺激细胞中的低水平IL-8。由NF-κB和JNK途径介导的转录激活对于IL-8诱导是必不可少的,而活化的蛋白-1和CCAAT-Enhancer结合蛋白位点不是诱导必不可少的,但似乎促进了最大转录激活。由P38 MAPK介导的第三信号的发生,由强炎症刺激如IL-1,TNF-α和LPS诱导,介导CXCL8 mRNA稳定化。重要的是,将后一种机制的整合与转录水平发生的那些机制提供了CXCL8蛋白质产量的最大增加87..
先前所示的转录脉冲方法用于证明CXCL8 3'-UTR在介导基础mRNA衰减和刺激诱导的稳定中的累积,并定义所涉及的信号通路51..包围该ARE区域CXCL8-UTR 3'的cDNA片段插入兔β珠蛋白DNA构建物的3'-UTR中,四环素反应性启动子的转录控制下。的β珠蛋白mRNA在该嵌合构建体转染的HeLa细胞的半衰期的测量揭示了无插入β珠蛋白的mRNA,它显示一个较长的半衰期,这表明的劣化的急剧加速,该CXCL8 3的亚克隆区域'非编码区含有介导的mRNA降解的序列。有趣的是,在报道构建体亚克隆的3'-UTR区的缺失突变体,发现该最小去稳定序列需要相邻包围富含AU的元件区域的存在,这表明的ARE是RNA顺式的主要但不是唯一的部分通过调控RNA结合蛋白中使用的元件51..此外,用IL-1的细胞处理显着增加了报告者mRNA半衰期,表明CXCL8 3'-UTR的亚克隆区域足以通过激活刺激来推断报告转录物的稳定性。
IL-1通过在地图激酶激酶激酶,MEKK1的控制下激活信号通路介导许多效果。在这项研究中前面所提到的,MEKK1的组成型活性形式的瞬时共表达也诱导内源性CXCL8 mRNA的半衰期的急剧上升,以及所述β珠蛋白mRNA的轴承CXCL8 3'-UTR序列。MEKK1调节多种调节途径,如NF-κB,啜饮/ JNK激酶,细胞外信号调节激酶(ERK)和P38 MAPK途径51..为了进一步确定哪条途径介导报告者mRNA稳定,温度等.51.使用显性负突变或组成活性激酶的过表达,选择性地激活不同的途径。这些实验揭示了MKK6是p38 MAPK通路的选择性激活物89.这表明p38 MAPK通路特异性参与了CXCL8 mRNA的稳定。在同一项研究中,使用了类似的策略来识别p38 MAPK的下游靶点有丝裂原活化蛋白激酶活化蛋白激酶(MAPKAP)2,也称为MK2。
值得注意的是,MK2激酶已被确认分别在调节IL-6和TNF-α的mRNA稳定性和翻译中起关键作用90.,越来越多的人认为它是转录后调控的重要守门人91..此外,在鼠巨噬细胞中进行的研究表明,MK2磷酸化是结合蛋白,非均相核核糖核蛋白(HNRNP)A0。该蛋白质结合在体外对于MIP-2,人CXCL1(GRO-α)的小鼠同源物,以及TNF-α和环加氧酶(COX)-2 mRNA92..在卢梭的研究中等.91.,上述MRNA通过LPS细胞刺激稳定,并用P38 MAPK级联的化学抑制剂的细胞处理废除了MIP-2 mRNA的LPS诱导的稳定化,以及MIP-2蛋白的产生。相同的治疗也防止了HNRNP A0的MK2依赖性磷酸化,以及该蛋白质与靶MRNA的结合,表明LPS诱导的几种炎性转录物(包括MIP-2趋化因子)的稳定性是P38依赖性过程最终针对与ARES相互作用的调节蛋白92..
一些炎症基因,如COX-2、IL-6、TNF-α和GM-CSF,参与了p38 MAPK在mRNA稳定和/或翻译中的参与32那51.那92.那93.,表明P38 MAPK途径充当炎症反应的有效放大器。通过使用高度富集的这种基因的cDNA阵列,研究了P38 MAPK激活对核心基因的mRNA稳定性的影响65..用LPS刺激THP-1单核细胞,并且在P38MapK抑制剂SB203580的存在或不存在下用LPS收获或进一步处理。有趣的是,该研究表明,LPS诱导的基因的MRNA稳定性的增加仅受P38 MAPK仅在含有含量的靶标中调节。在那些促炎基因中鉴定了几种趋化因子,包括CxCl1,CXCl2,CXCL3和CXCL 3和CCL2,CCL3和CCL4,显示P38 MAPK活性后mRNA衰变率的透明差异65..如CXCL8 mRNA所证明,进一步的研究是验证在P38 MAPK介导的这些分子的P38 Mapk介导的稳定化中的参与。51.,并进一步评估下游信号分子和RNA结合蛋白调节新鉴定的趋化因子靶标的mRNA周转。
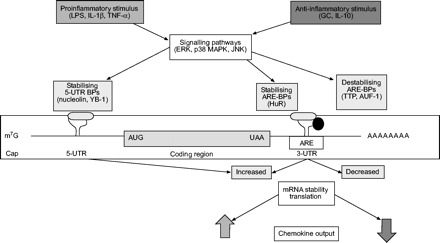
其他应激诱导的激酶途径,如ERK和JNK,也被证明可以调节mRNAs的细胞质转运和周转18..这些信号通路可能是介导趋化因子mRNA衰减变化的p38 MAPK的替代或补充,可能是通过因子与转录本其他区域的不同基元相互作用。例如,在Jurkat细胞中,IL-2 mRNA的5 ' -UTR中存在一个jnk响应元件,通过与rna结合蛋白nucleolin和YB-1的相互作用,将刺激诱导的稳定性传递给该转录本37(fig. 1⇓),并与IL-2 mRNA的3 ' -UTR元件合作。FMLP诱导的CCL20 mRNA稳定性增加似乎与ERK途径有关66..此外,调节RNA周转的RNA结合蛋白主要由其他翻译后修饰(例如甲基化)调节94.,而这些信号通路在调控参与趋化因子mRNA周转的蛋白质方面的作用尚待探索。
调节信号和RNA确定剂可能介导趋化因子mRNA的转录后调节。转录后调节,由富含腺苷 - 脲酸酯的元素(ARES)或位于MRNA分子的另一部分中的其他调节序列介导,例如5'-未转换的区域(UTR),可以介导专业和抗炎症信号旨在迅速调整趋化因子表达水平以响应组织环境的变化。5'或3'mRNA UTR中的调节序列被设计为茎环结构,以突出其次要结构的重要性,除了它们的序列,它们的功能。已经显示出促炎刺激激活不同的信号传导途径,以便在与增加的基因转录中进行mRNA稳定和增加的翻译,以增加趋化因子水平,如CXCL8中P38丝裂原激活的蛋白激酶(MAPK)的参与所述。mRNA稳定。相反,还显示出转录后调节,抗炎信号,例如糖皮质激素(GCS)或白细胞介素(IL)-10,以降低趋化因子的产量。对于被认可的大多数趋化因子进行后转录调节,调节该过程的信号传导途径的同一性尚未完全未被揭露,也不是这些途径影响到治理mRNA的下游RNA结合因子的机制运输,稳定性和翻译。RNA稳定因子表达的增加,或者对其竞争性结合有利的翻译后修饰(磷酸化,甲基化)的诱导可能是增加MRNA稳定和/或趋化因子的翻译,从而有助于增加趋化因子输出(↑)。相同的结果可能通过表达的降低,或通过通过刺激诱导的结合亲和力的变化从其RNA结合位点移位mRNA腐烂因子。 Conversely, a decrease in chemokine output (↓) could be due to increased synthesis or increased binding activity of RNA decay-promoting factors, or an opposite effect on the expression or function of mRNA-stabilising proteins. Ultimately, it is the regulation of the interplay between factors that positively or negatively affect mRNA stability and/or translation that could determine how either pro- or anti-inflammatory mediators post-transcriptionally affect the level of chemokine production. LPS: lipopolysaccharide; TNF: tumour necrosis factor; ERK: extracellular signal-regulated kinase; JNK: c-Jun N-terminal kinase; BP: binding protein; YB: Y-box binding protein; TTP: tristetraprolin; AUF: ARE/poly(U)-binding/degradation factor.
RNA结合蛋白作为趋化因子的mRNA周转的介体:的HuR的细胞因子诱导的CCL11 mRNA稳定的作用
CC Chemokine CCL11显示出强烈且选择性化学抑制剂和朝向嗜酸性粒细胞的活化性能95.,一些研究已经证实这种分子在过敏性炎症中起着关键作用12.和其他生物学功能,如血管生成96..CCL11通过IL-4强烈地上调在气道上皮细胞中,特别是与TNF-α组合80那97.,其表达被GCs严重抑制80.使用用全长CCL11启动子构建体转染的上皮细胞的几项研究表明,细胞因子诱导的上调以及对肠昔林基因的GC介导的抑制似乎仅通过转录调节介导78.那80.CCL11的3'-UTR在富含TA的地区的背景下包含串联Auuua序列85.,表明可能存在转录后调控。事实上,这已经被证明了在体外即CCL11表达在mRNA更新的气道上皮细胞中的水平临界调节。该强效外用GC,布地奈德,诱导细胞因子诱导的CCL11生产的显著下降也加速其mRNA的衰变80.TNF-α联合IL-4对eotaxin蛋白分泌的协同作用最强80,显着提高了eotaxin mRNA的稳定性55..这种变化似乎是由CCL11 mRNA的3 ' -UTR介导的,因为布地奈德诱导的mRNA衰减加速和细胞因子诱导的mRNA稳定性增加都是通过转录脉冲方法复制的,其中,在转染的国立卫生研究院3T3细胞中,在布地奈德或TNF-α + IL-4治疗后,监测带有CCL11 3 ' -UTR的嵌合β-珠蛋白报告mRNA的表达55.那79..
众所周知的是TNF-α与Th1或Th2细胞衍生产品,如IFN-γ和IL-4之间的协同作用,提供了一种用于过程的Th1 / Th2应答优先表达的基因的上调了强大的放大信号,以及作为在这些反应的选择性激活和炎症细胞的募集8.那10..特别地,IL-4和TNF-α的组合使血管细胞粘附分子-1的表达在内皮细胞中,诱导来自上皮细胞的TH2细胞和嗜酸性粒细胞化学引起的表达,例如CCL17,CCL22和ETAXINS10..鉴于这种相关的促炎反应,该细胞因子组合促进CCl11 mRNA稳定化的机制可能代表一个显着的促炎途径。Atasoy等.55.发现了与are结合的蛋白HuR,它决定了mRNA的稳定性和/或靶转录本翻译的增加98.-100.,发挥作用在介导细胞因子对CCL11表达的影响。HUR(也称为华)是HU蛋白质系列RNA结合因子的成员,其与果蝇胚胎异常视觉(ELAV)蛋白质家族同源。HUR是唯一普遍的表达ELAV蛋白,而该家庭(集线器C和D)的三个另外成员仅在神经元组织中表达,仅具有额外的枢纽表达式101..赫尔已被证明绑定在体外MRNA编码基因的元素,其关键调节增殖和应激反应性,例如P21,细胞周期蛋白A,细胞周期蛋白B1102.那103.,以及转录因子,如c-fos104..的HuR的独特mRNA稳定功能也已记载,通过使用嵌合含有ARE-构建体和在细胞过度的HuR30那55..
在atasoy的研究中等.55.,用TNF-α和IL-4治疗人气道上皮细胞诱导HUR的细胞质定位,与HUR功能的激活相关的过程,并在细胞应激条件下发生。103..此外,这种治疗增强了HUR对内源CCL11 mRNA的结合。实际上,使用小鼠单克隆抗体的小鼠单克隆抗体,从通过免疫沉淀(IP)由Immocopipipitipitipitipitipitipition(IP)的MRNA池中扩增来自通过用于刺激的细胞的裂解物而获得的mRNA池。细胞因子刺激导致CCL11 mRNA中的> 40倍富集在未刺激的样品上。最后,在与模拟转染的细胞相比,在上皮细胞中用TNF-α和IL-4处理时,CCL11表达显着增加。这种增加至少部分地提高了mRNA稳定性,这是使用静脉内处理的细胞因子处理的细胞上转染的细胞因子处理的细胞的评估55..
户珥的细胞因子可以激活的转录后调控的重要性提供了直接证据的机制T-cell-derived产品,结合炎症介质,引起强烈的趋化因子upregulation生产从上皮细胞,通过这样做,维持一个促炎的循环。有趣的是,HuR被越来越多的人认为参与了大量含are基因的mRNA稳定,这些基因是炎症和免疫反应的关键介质。关于CCL11的报告55.已加入第一个CC趋化因子至基因列表中,在几年内,包括TNF-α,IL-3,IL-6,CXCL8,GM-CSF,COX-2,血管内皮生长因子,转化生长因子-β,诱导型一氧化氮合酶,CD154(CD40配体)和β-肾上腺素能受体作为HUR靶标34那41.-43.那45.那105.-112..对于这些基因,HuR可以结合到其转录本的3 ' -UTR或包含目标3 ' -UTR的嵌合结构上,同时增加了其mrna的稳定性。这些数据强烈表明,HuR在炎症中的调节作用。目前,HuR在再现极化炎症反应的实验条件下上皮源性趋化因子表达中的作用正在进行系统研究。
在上的HuR激活机制的深入研究113.研究发现,应激诱导的HuR在细胞质中的易位被腺苷单磷酸激活蛋白激酶(AMPK)独特地抑制,AMPK是一种作为代谢应激细胞传感器的酶114..结果,安培抑制了对其目标的下游结合,以及它们的表达和稳定性。相反,AMPK的抑制显着增加了HUR的细胞质易位,这与增加的HUR功能相关113..在该研究中确定AMPK作为的HuR激活,其他的应力 - 调节蛋白激酶是至关重要参与转录后调控,如蛋白激酶的调节剂(PK)C和MAPK(P38,JNK,ERK),没有影响的HuR细胞质迁移113..虽然HuR的易位似乎完全依赖于AMPK,但一些报告表明,HuR与细胞质中靶蛋白的结合可以被其他信号通路调节。例如,HuR与几个靶点的结合已经被报道受p38 MAPK的调控107.那115.那116.或者通过ERK途径117..这可能是由于与这些途径中尚未识别的靶点相互作用,因为据报道HuR不是一个磷蛋白,并受甲基化调控94.那107.那116..
目前正在进行的研究正在研究细胞因子是否以类似于应激诱导的激活的方式促进HUR的细胞质定位,即通过抑制AMPK,或通过激活P38 MAPK级联的抑制,或调节其与炎症和趋化因子靶标的时尚。这种激酶途径在调节CCL11和其他趋化因子的表达中的作用118.那119..
趋化因子如抗炎分子的靶的转录后调控:GC和IL-10
在由于损伤或感染而激活免疫反应后,炎症和抗炎过程以协调的方式发生,目的是通过严格控制炎症反应的持续时间和强度来对抗致病原因,同时防止或尽量减少对宿主的组织损伤。在这些抗炎过程中发生的基因表达变化也可以通过转录后调节机制实现,就像促炎症过程一样。这些机制在抗炎作用中的作用是一个相对较新的研究领域,它开辟了新的和令人兴奋的研究途径,旨在确定新的调节途径和可能用于治疗目的的分子。鉴于趋化因子在慢性炎症的建立和维持中的重要性,了解其转录后调节的调节在多大程度上可能有助于通过抗炎剂(如GCs)或内源性免疫调节分子抑制其表达是很有价值的,比如IL-10。
趋化因子基因在GCs转录后调控的炎症基因中越来越多地被发现(表3)⇑)69.那78.. 然而,GCs影响趋化因子mRNA稳定性和翻译的分子机制尚未完全阐明。关于涉及的顺式元件,GCs加速趋化因子mRNA衰减可能是依赖性的,正如先前对IFN-β和COX-2所证明的那样93.那120.这些元素可能在GC诱导的气道上皮细胞eotaxin抑制中发挥作用,因为GC处理加速了含有are的eotaxin 3 ' -UTR的报告细胞的衰变79..在3'-UTR中的存在本身并不总是预测GC介导的趋化因子mRNA变换的变化。例如,尽管MIP-1αmRNA的3'-UTR中存在四种Auuua序列,但MRNA衰减不考虑在人单核细胞中施加的地塞米松施加的MIP-1α。121.同样,平滑肌细胞中GCs通过5 ' -UTR的一个独特序列而不是含有are的3 ' -UTR降低了大鼠MCP-1 mRNA的稳定性76..此外,在气道上皮细胞中,预烯烷基酯缩短了不少的MCP-4 mRNA的半衰期80.这些数据表明,在某些情况下,ARE可能是不涉及的,或者不足以促进调节蛋白的结合并传达对mRNA趋势的调节作用。进行这种过程可以涉及3'-UTR中存在的其他尚不特异性的顺式元素,或者在趋化因子的MRNA的其他部分中存在。这些额外的序列可以与Ares或独立协同工作,并有助于实施转录后的GC行动。重要的是要指出,与mRNA稳定性的变化相关的序列的存在是不足以推断出某一mRNA的转录后调节。这些决定簇对于形成MRNA分子的二次结构至关重要(即。茎环或5'-和3'-utrs之间的接触,最终允许通过RNA结合蛋白的结合现场识别,其可以促进或延迟mRNA稳定性和翻译17.那28那122.二级结构和不同的蛋白质,以这些mRNA的结合位点的结合亲和力,反过来,由几个细胞内的参数,如离子强度和温度的影响122而且,可能是其他未知因素。此外,RNA结合因子及其活化的表达也可以是刺激和细胞依赖性,使得转录后调节对单个转录物表达的贡献可以根据细胞来源和环境而变化。通过在文献中报告的MRNA衰减对CXCL8上GCS抑制作用的不同贡献,给出了这种选择性水平的良好举例。在人的成纤维细胞中,地塞米松以蛋白质合成依赖性方式通过TNF-α诱导的CXCL8 mRNA衰减增加74..类似地,对于人骨髓基质细胞,在核运行实验,由IL-1β诱导的CXCL8的转录不是由与地塞米松细胞治疗抑制,而被发现趋化因子的mRNA降解由GC处理来加速123.相反,在原代上皮细胞中,GCs对CXCL8的抑制并不是由于对mRNA衰减的影响124.
大多数监管基因 - 蛋白质相互作用,调节他们的信号通路和地方选区的对这些参数的影响仍没有趋化因子的生物学特征决定的。有由糖皮质激素对转录后事件充当多个分子机制,而且他们还远未充分理解。针对这些机构的鉴定研究最近被审查69..
炎症和免疫反应也被内源性免疫调节分子如IL-10下调。该细胞因子由CD4+ t调节性和抗原驱动的Th2细胞以及其他众多免疫细胞产生,是巨噬细胞中基因表达的一种有效的负调控因子58.那125-127.转录后效应已被证明在il -10介导的基因调控机制中发挥相关作用128那129.IL-10降低小鼠和人单核细胞和巨噬细胞衍生的趋化因子的mRNA稳定性,例如CCL3,CCL4和CXCL8,由炎性刺激细胞诱导,例如LPS,IL-1β和细胞外基质组分透明质酸58.那126那127那129.在趋化因子mRNA衰减上的IL-10活性的分子机制已经进一步定义了在研究LPS和IL-10对小鼠巨噬细胞中KC(鼠CXCL1)的转录后调节的相反影响59..在这项研究中,LPS促进内源性KC mRNA的稳定性,以及一个转春节监管的构建表达KC mRNA的。LPS处理的细胞与IL-10共培养表明,该细胞因子促进KC的mRNA通过拮抗LPS-诱导的mRNA稳定,而不是通过在mRNA降解过程有直接影响主要衰减。事实上,使用的Tet-可调节的系统,IL-10没有变化,在不存在LPS,KC mRNA降解的速率的。KC mRNA稳定性的由LPS和调节IL-10的拮抗作用均发现是依赖。因此,IL-10与LPS敏感途径中的干扰可能引起ARE介导的事件,调节诸如上游信号传导途径介导的mRNA稳定效果在RNA结合蛋白的表达或功能的改变,或规定脂多糖。
转录后调控趋化因子的:未来的挑战
迄今为止所描述的研究表明,趋化因子的转录后调节受到越来越多的关注,并且越来越重视这些机制在确定炎症反应程度方面的影响。
许多问题仍有待解决。首先,需要确定趋化因子转录物调控区中存在的RNA基序,如5′-和3′-UTR,并且需要验证它们介导内源性转录物和报告结构稳定变化以及影响翻译的能力。这些基序的定义对于识别可能与这些序列相互作用的RNA结合蛋白至关重要。最近,被定义为“核糖经济学”的实验方法(由J.Keene首创)极大地促进了对RNA结合蛋白与其靶点之间关系以及这种关联的功能结果的了解130.这种方法是基于血缘关系的假设一组共享一个信使rna分子识别主题,如战神,可以通过互动与共同监管rna结合蛋白,从而创建记录的子集的命运决定转录以协调的方式,在转录后操纵子23那24.鉴定与给定的RNA结合蛋白相关的MRNA的子集体内在特定条件下,实验的方法是利用使用特异性抗体用于RNA结合蛋白mRNPs的IP,并显示相关的mRNA的通过杂交测定的身份。在最近的一项研究阵列,与相关的HuR成绩单池已在人类结肠癌细胞系使用这种方法确定的RKO28.主序列的组合计算分析和围rMA靶的初级结构允许鉴定富含17-20碱基长的尿嘧啶的RNA基序。该结合基质被发现在以前已知的大多数转录物中,该转录物被扰动调节,包括CCL11。使用该方法,可以预测,随后在基因数据库中的转录物中验证,验证的新靶标。
随着对更多rna结合蛋白识别基元的认识的增加,识别趋化因子mrna中的这些关键区域将有助于识别与趋化因子表达可能相关的调控分子和通路,从而可被治疗靶向。
其次,距离调节趋化因子后转录对照控制的信号通路仅开始被识别,到目前为止所进行的研究已经揭示了它们的复杂性。如前所述,是介导的调节可以通过不同的途径介导,有时以刺激或细胞特异性的方式介导。例如,当LPS诱导时,CXCL3 mRNA的稳定性对THP-1单核细胞系中的P38 MAPK抑制敏感65.而在IL-1诱导的hek293细胞中则没有31.还需要建立一定的信号转导通路是否控制RNA的营业额或翻译。的MAPKAP激酶(MK2),例如,调控对ARE介导的IL-6和IL-8 mRNA的稳定性,同时控制ARE-依赖TNF-α的翻译控制51.那90..
第三,rna结合蛋白介导趋化因子转录后控制的生物学需要阐明。在免疫激活后,含有are的炎症基因表达的快速、短暂的增加是通过具有相反功能的rna结合蛋白的整合活性在转录后进行调控的107..例如,在Jurkat细胞中,RNA电动性移位测定显示MRNA稳定蛋白质最初与GM-CSF 3'-UTR结合,响应于丝率的激活,以及随后的mRNA衰减促进因子结合,如mRNA衰减促进因子作为TTP,如下107.那131.实际上,围绕T细胞激活后,enr诱导ur先前131两种蛋白部分重叠,结合一个含are的3 ' - uts子集,如TNF-α、GM-CSF、IL-3和c-fos104.那131.
户珥的建立作为调停者的细胞因子诱导的稳定CCL11 mRNA表明类似的途径可能发生在趋化因子的规定和打开了一个广泛的监管调查因素参与了这一过程,这些绑定到RNA或其他蛋白质,可能与rna结合蛋白结合,促进或抑制趋化因子mRNA运输、转换或翻译的机制(图1)⇑)。
最近的几项研究揭示了不同类型的癌症的HuR表达增加和激活。在这些情况下,的HuR被发现结合并协调在肿瘤血管生成和生长相关因子的转录后调控,在人类疾病提供转录后操纵子模型的验证40-42..免疫应答和炎症的特征还在于通过增殖反应和通过重塑过程,其包括血管生成132,使这些模型也适用于这些生物过程。可以预见,促炎症介质刺激后早期反应基因的异常mRNA稳定可能有助于慢性炎症条件的建立。事实上,控制这一过程的RNA结合蛋白,如HuR,可能不再以瞬时方式发挥作用,而是持续激活,因为它们本身是炎症介质启动的信号通路的目标,从而延长转录稳定性并长期维持炎症反应。
人们对这些RNA结合分子的功能以及其功能改变在疾病中的潜在作用的认识不断提高,导致在人类和小鼠中对其组织分布和亚细胞定位以及调节其功能的刺激和信号通路进行了更系统的研究113.那115.那116.那133-138.未来的任务应该是在炎症和过敏过程中寻找RNA结合蛋白表达,功能和信号传导的改变的研究,其中趋化因子和通过其功能调节的其他促炎分子起着重要作用。此外,有必要将这些发现与其目标MRNA的半衰期或翻译中的表达和变化相关联139.rna结合因素似乎转录调节的协调表达多个基因参与一个生物过程,识别异常水平或功能可能成为一个重要的治疗目标,作为活动的调制多个目标的蛋白质含量,影响很大,因此,传达一种强大的消炎作用。
结论
炎症反应的幅度可以通过影响的参与这一反应,包括趋化因子的许多关键基因水平的转录后调节机制受到很大的影响。它越来越清楚这些机制是扰动可能是致病32那46.那47.那140..这些过程的分子基础是目前研究的重点,旨在更深入地了解信号通路、调控序列和结合因子,最终传递mRNA的转换和翻译的变化。这些机制的细胞和刺激特异性的定义对于考虑这些新的、重要的途径作为抗炎治疗的靶点也至关重要。
致谢
C. Stellato感谢V.Casolaro,S.N.Georas和R.P.Schleimer有用讨论审查的主题,以及L.A. Beck的友情帮助与趋化因子命名的表格帮助。
- 已收到2004年10月21日。
- 公认2005年6月28日。
- ©ERS期刊有限公司