摘要
肺纤维化组合和肺气肿联系的综合征尚未得到全面描述。
本文作者回顾性研究了61例胸部计算机断层扫描的上区肺气肿和下区肺纤维化的弥漫性实质肺疾病患者。
患者(所有吸烟者)包括60名男性和一名女性,平均年龄为65岁。所有患者都存在于劳累的呼吸困难。在87%和43%的手指杆上发现基底噼啪声。肺功能测试如下(平均值±SD.):总肺容量为88%±17,强制生命能力(FVC)88%±18,强制呼气量一秒(FEV1)80%±21(%预测),FEV1/ FVC 69%±13,肺部37%±16(%预测)的一氧化碳扩散能力,一氧化碳转移系数46%±19。肺动脉高压在47%的诊断患者中存在,随访期间55%。患者从诊断中遵循2.1±2.8毫秒的平均值。生存率为2 YRS为87.5%,5岁为54.6%,中位数为6.1毫秒。诊断下肺动脉高压的存在是预后的关键决定因素。
作者特此是个性化计算机断层扫描定义的肺纤维化和肺气肿的综合征,其特征在于亚内正压测定法,气体交换严重损害,肺动脉高压率高,存活率差。
肺气肿和特发性间质性肺炎,包括特发性肺纤维化(IPF),是由不同的临床、功能、放射学和病理特征定义的实体。合并肺纤维化和肺气肿(CPFE)已在一系列IPF患者中被提及,或已成为病例报告或短系列的主题1-3.,但迄今为止没有在大型患者队列中专门研究过。目前的研究详细分析了61例计算机断层扫描(CT)的均质组均匀组临床特征的详细分析,从而导致特征实体的个性化,进一步表明存在肺动脉高血压(PAH)在诊断中是这些患者预后的关键决定因素。
患者和方法
案例招聘
这项回顾性多期形研究由Groupe d'Etudes et de Recherche Sur Les Malladies“orphelines”肺(Germ“O”P)进行了,这是一个致力于罕见(所谓的“孤儿”的研究))肺部疾病。一封信被送到网络的所有参与的医生,要求他们向细菌“o”o“p登记处,任何一份CPFE在1985年1月和2003年12月之间遇到的任何案件。然后通过发送给的详细问卷来回顾临床数据。每个参与的医生都报告过案件。数据收集于2004年7月1日结束。
选择案件
如果满足以下标准,套件是可以接受的。1)CT扫描对肺气肿的存在,定义为与垂直的正常肺相比的衰减和垂直的衰减区域,由非常薄(<1mm)或无壁,和/或多个大疱(> 1厘米)的脊髓覆盖上部占主导地位。2)CT扫描具有显着肺纤维纤维化的弥漫性实质肺病,定义为具有外周和基础优势,蜂窝,建筑畸变和/或牵引支气管扩张或支气管切除术或支气管切除术的网状不透明度;焦点玻璃透露度和/或肺泡冷凝区域可能是相关的,但不应该突出。
只有CT扫描可供审查的情况。
患有CFPE诊断时的结缔组织疾病的患者被排除在研究中,以及患者诊断其他间质性肺病,如药物诱导的间质性肺病,肺炎,过敏肺炎,结节病,肺组织细胞症。,淋巴胆管瘤和嗜酸性肺炎4..
临床分析
作者回顾了在诊断和随访期间的医疗记录、肺功能检查和实验室检查。
胸部的高分辨率CT(HRCT)扫描在薄膜上通过两名作者分别审查了临床资料的作者,在不间断的情况下进行第三个分析。他们被要求指定下叶异常的CT模式是否是IPF的典型,或强烈暗示IPF或抗纤维非特异性间质性肺炎4..按照其他地方定义的,收集数据用于肺气肿特征和主要间质性异常5..
根据国际标准审查,在可用时,肺活量检查4..
根据欧洲呼吸学协会指导来进行肺功能测试188bet官网地址6..肺泡-动脉氧差P.(a-a),o2估计呼吸室空气的肺泡氧分压(P.A,O.2)动脉血液中氧的分压(P.A,O.2), 在哪里: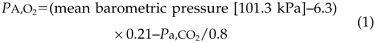 P.A,CO.2是动脉血中二氧化碳的分压。
P.A,CO.2是动脉血中二氧化碳的分压。
PAH由收缩动脉肺部压力≥45mmHg定义,如超声心动图估计的TRICUSPID反弧流动估计。
数据分析
使用Kaplan-Meier方法进行存活分析,终点死亡或审查。如果患者仍然存在于最后的接触(n = 43),则接受肺移植(n = 2),或者从CPFE(n = 2)以外的已知原因死亡。死亡原因被认为是由于CPFE未知(n = 4)。使用对数级测试进行生存的比较。值显示为平均值±SD.除非另有指定。P <0.05被认为是显著的。
结果
临床表现
共收到73份完整的问卷进行分析。12例被排除,因为在诊断CPFE时存在相关结缔组织疾病(皮肌炎,n = 2;类风湿关节炎,n = 1;系统性硬化症,n = 1),因为CT扫描无法复查(n = 7),或因为CT诊断标准不符合(n = 1)。本研究共纳入61例患者。在两个大型转诊中心收集了33名患者(里昂L. Pradel医院,21例;博比尼阿维森纳医院12例);每个核心作者收集的病例≥3例;小组的其他参与者收集了一两个案例(见致谢)。根据流行病学部门的记录,估计CPFE占特发性弥漫性实质肺疾病病例的约5-10%。
所有患者,但一个是男性,所有患者都是当前或出吸烟者(表1⇓)。出吸烟者戒烟了10.6±10.4岁的时间。两名患者有传染性肺炎的历史;另一位患者患有急性呼吸窘迫综合征的历史,继发于氨暴露。十四名患者(23%)具有动脉粥样硬化冠状动脉疾病(n = 9)或动脉粥样硬化外周枢动疾病的历史(n = 5)。
CPFE的第一个症状和诊断之间的平均时间为2.3±4.5 YRS(范围0-19 YRS;中位数43天)。表1中列出了诊断的特征和临床表现⇑.主要临床症状伴有呼吸困难,在所有患者中存在劳累,并咳嗽在一半的患者中。在43%的病例中报告了手指杆。肺部的一系列肺部发现90%的患者的异常,其中由肺部下部区域的双侧裂纹组成87%,很少与喘息(13%)相关。
没有患者符合尘肺病的诊断标准,没有人有显著的环境抗原暴露。
肺气肿的成像诊断在鉴定纤维化变化16例,中位数为4.7毫升(0-10.7);在肺气肿之前只观察到纤维化只有三种情况;31例患者同时发现肺气肿和纤维化(没有胸部X线X型X型X型X型X X X XFEA,在11例中可用)。
生物学和支气管肺泡灌洗液
血红蛋白水平为14.9g·dl-1±2.1,并且> 16 g·dl-1在14名患者中。水平α.1- - antiTrypsin低(0.19 g·l-1)一例为PiZZ纯合的患者;另一名PiMZ表现型的患者的正常水平α.1- antiTrypsin(1.6 G·L.-1)。
在27名患者中进行了支气管肺泡灌洗(BAL)。BAL白细胞计数为240±200×106.·L.-1(范围71-760)。BAL差异细胞计数如下:巨噬细胞76%±24(范围10-90),中性粒细胞10%±19(2-73),嗜酸性粒细胞2%±10(0-43),淋巴细胞5%±9(0-43)。
抗核抗体中的44例患者中的17例(39%)中有17例,中值滴度为1/160(范围1 / 64-1 / 1,280),其中10个,其中10个具有均匀的图案和五种具有斑点图案的五种,具有抗- 没有双链DNA。在20例中的六种患者中发现循环免疫复合物,43名患者中的四种患者中的类风湿因子中有四种。在35名患者中,在35名患者中,存在抗替诺罗氏醇细胞质抗体,其中4例在35名患者中,没有抗蛋白酶3或抗蛋白酶酶对ELISA的特异性。
肺功能测试
15例患者体重指数正常(18.5 ~ 25),36例患者>25正常(60%),无一例患者体重指数<18.5。对23名患者进行了6分钟步行测试,其中9名患者在测试期间接受了吸氧;6分钟步行距离为336±139 m(范围50-548),脉搏血氧仪测量动脉氧饱和度下降(S.P,O.2)9±6%(0-20%)和aS.P,O.2在测试结束时为85±6%(74-96%)。
肺功能参数列于表2中⇓.尽管所有患者的CT扫描均有明显的肺气肿改变,但1秒内平均用力呼气量(FEV)1)/用力肺活量(FVC)为69%,只有一半的患者(61例中30例)表现为阻塞性通气缺陷,根据FEV定义1/ FVC <70%。FEV.129例(48%)患者的预估(% pred) <80%,平均用力呼气流量在FVC (FEF25-75%)57名测试患者中的48例<80%(82%)。改善FEV.1在支气管扩张剂上,无含15%。在56名患者中的12例中发现了10%的肺容量(TLC)所示的限制性通风缺陷(21%)。TLC> 120%PRED仅占两名患者,并且在无残留的体积> 200%pred中存在。56名患者中有42例(75%),肺量正常。一氧化碳的转移系数(T.L,CO.)中56例(98%)的pred值<80%,而肺转移系数(K.CO.)57例患者中的54例(97%)中的50%。总体而言,61名患者中有20例(33%)中的20个肺活量测定法正常,其中包括16个常规TLC。减少T.L,CO.是14名患者唯一的异常功能测试。共有50名患者(82%)在休息时缺氧(P.A,O.2<10 KPA)。在运动,P.A,O.221例患者中有18例(86%)的血压低于10 kPa,平均下降−1.5±1.6 kPa。
肺动脉高血压
43例患者在诊断时进行超声心动图检查,49例患者在随访期间进行超声心动图检查。诊断时PAH患病率为47%,随访时患病率为55%。诊断时平均收缩期肺动脉压为48±19 mmHg(范围21-96),随访时为52±20 mmHg(范围22-96)。6例患者经右心导管确认肺动脉高压,4例患者平均肺动脉压≥40 mmHg(中位40 mmHg,范围24-54)。随访期间11例(18%)发生右心衰。
胸部和病理学的计算断层扫描
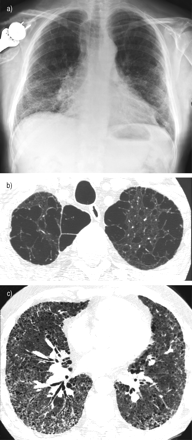
根据纳入标准,胸部的CT扫描显示出肺气肿的共存,具有上部区域优势和实质肺病,暗示所有患者的下叶肺纤维化(图1⇓)。放射审查的主要结果总结在表3中⇓.
典型肺纤维化和肺气肿的典型案例。a)胸部射线照片显示下叶片和高型肺部区域的双侧渗透不透明。b)肺部上部区域的胸部计算机断层扫描(CT),显示出主要的内含物和探针肺气肿。c)肺部下部区域的胸部CT,显示出网状不透明度,蜂窝和牵引支气管扩张。在该患者中进行的肺活检显示出上裂片的内瓣肺气肿和常用的下叶的常规肺炎。
除了两名患者的所有患者中,中部区域存在于中部区域。探针肺气肿特别频繁(93%)。大疱是在一半的患者中看到过的。
蜂窝状,网状内部不透明度和牵引支气管扩张分别是最常见的结果,分别为95%,87%和73%的病例。在三分之二的患者中存在非突出的磨玻璃衰减。空气空间固结和微渗都很罕见。在所有情况下,在56例(95%)中,在所有情况下占据较低和/或中瓣的纤维化变化占主导地位。下裂片中的CT模式是典型的IPF,31例患者(51%),强烈暗示IPF或抗纤维非特异性间质性肺炎(31%)(34%),并在其余情况下表现出具有主要网状不透明度的复杂模式。
开放肺活检或分泌植检肺的组织学分析可在8例中进行审查,并确认了上叶中主要的内含物肺气肿。在五种病例中,患有常春性肺炎的间质性肺炎,在一个病例中,在一个案例中组织肺炎,在一个案例中组织肺炎,在一个案例中有难以分配的间质肺炎。
治疗和预后
由于肺纤维化,一半的患者(30分中的30个)接受口服皮质类固醇,从最小的每日剂量为0.5 mg·kg-1泼尼松或泼尼松。十三个患者(21%)接受了进一步的免疫抑制或免疫调节剂。十四名患者(23%)接受长期吸入皮质类固醇。在只有五名患者(8%)的治疗中获得限制性通气缺陷的一些改善,而11名患者在后续期间临床(18%)和29例稳定(18%)和29例(在16名患者中,临床结果不是可评估的)。36名患者提供胸部的后续CT扫描,显示出肺气肿病变的恶化,纤维化变化1111中的纤维化变化,两种液体渗透性的改善,其余情况下稳定的异常。三十名患者(49%)在随访期间接受长期鼻氧疗法,其中包括在随访期间氧治疗的17个。20名患者(33%)为呼吸困难的急性增加而入住。
诊断后的平均随访时间为2.1±2.8毫克(0-12 YRS),并且从肺部表现前的总时间间隔到最后一次随访(或死亡)平均为4.6±5.6 YRS(测距0.2-22.2 YRS)。两名患者在诊断后接受了肺移植5.6和11.7 YRS。四十七名患者在最后一次随访中活着。十四名患者在那段时间内死亡,中位时间间隔从诊断到3.2 YRS死亡。死亡的原因是呼吸衰竭(n = 7),肠道恶性肿瘤(n = 1),术后败血症(n = 1),肺移植后的手术并发症(n = 1),未知(n = 4)。
生存分析
用Kaplan-Meier方法计算的存活率为1 yr,87.5%,2岁,5岁,5岁,中位数为6.1 yrs(图2⇓)。
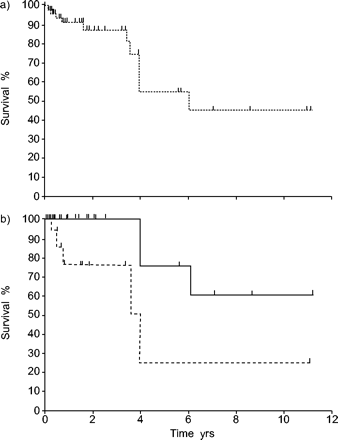
a)肺气肿合并纤维化患者生存情况(Kaplan-Meier分析);5年生存率为55%。b)诊断时根据肺动脉高压(PAH)对合并肺气肿和纤维化患者进行Kaplan-Meier生存率分析(—:无肺动脉高压,收缩期肺动脉压< 45mmhg, 5年生存率75%;----: PAH,收缩期肺动脉压≥45 mmHg, 5年生存率25%);p = 0.03。
检测临床、放射学和功能变量对生存率的影响。唯一具有统计学意义的生存差异(风险比= 4.03,95%置信区间(CI): 1.170-27.92, p = 0.03)是在诊断时PAH患者之间发现的(中位生存3.9年,95% CI: 1.3-6.6;平均生存率4.8年,95% CI: 1.6-8.0;5年生存率25%)和非肺动脉高压患者(中位生存率未达到;平均生存率9.1年,95% CI: 6.5-11.7;时间埋葬生存75%;图2⇑)。收缩动脉肺压力相关K.CO.(Spearman等级系数= 0.36; p = 0.031)但与其他肺功能参数(数据未显示)。在临床,放射功能和肺功能参数(数据未显示的数据)诊断时,患者在患者之间观察到或没有PAH的患者之间没有显着差异。
讨论
本研究对影像学标准定义的61例同质CPFE患者进行了综合分析,导致了特征实体的个体化。诊断时PAH是这些患者预后的关键决定因素。
患者几乎完全是男性。一切都是现任或出吸烟者。诊断(65岁)的中位年龄,手指杆的患病率(43%),魔术型细腻吸气裂纹的存在,占胸部一批患者的基础区域,以及BAL差分细胞模式与IPF中发现的类似7..在三分之一的患者中发现了非特异性的抗核抗体,但它们在CPFE的诊断中没有任何结缔组织疾病。
自从CPFE鲜为人知的成像特征,在这种描述性研究,作者选择包括弥漫性肺实质疾病患者纤维化的暗示低叶(与上部叶肺气肿有关),而不是限制入选标准只有那些典型的IPF患者CT模式。然而,所有病例的CT模式均为间质性肺炎,其中84%的病例CT模式为IPF或纤维化非特异性间质性肺炎。目前作者怀疑肺气肿可能改变IPF的CT模式,因此IPF的放射学诊断标准可能不适用于CPFE。因为它们把限制的证据作为一个主要标准4.,美国胸部社会/欧洲呼吸道学协会在没有手术肺活检的情况下诊断IP188bet官网地址F的标准并不适用于与肺气肿联合时对特发性间质肺炎的诊断。蜂窝状,网状内部不透明度和牵引支气管扩张酶是最常见的发现。虽然根据含有标准不包括突出的磨玻璃不透明度的病例,但一些底玻璃不透明性比IPF更频繁地存在4.暗示吸烟有关的间质肺病,例如脱泥性间质肺炎和呼吸支气管炎 - 间质性肺炎,可能存在于含有CPFE的一些重型吸烟者中。如孤立病例所报道的,一些患有非特异性间质性肺炎的组织学模式也可能存在于一些CPFE和地玻璃不透明患者中8..抗开肺活检或肺移植的8例CPFE患者的分析表明通常的间质性肺炎是下叶中的主要模式,其中一个病例在一个案例中具有脱皮间质肺炎。
CPFE患者的肺功能试验显着不同于IPF患者的患者和肺气肿患者的患者。正如以前的报告所述1那9.,肺体积的平均值在正常近,因此与一氧化碳转移的明显受损的容量显着受损。FEF的测量25-75%可能比FEV更有用1检测CPFE患者的阻塞性肺疾病。肺的恶性膨胀和肺气肿区域的高顺应性可能补偿下叶纤维化造成的容积损失,而肺气肿和纤维化可能对一氧化碳转移和运动低氧有加性或协同效应。四分之一的患者肺量和薄层色谱测定正常。因此,如果没有测量一氧化碳转移和/或运动血气,肺量低于正常或正常的患者可能识别不出CPFE。
由于上部肺气肿和下部区域纤维化可能偶尔都会错过普通胸部射线照片,因此需要仔细分析胸部HRCT,以准确诊断该综合症。富含吸烟导致的上裂片中的内瓣的内肢是肺气肿的主要放射介绍,而Pancinar肺气肿是没有看到的,但是众所周知,HRCT是不准确的,以区分灵芝从肢体肺部区分Pancinar10..本研究的一个新发现是鼻中隔旁肺气肿(也称为远端腺泡肺气肿)的显著流行率(>90%),提示这可能是CPFE的一个标志。隔旁肺气肿与吸烟有关11.,并且可以自身模仿间隙和隔间线。然而,在目前研究患者的下部区域观察到肺纤维化的真正渗透不透明性。间质透明度和肺气肿之间的关系是可变的,在某些情况下,近距离基地的纤维化病变的肺气肿病变,从上裂片中的肺气肿和相邻肺的纤维化到蜂窝肺中的嗜肺血管中的嗜纤维和纤维化病例,探针肺气肿,其纤维化般隔膜在剩余的情况下的纤维化等。
间质肺病患者的存活时间存在显着的异质性4..由于预后的估计可能对药物治疗决策产生影响,因此对患者的移植和信息的转诊试图确定可靠预测生存的指标变得越来越重要。本研究提供了CPFE患者的第一次存活分析。中位生存率为6.1岁,比在初步访问时间不到35个月的中位生存,更好地生存,比在大型活组织检查常常间质性肺炎的大型研究中出现了更好的存活率12..然而,在没有纤维化的情况下,CPFE的存活率比预期的肺气肿更糟糕,其中在FEV的患者中观察到近100%的2年份存活1预测的三分之一13.那14., 5年死亡率为19%α.1- antiTrypsin缺乏15..
CPFE患者的肺动脉高压患病率特别高(诊断时接受超声心动图检查的患者中近一半),高于IPF的报道16.-18.或慢性阻塞性肺病(COPD)19.那20.,即使在疾病的晚期。在大多数情况下,超声心动图是作为呼吸困难患者常规调查的一部分进行的。然而,这项研究是回顾性的,并非所有患者都有超声心动图,使超声心动图可能已经更常见的患者更严重的疾病,因此不能排除肺动脉高血压的可能性更高。甚至假设没有接受超声心动图的患者可能没有肺动脉高压,肺动脉高压的最小计算患病率仍然是33%的诊断和44%在随访期间。相比之下,在某些情况下,超声心动图可能错过了肺动脉高压,因为三尖瓣流动流量在高达3个COPD患者中不可衡量。21.(尽管胸部过度下降可能在肺气肿中的CPFE中可能不那么重要)。这种患病率不可能是由于在特别晚期的患者学习患者,而是反映了CPFE的自然历史。肺动脉高压尽管静止时患有相当温和的白昼血氧血症,可能反映了毛细血管和纤维化(而不是唯一的低氧肺血管收缩)的毛细血管床的减少,如此K.CO.还有收缩期肺动脉压。值得注意的是,诊断时存在肺动脉高压是生存的独立预测因素。PAH已被证明显著影响COPD患者的生存20.,但IPF患者尚未明确证明这一点,尽管胸部射线照片肺动脉高压的证据与较差的预后有关12..
CPFE的病理生理学是未知的。所有患者都存在烟草吸烟的历史,这表明它可能是这种综合征病理生理学的强烈决定因素。吸烟的作用在肺气肿中很好地建立14..案例控制研究表明,吸烟也可能是IPF发展的危险因素22..此外,烟草吸烟可能会在IPF患者中改变肺功能23.那24..有人认为,肺上区纤维性下区牵引可能导致肺气肿1.然而,射线照相纤维化变化很少在肺气肿的发作之前,表明CPFE中的肺气肿仅导致纤维化肺缩回。可能会推测肺气肿和纤维化可能在某些情况下与共同的环境触发和(或)遗传易感性因子有关,烟草曝光发挥着核心作用。因此,CPFE可以由患者在患有患者的吸烟有关的肺气系中的吸烟有效的间质肺病产生(后者可以促进蜂窝状的肺部)中的巧合。
CPFE中的治疗选择有限。这种回顾性系列中皮质类固醇或免疫抑制治疗没有显着益处。烟草吸烟应停止。干扰素 -γ.在IPF中有效25.,导致小鼠肺气肿26.,因此在CPFE中不可取。在肺气肿、IPF和CPFE的背景下,尚未评估肺动脉高压的具体治疗方法。
总之,胸部计算机断层摄影下叶片上裂片的组合肺气肿综合征导致特征函数型材,具有肺部的肺部,肺的一氧化碳漫射能力强烈损害,运动中低氧血症,因此除了特发性肺纤维化和肺气肿之外,应该得到这个实体的个性化。尽管亚型肺活量测定,但可能对其肿大的血液造成,肺纤维化组合和肺气肿是严重的实体。诊断下肺动脉高压的存在是预后的关键决定因素。
附注添加到证明:自提交本文以来,在过表达肿瘤坏死因子的转基因小鼠中证明了与肺气肿和纤维化均一致的病理变化。α.27.,这可以代表肺纤维化和肺气肿联合的实验动物模型。
致谢
作者谨感谢C.Oyakim,R.更简单,J.O.Maillard,C.Comptère,G.Brinchault和S. Guillot在数据收集中提供帮助,以及S.Bart和C.Silarakis进行数据输入和秘书工作。作者还要感谢M. Brauner(Bobigny)审查CT扫描和F. Thivolet-Béjui(HôpitalL.Pradel,里昂),M.Kambouchner(HôpitalViCenne)和E.Brambilla(格兰诺布尔)用于病理分析。
肺部疾病“孤儿”研究小组(GERM“O”P)的下列成员包括一个或多个病例参与了这项研究:P. Carré (Carcassonne), F. Chabot (Nancy), G. Chatté (Caluire), d . Coëtmeur (Saint-Brieuc), j . f。Cordier(里昂),V. Cottin(里昂),I. Court-Fortune (Saint-Etienne), B. Crestani(巴黎),J.C. Dalphin (Besançon), P. Delaval (Rennes), G. Devouassoux(里昂),A. Dietemann (Strasbourg), B. Gentil (Bourgoin), M. Humbert(巴黎),D.以色列- biet(巴黎),J. Lacronique(巴黎),M. Mairesse(比利时Namur), E. Marchand(比利时Yvoir),H. Nunes(博比尼),M.雷诺-高贝尔(马赛),I. Tillie-Leblond(里尔)和D. Valeyre(博比尼)。
- 已收到2005年2月23日。
- 公认2005年6月29日。
- ©ers Journals Ltd