摘要
在肺血管疾病中,肺血管床的改变将导致肺血流动力学的改变。本文综述了几种生理学原理的应用,通过新技术无创测量这些变化。
肺血管病患者肺血管床的血流特征改变。磁共振成像和计算机断层扫描技术的最新发展使这些异常流动模式的可视化和量化成为可能。肺灌注信息也可以通过电阻抗断层扫描测量肺内的电阻抗变化来获得。测量肺血流量的一个更间接的方法是测量乙炔(一种灌注受限气体)的吸收。关于肺血管床的信息也可以通过测量肺血管内皮的呼出产物,如一氧化氮来获得。
尽管所描述的所有技术都提供了诊断或监测肺血管疾病的新方法,但这些技术的临床数据有限。因此,在这些技术应用于临床实践之前,必须进一步改进和评估其临床价值。
系列“呼吸监测:用新工具重温经典生理原理”
编辑:M.I. Polkey, R. Farré和A.T. Dinh-Xuan
本系列的第5条
低动脉压和周围血管阻力(PVR)是肺循环的特征。低压和阻力都是肺血管床的特殊功能和解剖结构的结果。肺血管床由高度可扩张的血管组成,这些血管能够容纳大量的血容量增加,就像在运动中一样,同时通过肺微血管床的扩张和再扩张保持低压1.在影响肺血管的疾病中,肺血管的丧失和肺血管的梗阻性病理改变,如血栓性病变、内侧肥大和内膜纤维化,导致PVR和肺动脉压(PAP)升高。然而,由于肺血管床的扩张性和募集能力大,正常静息PAP在病程中上升较晚,此时肺血管床已被阻塞达70%。对于诊断肺血管疾病最常用的无创技术——多普勒超声心动图,PAP升高是诊断肺血管疾病的前提2.通过这种方法估计PAP来评估肺血管疾病需要在诊断之前有广泛的肺血管损伤。此外,PAP似乎是监测疾病进程的一个相当不敏感的变量3.- - - - - -5.因此,更敏感的非侵入性肺血管床评估技术不仅是诊断早期肺血管疾病所需要的,而且可能提供一个更好的工具来监测治疗效果。本文旨在介绍一种新的无创测量肺循环特征的方法。
测量肺血管功能
由于肺微血管床不能无创可见,只能间接获得其功能的信息。近年来已经发展了几种测量肺血管床特征的方法。最直接的方法是通过对比液通过肺部来测量肺灌注。磁共振成像(MRI)和计算机断层扫描(CT)的最新进展使实时研究肺小血管的肺灌注动态成为可能。另一种方法是测量心脏周期中电阻抗的变化,因为电阻抗的变化与血容量的变化成正比。基于这一原理,电阻抗断层扫描(EIT)被开发出来,使可视化和测量心脏周期内肺血容量的变化成为可能。一种更生理学的方法是通过吸收乙炔来估计毛细血管血流,乙炔是一种灌注有限的气体。最后,可以分析呼出空气中内皮因子的产生,如一氧化氮(NO),作为肺内皮功能的指标。由于这篇综述的重点是肺血管床本身,其他有前途的技术将不讨论针对右心脏。
对比增强磁共振成像
动脉或小动脉的局部狭窄,如肺动脉高压(PAH),将导致局部较高的阻力,从而导致这些动脉供血区域的灌注减慢。因此,通过肺灌注测量肺血管床的特征需要具有良好的空间分布和时间分辨率的技术。对比增强MRI (ceMRI)本质上是快速和三维(3D)的:在任何二维(2D)图像平面上,都可以在连续的时间间隔(约150毫秒)内获得功能2D灌注图6.这种动态2D ceMRI已证明其在恶性结节的特征价值,即注射造影剂后信号快速增加7.另外,肺的全3D覆盖(MR血管造影)可以在3秒的时间步内获得,甚至更快8,9.在这个过程中,以钆为基础的MRI造影剂通过静脉注射来缩短周围氢核的纵向松弛时间。作为一种选择,MRI采集由ECG R波触发,以测量心脏周期同一阶段的后续灌注图。病人被指示在采集过程中屏住呼吸。MRI灌注成像平面可以选择适合临床或研究问题的位置和方向。为了进行动态分析,必须知道动脉输入功能,因此灌注图像中应该包括右心室(RV)或肺动脉主干。心脏短轴图像平面的优点是,肺输入函数(造影剂到达右心室)和肺输出函数(到达左心室)都可以从相同的采集中获得(图1)⇓).为了对肺的所有区域进行最佳覆盖,冠状面是首选的,其中肺动脉主要包括在一个图像平面中,以获得输入函数(图2)⇓).迄今为止,很少有临床研究利用动态肺灌注数据。到目前为止,时间分辨3D MRI灌注已用于测量射频消融治疗房颤后肺静脉狭窄的影响;灌注缺损被可靠地证实8.Fink还应用了动态三维MRI灌注et al。10和Ohnoet al。9显示肺栓塞的楔形缺损和PAH的延迟灌注。图3⇓分别展示了两例轻度和中度肺动脉高压患者的区域肺灌注时间曲线。受试者仰卧于1.5特斯拉全身“Sonata”MRI系统中(Siemens Medical Solutions, Erlangen, Germany)。灌注分析的兴趣区域(5 cm×cm区域)在肺前和肺后区域绘制。从造影剂到达RV开始,到随后的20次心脏跳动,分析每一次心脏跳动的灌注。轻度PAH患者的灌注曲线显示,肺后区和肺前区分别在注射后第5次和第8次心跳时出现峰值增强,后区增强较早。在第20次心跳时,这种反差很大程度上被冲淡了。中度PAH患者的类似曲线显示,目前仅在第14和第17次心跳时出现峰值增强,前后肺区无明显差异。在第20次心跳时,没有心跳衰竭的迹象。从这些曲线可以看出,PVR的增加导致造影液通过肺外周部分的速度变慢,区域分布不再由重力决定。后者可以解释为,在更严重的多环芳烃患者中,肺压力超过了正常受试者中存在的重力效应。 The enhancement curve in figure 3⇓为MR信号强度增加的百分比。对于区域灌注的绝对定量,有必要将MRI信号强度曲线与gamma变量曲线拟合6,考虑肺动脉主干增强曲线。这是区分心力衰竭引起的灌注不良和PVR增加引起的灌注不良所必需的。
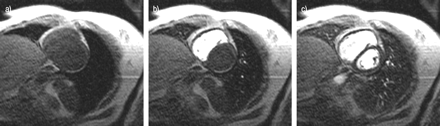
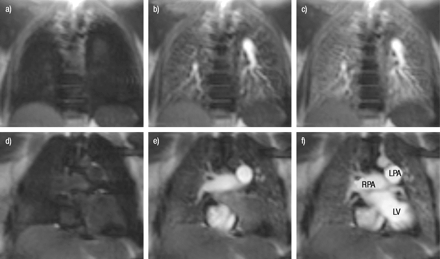
磁共振成像灌注样例图像:基线(a),造影剂到达右心室(b),造影剂到达肺部(c)。视野290×380 mm,像素大小2.8×2×8 mm,由ECG R波触发,每心动周期一幅,触发延迟365 ms。在肺的前部和后部,5厘米的区域2进行动态灌注分析。
磁共振成像灌注图像在肺动脉高压病人,在两个不同的冠状面t = 0年代对比(a, d)到来之前,在t = 6 (b, e)和t = 8.7 s (c、f)。对比抵达t = 6 s从信号明显增加右心室(e), 8.7年代的对比在肺部达到峰值水平,也才会出现在左心室(f)。采集参数:体素大小3.5×2.7×10 mm,切片距离40 mm,单发稳态自由进动脉冲序列,每150 ms一幅图像。在本例中,应用了90°饱和脉冲,反转时间为90 ms。左室:左心室;LPA:左肺动脉;右肺动脉。
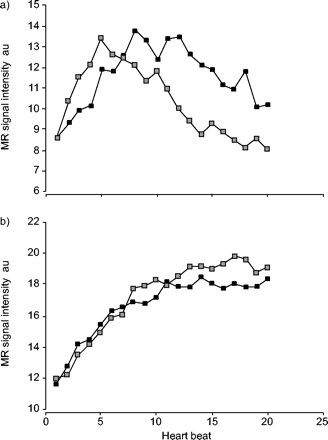
a)肺前后区灌注曲线,右心室造影剂到达后连续20次心跳,轻度肺动脉高压(肺动脉压(PAP)收缩压/舒张压/平均(s/d/m) = 43/20/31 mmHg)患者。x轴为造影剂到达右心室后的心跳。y轴为前后区磁共振信号强度。b)中度肺动脉高压患者的灌注曲线相似(PAP s/d/m = 49/31/40 mmHg)。▪:前;▓:后。
因此,ceMRI具有在2D或3D中以高时间和空间分辨率量化肺灌注的潜力。此外,在同一MRI调查中,可以获得右心室的功能变量和整体肺流量的绝对量化,这可能使MRI在不久的将来在肺血管疾病患者的诊断和监测中发挥重要作用11,12.
计算机断层扫描
不同形式的CT是一种非侵入性技术,可以量化通过肺血管床的血流量。这项技术是基于检测对比后肺密度的变化。肺血流量是通过计算感兴趣区域(ROI)的相对灰度或Hounsfield单位(由空气、肺实质和血液组成)肺实质在感兴趣区域(ROI)中的百分比,与大血管内的时间密度曲线进行比较来表示单位体积肺实质的血流量。结果也可以在使用彩色比例尺的定量灌注图中描绘。该方法可测量以mL·min为单位的绝对肺血流量−1·毫升−1肺部组织。为排除肺内主要血管的影响,可选择肺外周部位的感兴趣区。到目前为止,只有电子束计算机断层扫描(EBCT)被用于研究肺组织的灌注(图4)⇓)13- - - - - -15.EBCT是一种使用外部电子源来唤起辐射的技术,可以实现非常快的旋转时间和减少运动伪影。然而,EBCT并没有广泛应用,尤其是在欧洲。EBCT用于研究重力对肺灌注分布的影响16.研究人员使用EBCT发现,因系统性硬化症引起的继发性肺动脉高压患者肺依赖和非依赖部分之间的密度梯度降低17.琼斯et al。18还发现肺动脉高压患者的灌注垂直梯度缺失,与健康受试者相比,肺动脉高压患者的灌注明显减少。此外,在给予腺苷(一种用于右心导管插管时肺可逆性测试的血管扩张剂)后,测量了肺动脉高压患者的肺灌注增加。在过去十年左右的时间里,随着更快扫描仪的出现,在灌注研究中使用传统CT系统的可行性增加了。目前的多层排CT (MDCT)≥16个探测器,理论上可以对肺切片进行容积灌注成像。然而,CT灌注研究一直局限于胸部以外的其他区域19,20..图4⇓图示多层螺旋ct灌注。采用四排CT系统(SOMATOM Volume Zoom;西门子,Erlangen,德国)。为绘制肺灌注定量图,在肺动脉主干水平进行测量。中叶可见肺实质灌注显著减少。图像与肺血管造影吻合良好,灌注缺损也清晰可见。多层螺旋ct是一种很有前途的测量肺部血流量的技术,并被广泛应用。EBCT和多层螺旋ct的一个缺点是高剂量的辐射。EBCT的一个主要缺点是目前大多数中心都没有扫描仪。由于常规CT对肺实质的评估是呼吸困难患者正常工作的一部分,在同一过程中获得肺血管床的定量信息是很有吸引力的。 However, there is no information available about the value of this technique for the diagnosis or monitoring of pulmonary vascular disease. Furthermore, this technique requires further technical improvement and standardisation to be clinical useful. Finally, the relationship between parenchyma density and pulmonary perfusion should be clarified in order to distinguish primary vascular involvement from loss of alveolar structure.
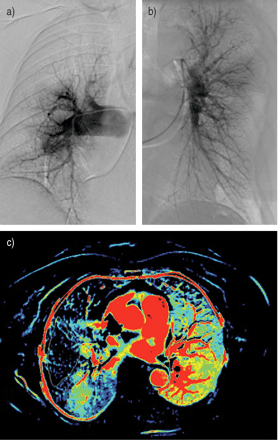
慢性长泡栓塞性肺动脉高压患者的血管造影及灌注研究。a, b)肺血管造影,显示右肺多发灌注缺损,c)肺动脉主干水平组织灌注定量图;颜色表示灌注速率,单位为mL·min−1·100毫升−1组织。红色是刻度的高端,蓝色是低端。注意中间叶几乎无灌注,这与肺血管造影相符。
电阻抗层析成像
胸内电阻抗的变化与心脏和通气事件密切相关。由于阻抗与血容量呈反比关系,因此可以通过测量阻抗来量化肺内血容量的变化。由于肺小血管在肺中含有最大的血池,具有最大的扩张性21,22时,这些血管主导了肺血管床搏动相关容积的增加,从而主导了阻抗的变化。因此,该信号可能包含有关肺阻力血管的重要信息。EIT是一种技术,它可以成像和量化阻抗变化的肺部灌注差异。大多数研究使用的是Barber和Brown在20世纪80年代开发的谢菲尔德应用电位层析仪Mark I(谢菲尔德,英国)及其继任者谢菲尔德APT as - 01p23.该系统在一个环中使用8或16个电极。如图5所示,在相邻电极对上依次施加≤5ma的恒定电流⇓.将电极之间的电位差重建为电极所跨越的平面内阻抗的图像。电极在第三肋间隙绕胸腔环状附着,心电门控可获得肺灌注图像24.由于目前可用的大多数EIT系统中使用的算法,只能成像阻抗的差异。为了研究肺灌注相关阻抗变化,选择舒张末期图像作为参考图像。在收缩期,血液被泵入肺血管床,这导致血容量比舒张末期容量增加,导致电阻抗降低。
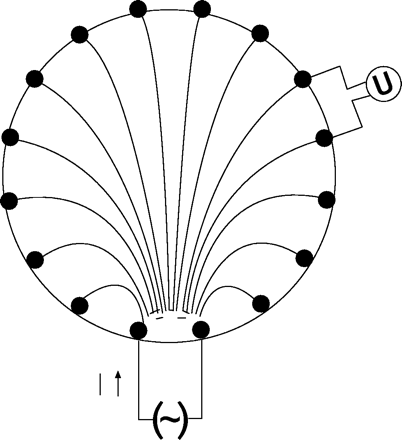
谢菲尔德法电阻抗层析成像原理。电流依次注入相邻电极对,并测量剩余电极对中的电位差(U)。利用滤波后的反投影,沿等势线(如图)进行图像重建。
首批探讨EIT检测肺血管床病理改变可能性的临床研究显示,肺气肿患者肺灌注阻抗变化明显小于健康人,明显反映了肺气肿患者肺血管床减少24,25.最近的两项小型研究表明,肺小血管的血管收缩和血管扩张的影响可以通过EIT监测26,27.在第一项研究中,研究了epoprostenol诱导的肺血管舒张对PAH患者EIT信号的影响26.研究表明,阻抗的变化与PVR的降低密切相关。在第二项研究中,健康受试者通过吸入缺氧空气(含氧量14%)诱导肺血管收缩,导致EIT信号降低。研究了6例活动性低氧性肺血管收缩的肺气肿患者的肺血管扩张。通过吸入100%的氧气,患者可获得低氧血管收缩的释放。在呼吸室内空气和高氧状态下进行EIT测量。100%含氧时阻抗变化显著增加,但并非所有患者都如此,而每搏量和心率保持不变27.
最近的技术进步带来了新型EIT机器的前景,这些机器能够重建心脏周期内绝对阻抗变化的3D图像,而不是相对阻抗变化28,29.虽然在确定肺血管床特征方面,EIT在理论上优于其前辈,但最终还是要根据临床数据来决定它是否是监测肺循环的有用工具。
乙炔吸收
在健康和疾病中,最广泛使用的肺血管功能无创参数是一氧化碳转移因子(TL,有限公司)30..TL,有限公司传统上用单呼吸法估计休息。这项技术是一项有价值的常规肺功能检查。虽然对肺动脉高压有降低作用,但对肺血管疾病的诊断价值有限31,32.测量乙炔(一种限制扩散的气体)的吸收可能比一氧化碳(一种限制扩散的气体)更准确地指示肺血管功能33.目前有两种测量乙炔吸收的方法。第一种是乙炔换气法,在换气过程中对多种气体进行逐气快速分析。乙炔消失曲线斜率用于计算肺毛细血管血流量,在没有分流血流量的情况下,肺毛细血管血流量等于心输出量。乙炔换气可采用开路换气34- - - - - -36或闭路换气37,38.几项研究报告了对健康受试者和肺动脉高压患者心排血量的准确估计39,40.这可能对监测肺血管疾病患者有价值,因为卒中量是一个比PAP更敏感的监测治疗效果的指标41.
第二种方法是纽斯发明的单次呼气吸气法et al。42,可在运动过程中进行(图6⇓).如果乙炔的吸收速率与肺毛细血管血流量成正比的假设成立,那么肺毛细血管血流量可以通过乙炔呼气曲线的斜率来测量43.拉梅奇et al。44改进了单次呼气技术,通过快速分析休息时和运动时单次缓慢呼气中乙炔、甲烷和一氧化碳的变化,发现肺部血流量和一氧化碳的变化TL,有限公司可以通过这种单次呼气技术准确测量。对健康受试者和心脏病患者的进一步研究表明了这种方法的准确性45,46.最近,黄et al。47提供了健康受试者休息时和运动时的预测方程,表明运动时乙炔吸收增加47.乙炔吸收的增加是否反映了肺血管招募的程度或肺血流量的增加尚不清楚48.此外,目前作者实验室未发表的数据显示,通过吸入法测量的乙炔吸收在PAH患者中异常低,这表明该测试的理论假设在这些患者中不满足。对这一发现的一种可能的解释可能是,多环芳烃中毛细血管的高流速与死区增加相结合,降低了乙炔的吸收率。虽然这种测量值与参考值之间的差异似乎可以作为肺血管疾病的诊断工具,但在评估吸气法的临床价值之前,应首先澄清这种差异的生理基础。
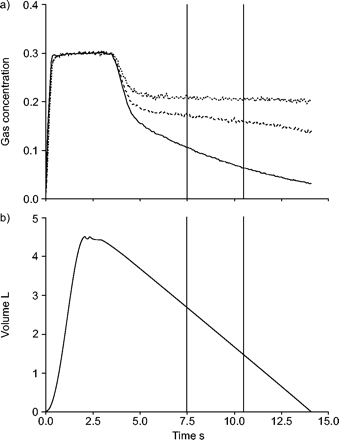
乙炔单次呼气吸气技术原理,吸气,3秒屏气,通过节流器持续缓慢呼气。在持续缓慢呼气时,甲烷(长)、一氧化碳(长)和乙炔(长-长-长)的浓度由快速红外分析仪(a)测定。根据乙炔消失的速率计算肺毛细血管血流。7.5到10.5 s之间的区域是曲线中用于计算毛细血管血流的部分(b)。
呼出的一氧化氮
一氧化氮是一种具有调节肺和外周血流量、血小板功能、免疫反应功能的分子,也是一种神经递质49.NO由NO合酶合成,这些合酶存在于呼吸系统、上皮细胞和内皮细胞以及神经组织中。血管内皮细胞产生的NO在肺循环调节缺氧反应中起重要作用50,流量增加51剪应力52通过促进血管舒张和抑制平滑肌细胞生长53.Giaid和Saleh先前的研究表明,高血压性肺血管疾病患者内皮细胞中NO合酶的染色减少54.此外,肺血管床减少,内皮细胞减少,即使内皮细胞功能正常,也会导致NO生成减少。
NO可以从呼出的空气中测量55它被认为反映了肺中不同腔室产生的NO,取决于呼气时的流速55.在缓慢呼气时,NO的测量反映了气道上皮细胞产生NO的情况,这用于监测哮喘的炎症56.在较高流速和洗出死亡空间体积后测量NO被认为可以反映肺血管床内皮细胞产生肺泡NO55.因此,在较高流速下测量呼出NO可能是监测肺血管床病理特征的一种方法。
市面上有几种自动设备,可以在吸入无游离空气后,通过单次呼气测量无浓度。NO通常以十亿分之一表示,浓度随呼气流速而变化57.因此,呼气时应记录流速,并使用流量电阻将流速保持在恒定水平,并略微提高压力,以最大限度地减少来自鼻腔空气的污染58,59.
初步研究显示,呼出NO可降低全身性疾病继发肺动脉高压患者的NO水平。临床et al。60在34例COPD患者中,经多普勒超声心动图测量的呼气NO输出与收缩压PAP呈负相关。由于这与肺功能的任何测量都没有相关性,特别是与肺的一氧化碳扩散能力没有相关性,作者得出结论,失效no水平的降低是内皮释放受损的结果。在另一项研究中,罗拉et al。61测量系统性硬化症患者呼出NO。他们发现,与健康对照组相比,系统性硬化症患者体内NO含量增加。将患者分为肺动脉高压组(多普勒超声心动图测量的收缩压PAP为>30 mmHg)和无肺动脉高压组,结果显示肺动脉高压组NO生成量低于无肺动脉高压组。这种关系也存在于间质性肺疾病。
在原发性肺动脉高压引起的内皮功能障碍患者中也测量了NO的释放。克雷莫纳et al。62与20名健康志愿者相比,8名原发性肺动脉高压患者的呼出NO含量较低。呼出NO的减少与肺毛细血管体积的减少有关。与此研究相反,莱利et al。63发现原发性肺动脉高压患者和健康志愿者体内过期no之间没有差异,尽管健康组在运动时no生成增加,而患者组保持稳定。最后,阿甘et al。64研究表明,先天性心脏病导致的肺动脉高压患者吸入雾化的epoprostenol后呼出NO增加,但在健康志愿者中没有。因此,在呼出气体的高流速下测量呼出NO可能包含有关肺血管床的重要信息。然而,由于文献中的数据相互矛盾,呼出NO在肺动脉高压诊断或监测中的作用尚不清楚,应在不久的将来阐明。
结论
肺部的气体交换需要通气和灌注,这两者需要匹配。肺功能测试和成像技术目前能够非常详细地绘制通气系统的功能。相反,肺循环的功能不能如此详细地进行无创检查。即使有创性测量PVR似乎也不可靠,如果肺部血流量也发生改变65,66.因此,使用6分钟步行试验评估运动能力是肺动脉高压临床试验中应用最广泛的主要终点。虽然这种方法已经成功地评估了功能3级和4级患者的治疗效果,但这种非特异性参数不能用于肺动脉高压早期阶段的治疗效果评估。挑战仍然是找到一种非侵入性技术来诊断和监测早期肺血管疾病。因此,最近发表了《肺动脉高压终点会议》67,建议继续发展描述肺血管功能的新技术。
为了临床目的,任何新方法都应该简单易行,并提供可重复的数据。EIT和吸气法测定乙炔吸收均符合上述标准。此外,两种方法均可在运动过程中使用,对肺动脉高压的早期诊断有一定价值。虽然初步资料显示肺动脉高压的阻抗和乙炔吸收降低,但尚无资料表明该方法对肺动脉高压诊断的临床价值或对疾病监测的价值。因此,在进一步技术改进的同时,应评估这些检测在肺血管疾病中的临床价值。
与EIT和吸气法相比,CT和MRI测量提供了更直接的肺灌注定量分析。两种方法的结果表明,这些技术不仅能提供肺血管床的结构信息,还能提供肺血管床的功能信息。这两种技术将在不久的将来进行进一步的技术改进,使快速分析肺灌注成为可能。虽然EBCT和MRI的数据都很有希望,但这两种技术在肺部疾病诊断方面的临床价值尚未得到评估。此外,这两种技术在技术上都要求很高,而且价格昂贵,因此在不久的将来不太可能被常规使用。
近年来,在肺动脉高压的病理生物学的新见解导致开发了几种有效的新治疗晚期这种疾病。虽然这些药物可能改变疾病的自然病程,但它们并不能治愈疾病。出于这个原因,人们有兴趣在其自然史的早期治疗这种疾病。由于评估肺血管疾病早期阶段的治疗效果关键取决于准确和非侵入性的工具来诊断和监测肺循环的早期病理变化,因此在大量患者群体中进一步发展和临床评估技术是有必要的。
脚注
本系列以前的文章:1号:Man WD-C, Moxham J, Polkey MI.磁刺激测量呼吸和骨骼肌功能。呼吸呼吸J2004;24: 846 - 860。2号:Farré R,蒙特塞拉特JM,纳瓦加斯d睡眠期间呼吸力学的无创监测。呼吸呼吸J2004;24: 1052 - 1060。3号:Calverley PMA, Koulouris NG。流量限制和动态恶性膨胀:现代呼吸生理学的关键概念。呼吸呼吸J2004;25日:186 - 199。4号:史加诺。从语言理解呼吸困难。呼吸呼吸J2005;25日:380 - 385。
- 收到了2004年10月25日。
- 接受2004年12月28日
- ©ERS期刊有限公司