摘要
肺气肿是与基质蛋白和蛋白酶活性的改变相关联。这些改变可以通过细胞凋亡被链接到程序性细胞死亡,潜在地影响肺结构和肺功能。
为了评估肺气肿中的细胞凋亡,我们分析了10例肺气肿患者和6例无肺气肿(正常)患者的肺组织。形态分析显示肺气肿肺中肺泡细胞,细胞核卷曲,具有凋亡特征。采用末端脱氧核苷酸转移酶介导的dUTP镍端标记(TUNEL)和凝胶电泳检测DNA片段。TUNEL显示,肺气肿组的细胞凋亡高于正常组。在肺气肿肺中检测凋亡标志物,包括活性caspase-3、聚(adp -核糖)聚合酶蛋白水解片段、Bax和Bad。线性回归显示细胞凋亡与细胞表面积呈负相关。肺气肿的肺显示较低的表面积和细胞增殖增加。细胞凋亡和增殖之间没有相关性,这表明,尽管在肺气肿期间这两个事件都增加了,但它们并不处于平衡状态,可能导致肺表面积的减少。
总之,与肺气肿实质损害相关的细胞机制包括凋亡和细胞增殖的增加。细胞凋亡与肺气肿扩大相关,支持肺气肿进行性的流行病学证据。这些数据扩展了对肺气肿发病过程中肺内的细胞动力学和结构变化的理解。
肺气肿的发病机制主要是蛋白酶-抗蛋白酶失衡1那2.该模型表明,细胞外基质(ECM)降解酶及其抑制剂水平的改变导致肺基质成分的损失。与正常肺相比,肺气肿肺中蛋白酶表达升高和ECM缺失的研究支持了这一假设3.-6..然而,该假说并没有阐明肺气肿发病机制的所有方面,如潜伏的腺病毒感染的作用7..它也不能解释肺气肿的加速和破坏性,即使在病人停止吸烟之后8.那9..
为了澄清替代细胞机制是否有助于肺气肿发病机制,调查的重点是程序性细胞死亡的细胞凋亡的作用10-12.Yokohori等.12检测到肺泡壁上皮细胞的增加增加(尽管在肺气肿肺中不是内皮细胞)。卡萨哈拉和松岛11肺气肿肺组织中肺泡间隔和内皮细胞凋亡,血管内皮生长因子(VEGF)表达降低。在早期研究的基础上,研究表明阻断VEGF受体信号诱导大鼠的细胞凋亡和随后的肺气肿10,科学家发现,与正常人和哮喘患者相比,肺气肿患者诱导的痰液中VEGF水平显著降低13.这些研究表明,内皮细胞维持因子的缺失与肺气肿的发病机制有关。此外,最近发现细胞凋亡在肺气肿中的作用不仅是相关的,而且是潜在的致病因素14.直接气管内输送活性caspase-3导致肺泡上皮丧失和肺气肿样结构改变。细胞凋亡发生在无炎症的情况下,显示了程序性细胞死亡在这种疾病中的特殊作用14.本研究进行了评估肺部肺气肿患者肺细胞凋亡,增殖和组织面积之间的关系。
材料和方法
人类肺样本
根据机构指南,在美国纽约纽约哥伦比亚长老会医学中心采集了16名患者的人体肺组织。10个样本来自肺气肿患者:5个来自肺移植,5个来自肺减容。患者术前戒烟≥6个月。6个正常样本来自意外死亡的受害者或未使用的供移植的肺。作为比较,肺组织取自非特异性间质性肺炎(n = 6)、嗜酸性肉芽肿(n = 3)、过敏性肺炎(n = 3)和淋巴管平滑肌瘤病(n = 2)患者。
免疫组织化学染色凋亡和细胞增殖
手术切除的组织用福尔马林固定,石蜡包埋。采用人增殖细胞核抗原(PCNA)抗体免疫组化切片评价细胞增殖情况;克隆PC10;Sigma,圣路易斯,MO,美国)。生物素化二抗采用亲和素-生物素复合物(Vector Laboratories, Burlingame, CA, USA)检测。在×40放大镜下测定pcna反应细胞占总细胞的比例(增殖指数)。免疫染色还使用抗人Bad和Bcl-2(美国KY KY转导实验室,Lexington)和Bax(美国加利福尼亚州圣地亚哥PharMingen)的抗体。切片用苏木精复染。
肺组织超微结构分析
采用2.5%戊二醛固定的肺组织进行透射电镜观察。组织用PBS冲洗,用2%四氧化锇冷冻固定。超薄切片用透射电子显微镜(1200 EX II, 80 KV;Jeol Sundbyberg、瑞典)。
空域扩大的形态分析
根据立体学方法计算苏木精和伊红染色肺切片(5µm)的平均线性截距、内表面积和肺体积分数15-18.使用Macintosh电脑和Image Pro成像软件(Media Cybernetics, San Diego, CA, USA)捕捉数字图像。在每个×40系列肺切片的10个不同区域上叠加了以1毫米间隔的水平线组成的半透明网格。这些线与肺泡壁相交的计数被用来确定内部表面积。这些线的端点接触肺泡壁的次数被用来计算肺泡肺容积分数。每个组织切片从10个随机区域收集数据。
原位DNA分裂标记
DNA切割使用末端脱氧核苷酸转移酶(TdT)介导的dUTP镍端标记(TUNEL)测定。采用死端比色法细胞凋亡检测系统(Promega, Madison, WI, USA)对连续肺切片进行生物素-链霉亲和素-辣根过氧化物酶或荧光素TUNEL标记DNA链断裂原位细胞死亡检测试剂盒(勃林格曼海姆,印第安纳波利斯,美国)。作为阳性对照,肺切片用RNAse-free DNAse I (Boehringer Mannheim)处理。作为阴性对照,在平行反应中省略了TdT酶。在×40放大镜下测量每个肺样本> 3000个实质细胞中tunel阳性细胞与总细胞的比例(凋亡指数)。
评估DNA碎片
为了测定DNA梯形,在1.2ml消化缓冲液中消化了四种催眠和三个正常的肺样品(100mg湿重)(0.1mg·ml-1蛋白酶K, 10 mM三盐酸,0.1 M NaCl, 25 mM乙二胺四乙酸(EDTA), 0.5%十二烷基硫酸钠,pH 8.0)。用酚-氯仿/异戊醇提取蛋白,用10 mM Tris-HCl、1 mM EDTA、pH 8.0透析,取1µg·mL-137℃下取rna ase A 1 h,重复透析。DNA(30µg)在含0.1µg·mL的1.4%琼脂糖凝胶上电泳-1溴化乙锭。由于加工和DNA纯化过程中的组织损失和/或剩余样本的起始材料不充分,只有7个样本进行了评估。
肺匀浆的免疫印迹
Intact and cleaved caspase-3 expression was determined in six emphysematous and five normal lung samples homogenised in protein extraction buffer (20 mM Tris-HCl, pH 7.4, 0.15 M NaCl, 0.02% NaN3.1毫米苯甲烷磺酰氟,2毫米N-ethylmaleimide 10µg·毫升-1Leupeptin,1μg·ml-1抑肽酶,10µg·毫升-1pepstatin A, 1mm EDTA)。采用人caspase-3抗体(克隆C31720;caspase-3(克隆67341A;poly (adp -核糖)聚合酶(PARP,克隆G734;Promega), caspase-3的底物。
统计分析
采用非配对t检验或单因素方差分析对形态测量的结果进行分析。采用线性回归和Pearson相关分析表皮面积与细胞凋亡和增殖指数之间的关系。Pearson相关(r)的值接近+1.0或-1.0,这取决于这些因素是直接相关还是负相关。线性回归值(R2)接近最优值+1.0,并表明数据与回归曲线的拟合程度。数据以平均值±表示sd.p值<0.05被认为显著。
结果
肺表面积,平均线性截距和体积分数
采用组织形态测量法对所有肺标本进行表面积测量,定量结果见表2⇓.如所预期的,从肺气肿患者的肺组织与正常的肺相比,表现出更低的显著表面积。从肺气肿患者的肺切片显示出增加的平均线性截距,减少的表面积,并与正常的肺切片的分数相比肺容积。
细胞凋亡形态学检测
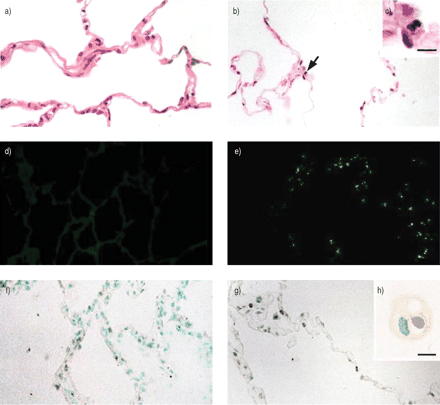
图1显示苏木精和伊红染色的正常和肺气肿肺组织切片⇓.分布于肺气肿肺组织的细胞表现出核轮廓的褶积(凋亡细胞的形态学特征)⇓).这些核改变不像典型的组织坏死那样集中在灶状区域。凋亡细胞包括内皮细胞、上皮细胞和成纤维细胞。肺泡间隙或肺泡间隔的中性粒细胞浸润可忽略不计。
人肺组织形态学检查和末端脱氧核苷酸转移酶介导的dUTP镍端标记(TUNEL)染色。正常(a)和肺气肿(b)肺切片苏木精和伊红染色。b)和c)中的箭头表示核固缩和旋回。d, e)异硫氰酸荧光素标记的正常和肺气肿肺组织的TUNEL反应。f, g)正常和肺气肿肺切片的生物素化TUNEL反应。h)鉴定细胞质中含有tunel阳性物质的巨噬细胞样细胞。标尺= 10µm。
细胞凋亡的生化表征
原位检测DNA切割的
图1d-h显示了正常和肺气肿肺切片的TUNEL反应⇑.在肺组织中进行了异硫氰酸荧光素(FITC) TUNEL的敏感性和特异性,以及生物素化TUNEL反应来分析凋亡细胞。使用fitc标记的核苷酸的TUNEL反应(图1d⇑e)在正常肺中很少或没有标记(0.17±0.18%),而在整个肺气肿组织中有更多标记强烈的细胞(2.6±1.1%;p = 0.0002)。采用生物素化核苷酸进行TUNEL检测(图1f)⇑TUNEL阳性(6.1±3.5%;p < 0.01)。用生物素方法获得较高的凋亡值可能是由于炎症细胞过氧化物酶活性引起的背景升高。在整个肺气肿标本中,肺泡和间充质细胞均显示TUNEL阳性。此外,还可以看到几个具有tunel阳性胞浆体的巨噬细胞样细胞,具有吞噬凋亡细胞的特征(图1h)⇑).对弥漫性间质性肺疾病患者的肺切片进行TUNEL检测与正常样本相似。没有TdT酶的检测没有反应性(数据未显示)。
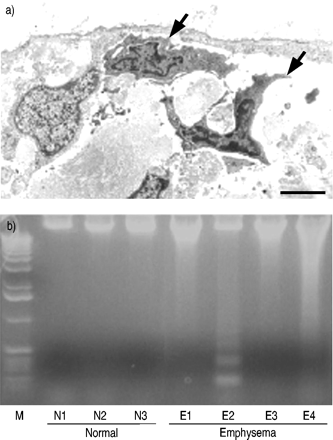
肺气肿肺超微结构分析证实了多种细胞类型的凋亡形态学改变。最显著的特征是细胞质缩合和空泡化,染色质缩合和结缔组织降解。电子显微镜(图2a⇓),肺气肿肺组织显示两个凋亡细胞与一个健康细胞紧密对应。这些细胞表现为胞浆和核浓缩,细胞形状不规则,具有凋亡特征。
人肺细胞凋亡的生化分析。A)电子显微照片显示肺气肿肺截面肺泡隔膜的超微结构。与正常细胞相邻的凋亡细胞(箭头)表示细胞质缩合和收缩,核染色质凝结。还观察到与细胞外基质接触的接触丧失。秤杆=2μm。b)从三个正常和四个蓄水肺中分离DNA,并通过琼脂糖凝胶电泳分析(30μg每巷DNA)。来自所有肺气肿样品的DNA显示出涂片,来自具有严重肺气肿的患者的样品E2,揭示了广泛的阶梯。泳道1显示1 kB DNA梯子。
然后使用DNA阶梯生化分析检测肺气肿样本中细胞凋亡的存在(图2b)⇑).可将由正常样品DNA的琼脂糖凝胶电泳显示完整的高分子量物质。与此相反,样品E2,从与最临床和以形态严重肺气肿,证明用的〜180个碱基对片段的最广泛的梯状图案的患者。样品E1,E3和E4来自患者不太严重的肺气肿比E2。这些样品没有表现出梯状,但仍然没有显示在凝胶上涂抹。
肺匀浆中活化的caspase-3和分裂的PARP的表达
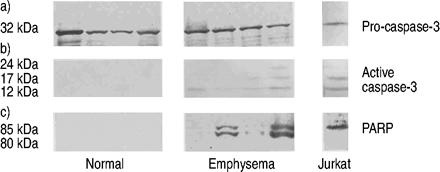
半胱天冬酶是一种导向的半胱氨酸蛋白酶,在执行细胞凋亡中具有枢轴作用,而不是坏死。因此,进行了正常和肺气肿组织的Caspase-3 Western印迹分析(图3⇓).在正常和气肿肺匀浆中检测到前caspase-3 (32 kDa),频率相似(图3a)⇓).这些发现被抗caspase-3的兔多克隆抗体证实(数据未显示)。然而,活化的caspase-3亚基(p17和p12)仅在肺气肿的肺匀浆中检测到(图3b)⇓).此外,特异性反应PARP的蛋白水解片段的抗体,活性CASPase-3的基材,在肺气肿致致型但不在正常肺部的反应性(图3C⇓).The additional band running at 80 kDa may represent further degradation of PARP.
人肺中Caspase-3活性和聚(adp -核糖)聚合酶(PARP)裂解。Western blot分析来自正常和肺气肿人肺的匀浆液(每通道120µg蛋白)。a)所有样本均可见前caspase-3表达(32kda)。最后一条线显示了抗fas抗体刺激的Jurkat细胞裂解物的反应性,作为阳性对照。b) caspase-3前型表达。用兔多克隆抗体检测肺气肿样本中含有24 kda中间形式的12和17 kda片段的表达。c) caspase-3的底物PARP的蛋白水解片段在肺气肿肺组织匀浆中表达,而在正常肺中不表达。80 kDa的附加带的存在可能代表PARP的进一步降解。
凋亡相关蛋白Bcl-2、Bad、Bax在人肺中的表达
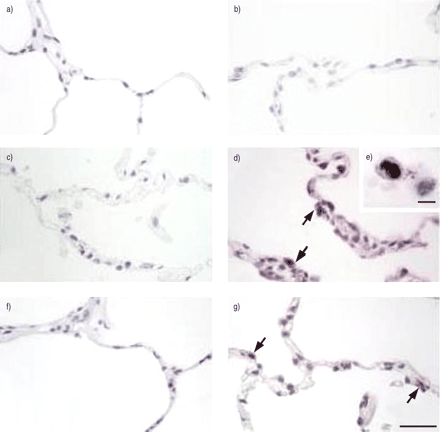
凋亡的开始和进展是通过Bcl-2家族的几种蛋白发生的,包括Bcl-2、Bad和Bax19.在正常和肺气肿肺组织中这些蛋白质的免疫组织化学染色在图4中示出了⇓.Bcl-2在正常和肺气肿肺组织中均未检测到(图4a)⇓此外,Bax和Bad在正常肺组织中未检测到表达(图4c)⇓然而,这两种蛋白在肺气肿的肺中均有表达(图4d)⇓和4 g⇓).在肺气肿样本中,Bax染色定位于肺泡上皮细胞(图4d)⇓,箭头),而在似乎是上皮细胞和间充质细胞的情况下分布了不良染色(图4G⇓,箭头)。有趣的是,几个巨噬细胞样细胞显示夹杂物Bax的阳性材料在它们的细胞质(图4G⇓).
人肺组织切片免疫组化Bcl-2、Bax、Bad染色。Bcl-2在正常(a)和肺气肿(b)肺组织中均未检测到。Bax和Bad蛋白在正常肺组织中未检测到表达(c, f),但在肺气肿肺样本中均存在(d, g)。在肺气肿样本中,Bax染色在肺泡上皮细胞中检测到(d,箭头),而Bad染色分布在上皮细胞和间充质细胞中(g,箭头)。此外,一些巨噬细胞胞浆中可见bax阳性物质(e)。标度条分别为20µm (e)和60µm (g)。
表面积,细胞凋亡和细胞增殖的个体值
使用散点图给出各个样品中表面积,细胞凋亡和增殖的值(图5⇓).肺气肿标本的表面积和细胞凋亡分布广泛,但与正常肺有显著差异。肺气肿样本显示平均肺表面积低于正常肺(图5a)⇓).所有肺气肿样本的细胞凋亡水平均高于正常样本(图5b)⇓).图5b数据⇓来自Fitc Tunel计数凋亡细胞。还使用免疫组织化学对PCNA进行检查的细胞增殖水平(图5C⇓).有趣的是,肺气肿肺细胞增殖水平高于正常肺(p<0.05)。
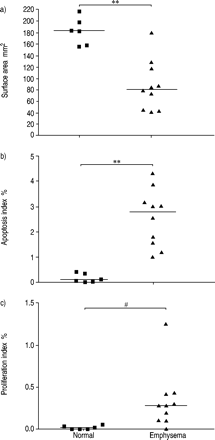
单个肺样本的散点图。直线代表中值。表面面积测量(a)和异硫氰酸荧光素末端脱氧核苷酸转移酶介导的dUTP镍末端标记(b)与正常样品有显著不同。c)肺气肿组的平均增殖率高于正常组。#: p = 0.049;* *: p < 0.01。
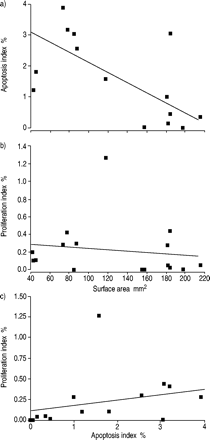
组织形态测定与细胞凋亡、增殖指数的相关性及线性回归分析
细胞形态学和组织形态学研究的结果表明,细胞丢失和肺结构之间存在潜在的联系。因此,肺表面积与细胞凋亡(FITC TUNEL)之间的关系,由单个样本的TUNEL染色确定(图6a)⇓),是策划。随着肺表面积的减少,细胞凋亡水平升高(r =−0.75;p = 0.001)。接下来,比较细胞增殖水平相对于表面面积。虽然细胞增殖(PCNA染色)明显高于肺气肿肺,但细胞增殖与表面积之间没有显著相关性(图6b)⇓).此外,检测到细胞凋亡和增殖之间没有统计相关性,尽管回归线的正斜率表明更高的增殖率可以在样品与细胞凋亡(图的更高的速率来发生。图6c⇓).这些数据表明,细胞丢失(凋亡)和细胞替换(增殖)的动力学可能是肺气肿发病机制的一个关键特征。
细胞表面面积、凋亡(异硫氰酸荧光素末端脱氧核苷酸转移酶介导的dUTP镍端标记)与细胞增殖的关系显示了个别病人的价值。a)通过线性回归观察到比表面积与凋亡指数呈负相关(p = 0.001)。表面面积与增殖(b)或凋亡与增殖(c)之间没有显著相关性,尽管肺气肿样本中这两种细胞指标均较高。然而,回归线的正斜率提示细胞凋亡和增殖同时增加。
讨论
目前的研究表明,在肺气肿患者的肺组织中,细胞凋亡导致广泛的细胞死亡,并伴有结缔组织降解。通过细胞形态学、DNA片段化和凋亡相关蛋白表达等多种方法证实了细胞凋亡。这些结果证实并扩展了其他人的观察结果10-12.此外,这些数据提供了细胞凋亡与肺气肿过程的形态测量的相关性。
本研究中显示细胞凋亡的每一种方法都提供了细胞凋亡在肺气肿发病机制中的潜在作用。形态学分析可见凋亡细胞散在,无组织炎症。超微结构分析证实凋亡细胞胞浆和核浓缩。这些特征将细胞凋亡与组织坏死区分开来20..后者坏死细胞表现为细胞肿胀和质膜破裂,而细胞核相对完整。此外,在组织坏死中,还存在相关的炎症反应。本研究中肺气肿组织细胞形态特征与细胞凋亡一致。
通过DNA断裂证实细胞凋亡原位末端标记和凝胶电泳。然而,没有特定的细胞类型主要受到影响。这些结果与Kasahara及其同事的观察结果相似10那11,肺泡间隔和内皮细胞均出现凋亡。在弥漫性肺间质疾病患者中TUNEL无反应,提示细胞凋亡对肺气肿的相对特异性。这些结果也与Kasahara及其同事的观察结果一致10那11在原发性肺动脉高压患者的肺中未发现凋亡。肺泡巨噬细胞中tunel阳性物质的发现表明,巨噬细胞作为凋亡细胞的清扫者,在其他细胞系统中也显示了这一作用21.目前的作者扩展了之前的发现,证明了在肺气肿肺组织中凋亡和caspase激活的生化证据。caspase活化序列是凋亡通路中不可缺少的过程22.Caspase-3作用于细胞凋亡损伤的下游,在蛋白水解的靶向分子中起关键作用23.PARP蛋白水解为85-kDa片段,如本研究中肺气肿样本所示,是由caspase-3介导的特定事件24.
目前研究的一个重要发现是在肺气肿样品中凋亡和细胞增殖的升高(图5B⇑分别和c)。有趣的是,相关分析显示,细胞表面积与细胞凋亡呈显著的负相关关系(图6a)⇑),细胞表面积与细胞增殖无相关性(图6b)⇑).这些数据在一起表明,尽管在肺气肿中增加了细胞参数,但细胞凋亡和增殖可能与肺表面积不具有相同的关系。这种机制可以解释疾病进程的加速,破坏性,超过传统的弗莱彻曲线预测的速率,即使在患者戒烟后,也是如此8.那9..有趣的是,细胞增殖的增加可以解释为什么细胞凋亡率的升高并不会导致实质的完全丧失。
最近,Yokohori.等.12并分析了肺气肿肺细胞凋亡和细胞增殖情况。他们检测到的PCNA染色水平(肺气肿肺的中位数为~ 2.5%,正常肺的中位数为0.1%)和生物素TUNEL染色水平(肺气肿肺的中位数为0.9%,正常肺的中位数为0.1%)比目前的作者高得多。这两位作者的研究结果与横堀洋的不同的原因是什么等.12可以在样本人口中休息。首先,目前研究中样本人口的平均年龄是年轻的,肺气肿样的样本来自吸烟历史较短的患者,平均40.9包-YRS与yokohori研究中的样本的平均水平为95包。等.12.在目前的研究样本是从谁曾到肺组织收集戒烟≥6个月前肺气肿患者采集。另外,虽然没有报告空域的形态作出评估,有可能是由Yokohori研究样本等.12有比目前研究中更严重的肺气肿。最重要的是Yokohori研究中的正常样本等.12来自肺癌患者,这可能具有比在当前研究中的对照组中的正常肺样品更高的增殖能力。
Bax在肺气肿中的表达,而不是在正常肺中的表达,提供了细胞凋亡的联系。Bax蛋白是促凋亡分子,当细胞与ECM粘附耗尽而死亡时,其表达增加25.Bax蛋白抵消Bcl-2蛋白的保护作用,激活caspase22.目前的研究数据显示,在肺气肿肺样本中,Bcl-2无表达,Bax升高,反应不良。胞浆内可见含有bax阳性颗粒的巨噬细胞样细胞。这是一项有趣的发现,在一种涉及蛋白酶水平增加的疾病中,可能会破坏基质来修改细胞粘附和信号传递。
目前的研究扩展了细胞凋亡在肺气肿中发生的观察,但没有完全阐明细胞凋亡的机制。从直观上看,细胞凋亡可能与细胞外基质的破坏有关。重要的是,细胞凋亡的观察并不能否定蛋白酶在肺气肿发病中的作用。事实上,它可能代表了一个连续的破坏性过程,在这个过程中,基质附着的缺失导致细胞Bax和caspase-3活性增加,驱动肺泡细胞的凋亡。增加的蛋白酶负荷可能导致局部基质的损失。因此,可以想象,发生在肺气肿中的细胞死亡可能是由于基质粘连丧失而导致的程序性细胞死亡26.当然,肺气肿的增加的蛋白酶负担可能会丧失基质,细胞表面受体,细胞分离和随后损失细胞存活所需的信号传导。此外,其他机制,例如激活细胞表面死亡受体或Fas配体的参与27,可能在肺气肿肺细胞的损失的作用。可替换地,信号诱导细胞凋亡和肺气肿,提示内皮生长因子的抑制VEGF受体的阻断在疾病的发病机制中的作用10那11.
无论最初的细胞损伤如何,目前的研究表明,细胞凋亡发生在肺气肿肺中,伴随疾病进展。这是一种机制,可以解释在疾病进展期间肺的破坏。大量研究表明,细胞凋亡在各种人类慢性疾病中发挥着重要作用,包括神经退行性疾病、心力衰竭、动脉粥样硬化和病毒性疾病28.在这些疾病中,抗凋亡药物有望治疗患者或减缓疾病进展。其中许多药物正在评估中,有可能用于破坏肺气肿的进行性组织损失特征。
要在当前作者的知识,没有以前的报告中已经研究细胞力学和肺泡结构的损失之间的关系,这里的报道。作为形态肺表面积在细胞死亡的增加落入表明细胞的有助于降低肺泡隔的完整性的损失,导致增加的肺顺应性和弹性降低。这一假说是由在小鼠肺蛋白酶交货肺气肿诱导研究支持14.然而,考虑到逆转序列中的事件,可以想到沿着肺泡壁的基质损失诱导细胞死亡而没有细胞增殖的补偿增加。尽管如此,仍有许多工作仍有待进行,以确定肺气肿进展过程中涉及凋亡的机制。
致谢
作者感谢M. Selman(墨西哥国家呼吸研究所,墨西哥DF)慷慨赠送了间质性肺病患者的组织切片。
- 收到了2004年2月24日。
- 公认2004年10月15日。
- ©ers Journals Ltd