摘要gydF4y2Ba
据报道,活性氮(RNS)参与慢性阻塞性肺疾病(COPD)的炎症过程。然而,目前尚无RNS在COPD中的调节研究。据推测,抑制黄嘌呤氧化酶(XO)可能通过抑制超氧阴离子的产生来减少COPD气道中RNS的产生。gydF4y2Ba
10名COPD患者和6名健康受试者参与了这项研究。XO抑制剂别嘌呤醇(300 mg·天)gydF4y2Ba−1gydF4y2Ba订单。gydF4y2Ba4周)给COPD患者服用。通过诱导痰中3‐硝基酪氨酸免疫反应性和XO酶活性以及呼出一氧化氮(eNO)浓度评估气道中RNS的产生。gydF4y2Ba
与健康受试者相比,COPD患者气道中的XO活性显著升高。给别嘌呤醇可显著降低XO活性和硝基酪氨酸的形成。相反,别嘌呤醇组eNO浓度显著升高。gydF4y2Ba
这些结果表明,口服黄嘌呤氧化酶抑制剂别嘌呤醇可减少慢性阻塞性肺疾病患者气道活性氮的产生。这种干预可能对未来慢性阻塞性肺疾病的管理有用。gydF4y2Ba
本研究由日本东京文部科学省科学研究基金12470132和14657143资助。gydF4y2Ba
慢性阻塞性肺病(COPD)是一个重大的医学问题,有证据表明,它在世界各地都在增加gydF4y2Ba1gydF4y2Ba- - - - - -gydF4y2Ba3.gydF4y2Ba。尽管COPD的确切炎症机制尚不清楚,但据报道,炎症过程在疾病的持续发展中发挥着重要作用gydF4y2Ba4gydF4y2Ba。gydF4y2Ba
吸烟是慢性阻塞性肺病中观察到的炎症的主要诱因,尽管戒烟者显示出与当前吸烟者相似的气道炎症gydF4y2Ba5gydF4y2Ba。因此,内源性机制似乎参与了COPD炎症过程的发病机制。氧化应激可能是慢性阻塞性肺病炎症过程放大和延续的机制之一gydF4y2Ba4gydF4y2Ba。在呼吸道的炎症/免疫过程中,一氧化氮(NO)的高水平产生被认为是一种宿主防御机制,尽管它也可能导致呼吸道损伤,并有助于COPD的病理生理学gydF4y2Ba9gydF4y2Ba。一氧化氮的不良作用被认为部分是由其与超氧阴离子反应产生的,超氧阴离子从浸润的炎症细胞(如巨噬细胞和中性粒细胞)中释放出来,产生强活性氮(RNS),如过氧亚硝酸盐,导致蛋白质中酪氨酸残基的硝化gydF4y2Ba10gydF4y2Ba- - - - - -gydF4y2Ba12gydF4y2Ba。最近,RNS产量增加,评估gydF4y2Ba通过gydF4y2Ba据报道,诱导痰中对3‐硝基酪氨酸免疫反应的细胞数量增加gydF4y2Ba13gydF4y2Ba。这一测量值与COPD严重程度之间存在相关性,表明RNS可能在COPD炎症机制中起重要作用。gydF4y2Ba
在本报告中,对COPD受试者进行了别嘌呤醇,一种黄嘌呤氧化酶(XO)的抑制剂,一种负责超氧阴离子产生的酶,并评估了硝基酪氨酸形成的变化。gydF4y2Ba
方法gydF4y2Ba
主题gydF4y2Ba
10名COPD患者(9名男性)在知情同意后参加了研究。该研究得到了当地伦理委员会的批准,受试者年龄为52-76岁。他们的平均±sem用力呼气量在一秒钟(FEVgydF4y2Ba1gydF4y2Ba)为预测值的1.40±0.2 L(46.3±4.9%)。所有患者均符合美国胸科学会copd标准,且在研究前已停止吸烟≥1年。所有患者病情稳定,且未接受类固醇治疗≥6个月。所有支气管扩张剂治疗均在测量前≥24小时停止。gydF4y2Ba
研究协议gydF4y2Ba
在XO抑制剂(别嘌呤醇,300 mg·d)前和期间测定诱导痰中硝基酪氨酸免疫反应性、XO活性和细胞计数差异gydF4y2Ba−1gydF4y2Ba三剂gydF4y2Ba订单。gydF4y2Ba4周)给药。呼出NO (eNO)水平和FEVgydF4y2Ba1gydF4y2Ba同时还使用化学发光分析仪(280NOA;Sievers, Boulder, CO, USA)和干滚动密封肺活量计(OST 80A;Chest Co.,东京,日本)。停用别嘌呤醇4周后,重复上述步骤。gydF4y2Ba
测量一氧化氮浓度gydF4y2Ba
eNO的测量方法如前所述gydF4y2Ba14gydF4y2Ba。受试者以2.5 L·min的恒定流量从总肺活量呼出gydF4y2Ba−1gydF4y2Ba。口腔压力维持在1.96 kgydF4y2BaPgydF4y2Baa封闭膜,从而排除鼻源NO污染。在250 mL·min的样品流量下吸收呼出的空气gydF4y2Ba−1gydF4y2Ba通过gydF4y2Ba靠近口的侧口。至少连续两次记录,间隔时间为2分钟,两次可重复读数的峰值平均值用于结果分析。在进行肺活量测定前测量eNO。gydF4y2Ba
痰诱导及检查gydF4y2Ba
非诺特罗(400µg,吸入)预处理15分钟后,使用超声喷雾器吸入高渗盐水(4%)(MU‐32;日本大阪夏普株式会社;平均质量中值气动直径和输出分别为5.4 μ m和2.2 mL·mingydF4y2Ba−1gydF4y2Ba分别)。通过目视和倒置显微镜检查去除含有唾液的样品(鳞状上皮细胞)gydF4y2Ba15gydF4y2Ba。继续高渗盐水吸入15-30分钟,直到痰量为~ 1ml。gydF4y2Ba
痰样本立即用Sputasol (Oxoid Ltd, Basingstoke, UK)处理,体积是原始样本的四倍,以解离粘液的二硫化物键。混合物在旋涡混合器上搅拌15秒,并在巴斯德移液管中轻轻吸气以确保混合。样品摇15分钟,磷酸盐缓冲生理盐水(PBS;pH 7.4),以终止sputasol的效果。样品790×离心10分钟后gydF4y2BaggydF4y2Ba时,用50mm PBS (PBS体积为原痰体积的一半)重悬细胞球,用血细胞计测定白细胞总数。台盼蓝排除法测定细胞活力。计算总细胞密度和绝对细胞密度(每毫升处理过的痰)。细胞悬液(100µL)调整为1.0×10gydF4y2Ba6gydF4y2Ba细胞·毫升gydF4y2Ba−1gydF4y2Ba置于山东III型细胞离心机(山东南方仪器公司,Sewickley, PA, USA)的杯中,每个样品有四种制剂gydF4y2Ba15gydF4y2Ba。使用Hansel染色(Torii Pharmaceutical, Tokyo, Japan)对样品进行染色,以评估细胞差异计数gydF4y2Ba17gydF4y2Ba并保存在- 80°C,直到免疫细胞化学分析。gydF4y2Ba
ImmunocytostaininggydF4y2Ba
使用针对3‐硝基酪氨酸的抗血清对样本进行免疫染色。简单地说,每个样品在4%多聚甲醛固定液中固定30分钟。在3%双氧水和100%甲醇中室温孵育5 min可降低内源性过氧化物酶活性。PBS洗涤后,用一抗(多克隆兔抗硝酸酪氨酸免疫球蛋白(Ig)G, 1:100稀释;北部生物技术,普莱西德湖,纽约,美国)gydF4y2Ba13gydF4y2Ba在4°C下放置12小时。为了减少抗体的非特异性离子结合,将制剂与4%的脱脂牛奶在含0.3% Triton X (Sigma, St Louis, MO USA)的PBS中预孵育30分钟,然后与10%的灭活正常山羊血清在室温下孵育30分钟。当该抗体与过量的硝基酪氨酸孵育时,免疫反应性被阻断,表明该抗体对硝基酪氨酸具有较高的特异性。使用间接免疫过氧化物酶法和EnVision聚合物试剂(DAKO Japan Ltd,京都,日本),山羊抗兔IgG与过氧化物酶标记的右旋糖酐偶联,在室温下1小时观察免疫反应性。然后进行二氨基联苯胺反应,其中组织在200 mL PBS、10 mg二氨基联苯胺、72.5 mg叠氮化钠和112µL H的溶液中孵育gydF4y2Ba2gydF4y2BaOgydF4y2Ba2gydF4y2Ba(30%)。然后用Hansel染色液进行复染。两名合格的细胞病理学家对样本的来源不知情,对每个样本中的500个细胞进行了区分和免疫反应性细胞计数。两项得分的平均值被用于分析。gydF4y2Ba
黄嘌呤氧化酶活性测定gydF4y2Ba
用赤池法测定XO活性gydF4y2Ba等等。gydF4y2Ba19gydF4y2Ba。简单地说,如上所述制备处理后的痰标本上清液。紧接着,抑制剂鸡尾酒(冰冷的50mm磷酸钾缓冲液,含2mm乙二胺四乙酸(EDTA), 2mmgydF4y2BapgydF4y2Ba‐氨基苯甲磺酰氟,10 mM二硫苏糖醇,0.5µg·mLgydF4y2Ba−1gydF4y2Ba添加Leupeptin)。然后以790×离心10 mingydF4y2BaggydF4y2Ba上清液10万×再离心1 hgydF4y2BaggydF4y2Baat4°C。上清液通过0.45‐m Millipore过滤器(Millipore, Billerica, MA, USA)过滤。为了去除低分子量化合物(gydF4y2Ba如。gydF4y2Ba黄嘌呤和次黄嘌呤),然后用10 L PBS在4℃的纤维素管(无缝纤维素管尺寸8/32;三口纯化学工业,东京,日本)前测定XO活性。所有样品均在荧光光谱仪(650-40型;日立有限公司,东京,日本),激发波长为345纳米,发射波长为390纳米。检测混合物的体积为1.0 mL PBS,含有9µM蝶呤和50µL样品溶液。反应在37°C下进行1小时。为了测定XO活性,上述反应在9 μ M亚甲基蓝存在下进行。为确认活性的特异性,在样品中加入20µM别嘌呤醇。活性通过异黄蝶呤的形成来确定,并表示为每毫升每小时形成的异黄蝶呤的纳米摩尔。gydF4y2Ba
统计分析gydF4y2Ba
适当时,数据以平均值±sem或中位数(范围)表示。中位数数据的比较采用Wilcoxon符号秩检验,平均数据的比较采用非配对t检验。p<0.05为显著性变化。gydF4y2Ba
结果gydF4y2Ba
如表1所示gydF4y2Ba⇓gydF4y2Ba,别嘌呤醇对诱导痰中细胞总数无显著影响。然而,别嘌呤醇显著降低了硝基酪氨酸免疫阳性总细胞(p<0.01)、中性粒细胞(p<0.01)和巨噬细胞(p<0.05)的数量(表2)gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
基线时,中位气道XO活性为150.0 (58.3-515.0)nmol·mLgydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba异黄蝶呤,显著高于年龄匹配的健康受试者(45.4 (20.8-71.9)nmol·mL)gydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Baisoxanthopterin;N =6, p<0.01)(数据未显示)。别嘌呤醇给药后COPD受试者的活性显著降低至中位数89.7 (29.0-227.0)nmol·mLgydF4y2Ba−1gydF4y2Ba·hgydF4y2Ba−1gydF4y2Ba异黄蝶呤(p<0.01)(图1agydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
在别嘌呤醇给药期间,硝酸酪氨酸免疫阳性细胞计数也从中位数35.1%(20.8-70.9)显著降低到中位数15.6% (8.2-47.8)(p<0.01)(图1bgydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
相比之下,别嘌呤醇给药后eNO水平从中位数11.2 ppb(5.0-26.2)显著升高至中位数16.8 ppb (10.8-36.0) (p<0.01)(图1cgydF4y2Ba⇓gydF4y2Ba).别嘌呤醇引起的XO活性变化,硝基酪氨酸免疫阳性细胞计数和eNO浓度在停药4周后恢复到基线值(图1)gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
别嘌呤醇治疗未引起FEV变化gydF4y2Ba1gydF4y2Ba。FEVgydF4y2Ba1gydF4y2Ba别嘌呤醇给药前、后、停药后分别为1.42±0.16、1.50±0.19、1.44±0.17 L。gydF4y2Ba
讨论gydF4y2Ba
本报告显示,XO抑制剂别嘌呤醇可抑制气道中3‐硝基酪氨酸、过氧亚硝酸盐足迹和其他RNS的产生,并抑制COPD受试者XO活性的增加。gydF4y2Ba
硝基酪氨酸的生成依赖于NO的氧化gydF4y2Ba20.gydF4y2Ba。NO与超氧阴离子反应生成强氧化剂过氧亚硝酸盐,这被认为是过量NO产生不良影响的主要原因gydF4y2Ba21gydF4y2Ba。最近,据报道,通过诱导痰3‐硝基酪氨酸免疫染色评估的RNS产量在COPD受试者中显著升高gydF4y2Ba13gydF4y2Ba。此外,COPD患者气道梗阻性改变程度与硝基酪氨酸形成量之间存在显著相关性。gydF4y2Ba
过亚硝酸盐将硝酸盐添加到靠近酪氨酸羟基的位置3,生成稳定的产品3‐硝基酪氨酸gydF4y2Ba22gydF4y2Ba,具有高度的促炎作用gydF4y2Ba通过gydF4y2Ba氧化应激和脂质过氧化gydF4y2Ba10gydF4y2Ba。过氧亚硝酸盐还激活中性粒细胞和巨噬细胞释放的基质金属蛋白酶,这些蛋白酶能够降解肺实质细胞外基质的所有成分gydF4y2Ba24gydF4y2Ba并可能引起肺气肿变化。因此,调节过氧亚硝酸盐的形成应该有助于抑制COPD中观察到的炎症和破坏性过程。gydF4y2Ba
由于XO能够产生超氧阴离子,本研究中观察到的别嘌呤醇诱导的硝基酪氨酸还原似乎是由于抑制过氧亚硝酸盐的形成gydF4y2Ba通过gydF4y2Ba抑制超氧化物的产生。在本研究中,COPD患者诱导痰中XO的基线活性比健康受试者高4倍。用支气管肺泡灌洗液分析气道XO活性已被报道gydF4y2Ba通过gydF4y2Ba一种脱氧核糖核酸展开法gydF4y2Ba7gydF4y2Ba以及电子顺磁共振和高效液相色谱gydF4y2Ba25gydF4y2Ba。在这些报告中,与健康受试者相比,COPD患者的XO活性升高。这些先前的报告与本研究是一致的。gydF4y2Ba
在最近的一项研究中,在支气管哮喘和COPD受试者中观察到几乎相同数量的气道炎症细胞诱导NO合酶免疫反应gydF4y2Ba13gydF4y2Ba。然而,支气管哮喘的eNO浓度明显高于COPD。因此,我们假设COPD气道中产生的NO通过与超氧阴离子反应而被消耗gydF4y2Ba13gydF4y2Ba。在本研究中,XO抑制剂在COPD受试者中显著增加了eNO浓度,同时减少了3‐硝基酪氨酸的形成,支持了这一假设。gydF4y2Ba
硝基酪氨酸形成的另一途径gydF4y2Ba通过gydF4y2BaNO涉及依赖髓过氧化物酶(MPO)或相关过氧化物酶的机制gydF4y2Ba20.gydF4y2Ba。NO与氧反应生成亚硝酸盐。亚硝酸盐被MPO或其他相关过氧化物酶氧化,形成硝基氯和二氧化氮。这些活性氮中间体也参与酪氨酸的硝化。由于中性粒细胞来源的MPO在COPD气道中大量存在gydF4y2Ba27gydF4y2Ba,硝基酪氨酸形成gydF4y2Ba通过gydF4y2Ba这些途径也可能在COPD中硝基酪氨酸的形成中发挥重要作用。由于XO抑制对这些途径没有影响,在本研究中硝基酪氨酸的产生可能已被不完全抑制。gydF4y2Ba
在本研究中,别嘌呤醇对诱导痰中炎症细胞数量无显著影响。这一证据表明,内源性超氧化物不参与COPD气道炎症细胞的粘附和化学吸引机制。再一次,别嘌呤醇治疗对FEV评估的气道口径没有显著影响gydF4y2Ba1gydF4y2Ba。这表明内源性产生的超氧化物不表现出急性支气管收缩作用。然而,如前所述,超氧化物可能参与COPD气道的炎症过程gydF4y2Ba通过gydF4y2Ba与NO反应。慢性阻塞性肺病患者气道和实质的持续炎症可导致进行性气道梗阻性改变gydF4y2Ba2gydF4y2Ba。因此,有可能抑制超氧化物的产生gydF4y2Ba通过gydF4y2Ba内源性XO抑制可减缓COPD患者气道梗阻的进展。gydF4y2Ba
总之,研究表明,黄嘌呤氧化酶抑制剂别嘌呤醇可抑制黄嘌呤氧化酶活性,减少慢性阻塞性肺病患者气道中活性氮的形成。尽管有报道称别嘌呤醇可抑制慢性阻塞性肺疾病患者运动诱导的氧化应激,可能作用于骨骼肌水平gydF4y2Ba28gydF4y2Ba,本报告首次描述了别嘌呤醇对气道活性氮产生的抑制活性。目前,没有药物治疗能够抑制慢性阻塞性肺疾病气道的炎症过程。活性氮引起气道炎症gydF4y2Ba通过gydF4y2Ba氧化应激和脂质过氧化,以及通过激活蛋白水解酶gydF4y2Ba29gydF4y2Ba。内源性黄嘌呤氧化酶抑制减少活性氮的形成可能有助于减少慢性阻塞性肺疾病的炎症和破坏性过程。需要进一步的长期研究来证实这一假设。gydF4y2Ba
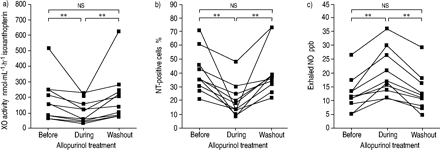
别嘌呤醇治疗对a)黄嘌呤氧化酶(XO)活性的影响;b)诱导痰中3‐硝基酪氨酸(NT)‐免疫阳性细胞计数;c)呼气一氧化氮(eNO)在给药前、给药期间和给药后(洗脱期)水平的影响。Ppb:十亿分之一;ns:无意义的。* *: p < 0.01。gydF4y2Ba
别嘌呤醇给药前、中、后诱导痰细胞计数差异gydF4y2Ba
别嘌呤醇给药前、中、后诱导痰中3‐硝基酪氨酸免疫阳性细胞计数gydF4y2Ba
致谢gydF4y2Ba
作者感谢B. Bell阅读了手稿。gydF4y2Ba
脚注gydF4y2Ba
↵gydF4y2Ba编辑评论见401页。gydF4y2Ba
- 收到了gydF4y2Ba2002年6月19日gydF4y2Ba
- 接受gydF4y2Ba2003年4月13日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba














