文摘
本研究调查了炎症反应主要培养人类支气管上皮细胞在慢性阻塞性肺疾病(COPD)和临床因素调节。
上皮细胞从14 COPD患者支气管镜活检(±sd)(平均年龄74.6±5.7岁,在一秒用力呼气量(FEV1)1.21±0.36 L, FEV1%预计51.1±15.8%,51.5±24.0 pack-yrs吸烟,吸入类固醇剂量1237.5±671.0µg·天−1医学研究理事会(MRC)呼吸困难评分3.18±1.33)和八个电流/ exsmokers与正常肺功能(年龄为60.4±13.5岁,FEV12.66±1.27 L, FEV1% pred 89.6±17.7%, 49±44 pack-yrs吸烟,MRC呼吸困难评分1±0)主要生长在文化和暴露于50 ng·毫升−1肿瘤坏死因子α。
慢性阻塞性肺病刺激细胞产生更多的白介素(IL) 6在24和48 h,和IL 8在6 - 24小时如果COPD细胞。这种反应在细胞从当前/ exsmokers未见。IL 6和IL 8应承担的产量降低COPD患者吸入类固醇。
炎症刺激后,支气管上皮细胞在慢性阻塞性肺疾病表现出显著的细胞因子反应未见的吸烟者与正常肺功能,这可能是被吸入类固醇治疗。
本研究联合研究委员会的支持下,圣巴塞洛缪医院,伦敦,英国。
慢性阻塞性肺疾病(COPD)患者表现出气道炎症加剧,特点是水平的提高白介素8 (IL)检测和肿瘤坏死因子(TNF)α诱导痰1,主要是嗜中性细胞渗透气道腔2淋巴细胞数量增加,黏膜下层和肺泡薄壁组织3。他们容易发作,住院的主要原因4和健康相关的生活质量的一个重要因素5。已经证明了稳定的频繁发作史的患者增加了诱导痰的地理IL 6和IL 8水平,而痰地理IL 6水平进一步提高COPD恶化6。这表明,慢性阻塞性肺病可能与增强气道上皮细胞的激活有关,特别是在恶化,但机制在很大程度上是未知的。
有越来越多的证据表明,以及作为一个重要的物理化学屏障保护黏膜下层,气道上皮细胞是一个新陈代谢活跃的中介在呼吸道疾病的病理生理学7。支气管上皮细胞合成和释放大量炎性因子结构上和应对外界刺激9,从而影响炎症细胞的趋化作用、招聘、激活和分化10。然而,支气管上皮的作用在慢性阻塞性肺病调节炎症过程中,在稳定条件下或在恶化,尚未确定。
本研究旨在评估响应由primary-cultured人类支气管上皮细胞(HBEC) COPD患者炎症刺激。肿瘤坏死因子α是应承担的促炎细胞因子在COPD气道11上皮细胞,刺激细胞因子释放12。刺激与肿瘤坏死因子α应承担因此用作模型可能发生什么,在某种程度上,在上皮水平在慢性阻塞性肺病急性加重。此外,因素调节上皮炎症反应在慢性阻塞性肺病检查,包括生理参数和吸入类固醇治疗。
材料和方法
研究对象
志愿者(n = 22)是前瞻性研究招募的患者接受常规临床显示支气管镜检查在伦敦胸腔医院,英国。十四COPD患者与正常肺功能和八个现任或exsmokers取样。慢性阻塞性肺病被定义为在一秒用力呼气量(FEV1)< 70%,年龄和身高预测β2受体激动剂在预测FEV可逆性1< 15%或200毫升的气流阻塞FEV就是明证1/用力肺活量(FVC)的比例< 70%。患者被排除在研究如果他们活跃的呼吸道感染,包括正在进行的或最近的急性加重的慢性阻塞性肺病,疑似肺结核、支气管扩张或哮喘。在手术之前,一份详细的历史从每项研究课题概述了他们的吸烟习惯(吸烟现状,多年的吸烟和包的数量每天吸烟20),药物历史包括吸入类固醇剂量,每天稳定的呼吸道症状和医学研究理事会呼吸困难评分。基线肺量测定法,在可能的情况下,arterialised毛细管耳垂血气体13也得到了前计划过程。
表1⇓显示了研究对象的生理特点。慢性阻塞性肺病患者比正常人(p < 0.05)。两组匹配的pack-yrs吸烟(p = 0.15),然而,8(51.7%)的COPD患者和6(75%)的正常受试者吸烟者。在慢性阻塞性肺病组,8例(51.7%)患者接受常规吸入类固醇在平均数±标准差1237±671µg·天−1。在当前/ exsmokers与正常肺功能,两个(25%)患者的最终诊断支气管癌,另一个(12.5%)被发现间皮瘤。所有的COPD患者支气管癌,所有受试者服用任何药物(除了吸入类固醇)可能影响他们的气道炎症反应。
每个志愿者接受fibreoptic支气管镜检查光镇静和局部麻醉下胸根据英国社会准则14。采用可旋转cup-biopsy支气管活检钳(奥林巴斯FB-19KR;Southend-on-Sea KeyMed有限公司,英国)的节段性或subsegmental船底座在对面任何放射性异常诱发支气管镜检查。活检是立即放置在冰冷的媒介199 (Sigma-Aldrich有限公司,普尔,英国)含1%庆大霉素(英国Roussel实验室有限公司中的)和组织培养在30分钟处理。
伦敦东部的伦理委员会和市卫生行政部门授予批准这项研究和全面的书面同意之前就从所有参与者获得他们的包容。
材料
所有试剂和化学物质的组织文化品位和Sigma-Aldrich有限公司提供的,除非另有说明。准备的解决方案都是透过0.20µm孔隙Minisart注射器过滤器(缝匠肌有限公司、埃、英国)在细胞培养。
支气管上皮细胞的文化
HBEC是使用外植体生长在初代培养细胞培养技术在实验室开发的。上皮是解剖远离任何潜在的固有层,切成更小的部分∼0.5毫米3在大小和无菌培养基199洗了三次。单一的上皮细胞被移植到6厘米应承担的猎鹰Primeria塑料培养皿中(正有限公司、牛津大学、英国)和1.5毫升的孵化完成培养基在37°C调湿大气空气二氧化碳的5%。培养基是由混合250µg牛胰腺胰岛素,250µg人类转铁蛋白,1.5毫升的抗生素/抗真菌的解决方案,3毫克l谷氨酰胺和2.5毫升NU-serum(通用生物制品有限公司,格洛斯特郡,英国)在199年100毫升的媒介。每道菜的媒介是维护媒介取代后7天,之后每48 h。
接触人类支气管上皮细胞肿瘤坏死因子α
文化已经观察到细胞融合后3 - 4周。实验前的那天,外植体被移除和文化都洗了,一夜之间在199年中孵化和抗生素/ 24小时的抗真菌的解决方案。HBEC文化然后洗两次与199毫升无菌培养基添加适当的试剂。肿瘤坏死因子α应承担的高暴露菜肴在这个由2.5毫升的ng·50毫升−1解决重组肿瘤坏死因子α应承担(欧洲研发系统,阿宾顿、英国)199年媒介和抗生素/抗真菌的解决方案。这个浓度的肿瘤坏死因子α应承担从生理决定不测量,但使用初步接触在实验室实验显示在ng·25毫升不够刺激−1但细胞死亡和细胞减少产品在100 ng·毫升−115。如果菜是孵化199 2.5毫升的介质和抗生素/抗真菌的解决方案。整除的上层清液收集后立即从文化菜的肿瘤坏死因子α应承担或控制解决方案(时间为零)。细胞培养,收集和整除的上层清液,24和48 h。所有样品都是储存在−70°C细胞因子分析使用定量夹心免疫测定技术(研发系统欧洲)。地理IL 6、IL 8和可溶性细胞间粘附分子(描述)量1水平测定细胞上清液。实验终止在48小时,在这段时间里,细胞被储存在−70°C细胞总蛋白分析被洛瑞et al。16。
分析
细胞因子释放HBEC绝对值的测量pg·µg细胞蛋白质−1在每个时间点。允许不同的基线细胞因子生产、细胞因子生产的百分比变化从时间0 0 - 6倍计算,每个实验组0-24和0-48 h。正态分布数据总结和平均数±标准差的倾斜的数据中位数(四分位范围(差))。连续变量与正态分布相比,一个未配对t检验,而那些非正态分布比较,Mann-Whitney U的测试或Wilcoxon符号秩检验,是合适的。细胞因子的水平,和生理等指标相关使用斯皮尔曼等级相关。
结果
文化和人类支气管上皮细胞的识别
上皮细胞的身份被确认在所有文化中通过光学显微镜,展示大量的细胞多边形形态。在随机选择的文化中,电子显微镜和采用免疫染色的细胞角蛋白进行使用单克隆抗体制备凸轮5.2(有限公司)正确认的上皮细胞。只有文化展示≥50%纤毛细胞,纤毛运动好,被用于实验,没有定性的差异程度之间cilliation或分化被认为在这个研究慢性阻塞性肺病细胞与正常肺功能与主题。与特定的单克隆抗体染色污染细胞类型,如成纤维细胞,没有任何证据表明这些细胞。
细胞因子的生产由人类支气管上皮细胞在缺乏肿瘤坏死因子α应承担的刺激
描述1生产应承担的慢性阻塞性肺病HBEC基线条件下较低的吸入类固醇治疗(ρ=−0.732,p = 0.039描述量1在24 h)。没有基线细胞因子之间的关系被认为在正常HBECs生产和任何上述生理或临床参数。
细胞因子对肿瘤坏死因子α应承担的刺激:慢性阻塞性肺病与当前/ exsmoker细胞培养
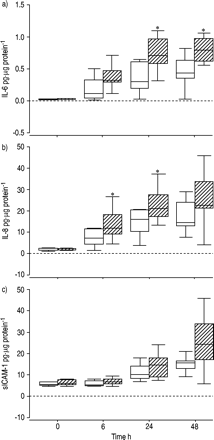
表2⇓地理显示中值(差)水平的IL 6、IL 8和描述量1生产在每个时间点如果细胞和细胞暴露于肿瘤坏死因子α在吸烟/ exsmokers没有气道阻塞,并从慢性阻塞性肺病患者细胞。细胞因子的绝对水平生产从细胞从当前/ exsmokers大于慢性阻塞性肺病细胞在每个时间点,不管刺激与肿瘤坏死因子α。然而,在当前/ exsmokers没有对肿瘤坏死因子α应承担的显著反应,以增加细胞因子的生产通过HBEC基线值。在COPD组,肿瘤坏死因子α应承担的必经暴露HBEC产生显著更大数量的地理IL 6 6 (p = 0.053), 24 (p = 0.006)和48 h (p = 0.015)相比,如果细胞(图1⇓)。同样,IL 8生产应承担更大的6 (p = 0.025)和24小时刺激组(p = 0.045)相比如果细胞(图1 b⇓)。增加的趋势描述肿瘤坏死因子α应承担的检测量1生产暴露慢性阻塞性肺病细胞被认为在48 h (p = 0.08;图1 c⇓)。
生产的)白介素(IL)高6 b) IL 8和c)可溶性细胞间粘附分子(描述)量1的控制(□)和肿瘤坏死因子(TNF)高α刺激(└)应承担primary-cultured慢性阻塞性肺疾病支气管上皮细胞。盒子代表四分位范围包含值的50%。酒吧延长最高和最低值,剔除异常值,水平线表示中位数的值。*:p < 0.05比较肿瘤坏死因子α应承担的刺激,如果细胞。
当细胞因子生产的百分比变化从时间零计算,显著增加描述量1生产针对肿瘤坏死因子α应承担的COPD组48 h (p = 0.014)。
吸入类固醇治疗对细胞因子的影响慢性阻塞性肺病生产从刺激人类支气管上皮细胞
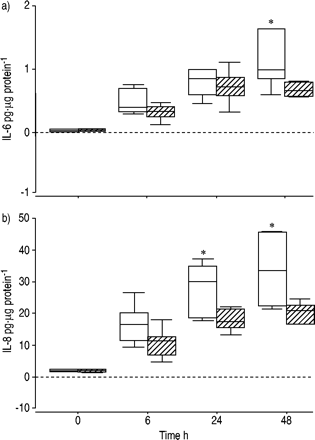
图2⇓地理显示IL 6和IL 8的慢性阻塞性肺病刺激细胞培养生产存在和缺乏常规的情况下,吸入类固醇治疗。中值(差)IL 6应承担的生产在前者48 h组是0.98(1.35)与(0.21)0.72 pg·µg细胞蛋白质−1在那些吸入类固醇(p = 0.03)。IL 6生产负相关与吸入类固醇剂量在所有时间点(时间- 6 h:ρ=−0.849,p = 0.016;0-24 h:ρ=−0.926,p = 0.003;0-48 h:ρ=−0.949,p = 0.05)。地理IL 8在24小时生产30.0前者组(17.1)和19.50 (7.75)pg·µg蛋白质−1steroid-treated组(p = 0.03)。在48 h, IL 8生产33.6(23.4)和21.7 (6.3)pg·µg蛋白质−1分别(p = 0.05)。之间没有直接的关系被IL 8水平和吸入类固醇剂量。吸入类固醇并不影响描述量1生产后的任何时间点刺激。
生产的)白介素(IL) 6和b)地理IL 8,肿瘤坏死因子α高刺激primary-cultured支气管上皮细胞在慢性阻塞性肺疾病(└)和缺乏(□)的常规,吸入类固醇治疗。盒子代表四分位范围包含值的50%。酒吧延长最高和最低值,剔除异常值,水平线表示中位数的值。*:p≤0.05。
吸入类固醇治疗肺量测定的相关标准;均值±sd FEV1患者吸入类固醇是0.98±0.08与1.50±0.41 L在那些不带他们(p = 0.027)。同样的平均FEV1% pred steroid-treated组为40.0±9.4与66年相比前者组(2.9)(p < 0.001),意味着FEV1/ FVC比率是61年38(9.5)和(7.5)(p < 0.001)两组,分别。
讨论
本研究调查了炎症反应由primary-cultured支气管上皮细胞在慢性阻塞性肺病,和临床和生理因素调节这些特征明显的患者。与当前/ exsmokers没有气道阻塞,上皮细胞从COPD患者被发现发布低水平的IL 6,应承担IL 8和描述量1基线条件下,但安装一个重要的细胞因子对肿瘤坏死因子α,未见在细胞正常的吸烟者。在COPD组IL 6和IL 8应承担响应较低细胞患者吸入糖皮质激素。
有趣的是,在这项研究中,基线条件下和肿瘤坏死因子α应承担的刺激后,降低绝对细胞因子水平被发现从细胞慢性阻塞性肺病患者比吸烟者肺功能正常。这可能是由于慢性阻塞性肺病HBEC缺陷细胞因子生产的主要文化或情况的反映在活的有机体内。外植体的细胞培养技术在实验室是一个建立和验证方法,曾被证明允许分化良好型的上皮细胞的生长与发现类似的形态和生化特征在活的有机体内17。然而,细胞的表型差异COPD患者与正常人也会影响测试结果报告。支气管活检显示上皮脱落,减少数量的纤毛18和减少纤毛细胞的比例19慢性支气管炎和慢性阻塞性肺病。在先前的研究支气管上皮细胞在文化、10%的细胞从吸烟者与正常肺功能报告纤毛,而从COPD患者几乎完全缺乏纤毛20.。虽然这并不是发现在目前的研究中,细胞的分化状态的差异文化可能解释,部分细胞因子水平的差异生产由慢性阻塞性肺病HBEC细胞和那些从当前/ exsmokers。这将需要检查在类似的研究。
也有证据表明本构细胞因子的生产在COPD气道上皮细胞可能下调。舒尔茨et al。21最近报道的实验结果符合目前发现,本构IL 8应承担的生产水平与慢性阻塞性肺病上皮细胞在初级文化,大约三分之一的从正常细胞。这是推测,这可能是由于改变了翻译后加工21。因素可能也存在在活的有机体内调节气道炎症反应,在细胞培养的无菌条件都不存在。殖民的存在下气道细菌也正越来越被认为是一个重要的独立的刺激在COPD气道炎症22。炎症细胞的合成招聘24,细菌之间的相互作用和其他细胞产品和肺上皮细胞25,可能占炎性细胞因子水平的增加隔离在痰及支气管肺泡灌洗液在慢性阻塞性肺病,和表达下调上皮炎症反应在基线条件下研究。大多数研究气道炎症的慢性阻塞性肺病已经使用痰或支气管活检和执行信息几乎没有关于气道上皮活动是否在这种情况下反映炎症在其他车厢。这需要进一步评估。
在炎症刺激如肿瘤坏死因子α应承担的,显著增加细胞因子的生产在慢性阻塞性肺病本构释放被上皮细胞,而不是那些从当前/ exsmokers与正常肺功能。最近的一项研究中,香烟烟雾的影响,比较了相似的细胞因子缺乏生产primary-cultured上皮细胞从正常的吸烟者,而细胞COPD患者再次显示出显著的反应20.。然而,与肺功能正常上皮细胞从正常受试者曾被证明产生良好的炎性细胞因子对肿瘤坏死因子α27。这些发现表明,气道上皮细胞之间的可能存在重要的差异吸烟者不发展慢性阻塞性肺病和那些,前者未能回应一种常见的炎症刺激。这可能是一个重要的保护机制在吸烟者不发展慢性阻塞性肺病,可能解释的微分表达式上皮肿瘤坏死因子α受体。这些没有了在目前的研究中,并进一步研究特征明显的主支气管上皮细胞正常的吸烟者和COPD患者现在需要。
增强后以慢性阻塞性肺病细胞分泌细胞因子肿瘤坏死因子α应承担的刺激也可能表明这个病人的气道炎症反应加剧。虽然不是COPD恶化的提供一个完整的模型,给定的炎症刺激的上皮细胞的反应可能对一般信息上皮反应在慢性阻塞性肺病恶化。肿瘤坏死因子α是一个无处不在的细胞因子,应承担一部分的最后共同通路的气道炎症过程。Upregulation IL 6和IL 8应承担的生产在回应这个炎症刺激可以影响慢性阻塞性肺病的病理生理学的重要炎症过程,包括增强炎症细胞的趋化作用的气道,Upregulation粘蛋白基因。因此这种反应可能的机制的一个组成部分,管理COPD恶化,可能部分解释了这个病人组恶化的趋势。
有趣的是,在这项研究中没有明显的描述还是1反应被认为在肿瘤坏死因子α应承担的刺激,虽然以前肿瘤坏死因子α应承担的是这个分子增强上皮的表达28,这是调节支气管活检在慢性阻塞性肺病患者29日。这些数据表明,描述量1生产由上皮细胞在慢性阻塞性肺病可能依赖于一系列的代数余子式。地理ICAM 1是人类鼻病毒附件上皮细胞的主要受体30.和人类鼻病毒已经被证明进一步诱导ICAM 1表达,从而促进炎性细胞招聘和激活在急性加重31日。气道上皮细胞在病毒诱导炎症发挥重要作用32病毒感染,最常见的人类鼻病毒,占很大比例的慢性阻塞性肺病急性加重33。这个细胞培养模型的一个限制是它没有考虑到常见的病毒引发的至关重要的作用在慢性阻塞性肺病恶化和上皮反应。考试这一发现可能会增加背后的细胞通路的机制的理解在COPD恶化。
一个潜在的重要的发现在这项研究中衰减的IL 6和IL 8应承担响应肿瘤坏死因子α在HBEC应承担的COPD患者定期,吸入类固醇治疗。而在体外证据表明抑制糖皮质激素对IL 6和IL 8生产上皮细胞系35以及中性粒细胞趋化性37和气道嗜中性38吸入类固醇治疗慢性阻塞性肺病的临床研究,在很大程度上显示这类药物的功效低。然而,这是显示最近吸入糖皮质激素可能降低慢性阻塞性肺病急性加重的严重程度39。在当前的基础上发现,这个机制可以减少exacerbation-associated炎症。它也表明,吸入类固醇可以减少COPD恶化频率40。在这项研究中,较低的本构描述的释放量- 1细胞来自患者吸入类固醇。因此,它可能是吸入类固醇有特定角色修改病毒相关急性加重,从而减少恶化的频率。类固醇撤退的慢性阻塞性肺病研究发现滞后之间的几周停用类固醇和下一个恶化41,这表明皮质类固醇疗法中介发布的影响,在本研究中可以看到,很可能在细胞因子转录改变的结果持续生产在体外。
总之,本研究表明之间的显著差异主要气道上皮细胞因子在慢性阻塞性肺疾病患者和生产吸烟者与正常肺功能,结构上和炎症刺激的反应。这些观察结果可能是重要的区分吸烟者不从那些患慢性阻塞性肺疾病,以及解释倾向在这种情况恶化。作者也表明上皮炎症反应在慢性阻塞性肺疾病可以被吸入类固醇治疗,这可能部分解释了临床观察吸入糖皮质激素对慢性阻塞性肺疾病急性加重的影响。
确认
作者要感谢g . Berlyne和m . Beckles求助获得活检标本。
- 收到了2002年10月14日。
- 接受2003年3月11日。
- ©人期刊有限公司