抽象
本报告回顾了肺部和肺外感染的表现贝氏柯克斯体。
发热,人畜共患病,是由于感染贝氏柯克斯。此形成孢子的微生物是小革兰氏阴性球杆菌,其为专性细胞内寄生虫。最常见的动物宿主是羊,牛,羊,猫,偶尔的狗。生物体达到高浓度接触受感染动物的胎盘。雾化分娩时发生感染遵循这种吸入气雾剂。有疾病的急性形式的三种不同的临床症状:非特异性发热性疾病,肺炎和肝炎。Q热的慢性形式几乎总是心内膜炎,但有时它表现为肝炎,骨髓炎或血管内感染。
疾病的肺炎形式的范围可以从非常轻微到严重肺炎,需要辅助通气。多轮混浊是胸片一个共同的发现。多西环素或氟喹诺酮治疗是优选的。敏感性对大环内酯类是可变的。
总之,贝氏柯克斯体当有适当的接触史和正在调查肺炎疾病暴发时,应考虑肺炎。
在1935年8月,E.H.德里克,病理学家,谁是微生物学和病理学实验室主任在昆士兰州卫生署,澳大利亚布里斯班,是通过在昆士兰州卫生和医疗服务的总干事联系,并责成调查中确诊的发热性疾病的爆发工人在布里斯班炮山屠宰场1。
吊杆2注意到这种疾病持续7-24天,以发烧、头痛、不适、厌食和肌痛为特征。血培养阴性,血清样本无流感、斑疹伤寒、钩端螺旋体病、伤寒和副伤寒抗体。吊杆2将疾病命名为Q(用于查询)发烧。
随后在澳大利亚和美国的调查导致了Q热病原的分离。它最终被命名为贝氏柯克斯体为了纪念在这一发现中起了重要作用的两位科学家伯内特和考克斯。
早期没有任何迹象表明,贝氏柯克斯是呼吸道病原体。
贝氏柯克斯体
贝氏柯克斯我s a pleomorphic coccobacillus with a Gram-negative cell wall that measures 0.2×0.7 µm and is an obligate intracellular microorganism3.。贝氏柯克斯经历阶段变化,类似于革兰氏阴性菌脂多糖(LPS)由光滑到粗糙的转变4。在实验感染动物中产生的第一种抗体是贝氏柯克斯蛋白(相II抗原),后来,抗体产生,以贝氏柯克斯LPS (I期抗原)。在第一阶段和第二阶段之间也有一个中间阶段5,6。在人类感染急性Q热的主要抗体反应是二期和慢性Q热病这是第一阶段抗原。有相I和相II细胞之间没有形态差异,尽管它们在它们的LPS的糖组合物确实不同7,它们在氯化铯中的浮力密度,以及它们对碱性染料的亲和力。有限合伙人的贝氏柯克斯是无毒的小鸡胚胎的剂量> 80µg·胚胎−1对比鼠伤寒沙门氏菌LPS是有毒物质在毫微克量6。
孢子状的形成解释了其中的原因贝氏柯克斯作为病原体如此成功。它可以在15-20℃下对上壁7-10个月存活,对于> 1个月肉在冷藏和在室温下在脱脂乳>40个月8。
流行病学
Q热是一种人畜共患病,直接或间接接触动物是其重要的流行病学。牛、绵羊和山羊是人类Q热的主要宿主;然而,在不同的国家,许多不同种类的动物都感染了贝氏柯克斯9。贝氏柯克斯已在节肢动物、鱼类、鸟类、啮齿动物、有袋动物和家畜身上发现3.。事实上,它会自然感染在五大洲发现的40种(包括12属)扁虱3.。虱子,螨虫和寄生虫苍蝇也感染10。贝氏柯克斯位于受感染动物的子宫和乳腺9。病牛可以摆脱贝氏柯克斯在牛奶中保存长达32个月11。大浓度贝氏柯克斯存在于受感染的胎盘和分娩过程中产生的气溶胶12。易感人群吸入这些受污染的气溶胶可导致Q热。这就解释了为什么在许多地区,每年的Q热暴发发生在牲畜开玩笑的时候13,14。宠物,包括猫、狗和兔子是一种新的来源贝氏柯克斯感染15- - - - - -19。在最近的研究中,野生褐家鼠被牵连的农场动物和猫之间的Q热链接的一部分20.。在法国,一个家庭暴发了Q热贝氏柯克斯受污染的鸽粪21。
在一些国家,家养或野生动物造成相当大的感染与这些动物接触在人与人之间,感染而在其他地区,如果任何一点传送给男人发生22,23。
贝氏柯克斯是一种非常成功的病原体。到1955年,贝氏柯克斯在51个国家发现五大洲24。在20世纪90年代,新西兰是少数几个国家,这是免费的一个贝氏柯克斯感染25。然而,发生在Q热的表现主要区别各个国家。在新斯科舍省,加拿大和西班牙的巴斯克地区,肺炎是Q热的主要表现26,27而在加那利群岛(西班牙南部)则是发烧和肝炎28。相反,在法国南部,肝炎和肺炎都可以观察到,但肝炎比肺炎更常见29。造成这些差异的原因目前还不清楚。值得注意的是,在纽芬兰的Bonavista暴发的Q热与接触受感染的山羊有关30.非特异性发热性疾病是感染的主要表现。然而,在新斯科舍省附近与猫有关的暴发中,肺炎(无论是否与接触受感染的猫、狗、兔子有关)是唯一的表现形式贝氏柯克斯感染15- - - - - -17。此外,在一个地理区域Q热可能是地方性或流行性和这两个极端之间来回移动。
在许多欧洲国家,尤其是英国,Q热仍然是一种重要的感染16,31,法国29,德国32、希腊33以及许多东欧国家34。
A review of Q fever in Germany from 1947–1999 revealed a cyclical incidence pattern with peaks occurring every 5–10 yrs32。全国各地的年平均发病率在百万分之0.1至3.1之间32。自1947年以来,共发现了40起疫情。羊是24次暴发的源头,而牛涉及4次社区暴发和2次屠宰场暴发32。
Q热的流行病学的某些方面似乎是唯一的欧洲。英国居民谁沿着公路在其农用车前往居住,开发Q热暴露的受污染秸秆,畜禽粪便,或灰尘农用运输车结果35。在瑞士山谷,沿着谁在这只羊前往和从高山牧场研制Q热路住415个居民36,37。谁住在六个村这些人靠近道路已经感染率高,范围从11.8-35.8%(平均21.1%),而那些谁住在离路面的村庄是感染(范围2.1-6.8%的显著低利率(平均2.9%))。涉及58人在意大利北部Q热的爆发与羊三个成群穿过5月底和6月初之间的区域通过相关38。的患病率贝氏柯克斯在这些鸡群抗体从45-53%不等。
两项研究记载,强风可能会导致感染贝氏柯克斯到点源的距离为11英里(18.3公里)13,39。
当气溶胶途径是主要的一个,由此人类被感染,很少有人对人的传播40- - - - - -42和感染通过血液污染或经皮途径43,44。人与人之间的传播非常罕见,因此不建议对因急性Q热病住院治疗的患者进行隔离。
流行病学研究表明,食用受污染的牛奶是Q热感染的一个危险因素45,46。然而,从实验证据,其中污染的牛奶加入到志愿者的矛盾47- - - - - -49。在病例对照研究中,Hatchetteet al。30.发现在纽芬兰卡普里恩合作社暴发Q热病期间,食用巴氏消毒干酪和吸烟都是获得Q热病的危险因素。
目前作者认为,感染途径可能解释了Q热在一些国家表现的差异例如肺炎新斯科舍省,加拿大与法国马赛:肝炎。目前的作者使用了五种不同的菌株贝氏柯克斯感染小鼠通过腹膜内或鼻内途径。只有那些感染滴鼻发展成肺炎,而腹腔感染肝炎发展,脾肿大和肺炎。支气管变化仅见于小鼠鼻腔接种50。这些数据已在Q热豚鼠模型中复制51。
很少发生垂直传播52,53但加强监测可能会发现更多的垂直传播病例。事实上,在法国南部的马提格镇,每540例妊娠中有1例并发Q热病54。
Q热的性传播已在小鼠中得到证实55和可行贝氏柯克斯已经在公牛精液中被证明了吗56。另外还有一点Q热性能够在人类中传播的建议57。米拉佐et al。58报道一个53岁的老男人谁开发作为睾丸炎Q热的并发症的情况下。睾丸炎有其发病后3天,患者有性交(病人的病发29天后)。十五天后,患者的配偶研制Q热。贝氏柯克斯脱氧核糖核酸(DNA)是在急性疾病发作后鉴定在索引壳体4的精液和15个月聚合酶链反应(PCR)
临床表现贝氏柯克斯体感染
感染是由于贝氏柯克斯可分为急性和慢性两种。慢性Q热几乎总是指心内膜炎,很少指肝炎。慢性Q热将不在本文中进一步讨论。
急性Q热主要有三种表现:1)发热自限;2)肺炎;和3)肝炎。
Q热肺炎
一个专家小组审查了关于肺炎的文献,并总结了社区获得性肺炎(CAP)的病因学,这是英国胸科学会制定CAP治疗建议过程的一部分59。在英国,1137名患者中有1.2%患有乳腺癌贝氏柯克斯肺炎,没有236名的患者在门诊的基础上,治疗肺炎的一项研究,并在重症监护病房治疗的185例均无此诊断59。在6项涉及654名欧洲大陆患者的研究中,他们接受了门诊治疗,0.8%的患者患有Q热性肺炎59。在23项涉及欧洲大陆6026名需要住院治疗的肺炎患者的研究中,0.9%的患者患有Q热性肺炎,而在澳大利亚和新西兰住院的453名CAP患者中没有人被诊断出这种肺炎59。令人惊讶的是,在北美因CAP住院治疗的1,306名患者中,2.3%患有Q热性肺炎59。但是,所有的来自北美系列案件是来自新斯科舍省的一项研究60。此外,对于未进行血清学研究贝氏柯克斯在所有进行了审查研究,这样的重要性贝氏柯克斯作为CAP的原因可能被低估。
症状和体征
几乎所有Q热肺炎患者都有发热的症状。各种其他症状经常出现,但头痛比肺炎患者更常见的其他病因61。事实上,患者Q热肺炎常状态头痛是最严重的疼痛,他们曾经有过。表1⇓给患者用Q热肺炎的症状和体征的范围内的各种研究报告61,62。表1⇓表明约有一半的Q热性肺炎患者在胸部检查时发现疑似肺炎的体征。当然,这意味着有一半的患者没有,因此,在最初诊断为肺炎,然后诊断为Q热时,常常需要较高的临床怀疑指数。
Q热肺炎引起的疾病范围从非常轻微到非常严重。后者并不常见,但根据作者的经验,超过300例Q热肺炎(约2%)需要进入重症监护病房。奥多描述的那个病人et al。63是由于需要机械通气21天Q热肺炎严重的呼吸窘迫综合征的一个例子。
这是很常见的各种肺外表现的是在介绍时明显或病情的过程中出现。这些包括骨髓坏死64,haemophagocytosis65,溶血性贫血66,淋巴结肿大模仿淋巴瘤67,短暂的发育不良性贫血68,脾破裂69、结节性红斑70。神经症状包括意识混乱、脑膜炎、脑膜脑炎、视神经炎和脱髓鞘性多神经根神经炎71- - - - - -79。心包炎和心肌炎也是Q热的表现的肺炎患者可能出现的80。
实验室检查
总白细胞计数通常是正常的,具有具有升高的计数的患者的25%。然而,lymphopaenia是常见的。血小板减少症可能存在于患者在演示文稿的时间的10%,但是,血小板增多,通常出现在疾病的恢复阶段。100万×10偶尔血小板计数9l−1被看见。低血清钠浓度可以存在,通常作为抗利尿激素不适当分泌的结果。肝功能检查轻度升高的情况并不少见。镜下血尿存在于患者的Q热肺炎〜50%。多种自身抗体已经在急性Q热进行了描述,包括抗线粒体抗体81,anticardiolipin抗体82,83和抗平滑肌抗体84。
Q热肺炎的胸部放射学表现
表2⇓和数字1 - 3⇓⇓⇓总结Q热性肺炎的放射学特征。在某些地理区域,如加拿大新斯科舍省,多发圆形浑浊物很容易使人联想到Q热性肺炎。其他情况,如由三尖瓣感染性心内膜炎引起的脓毒性肺栓塞,也可表现为多圆形肺混浊,尽管病史和体格检查可将两者区分开。然而,在许多情况下,胸片上的Q热肺炎并没有什么特别之处。
Q热肺炎实验室诊断
在大多数情况下,实验室诊断贝氏柯克斯感染血清学。补体结合89间接免疫荧光抗体检测是可行的90,91。后者是最好的。一些中心还提供酶联免疫分析90。在急性和恢复期样本中,抗体升高四倍或更多是诊断性的。一般来说,急性和恢复期之间的2周间隔就足够了。基于单一血清样本的诊断并不理想,然而,间接荧光抗体(IFA)的II期免疫球蛋白(Ig)M滴度为>1:64或II期IgG滴度为>1:256是近期的有力证据贝氏柯克斯使用IFA测试的感染。
贝氏柯克斯可在胚胎卵细胞或组织培养中分离。大多数实验室都无法合作贝氏柯克斯因为它的极端传染性的。壳小瓶技术是用于分离有用贝氏柯克斯和用于确定抗生素敏感性92。贝氏柯克斯已从Q热病肺炎患者(使用贝壳瓶技术中的组织培养)~ 15%的血液中分离出来,在抗生素治疗前和疾病的最初几天取样,以及在Q热病心内膜炎患者中的50%93。
治疗
抗菌药物敏感性测定C。burnetii这个问题一直存在,因为它是一种细胞内病原体。然而,长期以来人们一直在努力提供有关抗菌素敏感性的数据C。burnetii。三个模型系统已被用于:鸡胚,豚鼠,和细胞培养。一般来说四环素类,喹诺酮类,利福平,泰利霉素和克拉霉素是积极反对贝氏柯克斯97。有些菌株对红霉素敏感,有些则不敏感97。
Sobradilloet al。98在西班牙巴斯克地区对多西环素和红霉素治疗被认为是由Q热引起的肺炎进行了前瞻性、随机、双盲研究。血清学研究证实48例患者有Q热;23人每天两次服用100毫克强力霉素,25人每6小时服用500毫克红霉素,坚持10天。多西环素治疗组发热消退更快(3±1.6天)与3±2天;p = 0.05)。红霉素治疗组胃肠道不良反应较多(11与二为多西环素治疗的患者;P <0.01)。40日,胸片的48例患者中47是正常的。作者的结论是强力霉素比红霉素更有效,但他们认可的肺炎大多数情况下,自限性和良性性质,由于Q热。Kuzmanet al。99研究64例Q热肺炎。Twenty-two patients were treated with azithromycin (total dose 1.5 g administered over 3–5 days), 15 with doxycycline (100 mgb.i.d。其中15人接受了各种各样的其他抗生素治疗。阿奇霉素组平均发热时间为2.5天,强力霉素组为2天,其他抗生素组为3.5天。所有患者均治愈。Kofterids对1989-1995年间治疗的130例Q热性肺炎患者进行了回顾性分析et al。33。11个病人接受四环素成为无热的的意思是3天,患者42红霉素在平均4.26天,成为无热的患者和28β-lactam代理需要6.8天成为无热的。15%的克拉霉素治疗的患者在5天仍然发热,相比之下,35%的红霉素治疗的患者和没有一个四环素治疗的患者发热。
对19例Q热肺炎回顾性分析显示,11例用红霉素和八与β内酰胺类抗生素治疗。红霉素治疗组无发热成为第3天,而只有两个β内酰胺的治疗组分别为无热通过该时间(P <0.005)One hundred.。
Q热性肺炎的首选治疗方法是使用强力霉素10天。替代疗法是氟喹诺酮或大环内酯加利福平。后一项建议是根据的在体外药敏结果和传闻的经验。
结束语
临床医生应该知道的患病率贝氏柯克斯体在他们练习的地方感染。出现肺炎的患者应询问Q热的危险因素,如果存在这些危险因素,应收集急性和恢复期血清样本并检测抗体贝氏柯克斯体。如果确诊为Q热,应通知公共卫生当局,以便进行适当调查以确定感染源。
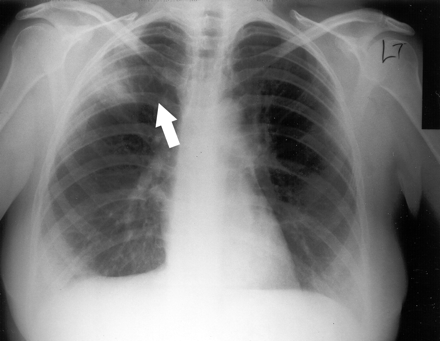
谁开发的Q热肺炎暴露于被感染的猫临产一个年轻的女的胸片。注意:右肺上叶不透明度(箭头)。
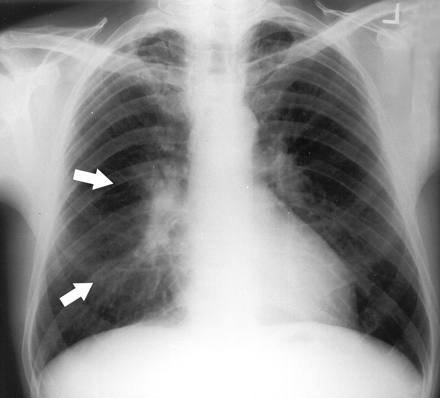
Q热性肺炎患者右肺门周围混浊(箭头)。
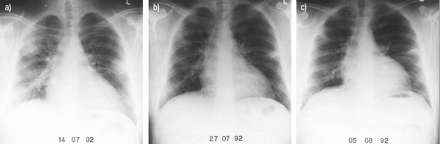
a - c) Q热性肺炎患者的系列胸片。注意多轮混浊。c)在第一次x光检查后3周出现了相当高的分辨率。
脚注
↵以前的articles in this series: No. 1:TärnvikA,伯格伦德L.土拉菌病。欧元呼吸杂志2003;21:361-373。2号:Mabeza GF,麦克法兰J.肺放线菌。欧元呼吸杂志2003;21日:545 - 551。
- 收到了2002年10月30日。
- 接受2002年11月26日。
- ©ERS杂志有限公司
参考
- 1.↵
- 2.↵
- 3.↵
- 4.↵
- 5.↵
- 6.↵
- 7.↵
- 8.↵
- 9.↵
- 10.↵
- 11.↵
- 12.↵
- 13.↵
- 14.↵
- 15.↵
- 16.↵
- 17.↵
- 18.
- 19.↵
- 20。↵
- 21。↵
- 22。↵
- 23。↵
- 24。↵
- 25。↵
- 26。↵
- 27。↵
- 28。↵
- 29。↵
- 30。↵
- 31.↵
- 32.↵
- 33.↵
- 34.↵
- 35.↵
- 36.↵
- 37.↵
- 38.↵
- 39.↵
- 40.↵
- 41。
- 42。↵
- 43。↵
- 44。↵
- 45。↵
- 46。↵
- 47。↵
- 48。
- 49。↵
- 50。↵
- 51。↵
- 52。↵
- 53。↵
- 54。↵
- 55.↵
- 56.↵
- 57.↵
- 58.↵
- 59.↵
- 60.↵
- 61.↵
- 62.↵
- 63.↵
- 64.↵
- 65。↵
- 66。↵
- 67。↵
- 68。↵
- 69。↵
- 70.↵
- 71。↵
- 73。
- 73。
- 74。
- 75。
- 76。
- 77。
- 78。
- 79。↵
- 80.↵
- 81.↵
- 82.↵
- 83.↵
- 84.↵
- 86.↵
- 86.
- 87.
- 88.↵
- 89。↵
- 90.↵
- 91.↵
- 92.↵
- 93.↵
- 94.↵
- 95。↵
- 96。↵
- 97。↵
- 98。↵
- 99。↵
- One hundred.↵











