文摘
白介素(IL) 9是调节许多细胞类型参与辅助2型反应的经典与哮喘有关,包括B - t淋巴球,肥大细胞、嗜酸性粒细胞和上皮细胞。相比之下,靶细胞中介IL-9的下呼吸道的影响仍有待确定。因此,作者评估IL-9的活动对人类肺泡巨噬细胞(AM)健康志愿者。
我之前与IL-9 preincubated脂多糖(LPS)刺激表现出氧化破裂,正如前面与il - 4所示。IL-9被废除的抑制作用anti-hIL-9Rα单克隆抗体,并存在IL-9受体是由免疫荧光显示。il - 4和IL-9未能factor-α调节肿瘤坏死,引发和il - 10释放LPS-stimulated。然而,一些观察表明,IL-9和il - 4法案通过不同的机制:1)interferon-γ对着干的IL-9-mediated抑制il - 4——但不是我氧化破裂;2)CD14表达下调了il - 4的表达而不是IL-9和3)生产的肿瘤生长factor-β由激活是由IL-9强,不是il - 4,并要求IL-9-mediated抑制氧化破裂。
这些观察提供额外的信息关于肺部interleukin-9的活动,与炎症或fibrosing肺相关流程。
c . Pilette目前野心家的昏聩国家de la任职(比利时、批准号支持3.4590.99),y Ouadrhiri Lancardis基金会(瑞士)。
最近,白介素(IL) 9可以发挥重要的作用在辅助(Th) 2型反应,尤其是哮喘[1]。更具体地说,它已经表明,IL-9强化IL-4-induced免疫球蛋白E (Ig)生产[2],刺激肥大细胞增殖和分化[3],激活嗜酸性粒细胞成熟[4]和刺激粘液的支气管上皮细胞[5]。与il - 4相比,已涉及细胞调节气道和肺泡空间,IL-9的下呼吸道的作用是差特征对于潜在的靶细胞。因此,IL-9可以调节炎症和纤维发生的过程发生下呼吸道,如小鼠暴露于二氧化硅粒子中所示IL-9施加保护性anti-fibrotic活动[6],但肺靶细胞调节这些影响并没有被确定。
当前作者最近显示[7],IL-9能够抑制在体外人类血液单核细胞激活脂多糖(LPS)释放氧代谢物和肿瘤坏死因子(TNF) -α,il - 4。由IL-9这单核细胞失活可能占的有益活动IL-9模型中观察到的致命endotoxaemia [8]。相比与其他Th2家族的巨噬细胞抑制因子,如il - 4、无效的IL-9迄今为止报道肺巨噬细胞。此外,据报道,分化的巨噬细胞,如滑膜[9]或肺泡巨噬细胞(AM)[10]可以表现出不同的反应相同的刺激相比,血液单核细胞。
因此,在本研究IL-9对人类的影响,代表居民的吞噬细胞参与肺[11]的一线防御,进行评估。更具体地说,氧化破裂,细胞因子释放,包括profibrotic细胞因子肿瘤生长因子的释放(TGF) -β,通过激活有限合伙人,进行了研究。这些影响与il - 4和干扰素(IFN) -γ相比,Th2和Th1细胞因子,被分别被调节的激活状态特别是关于呼吸爆发。
材料和方法
积极的重组体人(rh) IFN-γTGF-β买来Genzyme(英国剑桥)。RhIL-9和il - 4以及反IL-9R(α链)单克隆抗体(mab)产生了路德维希研究所,比利时布鲁塞尔分行。Anti-IL-9Rα克隆AH9R2马伯(鼠标IgG2a)是用于间接免疫荧光染色,和阻塞马伯hIL-9R(克隆AH9R7, mIgG2b)是专门用来抵消IL-9活动。人类IL-9纯化如前所述[7]。有限合伙人的大肠杆菌(血清型O55: B5)购买从Difco实验室(美国底特律,MI)和anti-TGF-β1马伯(克隆TB21, mIgG1) Biosource国际(贝CA)。
肺泡巨噬细胞隔离
人类正在从七个不吸烟的健康志愿者获得了支气管肺泡灌洗(BAL)标准化技术[12]后,从所有志愿者和批准的书面同意后落下帷幕过程由当地伦理委员会。落下帷幕的细胞,由巨噬细胞> 90%,作为评估Giemsa-stained cytospins,被允许在完整的罗斯威尔公园坚持塑料Memoral研究所介质(cRPMI) (Bio-Whittaker Walkersville,医学博士,美国)1 h在37°C不依从的细胞(主要是淋巴细胞)与cRPMI洗液。最后,我代表>总额的95%附着细胞镜检和流式细胞术。细胞生存能力评估的台盼蓝排斥试验至少90%。
氧化破裂试验
我(0.2×106·好−1)分布在96 -平底盘子(实验室的器具,正欲猎鹰,贝德福德,妈,美国),preincubated 24 h在37°C, 5%二氧化碳rhIL-9(路德维希研究所,布鲁塞尔,比利时),rhIL-4(路德维希研究所)(ng 20毫升−1每个)或rhIFN-γ(Genzyme,剑桥,英国)(200 U·毫升−1在cRPMI),刺激由有限合伙人(从20 h大肠杆菌血清型055:B5;美国Difco实验室、底特律、MI)(1µg·毫升−1)。细胞内氧化能力评估是所描述的低音et al。[13],使用2′,7′二氯荧光素(DCFH)乙酰乙酸盐(σ,圣,密苏里州,美国),这是氧化成高荧光DCF根据细胞内过氧化氢(H2O2)呼吸产生的破裂。裂解后0.1% v / v Triton x - 100(σ)磷酸盐(PBS),荧光在一个计算机化的微型板块量化荧光光谱仪(帕卡德仪器,,,美国)在530纳米485 nm激发/发射波长和DCF浓度已知浓度的标准曲线的推导出光纤荧光(σ)。结果修正总蛋白浓度在细胞溶解产物取决于bicinchoninic酸碱度方法(美国皮尔斯,罗克福德,IL)和被表示为nmol DCF每毫克细胞蛋白质。
细胞因子释放试验
我(0.5×106·好−1)分布在24-well板块(Falcon) preincubated 24 h和细胞因子,进一步刺激有限合伙人的氧化破裂的评估。浮在表面的收获和冻结在−20°C到细胞因子滴定。释放TNF-α量化了细胞毒性生物测定使用WEHI 64个细胞克隆13日如前所述[14],和rhTNF-α(勃林格曼海姆Gmbh,曼海姆,德国)作为一个标准。引发,il - 10和TGF-β1浓度测定酶联免疫吸附试验。从CLB工具包(阿姆斯特丹,荷兰)是用于il - 10定量,遵循制造商的协议。工具包Biosource国际(贝南、钙、美国)允许的决心TGF-β1释放其潜在的复合物后上层清液的酸处理;TGF-β1也是评估原油浮层。一夜之间,引发,96 -孔板被涂在4°Cµg·4毫升−1anti-hIL-8马伯(克隆6217.11σ)100毫米碳酸钠缓冲区,pH值9.6。在PBS洗液含有0.1% 20 v / v渐变和阻塞1 h 37°C和w / v 1%牛血清白蛋白在同一个缓冲区,rhIL-8标准(Biosource国际)和上层的孵化为2 h 37°C。盘子被孵化20 ng·毫升−1生物素化的多克隆anti-hIL-8 Ab(研发系统,明尼阿波利斯,美国在阻止缓冲区,洗后,与辣根peroidase-conjugated链霉亲和素(σ)。反应当时开发的0.03% v / H2O2衬底和0.42毫米3,3′,5、5′-tetramethylbenzidine色原在100毫米醋酸钠/柠檬酸缓冲,pH值4.9,停止与硫酸二氢2 M,读在一盘光谱仪450海里。的敏感性TNF-α生物测定为0.2 pg·毫升−1,引发,il - 10和TGF-β1免疫测定10 pg·毫升−12 pg·毫升−1和2个pg·毫升−1,分别。上层清液都是在重复化验。
免疫荧光染色
表面的表达IL-9受体(α链和IL-2Rγ单元)是被间接免疫荧光化验。我(0.2×106·好−1在4°C)孵化1 h和anti-hIL-9Rα马伯(AH9R2或AH9R7),或与anti-hIL-2Rγ马伯(克隆38024.11,mIgG1;研发系统),稀释在RPMIµg·10毫升含3%胎牛血清的边后卫。经过三洗液rpmi - 3%的边后卫,在4°C 1 h和孵化µg·10毫升−1fluoresceine异硫氰酸酯(FITC)共轭F (ab′)2羊的碎片anti-mouse免疫球蛋白(SAM-FITC;σ)在同一介质。是孵化与同型的搞笑和此后SAM-FITC代表消极的控制。三洗之后,我被固定在pbs v / v甲醛2% - 3%的边后卫在室温下15分钟,轻轻刮用橡胶警察在4°C蒙在鼓里,直到流仪结果进行FACscan(美国正欲,pgr CA)。额外的染色CD14 preincubated上午进行24 h和细胞因子通过直接免疫荧光使用FITC-conjugated anti-CD14马伯(克隆MøP9 mIgG2b;正欲)。
共焦显微镜,点(0.2×106·盖玻片−1)培养24-well 2 h的盘子,用cRPMI洗净,应用为IL-9R流仪分析AH9R2马伯,洗后的边后卫pbs - 3%和2%甲醛固定在同一个缓冲区,细胞被安装在幻灯片为2.5%,4-diacylbicyclo 2, 2, 2-octane(σ)Mowiol (Calbiochem-Novabiochem,达姆施塔特,德国),并分析了由mrc - 1024共焦显微镜(生物Rad实验室、里士满、钙、美国)使用63×客观在油浸。图像数字化记录和复制的影印机。流式细胞术和共焦显微镜,IL-9R正面和负面的控制细胞分别由野生型和hIL-9R-transfected Baf-3细胞。
统计分析
数据从实验中获得至少一式三份,重复三次,和结果表示为±sem手段。表示,从实验结果中执行复制或重复两次,然后表示为±sd方法。不同群体之间的差异观察进行分析时,运用t检验和Bonferroni调整进行多重比较,相同的控制条件。一个p < 0.05被认为是重要的。
结果
在LPS-stimulated IL-9和il - 4抑制氧化破裂
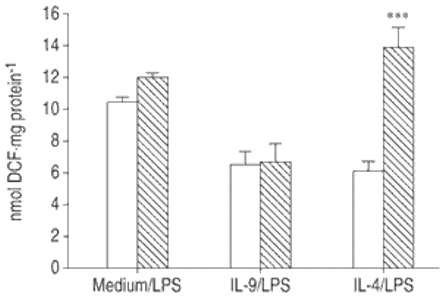
LPS刺激的20 h DCFH氧化增加约两倍,相比之下,如果是(图1所示⇓)。尽管IL-9并未显著调节氧化破裂如果(数据未显示),预培养24 h和IL-9表达下调的胞内氧化破裂LPS-stimulated (6.5±0.5与10.4±0.3 nmol DCF·毫克的蛋白质−1p < 0.001)(图1)的基线水平。也显示出了类似的抑制作用与il - 4 (6.1±0.3与10.4±0.3 nmol DCF·毫克的蛋白质−1(图1),p < 0.001)。相比之下,预培养的是IFN-γ稍微增加了氧化破裂,以应对有限合伙人尽管这种效应并不显著(图。1⇓)。
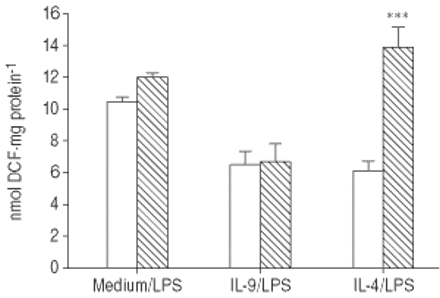
白介素(IL) 9、IL - 4和干扰素(IFN) -γ胞内氧化破裂在脂多糖(LPS)刺激肺泡巨噬细胞(AM)。数据提出了均值±sem从三个实验获得,一式三份。贴现:二氯荧光素。* * *:p < 0.001相比,如果我;# # #:与我相比p < 0.001 preincubated由有限合伙人中独自和刺激。
IL-9-mediated抑制氧化破裂的剂量和时间
我是与不同浓度的IL-9 preincubated评估LPS刺激后细胞内氧化破裂。一剂/响应曲线观察考虑抑制呼吸爆发的IL-9 LPS-stimulated(图。2⇓)。此外,预培养时间的24小时之前LPS刺激被要求观察IL-9的抑制作用是氧化破裂。因此,无显著抑制作用发生在我与IL-9 preincubated 4或8 h,并没有额外的抑制观察预培养时间> 24小时(数据没有显示)。
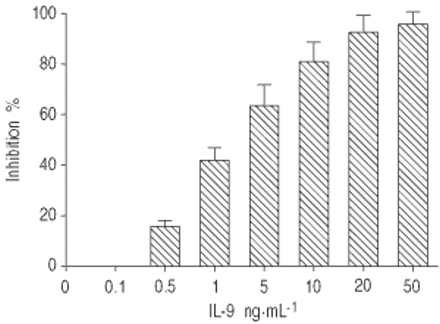
剂量效应引起的抑制白介素(IL) 9 lipopolysaccharide-stimulated肺泡巨噬细胞的氧化破裂。数据提出了意味着±sd (n = 3)。
IFN-γ废除il - 4,但不是IL-9,抑制作用在LPS-stimulated氧化破裂
的影响IFN-γ抑制由IL-9和il - 4在LPS-stimulated氧化破裂是被co-incubating评估细胞IL-9或il - 4和IFN-γ。抑制呼吸爆发的IL-9在LPS-stimulated维持在IFN-γ(6.6±0.1与6.5±0.5 nmol DCF·毫克的蛋白质−1ns)(图3所示⇓)。相比之下,IFN-γ完全废除il - 4的抑制作用在LPS-stimulated氧化破裂(13.8±1.3与6.1±0.3 nmol DCF·毫克的蛋白质−1,p < 0.001)(图3所示⇓)。
interferon-γ效果(┘)抑制由白介素(IL) 9和IL - 4在氧化破裂脂多糖(LPS)刺激肺泡巨噬细胞(AM) (□)。* * *:与我相比p < 0.001 preincubated与il - 4。
IL-9抑制作用在氧化破裂LPS-stimulated是专门被中和anti-IL-9Rα马伯
为了证实的观察效果的特异性IL-9感到呼吸爆发,我是使用中和anti-hIL-9Rα马伯IL-9孵化前(AH9R7)。预处理的是AH9R7(10µg·毫升−1)前1 h添加IL-9废除90±5%(平均±sem)的IL-9影响LPS-stimulated DCFH氧化。相比之下,没有重大变化是观察IL-9-mediated抑制作用与mIgG2b用作同型的控制(表1所示⇓),也在IL-4-mediated抑制anti-hIL-9Rα马伯(数据未显示)。
IL-9和il - 4无法调节生产TNF-α,引发和il - 10 LPS-stimulated
结构上,是释放TNF-α水平很低,也没有可检测量的引发和il - 10(图4所示⇓)。正如预期的那样,刺激我的有限合伙人20 h强烈诱导这些细胞因子的分泌。LPS-stimulated点,预培养IL-9或il - 4略减少TNF-α生产,但是没有达到统计学意义(分别为74.8±10.2,80.3±19.7,与102.4±17.6 pg·毫升−1ns)(图。4⇓)。相比之下,IFN-γ略强TNF-α释放LPS-stimulated (145±9.4与102.4±17.6 pg·毫升−1,p < 0.05)(图4所示⇓)。TNF-α相似,无显著观察引发释放的调制是用IL-9预处理,也与il - 4(图4所示⇓)。生产显然是被IFN-γLPS-induced il - 10 (22.5±4与45.3±9.2 pg·毫升−1,p < 0.001),也稍微减少IL-9和il - 4,但没有达到统计学意义(38.4±5.7,35.1±9.8 pg·毫升−1分别与45.3±9.2 pg·毫升−1ns)(图。4⇓)。
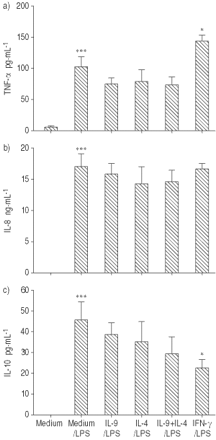
白介素(IL) 9、IL - 4和干扰素(IFN) -γ释放肿瘤坏死因子(TNF) -α,b)引发和c) IL - 10的脂多糖(LPS)刺激肺泡巨噬细胞(AM)。数据均值±sem (n = 3)。*:p < 0.05,相比之下我preincubated独自介质和LPS刺激;* * *:p < 0.001相比,如果。
il - 4但不是IL-9抑制表面CD14 LPS受体的表达
CD14检测表面的点,虽然较低程度比血液单核细胞[7]。CD14表达的表面点被预培养表达下调与il - 4(平均荧光强度(MFI) 42±4与84±6,p < 0.001)。相反,IFN-γCD14在增加,尽管这种效应低于统计显著性水平(MFI 111±5与84±ns)(表2⇓)。相比之下,IL-9不改变表面CD14表达水平(表2⇓)。
IL-9强烈强化TGF-β1的生产
略有增加TGF-β1的上层清液中观察到的如果是孵化IL-9 (68±9与39±8 pg·毫升−1在酸洗上层清液,p < 0.05)。更重要的是,生产的TGF-β1 LPS-activated感到强烈的IL-9 (366±21与109±23 pg·毫升−1在酸洗上层清液,p < 0.001)(图5所示⇓)。这种效应与il - 4和IFN-γ没有被观察到。此外,IL-9-mediated TGF-β1 upregulation是专门被中和anti-IL-9Rα马伯(118±14与366±21 pg·毫升−1,p < 0.001)(图5所示⇓),而不是控制mIgG2b。
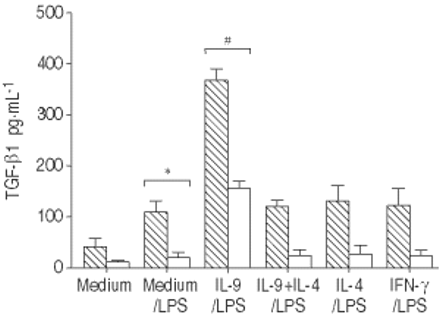
白介素(IL) 9、IL - 4和干扰素(IFN) -γ肿瘤生长因子的释放(TGF) -β脂多糖(LPS)刺激肺泡巨噬细胞(AM)。TGF-β在未经处理的(□)和由酸洗(┘)上层清液。数据提出了均值±sem (n = 3)。*:p < 0.05相比,如果我;#:与媒介是preincubated相比p < 0.05。
抑制氧化破裂的IL-9 LPS-activated取决于TGF-β1
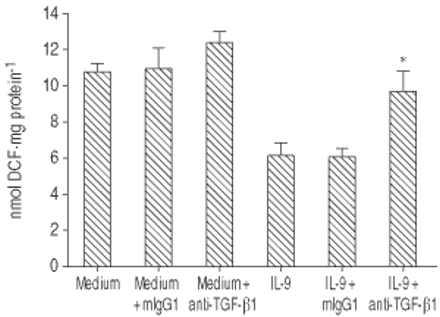
考虑到TGF-β已被确定为一个主要的巨噬细胞去活化因子,其分泌物被IL-9刺激,TGF-β可能调解IL-9在氧化破裂的抑制作用是解决。有趣的是,类似于血液单核细胞[7],呼吸爆发的IL-9-induced抑制LPS-stimulated是废除了封锁TGF-β1活动的一个特定的马伯,而不是控制mIgG1(图6所示⇓)。这个废除anti-TGF-β1马伯没有观察到在抑制诱导il - 4(数据没有显示)。
影响抗肿瘤生长因子(TGF) -β1单克隆抗体(mAb)白介素(IL) 9-induced抑制氧化破裂的脂多糖(LPS)刺激肺泡巨噬细胞(AM)。我是使用anti-TGF-β1 mAb或控制老鼠免疫球蛋白(mIg) G1, 2 h预孵化前24 h IL-9独自或中等。数据提出了均值±sd (n = 3),并代表两个实验。贴现:二氯荧光素。
是表达一种特定的受体IL-9吗
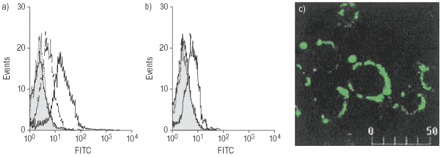
具体确定IL-9表面受体。IL-9Rα链的存在就证明是通过流式细胞术和共焦显微镜、免疫染色后使用不同的特定马伯(AH9R2和AH9R7)(图7所示⇓)。积极控制细胞(hIL-9Rα-transfected Baf-3细胞)表面荧光表现出类似的模式,而没有改变荧光观察直方图的野生型Baf-3控制细胞(数据未显示)。的表达水平由IL-9 IL-9Rα没有明显改变,il - 4或IFN-γ是培养24 h与这些细胞因子(数据未显示)。的其他亚基IL-9R复杂,IL-2Rγ(γc),也确定是(图7所示⇓),尽管后者受体的表达水平出现相当变量在不同志愿者(数据未显示)。
流仪分析)白介素(IL) 9 (R)α受体和b) IL-2Rγ链由肺泡巨噬细胞(AM)表达式。我是孵化AH9R2(——)或AH9R7(——)单克隆抗体(mAb)或反(h) IL-2Rγ和此后fluoresceine异硫氰酸酯(FITC)共轭羊anti-mouse免疫球蛋白抗体。自体荧光(阴影直方图)和控制(······)直方图也显示。这个数字是代表五个实验。c) IL-9Rα染色的是AH9R2马伯也评估了共焦显微镜(插图、规模=µm)。
讨论
作者曾表明,IL-9 Th2细胞因子[15],抑制活性氧中间体的生产(ROI)和TNF-α人类血液单核细胞[7]。所示,IL-9还可以调节人类的一些重要功能。因此,预处理和IL-9抑制LPS刺激后其后续生产ROI。相比之下,LPS-stimulated细胞因子释放的是没有明显影响IL-9和il - 4。有趣的是,与il - 4相比,这表现出类似的活动是呼吸道破灭,IL-9刺激TGF-β1的生产。此外,TGF-β1所需IL-9的抑制作用是氧化破裂。
与IFN-γ相比,代表的一个主要启动因素是呼吸爆发[16]和细胞因子释放[17],Th2细胞因子(il - 4、il - 10和IL-13)和TGF-β通常被描述为macrophage-deactivating因素。特别是,Bhaskaranet al。[18]表明,il - 4为氧化破裂失效是应对有限合伙人。相应地,在这项研究已经表明,IL-9抑制生产对LPS刺激的ROI。而ROI可能需要清除肺细胞内病原体[19],这些有毒代谢物的作用中也得到了证实肺组织损伤在活的有机体内[20]。因此,抑制H2O2代在激活il - 4和IL-9可能有一个重要的角色在组织损伤的预防一些炎症过程发生在肺泡。的兴趣在这方面,它是由il - 4和IL-9抑制性影响,这可能会出现冗余,可能由IFN-γ不同调制,与此同时在肺部免疫反应产生。因此,抑制il - 4的氧化破裂在LPS-activated招致敌对IFN-γ正如前面所示[21],相比之下IL-9。
相反的规定是氧化破裂,il - 4和IL-9并未改变一些细胞因子的释放。因此,il - 4和IL-9未能显著调节TNF-α的释放,引发和il - 10 LPS-stimulated点,虽然是一个倾向于抑制il - 10生产尤其如此。几项研究已经报道,il - 4由激活抑制炎症介质的释放,即TNF-α和IL-1β(22 - 24),il - 6[25],单核细胞趋化peptide-1 [10], il - 12[26]或前列腺素E2(27、28)。然而,其它的研究未能证明显著影响细胞因子il - 4的生产[29],以及在monocyte-derived滑膜巨噬细胞或巨噬细胞[9]。一个可能的解释的相对损失IL-9和il - 4活动组织巨噬细胞,比血液单核细胞,减少IL-2Rγ链的表达,受体的共同亚基特别是il - 4和IL-9 [30]。然而,目前的数据表明,il - 4和IL-9都可以调节,特别是对氧化代谢,IL-2Rγ是这些组织巨噬细胞表达的。
生产的TGF-β激活强烈会使IL-9,但不是通过il - 4。有趣的是,使用抗体中和TGF-β1,表明upregulation TGF-βIL-9的途径需要IL-9-mediated抑制是氧化破裂。与先前的研究表明这是在协议TGF-β处于待发状态是一个主要的巨噬细胞因子,特别是生产的ROI [31]。此外,这个观察可以解释,至少在某种程度上,需要预孵化期IL-9 LPS-activated是抑制氧化破裂。相反,TGF-β,产生潜在procytokine复杂,已被确定为一个主要的fibrosing代理(32、33)。虽然Th2炎症概要文件与纤维化相关肺部疾病如特发性肺纤维化[34]或bleomycin-induced肺纤维化[35],这Th2炎症和组织纤维化之间的关系仍然知之甚少。李et al。[36]最近表明,通过激活TGF-βIL-13诱发肺纤维化,表明TGF-β可能代表Th2炎症和肺纤维化之间的联系。目前的数据,表明TGF-βupregulation IL-9可以诱导的激活点,支持这个概念。相反,阿拉斯et al。[6]报道,IL-9抑制而不是强化矽肺肺纤维化小鼠模型中,这种效应是与silica-induced Th2两极分化的抑制有关。因此,其他机制可能发生在活的有机体内关于细胞因子网络或其他监管途径。更具体地说,它已经表明,H2O2能引起结缔组织生长因子(CTGF)[37]介导TGF-β对成纤维细胞胶原合成的影响[38]。因此,IL-9可能诱发肺profibrotic活动通过激活TGF-β分泌增加,氧化破裂可能防止差别而对这些组织纤维化通过限制CTGF的感应。
表面CD14表达的调制是代表一个潜在的细胞激活调控机制,因为这需要受体诱导信号事件导致炎性细胞因子的合成引起LPS [39]。当前作者已经证实CD14表达上是由il - 4表达下调,正如前面所示[27日40]。这是与IL-9相比,它没有影响CD14表达。此外,作者观察到IFN-γ可以中和CD14的减少是引起il - 4(数据没有显示)。这些影响可能代表失活或启动机制是通过il - 4和IFN-γ,分别对进一步LPS刺激。
在结论中,作者报告interleukin-9抑制活性氧的生产在肺泡巨噬细胞激活,同样interleukin-4。与释放肿瘤坏死factor-α相比,interleukin-8和-10年,这并不影响interleukin-9或4,肿瘤生长的生产factor-β1通过激活肺泡巨噬细胞强烈增强interleukin-9这肿瘤生长factor-β1 upregulation介导的抑制作用interleukin-9氧化破裂。最后,CD14表达的调节表现为肺泡巨噬细胞的潜在机制由interleukin-4失活,以及interferon-γ启动的,并不是与interleukin-9观察。这些观察强调监管途径的肺泡巨噬细胞活化辅助interleukin-9 2细胞因子和提供新的信息与肺泡巨噬细胞生物学。
确认
作者要感谢p Courtoy(细胞单位,细胞病理学研究所,鲁汶大学,布鲁塞尔)的共焦显微镜。
- 收到了2002年1月23日。
- 接受2002年6月10日。
- ©人期刊有限公司