摘要
在哮喘和慢性阻塞性肺病(COPD)患者中,通过吸入腺苷引起浓度相关性支气管收缩。腺苷诱导支气管收缩的机制似乎涉及与激活的肥大细胞的选择性相互作用,随后释放预先形成和新形成的介质。将腺苷信号与哮喘和慢性阻塞性肺病联系起来的进一步证据来自于发现许多在这些疾病恶化中发挥重要作用的细胞类型表达腺苷受体,并通过刺激这些受体显示相关效果。
因此,阻断这些受体可能是治疗哮喘和慢性阻塞性肺病的一种有价值的方法。最近,在许多炎症细胞类型中,包括肥大细胞、嗜酸性粒细胞、淋巴细胞、中性粒细胞和巨噬细胞中,发现了有望作为哮喘和慢性阻塞性肺病新疗法的腺苷受体靶点。A2B.受体表明人肺肥大蜂窝作为最具战略性细胞靶标之一。
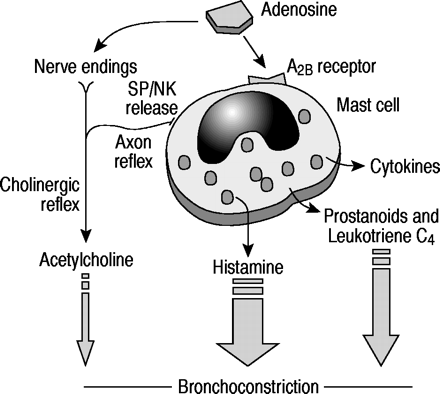
已建议腺苷在炎症气道疾病(如哮喘和慢性阻塞性肺病)(COPD)中发挥作用1-3..与正常对照相比,在哮喘患者的气道衬里流体中测量了腺苷的升高水平4..在敏化的兔子中,在过敏原攻击后肺灌洗液中已经报道了高浓度的腺苷5.,而在转基因小鼠中,腺苷受体转录本增加与肺部炎症和气道高反应性增加有关6..通过吸入的腺苷给药引发哮喘和COPD的受试者中的浓度相关的支气管内容7.那8.而核苷对正常个体的气道口径没有明显影响。由于这些初步的观察,相当大的努力已经指向揭示腺苷诱导支气管收缩的精细机制;这些似乎涉及到与激活的肥大细胞的选择性相互作用,随后释放预先形成的和新形成的介质9.-13.(fig. 1⇓).
图。1。-
腺苷导致哮喘和慢性阻塞性肺病中支气管内的提出机制。请注意,肥大细胞衍生的调解器在很大程度上涉及到对腺苷(最大箭头)的气道反应,而神经途径的作用可以忽略不计(最小的箭头)。SP:物质P;nk:neurokinins。
现在存在越来越多的证据表明,通过腺苷诱导的支气管内的气道反应性评估在区分来自COPD的哮喘,监测哮喘的抗炎治疗,测量疾病进展以及评估与过敏气道炎症相关的疾病活动的患者可能是有价值的。特别地,腺苷反应性与过敏气道炎症密切相关,最近在哮喘和活性过敏性鼻炎的研究中展示,其中气道对腺苷5'-单磷酸盐(AMP)的反应性,而不是甲素,与痰多相关嗜酸性粒细胞14.那15..
进一步证据通过在这些条件的加剧中起重要作用的许多细胞类型,表达腺苷受体并通过刺激这些受体表现出相关效果,进一步证据了与哮喘和COPD联系起来的哮喘和COPD。这些包括肥大细胞16.那17.,嗜酸性粒细胞18.,淋巴细胞19.,中性粒细胞20.和巨噬细胞21.那22..
在这篇文章中,腺苷受体信号在慢性炎症性气道疾病(如哮喘和COPD)中的病理生理作用的证据进行了综述。
哮喘和COPD中腺苷诱导支气管收缩的细胞机制
即使腺苷信号可能涉及许多在哮喘和慢性阻塞性肺病中被证实有相关作用的细胞类型,但只是在最近,腺苷吸入后的支气管收缩反应吸引了呼吸药理学和生理学研究人员的注意。到目前为止,还没有腺苷拮抗剂已被接受用于人体,但替代药理学方法表明,腺苷不太可能直接作用于平滑肌细胞在活的有机体内,但间接地通过激活在中间炎症细胞(如肥大细胞)或传入神经末梢(图1)上表达的嘌呤植物(图1)⇑).
神经通路
怀疑神经途径的激活有助于对腺苷的收缩气道反应。反射胆碱能成分的可能性最初由来自近交比大鼠研究的数据表明23.后来在临床调查中证实,其中通过吸入给予高剂量的抗胆碱能药物Ipratropium溴化物的预测显着减弱了哮喘中的AMP的支气管电机反应24..进一步支持对AMP诱导的支气管中的神经贡献来自于用Frusemide和硼酸酐制备的观察结果,两个环路利尿剂也可能通过调节气道中的感官神经反应来作用25..吸入这些药物实质上抑制了AMP的支气管收缩反应而不影响对组胺的反应26.-28..在几内亚猪在活的有机体内合成腺苷类似物,2-氯腺诺,被辣椒素衰减的支气管内29..此外,在BDE大鼠中,腺苷通过刺激产生神经肽的神经来引发肺部抗性增加通过先前的肥大细胞激活30..这些观察结果表明,来自感觉神经末梢的收缩神经肽的释放可能具有一些重要的介于介导嘌呤衍生物的气道影响。为了探测该假设,使用了重复的Bradykinin支气管扩张剂作为人类神经肽耗竭模型的反复的Bradykinin支气管扩张。对Bradykinin的反复挑战,足以响应于生态蛋白的15倍,导致随后的AMP反应的一些衰减,而不会影响气道对组胺的反应性31..然而,吸入的磷酰胺的中性内肽酶(NEP)的抑制未能引发amp引起的支气管痉挛反应的任何显着增强,这表明内源性神经肽的释放在对腺苷的气道反应中具有很小的重要性32..神经通路在COPD患者中腺苷诱导的支气管收缩中的作用尚未完全阐明。然而,路透社最近的一项研究表明等等。33.对COPD患者吸入的IPratropium溴后,对AMP响应性没有显着影响,这意味着迷失神经激活并没有发挥作用。这种对比哮喘患者的结果形成鲜明对比,其中溴化钙导致AMP的挑衅浓度增加〜2.5倍,导致急性呼气量在一秒钟(PC20)中落入强制呼气量20%24..在哮喘中,AMP可能会刺激肥大细胞释放组胺,从而产生叠加效应通过vagal-nerve刺激。在慢性阻塞性肺病中,AMP刺激时组胺释放量可能较小,不足以刺激迷走神经末梢。
肥大细胞
在哮喘和COPD的炎症活动期,肥大细胞可能在吸入腺苷的支气管收缩反应中发挥主要作用,这一事实表明体外腺苷显着增强了通过酶分散体获得的人肺肥大细胞释放组胺和其他新形成的痉挛性的释放34.那35.和支气管肺泡灌洗36..综上所述,肥大细胞可能主要参与吸入腺苷引起的支气管收缩反应通过释放颗粒衍生的预制介质。什么在活的有机体内证据是有支持这个吗?在哮喘中,已发现肥大细胞抑制剂,甘氨酸钠,Nedocromil钠和沙丁胺醇在更大程度上衰减了amp诱导的支气管细胞,而不是由光滑肌肉激动剂,甲咯孔引起的支气管扩张37.那38..另外,有强效的预测1- 已经显示了 - 亚胺氨氨酸受体拮抗剂,三丁胺和Asemizole,抑制急性支气管杆菌在哮喘和COPD患者中的吸入放大器反应33.那39.那40.更直接的证据表明,气道肥大细胞释放的组胺对腺苷诱导的反应至关重要,这来自于直接向哮喘支气管灌注AMP的工作10.或进入过敏性鼻炎患者的鼻子12.导致灌洗液中组胺和胰蛋白酶浓度的显着增加。
自H.1-Histamine受体拮抗剂不完全抑制AMP诱导的支气管细胞,必须考虑其他肥大细胞衍生介质的作用。除了预先形成的介质之外,还必须考虑其他肥大细胞衍生的调解体的作用。前列腺醇在对AMP的反应中的作用得到了效力的环氧酶抑制剂,例如吲哚美辛和絮凝剂,抑制核苷酸的收缩效应9.那41..此外,吸入给药的赖氨酸阿司匹林导致AMP响应的一些衰减11..更多的直接证据表明新生成的调解员来自Polosa的研究等等。10..除了支气管肺泡灌洗液中组胺和胰蛋白酶水平升高外,前列腺素D也有更大的升高2(PGD2)发现浓度。最近,有雅培的预留(ABT-761)42.和选择性半胱氨酸白三烯受体1 (Cys LT .)1)受体拮抗剂蒙特鲁斯特13.,已被证明可减弱吸入AMP引起的急性支气管收缩反应,因此提示了致痉挛白三烯的作用。
这些研究合理地支持肥大细胞衍生介质在哮喘和COPD中对腺苷的反应大大意义的概念,这可能是核苷与特异性肥大细胞表面受体的相互作用的结果(图1⇑).然而,涉及响应的特定肥大腺苷受体亚型是不知道的。
腺苷酸代谢途径
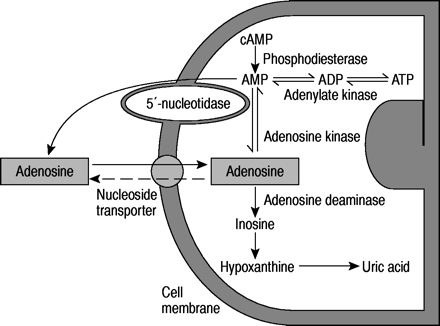
腺苷是一种核苷,由嘌呤碱、腺嘌呤、糖苷连接的糖、核糖组成。大多数胞外腺苷来源于质膜5′核苷酸酶对核苷酸AMP的酶切43.(图2⇓).虽然其中一些AMP是由细胞外三磷酸腺苷(ATP)产生的,但大多数可能来自细胞内AMP,因为它沿浓度梯度扩散到细胞外,从而遇到位于细胞膜上的5′核苷酸酶。胞内AMP主要来源于能量生成过程中二磷酸腺苷(ADP)和ATP的裂解。产生AMP的其他途径确实存在,但在数量上不那么重要。虽然大多数细胞内AMP正常情况下会转化为ADP和ATP,但在高能量需求和/或缺氧条件下,它会被5′核苷酸酶代谢成腺苷44..当大量渗透炎性炎性细胞竞争为有限的氧气供应时,这可能发生这种情况。通过将酶腺苷激酶转化为amp,细胞内腺苷的腺苷水平持续低质量45.但当能量需求较大时,腺苷也被腺苷脱氨酶降解为肌苷和次黄嘌呤46..细胞外腺苷通过与能量无关的核苷转运蛋白的操作延伸回电池47..由于细胞内的腺苷水平保持在较低水平,因此存在一个向内的浓度梯度(图2)⇓).
图2.-
在高能量腺苷磷酸酯的分解代谢期间(腺苷三磷酸(ATP),腺苷二磷酸(ADP)),形成细胞内腺苷5'-单磷酸(AMP),并且随着作为能量循环的一部分而不转换为ADP和ATP。然而,在高能量需求的条件下,不能重新转化放大器,并通过血浆膜5'-核苷酸酶代谢至腺苷。通过将酶腺苷激酶转化为氨基酶转化为氨基酶,但当能量需求较大时,腺苷与腺苷脱氨酸酶也降解腺苷和脱黄时,腺苷的细胞内水平较低。细胞外腺苷通过无关的核苷转运蛋白的操作扩散回电池。营地:循环放大器。
腺苷受体亚型:历史观点
细胞外腺苷一旦产生,就会引发与哮喘和慢性阻塞性肺病相关的各种细胞反应,这些反应主要是通过与靶细胞表面的G蛋白偶联受体相互作用介导的48..腺苷 - 摄取抑制剂双嘧达莫,增强腺苷诱导的效果的能力导致了建议,其可能通过位于细胞表面上的特异性受体的刺激来介导其作用49.那50..另外,已知常常用于分辨哮喘和COPD的气道阻塞的药物,通过治疗血浆水平(20-120μm)通过腺苷受体拮抗活性衰减腺苷诱导的支气管细胞。在20世纪80年代初,对腺苷受体的理解仅基于“特异性”激动剂/拮抗剂的活性,并限于A之间的分裂1受体(减少细胞内循环amp(营地)水平)和a2受体(增加细胞内cAMP)51.那52..腺苷a的建议1当发现另一个黄嘌呤enProfylline时,茶碱的受体拮抗活动可能解释其临床效力,当发现另一个黄嘌呤enProfylline时,临床临床,但缺乏腺苷a1-receptor拮抗活动。enProfylline还能够在哮喘受试者中阻断腺苷诱导的支气管痉挛,尽管它缺乏一个1受体拮抗活性,在这方面比茶碱更有效。这次悖论当时被认为是对腺苷受体拮抗作用的证据,作为黄根植物的临床疗效的解释。在20世纪90年代,有关新腺苷受体亚型的信息为“enProfylline悖论”提供了可能的解释。分子克隆技术的应用扩展了已知的腺苷受体的范围,包括a3.受体53.和A.2B.受体(最初描述的A2受体现在被命名为A2A)54..恩profylline(以及茶碱)抑制配体与人重组腺苷A的结合2B.Ki为~ 7 μ M的受体55.那56.,在治疗剂量(5-25μm)之后,在烯丙基的典型血浆水平内井下出的值。稳定的腺苷类似物5'-N-乙基羧酰胺腺苷(NECA) - 从人肥氏细胞系HMC-1中释放白细胞介素(IL)-8的释放,似乎主要介导A2B.受体57.,被enProfylline封锁,尽管报告的研究使用了相对高浓度的药物(300μm)58..还显示茶碱,阻止NECA诱导的中国仓鼠卵巢(CHO)细胞中的CAMP积累(CHO)细胞转染人A.2B.Ki的受体刚为<7μm59..然而,恩profylline与A的亲和力很小1受体并不意味着A1受体在哮喘中没有作用。实际上,反义寡核苷酸对抗腺苷a1受体正在调查此目的60.
腺苷受体亚型的详细特征已经在人肺组织和分离的人支气管肺泡灌洗细胞中进行,试图确定它们在腺苷诱导反应中的药理作用。然而,现有的腺苷受体激动剂和拮抗剂的特异性有限48.那59.那61使鉴定腺苷受体亚型涉及艰巨的任务。然而,幸运的是,抗体或原位杂交探针最近已被用于不同的人类腺苷受体亚型。这些研究可以提供更确定的受体亚型识别和定位信息。
腺苷一1受体
腺苷A的描述1-receptor表达和分布已被广泛在哺乳动物中进行。绑定数据表示a1受体在正常的人肺中不是特别丰富,但它的存在,可能与神经有关,被功能研究支持。腺苷一1受体存在于人性化粒细胞上,激活促进趋化性62并增加对内皮细胞的粘附63那64.对于哮喘的特异性,已经证明,通过涉及A的上调的机制,抗原在出生时免疫的兔子对腺苷的气道过度反应性1受体65那66.在这些研究的优雅延伸中,组合的药理学和反义方法证实,腺苷受体介导的兔子中的支气管混合物由A介导1受体67.利用反义寡脱氧核苷酸对A1肺部的受体减少他们的数字,他们也能够显示没有A的敏感的动物1受体表现出降低支气管电脑的反应对过敏原挑战67.在最近对小鼠肺的研究中,已经检测到所有四个腺苷受体,其中有一个1-receptor成绩单是最丰富的成绩单6..这些作者还发现a的转录水平显著增加1, 一种2A和一个2B.腺苷 - 脱氨酶缺陷小鼠肺部的受体,与肺炎和气道高反应性增加了。虽然这些数据对腺苷A的证据提供了一些支持1受体作为过敏性哮喘或慢性阻塞性肺病的潜在治疗靶点,目前还没有证实这种受体亚型参与人类气道对腺苷的反应。
腺苷一2A受体
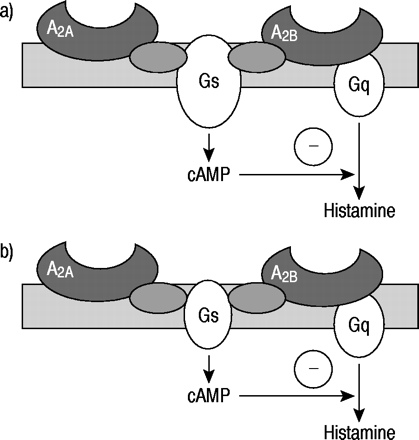
A.2A和一个2B.通过反向转录酶聚合酶链反应(RT-PCR)和人支气管肺泡灌洗肥料细胞鉴定受体57.那68.G-蛋白(GS)的亚基s - 绕腺苷a2A和一个2B.受体分别以其高和低亲和力为特征,用于腺苷2.A.2A与人类肺病最相关的受体是那些表达在肥大细胞上的受体57.那68,中性粒细胞69和t细胞70.与a相反2B.受体,A2A活化导致抑制人肥大细胞的组胺和胰蛋白酶释放68那71那72.这可以提供平衡的控制机制。在低浓度的腺苷时,只有通过较高亲和力的接合提供的断开信号2A受体占优势,因此下调肥大细胞中介释放(图3a)⇓).相反,在达到高浓度的腺苷的情况下,例如哮喘和COPD4.,低亲和力的相对重要性a2B.受体随着肥大细胞脱颗粒而增大(图3b)。除了对人肺肥大细胞的作用外,腺苷似乎对中性粒细胞也有重要作用。A的刺激作用是众所周知的2A受体将嗜中性粒细胞粘附到内皮63,防止在甲基Met-Leu-Phe刺激的中性粒细胞上的整联蛋白表达上调73并抑制活性中性粒细胞和单核细胞的升级74-76.因此,A2A受体激动剂可能在诸如COPD的疾病中表现出抗炎潜力,其中嗜中性粒细胞/单核细胞介导的组织损伤是强烈的牵连。不幸的是,A.2A受体有广泛的解剖分布(表1)⇓)它们对于在其他体结构和细胞系统中介导许多反应,包括抑制血小板聚集,血管扩增和对中枢神经系统的各种影响78.肺中的选择性局部作用是必要的,以避免不可接受的副作用。相反,特定的拮抗剂2A受体可能增强中性粒细胞激活并加剧炎症。
图3.-
假设腺苷增强哮喘患者气道肥大细胞组胺释放的机制示意图。a)正常情况下,刺激的高亲和力2A腺苷的腺苷受体导致产生大量的细胞内环状腺苷5'-单磷酸(阵营),其下调涉及组胺的生物化学途径。b)哮喘的可能场景,在存在高浓度的腺苷的情况下,低亲和力A的相对重要性2B.受体随着G蛋白偶联受体(GQ)蛋白的调节亚单位Q的普遍激活而变大,具有显着的肥大细胞脱粒。此外,G蛋白偶联受体(GS)功能的亚基S的下调导致CAMP产生的减少,随后对组胺释放的减少的阴性调节。
腺苷一2B.受体
近年来,应用分子克隆技术鉴定出人腺苷A2B.受体54..A.2B.受体在结构上与A密切相关2A受体,和a2A受体,可以在激活时抬起细胞内阵营。然而,在功能上,它似乎与a截然不同2A这表明,与腺苷酸环化酶直接相关的信号转导系统可能对腺苷酸环化酶的功能更重要79.的腺苷2B.受体最近在人支气管上皮中被免疫化学鉴定80和功能的2B.在内皮细胞,肌细胞,神经元,神经胶质细胞,神经细胞,成纤维细胞和肥大细胞中发现了受体57.那81.激活A.2B.人体肥大细胞系HMC-1增强IL-8释放的受体本身和增强脂栓12-肉豆蔻酸酯13-醋酸酯(PMA) - 诱导IL-8的分泌物58..HMC‐1细胞共表达A2A和一个2B.受体,两者都与腺苷酸环酶通过G-蛋白偶联,但只有一个2B.受体激活HMC - 1细胞释放IL - 8。因此,腺苷可能通过作用于肥大细胞A而参与炎症性呼吸道疾病的发病2B.受体增强促炎介质的释放2.考虑到吸入腺苷只引起哮喘和慢性阻塞性肺病患者的支气管收缩7.那8.并且对常规个体的气道口径没有影响,腺苷与来自患者的肥大细胞相互作用的方式是一种内在差异。虽然产生的反应体外由A.2B.HMC - 1细胞中的受体似乎模仿在活的有机体内在哮喘和COPD中吸入腺苷的反应,与正常对照相比,哮喘/ COPD患者的差异反应背后的分子机制仍然待阐明。有几种机制可以解释这些差异,包括差动耦合2B.对细胞内途径和受体水平的多样性的受体,例如基于对a的不同亲和力2A和一个2B.受体(图3)。虽然腺苷似乎主要通过炎症细胞中腺苷受体的激活介导其作用,但结合功能和放射性配体结合的研究表明,人气道平滑肌也是腺苷的直接靶点,其作用由时间依赖性a的不同贡献决定2B.和一个1腺苷受体82.因此,气道平滑肌中腺苷受体亚型的相对分布和活化可能影响诸如哮喘和COPD等疾病中的气道功能,并在治疗腺苷受体或呼吸道中改变核苷酸/核苷水平的治疗策略中的认证考虑。
一个人的论点2B.- 对哮喘和COPD的病理生理学是一体的影响,从考虑到茶碱的药理学性质的进一步支持。茶碱对人类的亲和力2B.治疗性血液浓度的受体,但没有选择,因为它显示了A的相似或更低的亲和力1和一个2A受体。鉴于腺苷A的有限作用1和一个2A上面概述的受体以及表现出治疗剂量的茶碱对腺苷的反应产生更大的抑制作用而不是抗组胺83,封锁A2B.受体似乎是该药物临床疗效的合理解释。此外,甲基黄嘌呤磷酸二酯酶抑制剂恩profylline与茶碱具有类似的抗哮喘活性84,最近被证明可以作为一种选择性的2B.- 治疗血液水平的拮抗剂58..选择性拮抗剂2B.受体可以为茶碱和enProfylline提供更有效和更安全的替代品。
腺苷一3.受体
这两个体外17.那85和在活的有机体内86那87研究已经证实A3.受体导致肥大细胞脱颗粒和/或增强肥大细胞脱颗粒响应过敏原在各种啮齿动物物种。然而,一个3.- 与人肺肥大细胞结合未发现-receptor蛋白18.,从而质疑其在腺苷诱导的人类支气管机制的相关性。现在累积了一个证据3.‐受体激活调节多种人类免疫炎症细胞的功能变化。例如,在人类肺中,A3.受体以相对高的密度在嗜酸性粒细胞上表达88并在激活时介导嗜酸性粒细胞趋化性的抑制作用18.那89.此外,这些作者证明了一个表达3.受体(信使核糖核酸(mRNA)和蛋白)在哮喘肺中增强18..最近,ezeamuzie和飞利浦90这些受体介导了人类嗜酸性粒细胞的两种重要抗炎功能:抑制脱颗粒和抑制氧自由基的生成。腺苷一3.-receptor激活也涉及:抑制肿瘤坏死因子(TNF)-α通过内毒素从人机单核细胞中释放91;内毒素或TNF - α在全人血液中诱导的中性粒细胞脱颗粒抑制76;以及T细胞功能的调制92.这些发现随后提出了这些受体的功能作用的问题。在哮喘和慢性阻塞性肺病患者的肺中发现的高浓度腺苷可能足以产生显著的抑制。在这种情况下,高水平的腺苷的存在可能是一种减轻嗜酸性和嗜中性炎症的方法通过一种3.-receptor激活。因此,选择性a3.激动剂可能是有价值的抗炎药物,在治疗如哮喘和COPD的情况下有有用的潜力,激活的嗜酸性粒细胞和中性粒细胞发挥重要作用。
结论
认识到腺苷受体在慢性气道炎症疾病发病机制中的潜在作用,提高了封锁这些受体可能是治疗哮喘和慢性阻塞性肺病的有价值的方法的可能性。最近,在许多炎症细胞类型中,包括肥大细胞、嗜酸性粒细胞、淋巴细胞、中性粒细胞和巨噬细胞中,发现了有望作为哮喘和慢性阻塞性肺病新疗法的腺苷受体靶点。然而,人肺肥大细胞似乎是最有吸引力的细胞靶点,因为其独特的药理特性和响应炎症刺激的功能作用。肥大细胞可能在哮喘和慢性阻塞性肺疾病的活动性炎症期对吸入腺苷的支气管收缩反应中发挥主要作用。刺激的2B.表达于人肺肥大细胞表面的受体可能是腺苷诱导的支气管痉挛的主要触发器。因此,开发具有强效和选择性的A2B.腺苷受体拮抗剂用于人类似乎特别有益,并可能进一步增加这些受体在生理和病理条件中的作用的知识。
- 已收到2002年2月12日。
- 公认2002年3月26日。
参考文献
- ↵
腺甘酸支气管刺激:哮喘中有希望的过敏性炎症标志物?胸部1997年;52.:919-923。
- ↵
Feoktistov I,Polosa R,Holgate St,Biaggioni I. Adenosine A.2B.受体:哮喘治疗的新靶点?。趋势Pharmacol Sci.1998年;19.:148.-153。
- ↵
Fozard JR,Hannon JP。腺苷受体配体:哮喘和COPD中作为治疗剂的潜力。Pulm杂志1999年;12.:111.-114年。
- ↵
Driver AG,Kukoly Ca,Ali S,Mustafa SJ。在支气管肺泡灌洗液中的腺苷哮喘。AM Rev Respir Dis1993年;148.:91-97。
- ↵
Ali S, Mustafa SJ, Metzger WJ。腺苷受体介导的过敏性兔模型中的支气管混合物和支气管高反应性。是杂志1994年;266:L271-L277。
- ↵
部分腺苷脱氨酶缺陷小鼠的腺苷依赖性气道炎症和高反应性。J Immunol2001;167:4676.-4685。
- ↵
Cushley MJ,Tattersfield Ae,Holgate St.在正常和哮喘受试者中吸入腺苷和鸟苷对气道阻力。Br J Clin Pharmacol1983年;15.:161.-165年。
- ↵
Oosterhoff y,de Jong Jw,Jansen Mam,Koeter GH,邮政DS。通过吸烟确定气道对慢性阻塞性肺病中的腺苷5'-单磷酸磷酸的反应性。AM Rev Respir Dis1993年;147.:553.-558。
- ↵
Phillips Gd,Holgate St.单独的口服萜脒和絮凝物与金支支支气管的反应的影响,在非含有哮喘中吸入腺苷5'-单磷酸盐的反应。AM Rev Respir Dis1989年;139.:463-469年。
- ↵
Polosa R, Ng WH, Crimi N,等等。哮喘支气管内腺苷激发后肥大细胞来源的介质的释放。am j respir crit care med1995年;151.:624.-629。
- ↵
Crimi N, Polosa R, Magri S,等等。吸入的赖氨酸乙酰胱氨酸(L-ASA)在哮喘受试者中衰减对腺苷5'-单磷酸盐(AMP)的支气管电机反应。欧元和J1995年;8.:905.-912年。
- ↵
Polosa R,Pagano C,Dokic D,Prossperini G,Church MK,CriCri N.组胺释放在过敏性对象中的AMP鼻塞上。胸部1999年;54.:230-233。
- ↵
Rorke S,Jennison S,Jeffs Ja,Sampson AP,Arshad H,Holgate St.Cysteinyl白三烯在哮喘中AMP诱导的支气管中的作用。胸部2001(新闻)。
- ↵
Polosa R,Ciamarra I,Mangano G,等等。支气管高反应性和厌氧炎症标志物中的鼻炎,具有过敏性鼻炎。欧元和J2000;15.:30.-35年。
- ↵
van den Berge M, Meijer RJ, Kerstjens HA,等等。PC20腺苷5 '‐单磷酸比PC20甲基胆碱与哮喘气道炎症的关系更密切。am j respir crit care med2000;163:1546.-1550。
- ↵
Marquardt DL,Walker Ba,Heinemann S.来自小鼠骨髓源细胞的两种腺苷受体亚型的克隆。J Immunol1994年;152.:4508-4515。
- ↵
ramkumar v,斯蒂尔gl,beaven ma,阿里h. a3.腺苷受体是独特的腺苷受体,其有助于释放肥大细胞中的过敏介质。J Biol Chem.1993年;268:16887.-16890。
- ↵
Walker Ba,Jacobson Ma,Knight da,等等。腺苷一3.嗜酸性粒细胞的受体表达和功能。AM J RECMIR CELL MOL BIOL1997年;16.:531.-537。
- ↵
Huang S, Apasov S, Koshiba M, Sitkovsky M2A细胞外腺苷受体介导的腺苷介导的T细胞活化和膨胀抑制的信号传导。血液1997年;90:1600-1610。
- ↵
Cronstein BN。腺苷调节中性粒细胞功能和抑制炎症通过腺苷受体在: Jacobson KA, Jarvis MF,编辑。实验治疗学中的嘌呤能方法纽约,Wiley-liss,1997年;PP。285.-293。
- ↵
Eppell Ba,Newell Am,Brown EJ。在单核细胞的分化期间表达腺苷受体对巨噬细胞体外:对吞噬作用的调节有影响。J Immunol1989年;143.:4141.-4145年。
- ↵
Hasko G,Szabo C,Nemeth Zh,Kvetan v,Pastores Sm,Vizi es。腺苷受体激动剂差异调节原始264.7巨噬细胞和内缺血小鼠的IL-10,TNF-α和一氧化氮产生。J Immunol1996年;157.:4634-4640。
- ↵
Pauwels R,Van der Straeten M.腺苷诱导支气管内的动物模型。AM Rev Respir Dis1987年;136.:374.-378年。
- ↵
Polosa R, Phillips GD, Rajakulasingam K, Holgate ST.研究吸入异丙托溴铵和口服特非那定对哮喘患者5 '‐单磷酸腺苷引起的支气管收缩的影响。J Allergy Clin Lmmmol1991.;87:939-947。
- ↵
Polosa R.吸入环路利尿剂:我们如何在哮喘中解释他们的调节作用?过敏1993年;48.:555.-558。
- ↵
用吸入法抑制5 '‐单磷酸腺苷和methacholine诱导的哮喘支气管收缩。欧元和J1990年;3.:665.-672。
-
O'Connor BJ, Chung KF, Miin Chen-Worsdell YM, Fuller RW, Barnes PJ。吸入呋塞米和布美他尼对哮喘受试者5 '‐单磷酸腺苷和焦亚硫酸钠诱导的支气管收缩的影响AM Rev Respir Dis1991.;143.:1329.-1333。
- ↵
Polosa R,Rajakulasingam K,Prossperini G,Church Mk,Holgate St.哮喘中吸入的Frememide和硼酸酐的AMP Airway对AMP气道反应性的相对障碍和时间课程。J过敏临床免疫杂志1993年;92:288.-297年。
- ↵
2‐氯腺苷诱导麻醉豚鼠迷走介导和阿托品抵抗性支气管运动反应。BR J Pharmacol.1990年;100.:251-256。
- ↵
Meade CJ,Mierau J,Leon I,Ensinging Ha。体内腺苷A3受体:N6.在BDE大鼠中,‐2‐(4‐氨基苯基)乙基腺苷通过类似肥大细胞的神经介导机制诱导支气管痉挛。J pharmacol exp ther1996年;279:1148-1156。
- ↵
Polosa R, Rajakulasingam K, Church MK, Holgate ST.重复吸入缓激肽可减轻哮喘气道中腺苷5 '‐单磷酸(AMP)诱导的支气管收缩。欧元和J1992年;5.:700-706。
- ↵
Polosa R,Santonocito G,Magrìs,等等。吸入磷酰胺抑制哮喘患者支气管对AMP反应的研究。欧元和J1997年;10.:2460-2464。
- ↵
Rutgers SR,Koeter GH,Van der Mark TW,邮政DS。口服萜脒和在患有COPD患者中AMP诱导的支气管中的IMPratropium的保护作用。中国Exp过敏1999年;29.:1287.-1292年。
- ↵
教堂MK,Pao GJ-K,Holgate St.机械分散的人肺肥大细胞组胺分泌的表征:抗IgE,钙离子孔A23187,化合物48/80和碱性多肽的影响。J Immunol1982年;129.:2116.-2121年。
- ↵
Peachell Pt,Columbo M,Kagey-sabotka A,Lichtenstein LM,Marone G.腺苷增强了人肺肥蜂窝的介质释放。AM Rev Respir Dis1988年;138.:1143-1151。
- ↵
Forsythe P,McGarvey LPA,Heaney Lg,Macmahon J,Ennis M.腺苷诱导人类Bal肥大细胞组胺释放。中国科学1999年;96:349.-355年。
- ↵
Phillips Gd,Scott VL,Richards R,Holgate St.NedocromiL钠和酸钠对吸入腺苷5'-一磷酸盐诱导的支气管混合物的影响。欧元和J1989年;2:210-217。
- ↵
Phillips Gd,Finnerty JP,Holgate St.吸入β的比较保护作用2-激动剂沙丁胺醇(沙丁胺醇)治疗哮喘组胺、甲基胆碱和腺苷5‐单磷酸引起的支气管收缩。J过敏临床免疫杂志1990年;85:755.-762。
- ↵
Rafferty P,Beasley R,Holgate St.组胺的贡献通过吸入过敏原和阿甲酸腺苷5'-单磷酸盐在特应性哮喘中引发的立即支气管细胞。AM Rev Respir Dis1987年;136.:369.-373。
- ↵
Phillips Gd,Polosa R,Holgate St.组胺h的作用1受体拮抗拮抗作用于浓度相关的AMP诱导的哮喘支气管中的支气管。中国Exp过敏1989年;19.:405.-409。
- ↵
Crimi N, Palermo F, Polosa R等等。吲哚美辛对腺苷所致支气管收缩的影响。J过敏临床免疫杂志1989年;83:921-925。
- ↵
van schoor J,Joos GF,KIPS JC,Drajesk JF,Carpentier PJ,Pauwels Ra。ABT-761,一种新的5-脂氧基酶抑制剂,在哮喘受试者中对运动和腺苷诱导的支气管混合物的影响。am j respir crit care med1997年;155.:875.-880年。
- ↵
Bodansky O,Schwartz MJ。5'-核苷酸酶。阿德中国化学1968年;11.:277-328年。
- ↵
Mentzer RM,Rubio R,Berne RM。从缺氧犬肺组织中释放腺苷及其在肺循环中的可能作用。是杂志1975年;229:1625-1631。
- ↵
拱门JRS,Newsholme EA。对代谢的控制和腺苷的激素作用。学生物化学论文1978年;14.:82-123。
- ↵
电车,例如Lauter CJ。在血浆膜酶的外径。物化学Biophys学报1974年;345.:180-197。
- ↵
Plagemann PG,Richey DP。培养物中的动物细胞核苷,核酸碱,胆碱和葡萄糖的运输。物化学Biophys学报1974年;344.:263-305年。
- ↵
腺苷受体亚型:特性和治疗调节。药理学年度报告1995年;35.:581..
- ↵
斯塔福德A.二吡酰胺的腺苷和腺嘌呤核苷酸的增强。BR J Pharmac Chemother1966年;28.:218-227年。
- ↵
Crimi N Palermo F Oliveri R等等。哮喘患者腺苷诱导腺苷诱导腺苷诱导的支气管痉挛的增强作用。过敏1988年;43.:179-183。
- ↵
范Calker D,Muller M,Hamprecht B.腺苷调节,通过两种不同类型的受体,培养脑细胞中的循环AMP的积累。J Neurochem1979年;33.:999-1005。
- ↵
Londos C,Cooper DMF,Wolff J.外腺苷受体的亚类。Proc Natl Acad Sci USA1980年;77:2551-2554。
- ↵
萨尔瓦特湾,雅各布森马,泰勒,他,林登j,约翰逊rg。人A3腺苷受体的分子克隆与表征。Proc Natl Acad Sci USA1993年;90:10365.-10369年。
- ↵
Pierce Kd,Furlong TJ,Selbie La,Shine J.分子克隆和表达腺苷A2B.来自人脑的受体。Biochem Biophys Res Comm1992年;187:86-93年。
- ↵
Robeva As,Woodard RL,Jin XW,等等。重组人腺苷受体的分子特征。药物开发Res1996年;39.:243-252年。
- ↵
菩提树j,泰国我,差价凡象H,金X,Robeva为。人A(2B)腺苷受体的表征:人胚胎肾203细胞和HMC-1肥大细胞中的放射性配体结合,蛋白质印迹,蛋白质印迹和偶联至G(Q)。摩尔杂志1999年;56.:705-713。
- ↵
Feoktistov I,Biaggioni I.腺苷的药理表征A.2B.受体。同联的人肥大细胞的研究2A和一个2B.腺苷受体亚型。生物化学杂志1998年;55.:627.-633年。
- ↵
Feoktistov I,Biaggioni I. Adenosine a2B.受体唤起人肥大细胞中白细胞介素- 8的分泌-与哮喘相关的恩profylline敏感机制J Clin Invest.1995年;96:1979年-1986。
- ↵
Klotz K‐N, Hessling J, Hegler J,等等。人腺苷受体亚型的对比药理学 - 表征CHO细胞中稳定转染的受体。Naunyn Schmiedeberg的Arch Pharmacol1998年;357.:1-9。
- ↵
Metzger WJ, Nyce JW。寡核苷酸治疗过敏性哮喘。J过敏临床免疫杂志1999年;104.:260-266。
- ↵
Collins Mg,Rovani Smo。腺苷受体亚型。趋势Pharmacol Sci.1993年;14.:361.-366。
- ↵
Cronstein Bn,Daguma L,Nichols D,Hutchison AJ,Williams M.腺苷/中性粒细胞悖论解决:人中性粒细胞拥有A.1和一个2促进趋化性和抑制o的受体2一代分别。中国投资1990年;85:1150-1157。
- ↵
Cronstein Bn,Levin Ri,Phillips Ni,Hirschhorn R,Abramson SB,Weissman G.中性粒细胞粘附到内皮的粘附通过腺苷A.1受体和抑制通过腺苷A.2受体。J Immunol1992年;148.:2201-2206。
- ↵
Felsch A,Stocker K,Borchard U.Borbol酯刺激嗜中性粒细胞对内皮细胞的粘附性腺体由腺苷A降低2受体激动剂。J Immunol1995年;155.:333.-338年。
- ↵
Ali S, Mustafa SJ, Metzger WJ。腺甘酸诱导的晚期气道阻塞过敏兔支气管收缩和气道平滑肌收缩:诱导腺甘酸A的证据1受体。J pharmacol exp ther1994年;268:1328-1334。
- ↵
El-Hashim A,D'Agostino B,Matera Mg,Page C.表征腺苷受体中腺苷诱导的支气管中的过敏性兔子。BR J Pharmacol.1996年;119.:1262.-1268年。
- ↵
Nyce JW, Metzger WJ。DNA反义治疗哮喘的动物模型。自然1997年;385.:721-725。
- ↵
Suzuki H,Takei M,Nakahata T,Fukamachi H.腺苷对人类培养肥大细胞在交联时对FcεRi的抑制作用。Biochem Biophys Res Communic1998年;242:697-702。
- ↵
瓦拉尼k,gessi s,dionisotti s,ongini e,borea pa。(3H)-CH 58261在人性粒细胞膜中的功能A2A腺苷受体标记。BR J Pharmacol.1998年;123.:1723.-1731年。
- ↵
Varani K, Gessi S, Dalpiaz A, Ongini E, Borea PA。通过(3H)-SCH 58261结合人类淋巴细胞膜A2A腺苷受体的特性BR J Pharmacol.1997年;122.:386.-392。
- ↵
Hughes PJ,Holgate St,教堂MK。腺苷抑制和增强了通过A2-purecineptor介导的机制从人肺肥大细胞中抑制的IgE依赖性组胺释放。生物化学杂志1984年;33.:3847-3852年。
- ↵
Peachell PT, Lichtenstein LM, Scheimer RP。腺苷对嗜碱性细胞和肺肥大细胞功能的调控。J pharmacol exp ther1991.;256:717-726。
- ↵
Wollner A, Wollner S, Smith JB。代理通过一种2受体腺苷抑制fMLP刺激的中性粒细胞上Mac‐1 (CD11b/CD18)表达的上调。AM J RECMIR CELL MOL BIOL1993年;9.:179-185。
- ↵
张勇,张玉华,张玉华2A受体在中性粒细胞白细胞中介导腺苷对甲状腺蛋白酶刺激的呼吸爆发的抑制作用。Naunyn-Schmiedeberg拱的杂志1996年;354.:262-267年。
-
Hannon JP,Bray-French Km,Phillips RM,Fozard Jr。腺苷受体亚型的进一步药理表征介导抑制氧化爆发在分离的人中性粒细胞中的抑制作用。药物开发Res1998年;43.:214-224年。
- ↵
Bouma Mg,Stad Rk,Van Den Wildenberg F,Buman WA。腺苷对激活的人单核细胞细胞因子释放的差分调节作用。J Immunol1994年;153.:4159-4168年。
- ↵
Collis MG, Hourani SMO。腺苷受体亚型。趋势Pharmacol Sci.1993年;14.:361.-366。
- ↵
Ledent C, vaugeis JM, Schiffmann SN,等等。缺乏腺苷A小鼠的攻击性、痛觉减退和高血压2A受体。自然1997年;388.:674.-678年。
- ↵
Feoktistov I,Goldstein Ae,Biaggioni I.在腺苷A中p38丝裂菌活性蛋白激酶和细胞外信号调节蛋白激酶激酶的作用2B.受体介导的人肥大细胞中的白细胞介素-8产生。摩尔杂志1999年;55.:726-734。
- ↵
Clancy JP,Ruiz Fe,Sorscher EJ。腺苷及其核苷酸通过a激活野生型和r117h cftr2B.受体耦合途径。是杂志1999年;276:C361-C369。
- ↵
Feoktistov I,Biaggioni I. Adenosine a2B.受体。杂志牧师1997年;49.:381.-402。
- ↵
Mundell SJ,Olah Me,Panettieri Ra JR,Benovic JL,Penn RB。通过外源和自分泌腺苷的人气道平滑肌中G蛋白偶联受体腺苷酸环酶反应的调节。AM J RECMIR CELL MOL BIOL2001;24.:155.-163年。
- ↵
口服茶碱对哮喘中腺苷诱导的支气管收缩的特异性拮抗作用。Br J Clin Pharmacol1985年;19.:685-692。
- ↵
Clarke H,Cushley MJ,Persson CG,Holgate St.静脉内培养基和烯丙基对组胺和腺苷5'-一磷酸刺激支气管内支气管的保护作用:对哮喘黄嘌呤衍生物作用机制的影响。米尔药戈尔1989年;2:147.-154。
- ↵
Thorne Jr,Danahay H,宽广克。致敏豚鼠肺和气管中腺苷受体激动剂的支气管素受体激动剂的反应分析。欧语J药狼1996年;316.:263-271年。
- ↵
Fozard Jr,Pfannkuche H-J,Schuurman H-J。腺苷肥大细胞脱粒3.大鼠的受体激活。欧语J药狼1996年;298.:293.-297年。
- ↵
谢培德,林丹,杜玲。腺苷导致血管收缩在活的有机体内.肥大细胞和A3.腺苷受体。中国保监会Res1996年;78:627.-634年。
- ↵
Kohno Y,Ji X,Mawhorter SD,Koshiba M,Jacobson Ka。激活A.3.人嗜酸性粒细胞上的腺苷受体升高了细胞内钙。血液1996年;88:3569-3574。
- ↵
郑旭,罗奇尼,白涛,王志强,王志强。腺苷一3.受体刺激抑制人嗜酸性粒细胞的迁移。J Leukoc Biol.1997年;62:465-468年。
- ↵
Ezeamuzie CI,飞利浦E.腺苷A3.人嗜酸性粒细胞的受体介导抑制脱脂和超氧化物阴离子释放。BR J Pharmacol.1999年;127.:188-194。
- ↵
Le-Vraux V, Chen YL, Masson I,等等。腺苷受体激动剂抑制人单核细胞TNF生成。生活SCI.1993年;52.:1917-1924。
- ↵
Gessi S,Varani K,Merighi S,等等。Jurkat T细胞A3腺苷受体的药理学和生化特征。BR J Pharmacol.2001;134.:116.-126。