摘要
在一项为期24周的双盲扩展至28周的核心试验中,研究了抗免疫球蛋白E药物omalizumab维持中重度过敏性哮喘患者长期疾病控制的能力。
在延长期间,最初的546名患者中有483人继续接受随机治疗,并在核心试验的类固醇减量阶段确定了最低可持续剂量的二丙酸倍氯米松(BDP)。允许同时使用哮喘药物,并且允许研究人员在必要时调整BDP剂量或将患者从BDP切换到其他哮喘药物。
更多的omalizumab治疗的患者(33.5%)比安慰剂治疗的患者(13.5%)能够在不需要吸入皮质类固醇治疗的情况下完成延长期。在整个延长期,奥玛珠单抗组的平均BDP当量剂量较低(25µg·天)−1)高于安慰剂组(43µg·天)−1).在延长治疗期间,76%的omalizumab患者维持了疾病控制,相比之下,59.4%的安慰剂患者没有哮喘加重。与安慰剂相比,奥玛珠单抗组在延长期间使用其他伴随哮喘药物的患者较少。omalizumab治疗耐受性良好,组间不良事件发生率相似。
总之,这些结果表明,奥玛珠单抗是一种有前途的长期控制过敏性哮喘的新药物。
这项研究由瑞士巴塞尔的诺华制药公司和美国CA南旧金山的基因泰克公司支持。
目前的哮喘管理指南强调联合药物治疗对控制潜在炎症疾病的重要性(如。吸入糖皮质激素),并缓解急性症状(如。具有短效吸入β2量受体激动剂)1,2.然而,一些患者在吸入高剂量皮质类固醇后仍有症状,并经常发作3.,4.此外,这种疗法的复杂性,如。使用不同给药频率的多个吸入器往往导致患者依从性差,这是长期成功控制疾病的主要障碍。因此,绝大多数患者的哮喘控制水平远远达不到哮喘长期管理的目标5.
近年来,越来越多的人认识到免疫球蛋白(Ig)‐E是过敏反应的关键中介,被认为是诱导和维持慢性气道炎症和哮喘相关症状的原因6.所有年龄的过敏性哮喘患者都有高于正常水平的血清IgE水平,这与支气管收缩器对各种刺激的反应增强和症状的发生有关7- - - - - -9.在这些患者中,接触过敏原会产生特征性的级联反应,由免疫效应细胞,特别是肥大细胞、T淋巴细胞和嗜酸性粒细胞协调10,11.因此,靶向参与过敏原特异性反应的因子,如IgE,是开发治疗哮喘的新治疗剂的一个有前途的基础。
Omalizumab (Xolair®,诺华制药公司,瑞士巴塞尔/Genentech公司,南旧金山,CA,美国)是一种重组人源单克隆抗IgE抗体,是首个在治疗IgE介导疾病方面进行临床评估的抗IgE药物12.Omalizumab通过与循环中未绑定的“自由”IgE结合来阻止过敏级联13.这导致游离IgE水平的显著降低和细胞IgE受体的下调14.单剂量omalizumab可使过敏性哮喘患者的游离IgE浓度迅速降低95%15- - - - - -17.
最近,作者报道了一项28周随机双盲、安慰剂对照试验的结果,该试验对象为吸入糖皮质激素无法充分控制的中重度过敏性哮喘患者。Omalizumab降低了哮喘发作的发生率和频率,同时减少了吸入皮质类固醇的需求18.omalizumab也改善了哮喘控制的其他指标,如症状评分、救援药物的需求和肺功能。Omalizumab具有良好的耐受性和良好的安全性。
在本研究中,报告了对核心研究进行24周双盲扩展的结果。
方法
研究设计与患者
核心研究的方法之前已经报道过18.简单地说,一项多中心、随机、双盲、安慰剂对照、平行组研究在欧洲、南非、澳大利亚和美国进行。患者在进入研究时均出现症状,尽管吸入糖皮质激素的剂量相当于500 - 1200µg·天−1二丙酸倍氯米松(BDP)。
在4-6周的磨合期,所有患者都改用吸入皮质甾体BDP治疗,以实现持续症状控制所需的最低剂量。磨合后,患者随机接受omalizumab或安慰剂,每2或4周皮下注射一次(≥0.016 mg·kg)−1·IgE(国际单位·mL−1)每4周)共28周。在治疗的前16周,BDP的剂量保持在恒定(类固醇稳定期)。在接下来的12周内,BDP的剂量逐渐减少,在临床可能的情况下,每2周减少基线剂量的25%,持续8周,以达到最低有效剂量(类固醇减少期)。在核心研究的剩余4周内,维持哮喘控制所需的最低BDP剂量。使用含有沙丁胺醇的抢救药物,由加压计量吸入器(100µg·扑−1),在整个研究过程中都被允许使用。不允许使用其他哮喘药物。
该研究是根据《赫尔辛基宣言》进行的,所有患者(或其法定监护人,如果患者<18岁)在进行研究程序之前都提供了书面同意。从每个研究中心的相关机构审查委员会获得伦理批准。
在核心研究之后进行了24周的双盲扩展,在此期间,患者继续接受随机治疗和最低有效剂量的BDP(可以相应地调整)。在延长阶段,允许使用伴随哮喘药物,允许研究人员在必要时给患者服用额外的哮喘药物和/或让患者改用其他哮喘药物。
结果测量
延长期间,哮喘加重,用力呼气量在一秒钟(FEV1), BDP的使用和伴随哮喘药物的使用进行评估。
急性发作定义为哮喘恶化,需要口服或静脉注射糖皮质激素治疗或患者最近BDP维持剂量的两倍。
由于在延长期间患者被允许从BDP改为其他吸入性皮质类固醇,因此根据美国国立卫生研究院哮喘诊断和管理指南制作了一个等效表,以便皮质类固醇的使用可以表示为“BDP等效”(表1)⇓).该等效表还用于确定在核心研究的磨合期间,当患者从常规吸入皮质甾体激素切换时给予的BDP剂量。
每次就诊均进行肺活量测定。要求患者在诊所肺功能测试前6小时内避免服用任何缓解药物。休息15分钟后,患者进行至少3次用力呼气动作。三个FEV中最高的1,记录每次访视所得的数值。在给药前进行肺功能检测。
在整个52周的研究中评估了omalizumab的长期安全性和耐受性。在研究期间,每2-4周收集一次不良事件的详细信息,记录所有事件,无论与研究药物的可疑关系,以及轻微、中度或严重程度。采用固相酶联免疫吸附法测定抗omalizumab抗体水平(Fab)19.
统计分析
使用所有进入延长期患者的数据进行统计分析。
使用通用Cochran-Mantel-Haenszel检验(van Elteren检验)分析每位患者哮喘加重的次数和至少经历一次哮喘加重的患者数量,并按给药计划分层(2或4周给药)。对在延长期过早停用的患者进行了调整,每2周错过延长期,在该阶段观察到的任何加重计数中增加一次加重。哮喘加重不被算作不良事件,除非它们很严重(如。导致住院)。这项研究证明了治疗之间在核心期哮喘加重数量上的差异18.
BDP剂量以核心研究剂量的基线百分比表示,在延长期每4周使用Wilcoxon-rank和检验进行分析。采用按给药计划分层的通用Cochran-Mantel-Haenszel检验,分析在延长治疗期间未使用吸入性皮质类固醇的患者百分比和整个延长治疗期间吸入性皮质类固醇剂量较基线减少≥50%的患者百分比。
FEV1采用协方差模型分析,拟合中心、性别、治疗计划和治疗为因素,基线为协变量进行分析。
不良事件发生率采用按给药计划分层的通用Cochran-Mantel-Haenszel试验进行检查。
以p<0.05(双侧)为统计学意义。所有的疗效参数分析在扩展进行事后.
结果
病人
随机分组到核心研究的546例(88%)患者中,共有483例(254例omalizumab, 229例安慰剂)进入了24周双盲扩展期。
安慰剂组(26.11.4%)的患者数量是omalizumab组(10.3.9%)的近3倍。撤回同意和失去随访是过早终止的最常见原因,在这两种情况下,安慰剂患者比omalizumab患者受影响更大。2例omalizumab患者因不良事件停用。导致停药的不良事件为前列腺癌和“眼、口、鼻窦严重干涩”。对第二例进行了广泛调查,发现在研究开始前1年症状已经出现。研究人员认为这两种情况都与研究药物无关。
表2报告了患者人口统计和基线特征的总结⇓.
哮喘急性加重
与核心研究一样,与安慰剂组相比,奥玛珠单抗组在延长期每位患者哮喘加重的次数显著降低(p<0.001)(表3)⇓).与安慰剂组相比,接受欧玛珠单抗治疗的患者经历至少一次病情加重的比例也显著降低(p<0.001)(表3)⇓).
二丙酸倍氯米松剂量
在延长期间,与安慰剂相比,接受omalizumab治疗的患者能够保持明显较低的吸入糖皮质激素摄入量(p<0.001)(图1)⇓).延长期间的平均BDP当量剂量为253µg·天−1在omalizumab组与434µg·天相比−1在安慰剂组。
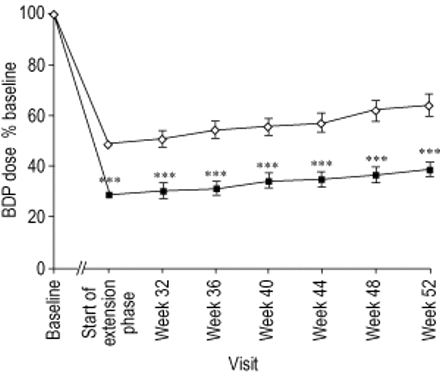
二丙酸倍氯米松(BDP)的等效剂量表示为基线的百分比。数据以均数±sem表示。▪:omalizumab;⋄安慰剂。* * *: p < 0.001与安慰剂。
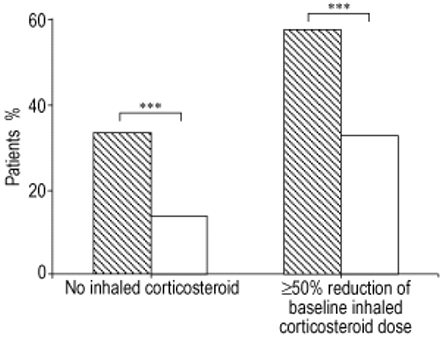
与安慰剂相比,奥玛珠单抗接受者在不需要任何吸入皮质类固醇治疗的情况下完成24周延长治疗的比例明显更高(图2⇓).此外,超过一半的omalizumab治疗患者使用相对于基线的≤50% BDP当量剂量的吸入皮质类固醇参与了延长(即。核心阶段开始)与大约三分之一的安慰剂接受者(图2⇓).
在延长期未使用吸入性皮质类固醇的患者,以及在整个延长期基线剂量减少≥50%的患者的百分比。镜像:omalizumab n=254;□安慰剂n=229。* * *: p < 0.001。
伴有哮喘药物的使用
在24周的延长期间,奥玛珠单抗组伴随哮喘药物的增加低于安慰剂组(表4)⇓).
一秒内用力呼气量
FEV差异无统计学意义1在延长期的任何时间点观察治疗组之间的差异。
安全性和耐受性
在核心研究中18, omalizumab治疗耐受性良好。在24周延长研究期间(p=0.548)和整个52周研究期间(p=0.579),治疗组之间不良事件的总体发生率具有可比性(表5)⇓).虽然在omalizumab组中检测到影响消化系统的不良事件(包括恶心、胃肠炎、腹泻、腹痛、消化不良和牙痛)发生率略高(影响32%的omalizumab患者)与在52周期间,25%的安慰剂患者),两组都没有常见的特殊不良事件。
9例(3.5%)omalizumab组患者和10例(4.4%)安慰剂组患者在延长治疗期间发生严重不良事件。这些患者包括4名(1.7%)安慰剂组患者和1名(0.4%)omalizumab组患者,他们经历了哮喘加重导致住院。
在24周的延长期间,没有出现提示免疫反应的不良事件。局部注射部位症状与5.3%的奥玛珠单抗注射组和4.3%的安慰剂注射组相关,其中大多数为轻度至中度严重程度。
使用omalizumab的患者没有出现抗omalizumab抗体。
讨论
抗炎药物被认为是治疗持续性哮喘患者的基石1.然而,目前的哮喘疗法的目的是在过敏过程开始后才减轻炎症和症状。由于IgE是过敏反应的诱导和进展的早期和核心因素,它是治疗哮喘的一个有前途的靶点。阻断IgE的一个明显优势是过敏级联在介质释放前的起始阶段被中断。
Omalizumab是一种重组人源单克隆抗IgE抗体,是首个在过敏性哮喘治疗中进行临床评估的抗IgE药物。本研究作者此前曾报道,在中重度过敏性哮喘患者中,28周的omalizumab治疗同时降低了哮喘加重和皮质类固醇需求,同时改善了疾病控制的其他参数18.这项为期24周的双盲扩展研究的结果显示,omalizumab继续降低哮喘加重的频率和发病率,同时允许持续减少吸入皮质类固醇和其他伴随哮喘药物的需求。
对延长期哮喘加重的分析显示,与安慰剂相比,奥玛珠单抗患者发生哮喘加重的人数显著减少。每位患者的平均恶化次数也显著降低,有利于omalizumab。这与核心研究期间的观察结果完全一致18即使使用omalizumab的患者保持较低剂量的吸入糖皮质激素,并使用较少的其他伴随哮喘药物,也能实现这一目标。安慰剂组在核心期观察到更频繁的停药趋势18持续延长,26例(11.4%)安慰剂患者过早终止延长,而10例(3.9%)omalizumab患者。这种不平衡可能反映了患者对治疗的总体满意度。
在延长治疗期间,与安慰剂组(32%)相比,更多的omalizumab组(57%)患者能够将吸入皮质类固醇剂量降低≥50%,并在整个延长治疗期间维持这一降低剂量。事实上,在延长的过程中,两个治疗组的吸入糖皮质激素剂量略有增加(图1)⇑)可能反映了在这一阶段,BDP剂量的变化和其他吸入性皮质类固醇的使用并没有被劝阻。
在临床试验中,哮喘的控制得到了显著改善,即使是对接受安慰剂治疗的患者也是如此。一种可能的解释是由于研究者的密切监测和反复鼓励坚持治疗方案而提高了依从性。需要长期治疗的哮喘患者的依从性往往很差,特别是那些需要吸入皮质类固醇的患者。在最近一项针对欧洲中重度持续性哮喘患者的调查中,最令人不安的发现是大量使用必要的支气管扩张剂药物,而少量使用抗炎药物5.新型哮喘药物,如omalizumab,大大减少了对吸入糖皮质激素的依赖,并且需要更少的给药频率,有可能通过提高依从性和促进长期治疗来改善哮喘控制。
两组FEV无显著差异1延长期治疗组之间的差异。这一结果并不出人意料。患者被允许在整个延长期同时使用哮喘药物,安慰剂治疗的患者比omalizumab治疗的患者使用更多的哮喘药物(表4)⇑).特别是,在本研究的这一阶段,支气管扩张剂的使用可能会混淆肺活量测定值。因此,添加一种不具有急性支气管扩张剂特性的抗炎剂,预计不会对FEV提供进一步的重大改善1.
其他研究也证明了这一点19, omalizumab的安全性是令人放心的,在整个52周的治疗期间,治疗具有良好的耐受性。
总之,本研究结果表明,omalizumab在过敏性哮喘患者的长期控制中是有效的,在控制疾病的同时减少皮质类固醇的需求。这些结果表明,奥玛珠单抗是一种很有前途的治疗过敏性哮喘的新药物。它可能特别适用于即使采用常规治疗也有持续症状的患者。该给药方案可大大提高需要复杂治疗方案的过敏性哮喘患者的依从性。此外,由于omalizumab对过敏性鼻炎的治疗有效19,对伴有肺、鼻、眼等症状的患者有益。
致谢
作者要感谢以下按国家列出的研究人员提供的患者数据。澳大利亚:鲁芬、西奇塔诺;奥地利: G.卡尔克;德国: C. Kroegel, K‐C Bergmann, H. Leiner;意大利: G.W. Canonica, G. D'Amato, G. Moscato, E. Marchi;荷兰: r.a albers, J.P.H.M. Creemers, E.F. Dubois, A. Greefhorst, P.B. Luursema, A. Sips;南非: A.P.福登,J.特布兰奇;英国: A. Millar, M. Spiteri, A. Tattersfield, K.F. Chung;美国: G. Bensch, T. Casale, L. Ford, A. Nayak, H. Beede, J. Yarbrough, S. Fineman, N. LaHood, G.G. Shapiro, J. Wolfe, E. Lisberg, T. Lee, A. Martin, H. Windom, B.Q. Lanier, W. Berger。
- 收到了2001年9月6日。
- 接受2002年2月8日
- ©ERS期刊有限公司