摘要
在最近的一例医源性库欣综合征病例中,一名囊性纤维化(CF)和过敏性支气管肺曲霉菌病患者使用伊曲康唑作为抗真菌药物治疗,布地奈德作为抗炎药物治疗,垂体-肾上腺轴完全抑制,这导致在作者的CF中心对所有使用伊曲康唑治疗的患者的垂体-肾上腺轴和性腺功能进行了系统评估。伊曲康唑可抑制CYP3A,从而干扰糖皮质激素、矿物皮质激素、雄激素、雌二醇的合成以及布地奈德的代谢。本研究的目的是评价伊曲康唑联合布地奈德或不联合布地奈德治疗患者的肾上腺和性腺功能。
25例同时使用伊曲康唑和布地奈德治疗的CF患者和12例单独使用伊曲康唑治疗的CF患者(6例CF患者和6例慢性肉芽肿性疾病患者)进行了促肾上腺皮质激素(ACTH)测试(250µg tetracosactid)。通过测量血浆-肾素、卵泡刺激素、黄体生成素、孕酮、雌二醇、睾酮、血清抑制素A和b来评估矿物皮质激素和性腺类固醇功能。另外30名CF患者的ACTH试验作为移植前计划的一部分作为对照。
同时使用伊曲康唑和布地奈德治疗的25例患者中有11例出现肾上腺功能不全。单独使用伊曲康唑治疗的患者和对照组CF患者均无病理性ACTH检测。在所有患者中未观察到矿物皮质激素和性腺功能不全。只有1例最初的病理acth测试患者随后恢复正常,其他10例患者在停止伊曲康唑治疗2-10个月后肾上腺功能有所改善,但仍未恢复正常。
在同时使用伊曲康唑和布地奈德治疗的25例囊性纤维化患者中,有11例观察到肾上腺糖皮质激素合成的抑制。其发病机制很可能是伊曲康唑通过降低/抑制代谢导致全身布地奈德浓度增加,从而抑制促肾上腺皮质激素分泌,并直接抑制类固醇生成。在联合治疗的患者中,建议定期筛查肾上腺功能不全。
过敏性支气管肺曲霉病(ABPA)的特点是双型免疫反应与免疫球蛋白(Ig) E和IgG抗体的真菌来自烟曲霉属真菌1.囊肿性纤维化(CF)患者的诊断率为~ 8%,支气管哮喘患者的诊断率为1-2%2- - - - - -4.与支气管哮喘患者一样,在CF患者中,ABPA的主要治疗方法是全身性糖皮质激素,但这与严重的副作用有关,特别是在生长中的儿童中5- - - - - -7.伊曲康唑是一种口服的三唑类抗真菌药物,最近被推荐用于治疗ABPA,作为一种有效的替代或类固醇保留疗法,没有严重的副作用8- - - - - -10.伊曲康唑与其他抗生素一样,由于支气管内屏障的存在和药代动力学的改变,尤其是肾排泄的增加,在CF患者中给予大剂量的使用11.布地奈德在许多CF中心作为消炎药使用12,13.大剂量布地奈德主要推荐给慢性感染的CF患者铜绿假单胞菌14但后来已扩展到包括其他细菌感染的CF患者。酮康唑和伊曲康唑等唑类是强抑制色素p450依赖酶,如17,20脱糖酶、16α-羟化酶、17α-羟化酶、18羟化酶和11β-羟化酶(活性下降),因此可能会影响肾上腺和性腺中的类固醇生成18,19.布地奈德经肝脏CYP3A代谢为16‐α‐羟泼尼松龙和6‐β‐羟布地奈德15,因此,在服用抑制CYP3A药物的个体中,代谢会降低。
由于伊曲康唑和布地奈德的药物相互作用,垂体-肾上腺轴和性腺类固醇生成的抑制频率在一组31例CF患者和6例慢性肉芽增生疾病(CGD)患者中进行了前瞻性研究,并与30例CF患者的对照组进行了比较,后者已作为移植前计划的一部分进行了测试。
患者与方法
病人
所有来自哥本哈根丹麦CF中心的接受伊曲康唑治疗的CF患者(n=31)都同意参加这项研究。截至1999年底,271例患者(11%)中31例(16名女性,15名男性,中位年龄18岁(9-33岁)接受大剂量伊曲康唑(400-600 mg·日)治疗−1, 10 mg·kg−1·天−1).5例患者同时使用强的松龙治疗,4例患者使用克拉霉素治疗。年龄在> ~ 15岁的女性中有8人使用口服避孕药,3人没有。5例年龄<15岁的女性患者中,1例为Tanner青春期4期,2例为4 - 5期,1例为5期,1例分期未知。
第1组:25例患者接受治疗,同时吸入大剂量布地奈德(spirrocort Turbohaler®,阿斯利康,阿尔贝特斯隆,丹麦)(800-1600µg每天,中位年龄18岁(范围9-33岁))和伊曲康唑。2组:6例患者单独应用伊曲康唑治疗。第3组:6例CGD患者,连续预防性服用大剂量伊曲康唑治疗ABPA(女2例,男4例),中位年龄24岁(15-32岁)。这些患者均未或曾使用布地奈德或克拉霉素治疗。第4组:将30例CF患者的促肾上腺皮质激素(ACTH)测试结果作为回顾性对照组(14名女性,16名男性),中位年龄29岁(21-43岁)。ACTH测试已作为肺移植术前评估的一部分。这些患者均未使用伊曲康唑治疗,但其中24例已使用大剂量吸入布地奈德治疗数年。其余6例未使用糖皮质激素治疗。
后续
病理ACTH测试结果,未使用强的松龙治疗的患者,开始使用氢化可的松替代治疗(10-12 mg·m−2·天−1停用伊曲康唑后。如果患者哮喘症状没有恶化,则慢慢停用布地奈德治疗。停用伊曲康唑后,每隔1-3个月用ACTH试验重新检测肾上腺功能。
方法
糖皮质激素和矿物皮质激素的测量
促肾上腺皮质激素测试
分别于静脉注射前(时间0)、静脉注射后30、60 min (注射。)注射250µg tetracosactid (Synacthen®,诺华医疗保健,哥本哈根,丹麦)。正常反应定义为血浆皮质醇增加到至少500 nmol·L−160分钟后(AutoDelfia, Wallac,芬兰)。在测试时接受强的松龙治疗的患者在测试当天没有服用药物。在这些患者中,使用高效液相色谱法(Merck, Hitachi, Japan)测量皮质醇,这种方法避免了皮质醇和强的松龙之间的交叉反应。
血浆促肾上腺皮质激素
在时间0时测量血浆ACTH(正常范围2-11 pmol·L)−1)使用放射免疫分析法(RIA) (Nichols研究所,诊断,CA,美国)。
统计数据
两组间比较采用非参数Mann-Whitney U检验进行统计学分析。对于两组以上的比较,采用非参数Kruskall-Wallis检验。p<0.05被认为是显著的。
道德
获得了伦理批准((KF) 01-046/00),研究根据赫尔辛基II宣言进行。
结果
糖皮质激素和矿物皮质激素功能
用伊曲康唑和布地奈德治疗的25例CF患者中有11例(44%)发现ACTH试验的病理低反应(1a组)(表1)⇓).11例患者中有8例血浆ACTH较低,2例正常,1例最初未测量血浆ACTH,但随后的分析显示正常(表1)⇓).部分患者接受泼尼松龙或克拉霉素治疗(表1)⇓).1例患者出现库欣综合征,伴月亮脸、条纹、面部毛发生长、头痛、情绪波动、胰岛素需求增加、糖尿病调节异常、HbA1c升高和月经不调(表1)⇓,病人没有。3)。
其余14例使用伊曲康唑和布地奈德治疗的CF患者(1b组)和6例单独使用伊曲康唑治疗的CF患者(2组)对ACTH测试反应正常(图1)⇓).2例患者使用克拉霉素治疗,2例患者使用泼尼松龙治疗。血浆- acth水平正常(图2)⇓).
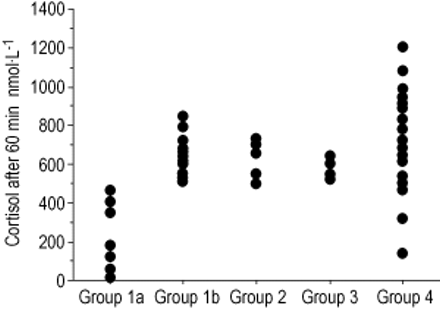
采用布地奈德和伊曲康唑治疗、对促肾上腺皮质激素试验反应低的患者(1a组,n=11)、采用布地奈德和伊曲康唑治疗、对促肾上腺皮质激素试验反应正常的患者(1b组,n=14)、单独使用伊曲康唑治疗的患者(2组,n=6)、采用伊曲康唑治疗的慢性肉芽肿性疾病患者(3组,n=6)在用四曲actid刺激60 min后血浆皮质醇最高水平(250µg)。对照组(第4组,n=30)。正常反应的最低水平是500 nmol·L−1.4组有2例<500 nmol·L−1由于在测试时使用了强的松龙。
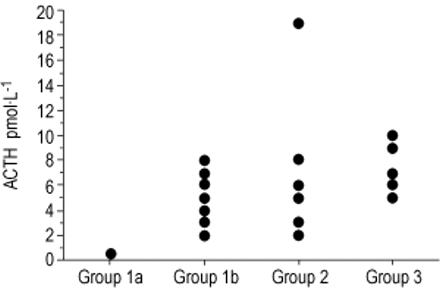
用布地奈德和伊曲康唑治疗但对ACTH试验反应低的患者(1a组,n=11)、用布地奈德和伊曲康唑治疗但对ACTH试验反应正常的患者(1b组,n=14)、单独用伊曲康唑治疗的患者(2组,n=6)、用伊曲康唑治疗的慢性肉芽肿性疾病患者(3组,n=6)的血浆促肾上腺皮质(ACTH)水平。
对ACTH试验病理反应低的CF患者的伊曲康唑累积剂量与对ACTH试验反应正常的CF患者的伊曲康唑累积剂量无显著差异(中位数420 g(范围3-788 g)。与453克(4.8-1047克)(p=0.95)。
单独使用伊曲康唑治疗的所有6名CGD患者(3组)对ACTH试验反应正常(图1)⇑)以及正常范围内的血浆ACTH(图2⇑).不同组间血浆ACTH值无统计学差异(p=0.1)。
对照组30例CF患者中,24例单独接受高剂量布地奈德治疗(组4),对ACTH试验有正常反应(图1)⇑).在这些患者中未检测到血浆促肾上腺皮质激素。
31例接受伊曲康唑治疗的CF患者血浆-肾素浓度正常(1a组:中位数21,范围7-84 mIU·L),均未观察到矿物皮质激素不足−1;1b组:中位18,范围5-46 mIU·L−1;第2组:中位数14,范围4-53 mIU·L−1;第三组:中位数21,范围11-107 mIU·L−1).肾素值在组内无统计学差异(p=0.9)。第4组未进行肾素测量。
性腺的函数
在接受伊曲康唑治疗的31例CF患者或6例CGD患者中,没有观察到性激素分泌的抑制。1例男性CF患者出现高促卵泡激素(FSH) (24.9 nmol·L)−1)和低血清抑制素B (<20 pg·mL−1)水平的观察表明缺乏支持细胞功能与目前的调查和正在研究的疾病无关。
后续
大多数最初进行病理性ACTH检测的患者病情改善,但在2-10个月的随访后,肾上腺功能未恢复正常(表1)⇑).6例患者停用伊曲康唑后,四麻药刺激的血浆皮质醇水平升高至~ 250-400 nmol·L−1.随后的测试仅显示肾上腺功能有缓慢的进一步改善。在2例患者中,以标准剂量氢化可的松替代可导致库欣综合征症状,包括月脸和糖耐量恶化。
停用伊曲康唑后,所有患者均接受特异性IgG亚类抗体严密控制答:来自烟24以便跟踪ABPA的活动。对于特异性IgG亚类抗体增加和ABPA临床症状加重的患者,停用布地奈德后重新开始伊曲康唑治疗。
在所有初始ACTH测试正常的CF和CGD患者中,大约3个月后进行了再次测试。所有这些患者的检测均正常。
讨论
25例接受伊曲康唑和布地奈德联合治疗的ABPA患者中有11例发现肾上腺功能不全。只有同时使用伊曲康唑和布地奈德治疗的患者出现肾上腺功能不全,而单独使用伊曲康唑或布地奈德治疗的患者均无肾上腺功能不全。11例肾上腺功能不全患者均无严重疾病或其他创伤。
在一名患者中观察到肾上腺皮质醇合成抑制并伴有库欣综合征,很可能代表布地奈德和伊曲康唑之间的药理相互作用。因此,本例患者的库欣综合征可能是由于抑制CYP3A4而导致布地奈德全身浓度增加,进而抑制垂体ACTH产生导致肾上腺功能不全。此外,伊曲康唑可抑制肾上腺甾体生成25.
唑类化合物的抗真菌活性是通过与细胞色素P450介导的14-去甲基化酶的结合和失活来发挥的,14-去甲基化酶负责将蓝甾醇转化为麦角甾醇,麦角甾醇是真菌膜的重要成分8,26.酮康唑已知可产生临床相关的相互作用27,并用于某些患者以控制垂体或肾上腺来源的高皮质醇症28,29.尽管伊曲康唑对CYP3A的抑制作用比酮康唑弱10倍在体外30.,是多种CYP3A4药物代谢的有效抑制剂在活的有机体内,包括一些合成糖皮质激素如。地塞米松和甲基强的松17.尽管其他唑类化合物(伊曲康唑、氟康唑和咪康唑)对真菌的亲和力高于人类酶系统,并且被认为诱导的副作用较小26,27,31在美国,这些药物在大剂量和长时间服用时也可能损害肾上腺功能25.
所有肾上腺功能不全患者血浆ACTH水平极低,提示布地奈德代谢降低可能是主要问题。如果伊曲康唑仅显著抑制类固醇生成,则应测量低血浆皮质醇水平的高水平血浆acth。伊曲康唑停药后,四麻药刺激的皮质醇水平最初仅达到低于正常水平。伊曲康唑,由于其在血浆中的半衰期长(天),特殊的动力学性质和高积累在各种组织32,33可能在细胞内作用较长一段时间,这可能解释了为什么停药后轴的抑制持续较长一段时间。促肾上腺皮质激素分泌提前达到正常水平,这可能反映了血清布地奈德的减少,从而重新建立了完整的垂体-肾上腺负反馈机制。
此前曾报道过口服糖皮质激素联合伊曲康唑治疗库欣综合征的患者34,35.病例研究库欣综合征和肾上腺抑制由于吸入类固醇治疗也有报道36,37.因此,每日剂量800-4,000µg二丙酸倍氯米松(BDP)(平均1465µg·天−1)可引起中度剂量依赖性肾上腺皮质抑制,但通过低剂量ACTH试验评估,BDP或布地奈德剂量较低(250-1058µg·m)−2,平均507µg·m−2)也会损害肾上腺功能37- - - - - -39.内源性皮质醇的产生可减少~ 20%的易感个体治疗剂量800微克布地奈德,每天两次40,41.然而,作者先前已经表明,布地奈德作为一种抗炎药长期用于CF患者,每日剂量为1,600µg,不会抑制肾上腺功能14.氢化可的松代谢也可能受损,如在标准剂量替代治疗期间出现库欣样症状的患者所见,因为该药物的代谢途径与布地奈德相同。
伊曲康唑和布地奈德之间的相互作用,诱导布地奈德的全身高水平,可能部分解释了报道的降低糖皮质激素剂量的能力6,9,10,42,43.如果是这种情况,使用伊曲康唑可以“节省”类固醇的剂量,但它的作用或副作用仍然存在。
一些作者提出,在伊曲康唑治疗期间,由于低钾、水肿和高血压的存在,可能存在药物性康氏综合征25,44- - - - - -46.在本研究中,正常的血浆-肾素水平表明,在任何患者中都没有涉及矿物皮质激素分泌。酮康唑与许多性腺不良反应有关,即。睾酮合成抑制,男性乳房发育和阳痿47- - - - - -49.然而,在目前的研究中,没有在任何患者中观察到性腺类固醇的抑制。据报道伊曲康唑对11β-羟化酶有更高的敏感性,并且相对保留C17-20裂解酶的活性(和雄激素活性)。25,26,34,这可能解释了肾上腺抑制而无性腺抑制的原因。
克拉霉素是一种大环内酯类抗生素,用于治疗CF患者的非典型分枝杆菌,对CYP3A有抑制作用,可能会干扰布地奈德的代谢50- - - - - -52但与伊曲康唑合用时应谨慎。此外,克拉霉素和伊曲康唑之间的双向相互作用,通过它们对CYP 3A4活性的影响,可能导致两者水平的升高53.
最近的研究推荐伊曲康唑作为有效的和类固醇保留治疗ABPA6,9,10,42,43.在一些患者中,ABPA临床症状的恶化和特异性IgG亚类抗体的增加答:来自烟结果再次给伊曲康唑。这些患者在重新开始伊曲康唑治疗后2-3个月内未观察到皮质醇产生的抑制。
肾上腺抑制似乎仅在布地奈德联合伊曲康唑治疗的患者中是一种风险,但它并不包括所有联合治疗的患者,尽管其累积剂量和治疗持续时间相似。副作用是由于全身类固醇浓度高、炎症和灌注程度影响吸收、治疗剂量和持续时间或个体受体易感性,目前尚不清楚。此外,个体患者中CYP3A4的数量差异很大,可能与抑制的程度相关,从而与给定抑制剂的可能效果相关。最后,同时服用其他药物可能会诱导或抑制CYP 3A4活性。
综上所述,当伊曲康唑或其他强效CYP3A抑制剂与类固醇(包括吸入类固醇如布地奈德)同时使用时应谨慎。作者建议对这类患者定期进行肾上腺功能不全检查。在肾上腺功能不全的情况下,氢化可的松替代需要额外的仔细监测,因为氢化可的松的代谢也可能受到损害。
- 收到了2001年5月29日。
- 接受2002年1月17日
- ©ERS期刊有限公司