抽象的
推测肥大细胞在气道壁上的分布和激活可能反映了它们在哮喘中的作用。
研究了从患有致命哮喘,非哮喘哮喘和非降压对照病例上的尸体术中的气道舱内施用桅杆舱内(完整和溶解)的密度。
在软骨性气道中,对照组肥大细胞的平均±se密度为27±9细胞·mm−2..它在非哮喘哮喘(24±2个细胞·mm−2.)致死性哮喘组(16±2个细胞·mm)减少(p<0.05)−2.). 在膜性气道中,对照组肥大细胞密度为155±21个细胞·mm−2.在非常规(270±51个细胞·mm的情况下,更高(p <0.05)−2.)和致命性哮喘(219±26细胞·mm)−2.). 软骨气道的平滑肌和粘液腺以及膜气道的平滑肌和外气道壁上的肥大细胞密度最大。哮喘患者脱颗粒肥大细胞的百分比较高(p<0.05),与疾病严重程度有关,软骨气道的脱颗粒肥大细胞百分比高于膜气道。致命性哮喘患者的平滑肌脱颗粒最大。
肥大细胞分布和脱颗粒在软骨气道和膜气道之间以及穿过气道壁时有所不同。肥大细胞脱颗粒与哮喘严重程度有关。近端气道脱颗粒的增加可能反映了刺激通过吸入途径。
该研究得到了澳大利亚西澳大利亚州西澳大利亚州哮喘基金会的支持。
哮喘是一种疾病,其特征在于气道炎症1.和改造2.. 有人提出,但尚未证实,炎症导致重塑。
炎症细胞与气道壁结构(受到重塑)相互作用的程度取决于气道壁上的炎症细胞的分布。两项研究3.,4.与非抗议的气道相比,已经显示出在隔离敏化的人支气管中的平滑肌层上发现的肥大细胞数量的增加。肥大细胞存在于哮喘患者的不同数量中5.–10.它们在炎症反应中的作用与它们储存、释放或合成的能力有关从头,炎症的介质11. 肥大细胞衍生介质的多重作用表明肥大细胞可能与气道结构相互作用。
当肥大细胞被激活时,它们部分或完全脱粒5..然而,这在哮喘中发生的程度及其与疾病严重程度的关系尚未量化。用于研究大小气道中气道壁上炎性细胞分布的进一步理由是确定通过抽样近端支气管树评估炎症的程度代表远端支气管中的气道炎症。因此,本研究的目的是检查肥大细胞的分布及其在没有呼吸道疾病的大型和小型气道的气道壁内的缩减程度,并将它们与哮喘患者进行比较。
方法
情况下
如果死亡原因是哮喘或突然死亡,而没有胸部创伤或疾病(哮喘除外),则在验尸官尸检时获得左肺或右肺。从家庭成员、通常的医生和医院档案中追溯获得病史。如前所述2.,病例分类如下。1) 对照组:无哮喘、喘息、使用哮喘药物或其他肺部疾病史;2) 非致命性哮喘:非呼吸性猝死,但有明确的哮喘史;3)致命性哮喘:仅因哮喘而死亡。如果无法获得病史的详细信息,则将病例排除在研究之外。该研究获得了查尔斯·盖尔德爵士医院伦理委员会的伦理批准。
组织学准备
肺部固定在福尔马林中,切割亚型型气道的横向块,切割副段水平,导致每种情况下12-18个大的软骨通气,从中随机选择该研究。从肺部血管切片中随机拍摄六个实质部分(3×2×1cm)。切割组织切片(5μm)并使用免疫氧化酶技术用抗氨酸氧化酶技术染色,用抗体细胞胰蛋白酶单克隆抗体AA1(Dako Patts,丹麦,丹麦)。
气道尺寸
如前所述,测量气道尺寸(气道内外壁厚度以及平滑肌、粘膜下腺体和软骨的面积)2..基底膜周长(Pbm)是直接用摄像机和数字化平板来追踪的。
细胞计数
计数具有可见细胞核的肥大细胞,并将其表示为前面讨论的每个隔室和细胞的总数−2.每个隔室区域(细胞密度)。计算每个气道隔间中的总气道桅杆计数的百分比。
能脱粒
在高倍镜下(×400),如果阳性染色的有核肥大细胞致密、致密、胞质边界完整且周围没有任何阳性染色颗粒,则将其归类为完整的有核肥大细胞(图。 1.⇓).所有其他有核的胰蛋白酶阳性细胞被分类为脱颗粒细胞(图2)⇓).将溶液的细胞表达为整个气道部分和每个隔室的核心AA1阳性细胞总数的%。
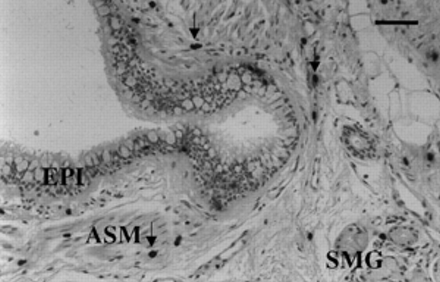
大的软骨通气道的横截面,显示在气道壁中存在的肥大细胞胰蛋白酶阳性细胞(箭头),包括上皮(EPI),气道平滑肌(ASM)和粘膜粘液腺(SMG)。大多数肥大细胞表现出浓密的均匀染色,细胞外胰蛋白酶阳性小,并且被归类为完整的肥大细胞。秤栏=100μm。
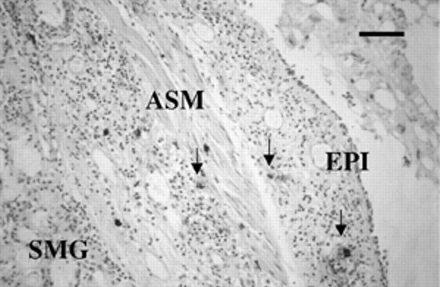
大软骨型气道的横截面,显示出现在气道墙壁中的肥大细胞胰蛋白酶阳性细胞(箭头),其显示出损坏的上皮(EPI),气道平滑肌(ASM)和粘液粘膜(SMG)。在本节中,大多数肥大细胞证明缺乏致密的均匀染色和丰富的细胞外胰蛋白酶阳性(箭头),并被归类为稀释的肥大细胞。秤栏=100μm。
如前所述,根据气道尺寸、细胞计数和脱颗粒指数计算观察者内误差2..所有测量都是由一名观察员(N.G. Carroll)进行的,不了解病例历史。
数据分析
从每种情况的装置计算的每个案例组的平均值用于分析。Bartlett对差异的均匀性的测试进行了。如果数据通常分布,则使用参数分析测试组之间的差异(方差的一种方式分析(ANOVA)),并且在通常不分布的情况下,使用非参数测试(Kruskal-wallis非参数Anova),然后使用DUNN的多个比较测试。概率值<5%被认为是显着的。
结果
总气道壁
在三个病例组中的每一个中检查的软骨或膜气道的大小(PBM)没有显着差异(表2⇓).
在软骨性气道中,非致死性哮喘和对照组横切面肥大细胞的绝对数量和密度均高于致死性哮喘(p<0.05)。在膜性气道中,致死性和非致死性哮喘患者的死亡率高于对照组(p<0.05)⇑).
气道墙隔室中的桅杆细胞密度
软骨航空公司
图3一⇓显示软骨性气道中不同气道壁室的肥大细胞密度。在对照组中,肥大细胞在气道壁上的密度变化为>50倍,平滑肌上的密度最高(74±17个细胞·mm)−2.),位于内气道壁中间(35±3个细胞·mm)−2.),粘膜腺(39±9个细胞·mm−2.)和外气道壁(7±1个细胞·mm)−2.),上皮细胞最少(1.5±0.4 cells·mm)−2.)和腔(0.2±0.1细胞·mm−2.).在粘膜粘膜腺中,在支撑基质组织内看到所有肥大细胞围绕着腺体,并且在个体浆液或粘液中没有细胞。在非致哮喘和致命病例中观察到类似的模式。然而,与对照例相比,密度在平滑肌,内气道壁和非致命情况下的上皮和致命情况下显着降低(P <0.05)。与哮喘的非致命病例相比,腔内中的肥大细胞密度较高(P <0.05),两者都高于对照案例(P <0.05)。与致命哮喘和对照的致命病例相比,粘膜腺体上的粘液细胞密度明显高(P <0.05)。在外气道墙中,案例组之间没有显着差异。
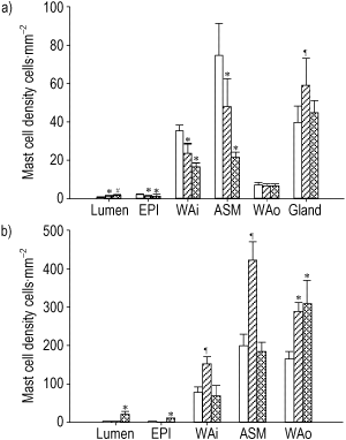
a)软骨和b)膜性气道中的肥大细胞密度。EPI:上皮细胞;WAi:内气道壁;ASM:气道平滑肌;WAo:外气道壁;腺:粘膜下粘膜腺。□:控制;├——3:非致命哮喘病例; :致命的哮喘个案。*:与对照组比较p<0.05;#:P <0.05与对照和非耐旱性相比;¶:与对照组和死亡病例相比,p<0.05。
:致命的哮喘个案。*:与对照组比较p<0.05;#:P <0.05与对照和非耐旱性相比;¶:与对照组和死亡病例相比,p<0.05。
不同气道壁室中肥大细胞总数的百分比
软骨航空公司
图4一⇓显示了软骨性气道中不同气道壁室中总肥大细胞的百分比。在气道壁内,肥大细胞在三个病例组中进入不同隔间的分布相似,除了粘膜下粘液腺,在哮喘病例中,总肥大细胞的百分比较高。在横切面上,肥大细胞在气管内壁和气管外壁所占比例最高。在上皮细胞中,对照组的肥大细胞百分比高于致死性和非致死性哮喘患者(p<0.05),而在气道腔中,致死性哮喘患者的肥大细胞百分比高于非致死性哮喘患者和对照组(p<0.05)。
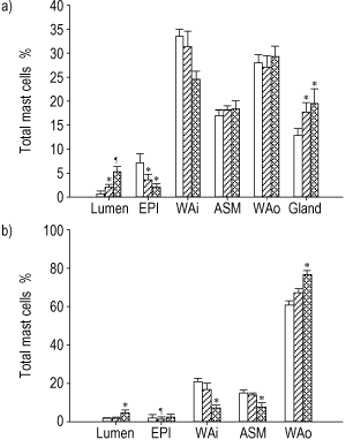
a)软骨气道和b)膜气道中肥大细胞总数的百分比。上皮细胞;WAi:内气道壁;气道平滑肌;WAo:外气道壁;腺体:粘膜下腺体。□: 控制└: 非致死性哮喘病例; :致命的哮喘个案。*:与对照组比较p<0.05;#:P <0.05与对照和非常规情况相比。
:致命的哮喘个案。*:与对照组比较p<0.05;#:P <0.05与对照和非常规情况相比。
膜的航空公司
图4 b⇑显示膜性气道中不同气道壁室中肥大细胞总数的百分比。肥大细胞的最大百分比出现在外气道壁,即膜性气道的最大隔室。在致死性哮喘患者中,与对照组和非致死性哮喘患者相比,外气道壁和气道腔的肥大细胞百分比较高(p<0.05),而内气道壁和气道平滑肌的肥大细胞百分比较低(p<0.05)。与非致命性哮喘相比,致命性哮喘和对照组的上皮中肥大细胞总数百分比较高(p<0.05)。
脱颗粒
在所有病例组中,软骨性气道中脱颗粒肥大细胞的平均百分比高于膜性气道(p<0.05)。与对照组相比,非致死性哮喘患者的脱颗粒肥大细胞百分比更高(p<0.05),致死性哮喘患者的脱颗粒肥大细胞百分比更高(表2)⇑).在软骨上,在不同的气道壁隔室中,控制和哮喘壳体组之间的脱粒差异(图5A⇓)和膜状(图5b)⇓)三个案例组的气道。然而,在致命哮喘的情况下,与对照和非哮喘哮喘案例相比,气道平滑肌肥大细胞下降显着升高。
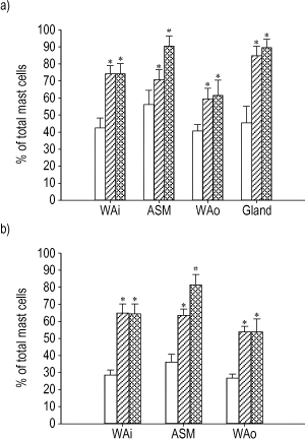
a)软骨气道和b)膜气道中脱颗粒肥大细胞的百分比。WAi:内气道壁;气道平滑肌;WAo:外气道壁;腺体:粘膜下腺体。□: 控制└: 非致死性哮喘病例; :致命的哮喘个案。*:与对照组比较p<0.05;#:P <0.05与对照和非常规情况相比。
:致命的哮喘个案。*:与对照组比较p<0.05;#:P <0.05与对照和非常规情况相比。
观察误差的变异系数为3%的气道尺寸,11%的细胞计数和10%的脱颗粒指数。
讨论
可以从检查气道墙上的桅杆细胞分布来获得洞察。首先,大库石气管的支气管活组织检查的小样本的程度在于可以评估气道墙壁或者在支气管树中更远侧位点的炎性过程的代表。本研究表明,内壁中的桅杆细胞密度不同于外气道墙壁,平滑肌和粘液腺体中的桅杆细胞密度。此外,近端气道的密度远低于远端气道的密度。其次,平滑肌和粘膜中相对较高的细胞密度表明它们可能在调节这些组织的功能方面是重要的。第三,肥大细胞扩滴对哮喘严重程度的关系表明,作为气道壁炎症中的效应细胞的活跃作用。第四,与膜支气管相比,软骨中的较数升级的桅杆细胞与激活这些细胞的吸入刺激相比一致。
本研究中的肥大细胞数量既显示为每横截面的总数,也为密度(细胞数·mm−2.测量区域)。该细胞编号估计方法是三维(3D)结构内的单元的简档计数,并且如果不满足某些条件,则可能受到偏差12.首先,需要以一种系统的随机方式对组织和感兴趣的领域进行取样。其次,所有感兴趣的细胞都必须有相同的被计数的概率。这主要取决于单元格的大小和方向。第三,测量参考区(即如果要确定气道体积中的绝对细胞数,则二维(2D)剖面面积应与该剖面所代表的三维体积相关。在本研究中,从肺采集到单个气道阻塞和切片的采样过程是系统和随机的。免疫组化染色鉴定细胞,但只有有核的细胞计数。肥大细胞核的大小无明显变化13与本研究中测量的参考部分相比,这个比例很小。由于作者无法定义全肺的初始参考体积,并且没有使用“查找”切片,因此本研究中的二维剖面计数无法转换为绝对细胞数的三维体积估计。然而,由于组间细胞核大小和方向不太可能发生系统的改变,作者认为这些限制不会影响组间比较。由于测量变异性主要是由于受试者和组织块变异性14,从肺部不同部位随机选择大量气道进行检查,并使用每个病例的平均数据比较各组间的细胞数量。因此,本研究中各组之间的相对细胞密度比较是有效的,并使数据与以这种方式报告细胞数量的许多其他已发表研究直接可比。
以前的气通道中桅杆细胞数的研究表明,与对照病例相比,哮喘的含量较高5.,6.,减少了8.,或类似.9,10,15,16肥大细胞的数量。研究之间的差异可能是由于哮喘严重程度的差异、不同方法的使用、治疗效果和脱颗粒程度的差异17–20. 据作者所知,以前没有研究系统地量化肥大细胞脱颗粒。高浓度的肥大细胞衍生介质,如组胺、前列腺素D2.(PGD2.),在局部过敏原攻击后的早期和后期哮喘反应中,白酮丙烯C4(LTC4)和胰蛋白酶液中观察到的白血管肺泡(BAL)液体21,提示肥大细胞脱颗粒。致死性哮喘患者的脱颗粒量最大,表明这些患者的肥大细胞活化增加。此外,在这些情况下,脱颗粒的增加可能导致对肥大细胞数量的低估(即不计数没有颗粒的细胞)。
在致死性哮喘病例中,肥大细胞脱颗粒量在粘膜下粘膜腺和气道平滑肌层最多。Pesciet al。22表现出慢性支气管炎患者粘膜腺体中稀释的肥大细胞数量的增加,其含有过量的粘液生产的疾病和布拉德11观察到白细胞介素-6阳性肥大细胞集中在粘膜下腺体附近7..有很好的记录,肥大细胞衍生的蛋白酶能够作为有效的促助剂作用,并且该组胺从活性的肥大细胞中储存并分泌,刺激平滑肌缩短和血管扩张23. 作者之前已经证明,气道管腔粘液分泌增加,并伴有适度的平滑肌缩短体内,可引起气道过度狭窄24,这可能会导致哮喘发作25. 这些发现提示肥大细胞在哮喘急性发作期间是一个重要的效应细胞。
与其他气道墙隔室相比,在光滑肌室比较的情况下,肥大细胞密度最高的发现类似于AMIT的结果et al。3.伯杰呢et al。4..目前的研究是第一个定量证据,表明肥大细胞是气道平滑肌层的主要细胞,在非哮喘患者和哮喘患者中,而平滑肌层中存在的细胞大多是脱颗粒的。康奈尔大学8.在致死性哮喘病例中,发现在软骨支气管平滑肌层附近有肥大细胞的聚集。在哮喘急性发作期间,肥大细胞的激活可能导致化学介质的异常释放,导致平滑肌和粘液腺的过度刺激。这一假设得到了哮喘患者在变应原激发后BAL液中肥大细胞来源介质量升高的发现的支持26哮喘发作期患者活检中的肥大细胞数量低于无症状期27.
可能导致气道壁中的桅杆细胞数在哮喘加剧期间减少的一种潜在机制是细胞从气道墙到气道内腔的运动。这是通过致命哮喘病例腔内的肥大细胞较长百分比的肥大细胞的观察来支持,与非哮喘哮喘和非惊厥对照病例相比。此外,在过敏原 - 吸入攻击后,在Atopic哮喘症的痰中观察到更高数量的肥大细胞20.肥大细胞数量减少的另一个潜在机制是细胞凋亡的增加。虽然本研究未评估肥大细胞凋亡的程度,因此不能排除其作为细胞数量减少的机制,但持续性炎症条件通常以延迟或受损的凋亡为特征。
与膜状(远端)气道相比,软骨(近端)气道中,本研究中的肥大细胞脱粒程度较高。推测这是一个主要原因,这是由于吸入的刺激,沉积物的主要原因是沉积的肥大细胞脱落的主要刺激发生在近端支气管中的粘膜表面。在本研究中,在所有哮喘患者中粘液腺中的粘液细胞脱粒水平显着高于在外气道壁中观察到的粘液腺体,表明选择性刺激肥大细胞。可以解释这一点的机制是神经肽能够诱导肥大细胞脱粒28在气道上皮中存在丰富的胆碱能神经,其具有局部轴向粘膜腺体的局部轴向途径29.因此,在粘膜表面的刺激和随后的神经肽的释放可能导致粘液腺的肥大细胞脱滴量增加。
与对照组相比,哮喘患者软骨性气道肥大细胞密度明显低于膜性气道。同样,康奈尔的研究8.也有报道称,与对照组相比,致命性哮喘患者在软骨性气道中气道壁的肥大细胞数量减少。对轻度哮喘患者近端支气管树支气管活组织检查中肥大细胞数量的研究显示了变化,因为一些研究显示气道壁内肥大细胞增多5.,30,有些仅在上皮细胞内6.另一些人则没有任何区别9,10,15,16. 这种变异可能是由于脱颗粒、细胞凋亡或抗炎治疗的作用。尽管如此,本研究清楚地表明,从近端支气管树获得的支气管活检可能并不总是代表气道壁或整个支气管树的炎症模式。
总之,除了明确定义的角色immunoglobulin-E-dependent对抗原刺激的反应在哮喘等过敏性疾病,有可能是肥大细胞可能显著增强宿主非特异性反应的许多功能急性炎症刺激,如在哮喘患者运动,吸入冷空气和高渗盐水。在短期和长期治疗策略中,应考虑气道中肥大细胞的单独活动。
- 收到了二○○一年八月二十三日。
- 认可的2001年11月27日。
- ©ers Journals Ltd














