抽象的
近几十年来,在高收入国家稳步上升,包括支气管哮喘,干草发热和特应性皮炎,包括支气管哮喘,过敏性疾病的患病率。这种现象的潜在机制仍然很大程度上是未知的。由于自然突变率低,因此旨在改变环境和生活方式的条件,以为发挥重要作用。
流行病学和临床研究提供了间接证据,即感染可能会阻止特性和特应疾病的发展。这被称为“卫生假设”。根据卫生假设,病毒和/或细菌感染可以通过刺激对细菌感染和延迟型超敏反应涉及的致答复,抑制与特应性反应相关的T-辅助(TH)-2免疫应答。
特别是,产前和幼儿期被认为是建立和维持正常Th-1/Th-2平衡的关键。另一方面,一些研究表明,感染会加剧既定的过敏性疾病,例如支气管哮喘,气道高反应性和特应性皮炎。因此,病毒和/或微生物感染和/或其产品可能对过敏和哮喘的发育具有双向影响。
本综述将重点关注最近与过敏性疾病和传染病之间相互作用相关的发现,主要重点是细菌感染。
很好地确定过敏和哮喘是由遗传和环境因素之间复杂的相互作用产生的。尽管毫无疑问,在基因组中的多个位点的遗传多态性有助于这些病症的发展的易感性,但即时环境也在确定发病,维护和哮喘的发病时间,维持和严重程度方面发挥至关重要的作用。关于过敏和哮喘患病率急剧上升的压倒性证据,以及尤其是在世界各地的高收入国家的发病率的巨大证据,强调了环境的贡献1,2.许多研究表明,在过去几十年里,过敏性疾病的发病率增加了好几倍。这种增加不能仅仅用遗传因素来解释,因为自然突变率很低,基因组的重大变化不会在几代之内发生。因此,最近的研究重点是识别和隔离造成这一现象的环境因素。最近,人们提出了所谓的“卫生假说”来解释流行病学数据3.,4.
过敏和哮喘与深度免疫放松管制有关,其特征在于T杆杆(TH)-2 T细胞的过量生产。很好地确定,TH-2效应功能由TH-1 T细胞产生负面调节。Th-1细胞似乎在防御各种微生物抗原的防御中发挥着关键作用,包括细菌,病毒和真菌感染。Hygenie假设表明,感染频率降低,较严重的感染和预防感染例如频繁使用抗生素会预防TH-1的成熟,因此,在自然暴露于过敏原后会产生过敏原特异性TH-2免疫应答。
这篇综述的目的是讨论支持和反对卫生假说的证据,重点是细菌感染,在较小程度上,病毒抗原暴露。
T-Helper 1,T-Helper 2和T-Helper 3免疫偏差的概念
在过去二十年中,在很大程度上揭示了过敏性炎症的细胞和分子机制。理解过敏免疫应答调节的突破随着不同的T细胞效应子子集被称为T-Helper(Th)-1和Th-2的发现5,6.两种T细胞亚群的特征在于细胞因子产生的独特模式。TH-1细胞产生干扰素(IFN)-γ,白细胞介素(IL)-2和肿瘤坏死因子(TNF)-β。相比之下,TH-2细胞由IL-4,IL-5,IL-6和IL-10的独占生产定义5,6(图1⇓).Th-1细胞在宿主防御中发挥着重要作用,针对各种微生物,包括病毒,细菌和真菌抗原,有助于产生免疫球蛋白 - (Ig)M和IgG抗体,肉芽肿的形成和细胞毒性的发育T细胞应答。最近,最初用于描述CD4 T细胞子集的Th1 / Th2概念扩展到包括CD8 T细胞7,8.相比之下,Th-2 t细胞在防御蠕虫感染中起着关键作用。这种类型的感染需要嗜酸性粒细胞的募集和激活以及IgE抗体的形成9,10..
进一步的研究已经解决了在t细胞亚群形成中的放松是否可能在某些疾病中发挥重要的病理生理作用的问题。由于过敏性疾病的特征是IgE的产生和嗜酸性粒细胞的局部招募,所以在呼吸道和皮肤过敏患者中进行的广泛调查显示Th-2 t细胞亚群在过敏性炎症中的重要性就不足为奇了。这些细胞控制IgE产生的调节通过IL-4和IL-13释放。此外,嗜酸性粒细胞和肥大细胞生物学的某些方面也受到CTH-2细胞监测的,包括成熟,募集和活化。此外,IL-5表示嗜酸性粒细胞的重要存活因子通过预防凋亡11.,12..
最近,已发现第三个T细胞子集被称为TH-3(图1⇓).除了IL-4和IL-10外,t细胞亚群还可产生转化生长因子(TGF)-β13.- - - - - -15..TGF-β超家族由许多结构相关的调控蛋白组成,除TGF-β外,还包括其他调控蛋白1tgf -β5抑制素,活力,骨形态发生和相关的形态发生蛋白,所有这些都在细胞生物学的许多领域具有重要意义16..TGF-β的五种亚型具有相同的生物学活性。这个家族的原型是TGF-β1一种最初从人血小板纯化的细胞因子。有趣的是,人类血小板代表了TGF-β最浓烈的自然来源17..在哺乳动物物种中只有TGF-β1TGF -β2, TGF -β3.已被识别和克隆。
TFG-β由每个细胞谱系产生,并且展示各种部分拮抗和多样的功能(表1⇓)16..TGF-β在免疫激活(上调粘附分子、增强趋化性和增强IgA的产生)和免疫失活中发挥重要作用。在一定条件下,TGF-β抑制CD4和CD8 t细胞的增殖,下调b细胞的多种功能,包括免疫球蛋白的产生和自然杀伤(NK)细胞的活性18.- - - - - -24..此外,细胞毒性T细胞也在TGF-β存在下下调。分辨炎症,特别是在慢性炎症期间,导致纤维发生和血管生成。两者也在紧密控制TGF-β。在粘膜组织中观察到TGF-β表达。肠道和鼻粘膜组织中的表达模式引发了粘膜耐受领域的许多研究。有充足的证据表明,特别是在粘液部位TGF-β直接参与口腔耐受的调节和维持25.- - - - - -27..
T细胞效应器的形成和维护不代表免疫系统的静态和固定功能,而是在几种调节水平上运行的大量动态可塑性。首先,在T细胞发育的水平下,T细胞效应子亚型的发育取决于许多信号和因子在同源以及非同源时尚中递送。抗原呈递细胞吞噬细胞糖和工艺抗原和现有的抗原肽通过主要组织相容性ii类分子。这些抗原肽结合到内质网的MHC结合槽上,然后转运到细胞表面。MHC +肽复合物与α/β- t细胞受体结合。除了这一同源信号外,还发现了一些有助于th亚型发展的非同源信号(图1)⇓).例如,Th-1 t细胞的发育是由IL-12和IFN-α触发的,而Th-2 t细胞的发育需要初始的IL-428..然而,目的初始IL-4的细胞来源并未令人信服地确定。已提出肥大细胞和嗜碱粒细胞的来源29.,30..最近提出了一个新概念,即t细胞效应的二分法也反映在抗原提呈细胞的水平上。特别是Kaliniski等等。32.已经提出了类似类型的树突细胞(DC)被称为DC-1和DC-2,这促进了TH-1的发育相对分别为th-231.,32..
在预先存在的Th细胞亚群的水平上表现出第二级可塑性(图1⇓).例如,Th-1来源的细胞因子IFN-γ是Th-2免疫细胞最有效的抑制剂反之亦然IL-4,IL-10和较小程度TGF-β,抑制TH-1 T细胞功能。此外,已显示IL-12和IFN-γ抑制TH-3效应T细胞。Naive T细胞没有预编程为发展到任一个子集是非常重要的。然而,呈递细胞(APC)/ T细胞相互作用部位的微环境对于这些T细胞效应的发展是决定性的。一旦单个T细胞为某种TH表型命中,该决定是固定的。到目前为止,尚未向单个细胞水平显示从一种表型中的重定向到另一个T细胞表型。
如何决定t细胞效应器的发展,以及决定反应结果的因素是什么?到目前为止,微环境的个体成分已经被确定,它们在某些t细胞效应表型的发展中发挥作用。它们包括:1)APC类型(例如b细胞相对树突状细胞);2)抗原的性质;3)抗原剂量(低剂量)相对高剂量);4)抗原遭遇的部位(粘膜相对系统性);5)初始抗原引发的年龄(前,后,成人)和其他人。这一概念对于自然发生的免疫应答的发展具有很大的实际重要性。它意味着每次抗原被传送到T细胞时,必须根据这是有害的抗原或无害的抗原或无害的抗原或其无害的识别和决定,以及哪种类型的T细胞效应器响应代表最合适的答案。
概念:特应性婴儿一开始是辅助性弱体
Th-1、Th-2免疫偏差的概念也适用于怀孕情况。在过去的几年里,已经揭示了胎母界面是一个免疫调节的高度活跃的部位。由于胎儿组织被认为是表达来自父亲和母亲的组织相容性抗原(HLA)的经典异体移植,因此必须避免这种异体移植的排斥反应。免疫系统已经发展了几种策略来阻止父系HLA抗原的识别,随后发展了针对这些细胞的细胞毒性t细胞反应。实现这一目标的一个主要策略与Th-1/Th-2概念有关。由于CD4和CD8 Th-1 t细胞都有介导移植排斥反应的任务,因此必须抑制这种危险t细胞反应的发展。至少,这部分是由Th-2和Th-3表型的细胞因子的深刻上调完成的。事实上,IL-4, IL-10和TGF-β的高表达1已经在胎母界面得到证实了吗33..胎儿和母体细胞都有助于这些监管事件。
同时,发生胎儿免疫系统的发展,并且至少,T-和B细胞隔室在妊娠的17至20周内在功能上设立。然后准备好遇到抗原并发展成成熟的T细胞效应器的这些淋巴细胞。几种研究人员提供了这种活性免疫成熟过程的证据。现在很好地接受抗原特异性T细胞存在于脐带血(CB)中存在34.,35..这些细胞确实是胎儿和而不是母体起源。已经证实了对包括酪蛋白,乳蛋白,乳蛋白和卵巢蛋白以及针对无害环境抗原的T细胞反应,包括房屋粉尘和某些花粉过敏原的T细胞反应。通过新生儿中存在抗原特异性分泌IgA抗体(SIGA)的存在,表明了B细胞隔室的活跃的子宫内发育。再次检测到牛奶和母鸡的蛋蛋蛋白酶抗体35..
这种T细胞成熟发生在TH-2和TH-3偏置环境中。这种环境显然对晚期胎生和早期生育后期的TH-1和TH-2表型的发育产生了显着影响。
几项研究表明,与非风险新生儿相比,在风险的情况下,甚至进一步减少了IFN-γ生产量的TH-1容量(表2⇓).针对这一问题的研究在几个主要的方法学方面有所不同。华纳等等。36.和近藤等等。37.评估了过敏原刺激的CB单核细胞中细胞因子的产生,并分别对婴儿进行了1年和6年的随访。结果参数为特应性湿疹和皮肤试验反应性。相比之下,唐等等。38.和马丁内斯等等。39.使用CB细胞的丝粉聚根刺激并分别遵循群组一六年。通过Piccinni的研究评估过敏原特异性T细胞克隆的细胞因子图案等等。40他们报告了为期三年的跟踪调查。普雷斯科特和同事35.,41.研究过敏原特异性T细胞应答,并提供了两年的彻底随访。它们确定了转录和翻译水平的细胞因子产生。无论是否用过敏原或丝分裂剂刺激CB细胞,与非缺失对照相比,已经注意到在每种情况下产生IFN-γ的进一步减少的能力。虽然数据相对于抑制的TH-1免疫力非常一致,但TH-2免疫的模式仍然是辩论的问题。在大多数研究中,除了Prescott和同事的研究外,还没有调查Th-2细胞因子产量35.,41..这些报告提供了初步证据,表明IFN-γ的减少可能与此类婴儿Th-2细胞因子的增加甚至持续升高有关。然而,值得注意的是,队列的规模很小,随访时间也很短。需要对明确的队列进行进一步的纵向研究,以积累足够的数据,允许前瞻性免疫调节策略,以重新调整高危婴儿的Th1/Th2平衡。
母亲致敏优先利于动物研究获得了第一种实验证据,从动物研究中获得了后代发育(图2⇓).这些研究表明,正常健康小鼠的后代在出生时IFN-γ产生受损,而致敏母鼠的后代IFN-γ产生受损的程度更低。暴露于异源过敏原后,与非过敏原小鼠的后代相比,过敏原致敏小鼠的后代产生了加速的th -2驱动的免疫反应42..这些数据表明,怀孕期间存在的Th-2/Th-0免疫对形成出生后暴露过敏原的Th-1/Th-2 t细胞谱具有决定性影响。
在抗原特异性反应水平上评估Th-1免疫存在的一个可靠的生物标志物是延迟型超敏反应(DTH)的发展。这是一个众所周知的现象,例如,婴儿特应性皮炎表达抑制反应,召回抗原在这个测试。不能只执行此测试体内,但也体外通过评估对抗原的淋巴增殖反应。在这方面的有用的原型抗原是对Dipheria-Pertussis-tetanus(DPT)疫苗接种后的Tetanus毒素(TT)的增殖反应。最近普雷斯科特等等。43.发表了一个优雅的研究,其中在DPT疫苗接种后的2岁婴儿中评估了对TT的淋巴增殖反应。响应模式与血清IgE的水平相关。它们在表现出缺乏淋巴增殖反应的婴儿中发现了几倍较高的血清IgE。相比之下,患有DPT接种疫苗接种后对TT的阳性反应的婴儿具有降低的血清IgE水平43..同样,这种观察进一步强调了TH-1免疫(如通过存在的存在评估)和TH-2免疫(如血清IgE抗体水平评估)之间的反比关系。但是,关于这两个事件之间的因果关系的问题仍然是开放的。是否能够安装适当的TH-1免疫反应允许不受控制的TH-2免疫力发育,或者患有已经升高的TH-2免疫力的婴儿是否能够进行适当的DTH反应仍有待研究。
感染与过敏和哮喘的发展/恶化之间的关系
在过去几十年的许多研究中,哮喘和呼吸道感染的总体负担之间的反比关系已经被报道。表3总结了这些研究⇓.虽然这些研究与一个有趣的概念有关,但有关病毒感染对预防/抑制过敏和哮喘的影响的致原因关系仍然是一个开放的问题。
毫无疑问,普通感冒是儿童和成人哮喘恶化最常见的原因58.- - - - - -62..其基本机制已被广泛分析和审查63..一种作用模式可能是气道炎症的附加效应,这是由已经发炎的黏膜组织对病毒感染的炎症反应引起的。一些研究发现有儿童毛细支气管炎病史的儿童哮喘发病率增加51.- - - - - -53.,56.,57.,64.- - - - - -70.病毒感染哮喘患者具有增强的细胞因子反应,显然导致组织中长期淋巴细胞和嗜酸性积累71..早期儿童毛细支气管炎的主要原因之一是呼吸道合胞病毒感染,这将被Schwarze和Gelfand广泛讨论72.在本系列中。
来自这些研究的数据和进一步的实验研究(稍后讨论)表明感染和过敏原暴露之间的时间在免疫后果方面可能具有重要意义。在感染和过敏原在暴露之间差距的情况下,感染可能具有保护作用。相比之下,感染和过敏原的暴露和过敏性/哮喘患者的感染之间的紧密定时关系可能具有疾病加重作用。虽然支持哮喘患者与病毒感染的哮喘恶化概念的证据相对较强,但细菌呼吸道感染与喘息的恶化的关联仍然相对较弱。例外是慢性鼻窦炎和哮喘症状之间的关联。将对鼻窦鼻窦感染到哮喘的数据主要是缔结的,并已被几个调查人员报告73.- - - - - -78..然而,因果关系一直难以证明。鼻窦感染可能导致哮喘急性加重的机制是已知的,但可能包括细菌从上呼吸道到下呼吸道的播散(后鼻程理论),鼻-中-支气管反射或感染引起的β-肾上腺素能阻滞的增强。
分枝杆菌感染的问题和芽孢杆菌(Bacillus Calmette-guérin(BCG)疫苗接种
分枝杆菌感染与芽孢杆菌(Bacillus)疫苗接种(BCG)疫苗接种的关系代表了评估TH-1和TH-2免疫之间的关系的另一模型情况。细菌感染,例如,百日咳博德特氏菌,histeria monozyogenes.,牛结核分枝杆菌,利什曼原虫和其他许多原虫都与IFN-γ产生增加有关,反映了Th-1免疫对防御和保护的需求79.- - - - - -82..由先天免疫系统的细胞产生的细胞因子,包括巨噬细胞和NK细胞响应于结核分枝杆菌和/或其组件至少可以转移,至少体外从Th-2/Th-0到Th-1的特异性t细胞的发展。这些细胞因子包括IL-12和IFN-α,它们在Th-1效应细胞的发育中起重要作用。
通过Shirakawa发表了一个解决这个问题的第一项研究之一,由Shirakawa发表等等。59..提交人报告说,与阴性响应者相比,BCG免疫日本学科,哮喘症状和特性的其他几个索引因素,阳性结核菌患者的可能性显着较小,并且七年和12年之间的特应症状的缓解症状阳性结核菌素响应者更容易。对这些调查结果的解释得到了密集的争论。纳入本研究的所有婴儿都经历了广泛的BCG疫苗接种时间表是重要的。在六年岁时,结核蛋白无反应者已被重新签名。对这些结果的最有可能的解释是,特应地位和DTH反应之间的反向关联可以简单地反映TH-1 / TH-2响应性的不平衡。在BCG疫苗接种后未能响应与Atopic症状的发展而不是BCG疫苗接种相关反应本身.瑞典调查人员的研究结果进一步支持这种解释,同样表明出生后的BCG免疫不影响学龄儿童的特应性疾病的患病率83.,84..
然而,在几内亚比绍斯的皮肤测试反应性定义的基础上,BCG疫苗接种和特性之间的反比关系已经在几内亚比绍85..然而,在该研究中,卡介苗反应模式尚未得到评估。相反,在瑞典进行的一项对未选择儿童的研究发现,在瑞典出生的儿童中,与卡介苗相关的婴儿特应性疾病没有减少84..相比之下,在许多出生在亚洲和南美洲的移民儿童中,卡介苗与较低的特应性疾病患病率相关86..这种有趣的观察可能指出族裔群体的差异。
区分卡介苗接种和分枝杆菌感染是很重要的。最近,von Mutius等等。87.据报道,哮喘患病率和报告结核病之间的显着反比相关性。为了进一步探索这种流行病学现象的潜在机制,若干研究人员已经采用了动物模型系统88.- - - - - -90..在一个这样的模型中,ige高应答BALB/c小鼠在卵清蛋白致敏前感染卡介苗。值得注意的是,卡介苗含有减毒分枝杆菌,可导致此类动物严重的全身分枝杆菌感染。因此,这反映了兼性胞内生物全身性感染的模式情况。结果表明,在过敏致敏前感染可防止IgE/IgG1抗体反应、立即阳性皮肤试验反应和气道高反应的发生,并可预防过敏性气道炎症。与此同时,抗卵清蛋白特异性IgG2a抗体显著升高,反映出ova特异性Th-1反应而不是Th-2反应的发展88..进一步的研究表明,这种效果是介导的通过在IFN-γ受体敲除小鼠中,由于分枝杆菌感染的保护作用失去89..但是,IFN-γ调解这种效果的确切机制尚不清楚。有趣的是,似乎细菌不一定必须活着,以防止自杀以来的过敏反应histeria monozyogenes.,分枝杆菌vacae要么乳杆菌也可以抑制小鼠的过敏反应80,91..
细菌成分:脱氧核糖核酸
识别和表征能够影响TH-1 / TH-2平衡的细菌组分是重大兴趣。在这种情况下,已显示细菌脱氧核糖核酸(DNA)对免疫系统产生巨大作用92..细菌(而非哺乳动物)DNA对先天和适应性免疫系统的许多细胞都具有有丝分裂特性。这些特性是由于含有寡脱氧核苷酸(ODN)的未甲基化“CpG基序”。93.,94..影响人免疫应答的关键CPG基序由Gacgtt序列和GTCGTT中的小鼠定义。磷酸盐骨干似乎是CpG-ODNS表现出其免疫调节性质的必要前提。
这种CPG-ODN的免疫原性已经过度研究,特别是在鼠系统中95.- - - - - -99..它们直接与APC的某些子集相互作用,包括DC鸟类,NK和B细胞100..CPG-ODN的DC激活导致抗原分子的表达水平增加以及抗原呈递和引发的增加101.,102..在几小时内,正在表达几个食芯碱和细胞因子,特别是IL-12,IFN-α和TNF-α,所有这些都在TH-1促销中发挥着重要作用。单核细胞和巨噬细胞表现出增加的抗体依赖性细胞细胞毒性。IL-12,TNF-α和IFN-α对NK细胞活性有直接影响103..它们能诱导IFN-γ,提高NK细胞的溶细胞活性。CpG-ODN在较小程度上也影响b细胞的活性104..b细胞迅速产生IL-6和IL-10,并表达水平增加的共刺激分子105..虽然t细胞不直接被CpG-ODN激活,但其反应和激活方式受到间接影响通过加强对APC的响应情况。因此,在CD4和CD8 t细胞亚群水平上的Th-1效应细胞的发育是暴露于CpG-ODN的一个主要结果106..
细菌和细菌提取物在治疗特别恶性疾病方面的治疗潜力一百多年前就已为人所知。在这方面,对卡介苗提取物进行了大量的研究。大约60年前,弗洛因德的佐剂,由分枝杆菌浸油提取物组成,被描述为具有类似治疗活动的免疫调节剂。定义为完全弗氏佐剂,这是产生Th-1免疫反应的最有效方式之一。然而,直到1984年,德永才等等。107.发现分枝杆菌对NK细胞基因组- dna的激活是卡介苗有效的抗肿瘤活性的原因107..该观察结果促进了对细菌DNA的免疫原性的进一步研究108.- - - - - -111..这种强有力的免疫反应表明,细菌DNA是脊椎动物免疫系统进化上保守的损伤,脊椎动物免疫系统将这种结构模式识别为危险信号。最近,合成的含有免疫刺激DNA序列的odn已被鉴定出具有佐剂活性并诱导Th-1样免疫反应。
除了抗肿瘤和细胞毒性活性之外,TH-1细胞通过直接抑制效果作为免疫调用剂的重要作用。基于此容量,最近探讨了CPG-ODN是否具有抗真人效应。这种预防和/或治疗潜力得到了广泛的分析,特别是使用过敏和哮喘的小鼠模型112..研究表明,在致敏小鼠被过敏原刺激之前,只给予CpG-ODNs一次注射或粘膜注射,就能比地塞米松更好地抑制肺和血液嗜酸性粒细胞增多症113..IL-3、IL-5水平和气道高反应性也降低,而IFN-γ水平升高。这种立即抑制过敏反应的现象最近在豚草致敏的另一个模型中得到了证实114..在该研究中,已经表明过敏原特异性反应的长期Th-1转移至少六周。CPG-ODN的这种治疗潜力在主要的桦树花粉过敏原的良好的动物模型系统中进一步探讨,这与临床上高度相关的过敏原型115..CpG-ODN与桦木花粉过敏原的共同率氢氧化铝过敏原,导致TH-1活性显着增加,导致IgG2A水平显着升高,随后减少了气道炎症。此外,气溶胶敏化后CpG-ODN的全身或局部/粘膜应用也诱导该TH-1依赖性抗体谱。作者得出结论,作为佐剂的这种CPG-ODN可能对全能疾病的新形式的特异性免疫疗法产生重要影响。在这种情况下,特别是粘膜途径可能具有进一步的潜力。虽然在几种动物模型系统中已经清楚地证明了预防性和治疗效果,但需要进一步研究来分析可能的长期和副作用及其在人类的效率。
细菌组分:脂多糖
若干横断面和纵向流行病学研究表明,农民子女、家中养有猪、狗或猫的儿童、从小在日托中心长大的儿童和大家庭的儿童的过敏原致敏和特应性疾病减少116.- - - - - -120..
一个有趣的“人类模型”可能在这一背景下提供进一步的见解,这是最近几位作者报告的观察结果,即在农场长大对特应性疾病的发展具有显著的保护作用。瑞士一项针对6-15岁学龄儿童的人口研究清楚地证明了这一点121..同样,在对5-7岁的年龄的历史上学校进入学校的大型调查中,农场上养育的儿童的患病率明显低于来自在农场上没有长大的同一村庄的同龄人122..此外,奥地利最近对8-10岁儿童的一项调查也证实了这些发现123..有趣的是,特应性湿疹的发展并没有受到父母的农业活动的影响。
农场中保护人们免受过敏和哮喘的环境因素的性质是什么?农民家庭的生活条件在许多方面与其他家庭的生活方式不同,包括更大的家庭规模,更多的宠物,经常使用木材或煤炭取暖,较少的母亲吸烟,更多的潮湿和独特的饮食习惯。在上述研究中,这些因素都不能解释这种影响。相反,与牲畜和家禽的接触被发现在很大程度上解释了农业和遗传性疾病之间的关系。
在所有这些环境环境中,革兰氏阴性细菌及其细胞壁组分内毒素(Lipopolysachare(LPS))可能存在丰富。实际上,职业病研究报告了农场环境中的高水平内毒素暴露124.,125..由于已知细菌内毒素诱导IFN-γ和IL-12产生,因此已经产生了假设,即儿童早期和婴儿期的慢性内毒素暴露可能会用于抗过敏和哮喘的发展。
这一假设是最近发表的两项研究的基础,这两项研究的目的是比较室内暴露于内毒素和室内灰尘与过敏原致敏对患哮喘和/或哮鸣的高危婴儿的影响。Gereda等等。126.在61名9-24个月大的婴儿家中,测量了室内灰尘内毒素和过敏原的浓度,医生记录了至少三次哮喘发作。同时,用一组常见的吸入剂和食物过敏原进行皮肤点刺试验,测量反映Th-1和Th-2活性的细胞因子。致敏婴儿家中的室内灰尘内毒素浓度明显低于未致敏婴儿。室内灰尘内毒素浓度的增加与IFN-γ产生CD4 t细胞比例的增加相关。
然而,最近另一个研究没有确认这一协会。公园等等。127.审查了房屋尘埃内毒素的协会,在出生后的前三个月内测量,在一年的499名儿童队伍中的第一年喘息,有一个或两个患有哮喘或过敏的父母。他们的结果表明,内毒素与喘息的风险增加有关,并且可能在患有过敏或哮喘史的儿童的第一年生命中促进持续喘息。这与呼吸道感染的影响无关,婴儿期喘息的最强烈危险因素之一。早期儿童感染和随后的哮喘发育之间的关联在Illi的出生队列研究中典雅评估等等。120..这项研究得出的最重要的结论是,在出生后的第一年里,有两次或两次以上普通感冒症状的儿童在7岁前患哮喘的风险降低了50%。相比之下,患有下呼吸道疾病的孩子在出生后第一年就会出现喘息症状。
LPS是促进Th-1 t细胞发育的细胞因子的有效诱导剂。LPS介导这种作用的一种机制是通过与LPS结合蛋白结合到LPS受体CD14上,CD14表达于各种APC上,特别是单核细胞和巨噬细胞。CD14基因5'连接区域的多态性最近被发现,并与特异反应的强度相关128..
这些横断面研究的数据提供了间接证据,表明LPS在变应性疾病的发展中具有保护作用。然而,潜在的分子和细胞机制仍不清楚,需要评估。
需要强调的是,LPS暴露的免疫后果取决于各种条件。结论是,在所有情况下,LPS曝光可防止过敏和哮喘是一项过度的过性化。暴露于LPS的源和途径也可能是重要的,因为LPS由几种细菌病原因产生(例如嗜血杆菌和沙门氏菌和寄生在肠道中的菊苣(例如Escherischia杆菌).在这种情况下,据报道,从新生婴儿的胃肠道殖民化乳酸杆菌和掌握(与那些有Clustridium固执的)与以后生活中特应性疾病的减少有关129..此外,众所周知,长期高剂量暴露于LPS可触发多种适应过程,导致巨噬细胞“脱敏”。
动物模型系统为评估脂多糖对过敏和哮喘的免疫生物学作用提供了机会。在这方面,现在很清楚,事件的顺序决定了结果。当LPS暴露发生在过敏原致敏/激发之前时,LPS的预防作用已被证明。在这方面,静脉注射LPS可减少豚鼠中抗原诱导的支气管收缩,而致敏早期暴露可防止大鼠的过敏性致敏130.,131..
相反,当LPS暴露在已经致敏的动物身上时,LPS促进了炎症反应(图3)⇓).这已经在几项研究中得到证实,包括最近的一项调查表明,暴露于致敏大鼠的LPS会加剧过敏免疫反应131.,132..为了进一步使这个问题复杂化,还记录了肿瘤内LPS甚至在没有过敏原暴露和/或敏化的情况下,即使在没有过敏原和/或敏化的情况下也能诱导豚鼠中的血清素和乙酰胆碱的支气管高反应性。
总之,现在有环境证据表明,在生命早期持续暴露于LPS可能对过敏和哮喘有预防作用。这种情况在动物模型系统的结果中得到了密切的反映,在变应原致敏之前暴露LPS具有良好的预防效果。相反,当过敏原致敏作用已经形成时,在后期暴露于LPS可能会加剧和促进炎症反应。这些实验数据可以解释细菌性和病毒性感染导致哮喘加重的临床观察。此外,这些生物学效应也取决于暴露途径,因为肠道LPS暴露可能有不同的影响。
细菌的组成部分:超级抗原
正如革兰氏阴性细菌分泌LPS作为主要的免疫调节成分一样,革兰氏阳性细菌提供,通过细菌超级抗原(肠毒素)的分泌是一种主要的免疫调节刺激(图4)⇓).细菌超人员行为通过一组生物学性质与常规抗原明显不同。与需要通过APC的常规抗原的常规抗原进行对比,细胞内加工,鉴定MHC-II类分子的鉴定和T细胞受体的MHC-II类加肽复合物,细菌超抗原差异差异。它们在MHC-II类分子上的常规T细胞表位 - 结合槽外结合,并用T细胞受体Vβ链交联MHC-II类分子。在常规抗原的情况下,这种APC细胞相互作用模式导致刺激<0.1%的幼稚T细胞。相反,识别定义的T细胞受体Vβ元素的细菌超抗原刺激高达25%的幼稚T细胞。这种相互作用导致剧烈的T细胞活化和细胞因子释放,通常是缺失和大多数T细胞的凋亡。
这种细菌超级抗原的一个主要来源是金黄色葡萄球菌。在特应性皮炎的病例中,产生毒素的皮肤的慢性定植S.金黄色葡萄球菌菌株已经成熟。在最近的横断面研究中~80%的特应性皮炎(AD)显示皮肤的慢性定植S.金黄色葡萄球菌>> 50%的孩子被毒素阳性菌株殖民134..然后评估毒素阳性或毒素阴性应变的定子是否与Scorad评估的临床严重程度有任何相关性(AD的严重性评分)。本研究的结果揭示了患有毒素生产的患者组中的特应性皮炎最严重的病例S.金黄色葡萄球菌菌株。这些数据导致假设细菌毒素对特应性皮炎的临床严重程度产生重大影响。
为了进一步探讨该问题,皮肤渗透T细胞的T细胞受体Vβ曲目与个体产生的毒素的模式相关联S.金黄色葡萄球菌菌株135..在激烈的皮肤炎症患者中观察到超抗原响应性T细胞的优先积累。通过Strickland进行的一项研究提供了超剧性疾病调节效果的额外迹象等等。136..作者表明,体外在美国,超级抗原具有激活和扩展表达特定t细胞受体Vβ基因片段的t细胞的能力,并增加它们的皮肤home能力通过这种皮肤归巢受体,皮肤淋巴细胞相关抗原的上调体外.
超级抗原的疾病调节作用也在人源化严重联合免疫缺陷(SCID)小鼠模型中得到了广泛的研究137..SCID小鼠由于抗原受体重组酶的缺陷表现出严重的免疫缺陷综合征。由于这种缺陷,成熟的T细胞和b细胞在这些小鼠中缺失,它们接受异种移植时不会产生排斥反应。从屋尘螨致敏患者身上转移特应性外周血单个核细胞可导致这些小鼠在抗原增强后产生屋尘螨特异性T细胞和b细胞反应。当用超抗原葡萄球菌肠毒素B (SEB)或屋尘螨变应原或两者的组合对重建的SCID小鼠进行表皮攻击时,真皮和表皮发生类似特应性皮炎皮肤损伤的炎症反应。当用SEB和屋尘螨变应原联合治疗小鼠时,观察到最严重的损伤。在最近的一项研究中,SEB已被应用于正常和特应性皮肤,导致t细胞流入皮肤,导致诱导特应性皮炎样皮肤损伤138..
至少在特应性皮炎中,S.金黄色葡萄球菌-衍生的超级抗原也可以以另一种方式发挥作用。在特应性皮炎患者亚组中检测到针对葡萄球菌肠毒素A (SEA)或SEB的特异性IgE抗体134.,139..这些超抗原特异性IgE抗体的存在与疾病严重程度和总IgE水平强烈相关。这些结果导致了结论,这些蛋白质也可以用作常规过敏原,导致过敏原特异性的T-和B细胞反应。在患者用超剧性分泌慢化S.金黄色葡萄球菌菌株中,这些毒素可以很容易地穿透受损的表皮屏障,直接与存在于真皮肥大细胞表面的IgE抗体结合。通过这种机制,肥大细胞被长期激活,释放促炎介质,使这些患者的瘙痒-抓痕周期持续下去。
另一方面,也证明了这种细菌超级抗原可以预防和抑制小鼠的过敏反应。当小鼠在变应原刺激(卵清蛋白)之前接受SEB皮肤治疗时,卵清蛋白诱导的过敏反应被阻止。尽管在这个模型中,超抗原处理最有可能导致适当的t细胞被显著激活,然后细胞被删除,但解释超抗原如何防止过敏反应发展的潜在免疫机制尚未被深入探讨。
结论
众所周知,过敏性疾病的炎症反应的特征在于存在TH-2介导的反应。IgE抗体代表重要的效应分子,嗜酸性粒细胞和肥芯细胞是直接超敏反应的主要效应细胞。在(遗传上)具有独特类型的免疫应答的易感个体,在过敏原暴露后启动模式。由于室内和室外过敏原普遍存在,一旦免疫应答朝向TH-2表型移位,慢性过程的免疫发作结果。显然,这个过程已经可以在子宫内环境中开始。由于许多但不是全部,微生物抗原引发了作为正常防御机制的TH-1免疫应答,提出了一个假设,提出了微生物感染的模式和频率之间存在负相关和过敏的发病和严重程度。哮喘。
该假设由流行病学数据支持,表明频率,图案和感染类型与过敏和哮喘的患病率之间的反比异性关联。然而,在患者到目前为止,尚未证明直接造成的关系。
实验体外已经采用了系统和动物模型来进一步分析微生物抗原对过敏免疫反应发展的影响。在此问题上对可用文献进行分析允许以下结论。首先,特定细菌抗原具有显着调节免疫应答模式的能力(图5⇓).这已经证明了细菌感染的模型(例如结核分枝杆菌感染和卡介苗)以及曾使用细菌成分的情况(例如LPS,细菌超抗原)。其次,相同的细菌抗原可以促进或预防过敏免疫应答(图6⇓).结果是批评性地取决于暴露于微生物抗原和过敏原致敏之间的时序。当微生物抗原有机会在过敏原之前在幼稚个体中发育TH-1免疫应答时,预防TH-1免疫应答的情况下会发生。相反,在已经TH-2炎症组织中的细菌抗原的急性或慢性遭遇通常会加剧过敏条件。第三,从目前的知识,单一的瞬时感染或疫苗接种不足以指导免疫应答,以指向这种强烈的TH-1模式,这可以防止生活中的过敏和哮喘的发育。相反,只有频繁和反复暴露于各种微生物抗原可能导致TH-1免疫力的持久诱导,这可能是最终阻止TH-2免疫力的发展,因此可以减少发育过敏和哮喘的风险。
这一概念主要基于实验数据,现在需要通过队列和干预研究在人体上进行测试。需要探索的是,如何在生命早期促进免疫系统发展强大的t辅助免疫系统。实验数据进一步表明,只有在免疫系统有机会对易感易感的易感个体进行变态T-helper 2免疫应答之前,才有可能采用T-helper 1免疫。
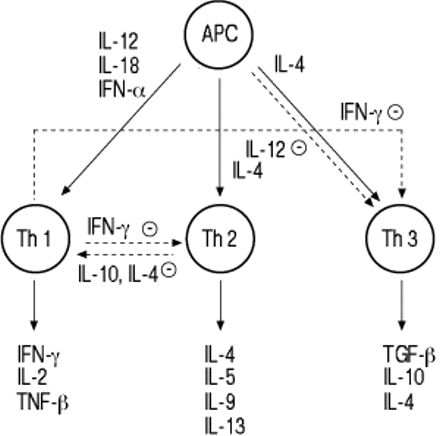
细胞因子对T-helper (Th)-1、Th-2、Th-3 t细胞发育和效应功能的正、负调节作用。正面效果:实心箭头;负面影响:虚线箭头。APC:抗原提呈细胞;IL:白介素;干扰素:干扰素;TGF:转化生长因子;TNF:肿瘤坏死因子。
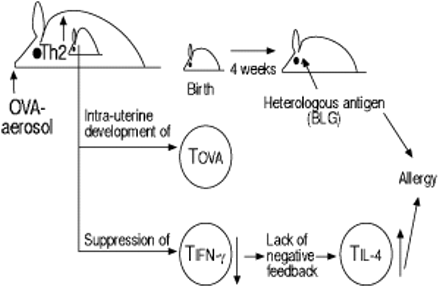
母体T-helper (Th)-2免疫以一种抗原依赖和独立的方式影响产前和产后免疫反应。Th:辅助细胞;BLG: beta-lactoglobulin;卵:卵白蛋白;il - 4: interleukin-4;干扰素-γ:移行细胞;Tova.: ova-specific t细胞;TIL-4.:IL-4产生T细胞;TIFN-γ.:产生ifn - γ的t细胞。箭头表示产量的增加或减少。
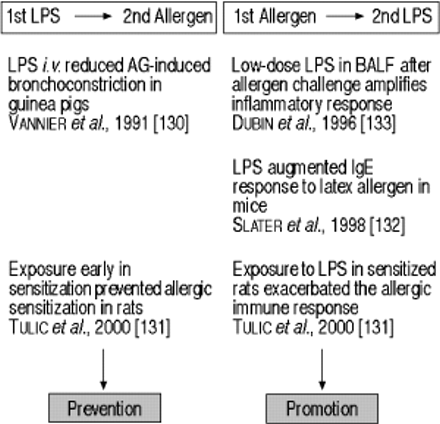
脂多糖(LPS)对过敏和哮喘的修饰。BALF:支气管肺泡灌洗液。
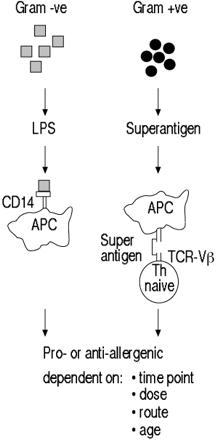
细菌毒素及其在过敏和哮喘中的假定作用。有限合伙人:脂多糖;APC:抗原提呈细胞;Th:辅助细胞;识别:t细胞受体。
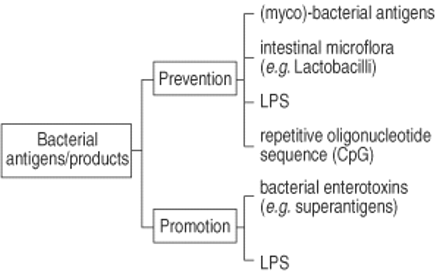
过敏和哮喘中细菌抗原及其产物的双向作用。有限合伙人:脂多糖。
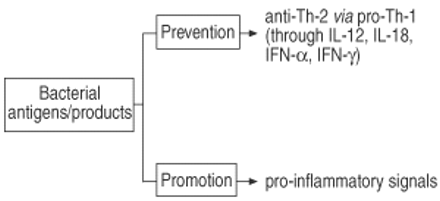
通过微生物抗原预防过敏和哮喘;事件序列和提出的行动方式。Th:辅助细胞;IL:白介素;IFN:干扰素。
脚注
↵本系列以前的文章:感染:特应性疾病和哮喘发展中的朋友或敌人?流行病学证据。EUR RESPIR J.2001;18:872-881。2号:呼吸道合胞病毒性毛细支气管炎与阻塞性呼吸道疾病的关系。EUR RESPIR J.2001;18:1044-1058。
- 已收到2001年3月20日。
- 接受2001年6月19日。
- ©ERS期刊有限公司














