抽象
这项研究的目的是评估在肺移植受者的体液免疫反应接种流感疫苗。
抗体水平包括在1999-2000三价流感疫苗的三种病毒抗原(A /悉尼/ 5/97样(H3N2),A / Beijing262 / 95样(H1N1)和B /山梨/ 16/98)were measured before and 4 weeks postvaccination in 43 lung transplant recipients and 21 healthy adult controls. The ability to develop protective antibody levels, a serological response, and the magnitude of change in levels were assessed.
体液免疫反应,接种流感疫苗是针对所有三种病毒抗原移植组显著降低。到A /悉尼,对照组的95%和移植组的40%开发保护水平(p = 0.0009);到A /北京,对照组的71%和移植组的30%开发保护水平(p = 0.004);和到B /山梨,对照组的48%和移植组的19%开发保护水平(p = 0.02)。相比,这些接收他克莫司(R = -0.3056,p值= 0.0463)时,这些收容环孢菌素具有较低的抗体应答。
在肺移植患者的体液免疫反应接种流感疫苗是很差。接收环孢素肺移植患者可以具有比那些接收他克莫司的较低的抗体应答。可能需要替代的预防策略。
感染流感病毒每年导致大量的发病率和死亡率。这是老年患者,患有慢性心血管和肺部疾病以及免疫功能低下者尤其如此1,2。接受免疫抑制药物治疗,如实体器官移植的患者,似乎对流感更容易受到感染,以及更容易的体验相关的并发症3-7。几个因素可能会使肺移植受者对呼吸道感染:1)移植肺(S)导致抑制咳嗽的去神经支配;2)淋巴引流的破坏;3)受损移植肺粘液纤毛清除;4)在排斥期间气道损伤的存在;5)共存在一个单一的肺移植受者的天然肺病理学;和6)高的水平的免疫抑制8。由于增加的易感性和风险,建议预防通过每年接种流感疫苗。然而,由于移植的患者都严重免疫抑制,免疫接种的有效性受到质疑。
传统上,接种流感疫苗的免疫原性的研究主要集中在体液反应。对接种的体液免疫反应进行了评估通过确定谁开发保护抗体滴度接受者的比例(即≥1:40),或谁开发血清学应答(即≥four倍的滴度增加)9-12。Nonmedication相关因素已被确定可以改变一个正常的宿主对疫苗的体液反应。特别是,它往往是在个人更免疫原性谁之前曾经抗原经验(即感染,预先免疫)10-13而中老年人的免疫原性较低14那些终末期肾脏疾病,以及那些具有先进的人类免疫缺陷病毒(HIV)感染9,10,13,15,16。在移植人群的体液免疫反应的研究,使用霉酚酸酯17或环孢素18,19并降低移植肾功能11,19,20均降低一些抗体反应的所有预测,而不是其他的研究。此前免疫和低龄是增加抗体应答预测10,21。在研究,使用加强剂量,这些并没有发现增加抗体产量3,10,13,19,21。
这项研究的目的是评估肺移植患者的体液免疫反应接种流感疫苗。为了最好的作者的知识,没有以前的研究集中于疫苗的免疫原性肺移植患者。
患者和方法
研究对象
Lung-transplant recipients, who were at least 3 months post-transplantation, were recruited from the Cleveland Clinic Foundation (CCF) lung transplant programme. Exclusion criteria included: egg allergy, acute febrile illness, or active treatment for an acute rejection episode. Healthy adult controls (aged ≥18 yrs) were recruited from the employees of the CCF. Exclusion criteria for controls included: egg allergy, a known immune function impairment, a known major organ disease, or use of immunosuppressive medication. The study was approved by the Institutional Review Board of the CCF and all study participants gave informed consent.
学习规划
这项研究是一项前瞻性观察队列研究,旨在确定肺移植患者接种流感疫苗的体液免疫应答。一组健康成年人为对照人群。Venous blood samples were collected prevaccination and 4 weeks postvaccination from both groups. All study participants received the 1999–2000 trivalent influenza vaccine containing A/Sydney/5/97-like (H3N2), A/Beijing/262/95-like (H1N1), and B/Yamanashi/16/98 antigens (Wyeth-Lederle, Marietta, PA, USA - Lot# 4008203). All blood samples were tested for antibody titres to these three antigens.
方法
对于血细胞凝集素抑制测定血液样品具有它们的血清分离,并在收集后冷冻(-20℃)立即保存。他们被送往冻结了一批在Glennan中心实验室在东弗吉尼亚医学院(诺福克,弗吉尼亚州,美国)分析在研究的结论。
血细胞凝集测定法使用表示包含在疫苗病毒株的血凝素的抗原进行。血凝抑制如先前所述进行22使用从一个在10两倍的血清的稀释液,以一个在1024。小于一个在10的滴度计算为五分之一。几何平均滴度计算。
分析
结果措施包括:1)的绝对抗体滴度和预接种后;2)在从预接种后至滴度的绝对变化;3)疫苗接种者的开发谁保护性抗体水平的百分比(定义为≥1滴度:40);4)疫苗接种者谁能够血清转化的百分比(定义为滴度一个≥four倍)。自变量收集和分析包括年龄,性别,时间,因为移植,免疫抑制药物的使用和水平,绝对淋巴细胞计数,事先接种状态,血清肌酐,总imunoglobulin(免疫球蛋白)-G水平,急性排斥反应。急性排斥反应所需的病状在A2B0或更高等级。
在对照组和移植组之间的人口统计变量的差异测试(对于连续变量和卡方分类变量Wilcoxon秩和检验)。在基线变量的差异进行了调整在所有后续测试。
抗体滴度进行方差分析(ANOVA用于数转化的连续变量和分类变量的Logistic回归),以查看是否有对照组和移植组前和接种后之间显著差异。采用Wilcoxon符号秩检验来检验组内差异以确定所述postvalue是否是从预置值显著不同。
到发生血清转化的抗原(最多三个最小零)的数量和抗原,其保护性抗体水平制定的号码(最小零,最多三个)分别计算。甲Spearman相关对各前面列出的独立变量的执行。这些计算值被用来评估用于独立变量,以移植组内的抗体应答之间的关联。
中值,25%四分位数,和75%四分位数或百分含量计算为汇总统计,以抗体滴度,其呈现为具有95%置信区间的几何装置(CI)的除外。在抗体滴度的变化都带有位数和四分位数,因为潜在的“零”改变范围(IQR)。显著差异具有p <0.05评价。样本大小是用90%的功率,以检测抗体反应假定为80%的对照组的反应和40%的移植组响应的差来计算。
结果
肺移植受者(N = 43)和健康成人对照(n = 21)和登记完成了研究。The median age (yrs) of the groups differed, 51 (IQR 43–60 yrs) in the transplant group and 42 (IQR 41–44 yrs) in the control group (p=0.008). The percentage of study participants who were male (56% of the transplant group and 43% of the control, p=0.33), and the percentage receiving the previous years' vaccine (100% of the transplant group and 86% of the control, p=0.52) did not differ between the groups. The characteristics of the transplant group are shown in table 1⇓。
抗体滴度可用于所有的参与者。The geometric mean titres were significantly lower in the transplant group both pre- and postvaccination (table 2⇓)。The ability to develop protective antibody levels was significantly less in the transplant group for all viral antigens (fig. 1⇓)。九十五每对照组的%,并移植组的40%开发保护水平,以A /悉尼(p值= 0.0009);对照组的71%和移植组的30%开发保护水平,以A /北京(P = 0.004);与对照组的48%和移植组的19%开发保护水平,以B /山梨(p值= 0.02)。The seroconversion rate was significantly lower for both influenza A antigens (fig. 2⇓)。到A /悉尼,对照组的52%和移植组的26%血清转化(P = 0.009);到A /北京,对照组的57%和移植组的19%血清转化(P = 0.004);和到B /山梨,对照组的24%和移植组的12%血清转变(p值= 0.16)。The absolute increase in titre was lower in the transplant group for all three viral antigens (fig. 3⇓)。用于控制和移植组中值(IQR)变化分别为:A /悉尼:73(26-240)与10(0-33)中,p = 0.0004;A /北京:30(12-120)与4(0-15)中,p = 0.0002;和到B /山梨8(0-40)与0(0-10),P = 0.01。
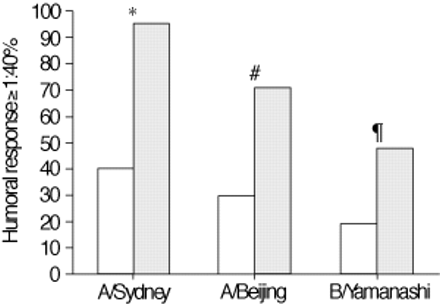
保护性抗体水平的发展。□:移植;┘:控制。*:P = 0.0009;#:P = 0.004;¶:P = 0.0164。
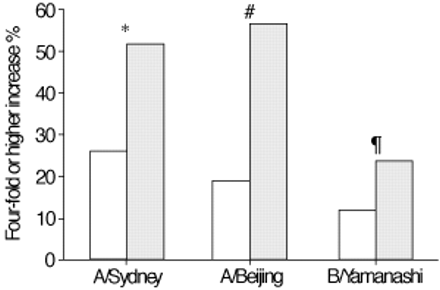
血清学应答发展。□:移植;┘:控制。*:P = 0.0085;#:P = 0.0022;¶:P = 0.1582。
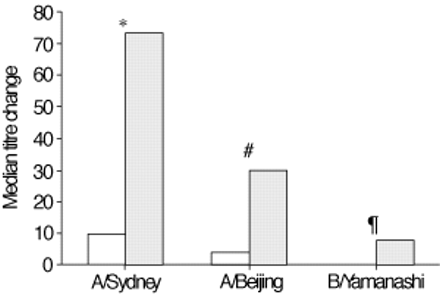
平均增加抗体滴度。□:移植;┘:控制。*:P = 0.0004;#:P = 0.0002;¶:P = 0.01。
独立变量进行了分析,以与其中个体表现出血清转化的抗原的数量,以及对其中有一个保护性疫苗接种后水平的抗原数的相关性。有使用环孢素之间(在统计学上显著负相关与他克莫司)和抗体反应性(r = -0.3115,p值= 0.0420对血清转化,并且r = -0.3056,p值= 0.0463防护水平的发展)。有一种趋势朝着降低与该组内的较高水平环孢素正在接收环孢素相关(r = -0.3834,p值= 0.0709两种抗体的应对措施)的抗体应答。43名移植受者的五个发展到所有三种病毒抗原的血清学应答。每个这五个被接受他克莫司(即five out of 20 in the tacrolimus group, zero out of 23 in the cyclosporine group) (fig. 4⇓)。有报道说,收到环孢素和他克莫司收到之间的其他自变量组的组间无显著差异。
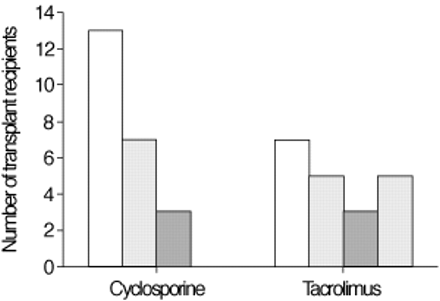
到发生血清学应答的抗原的数量。环孢菌素的患者中,n = 23;他克莫司的患者中,n = 20。□:0抗原;┘:1个抗原; :2个抗原;└:3种抗原。
:2个抗原;└:3种抗原。
的相关性表示的趋势没有达到包括统计显着性:较高的总IgG水平与更好的抗体应答相关(r = 0.278,P为血清转换= 0.07,和r = 0.262,P = 0.089用于保护水平的发展);与使用霉降低抗体应答相关(r = -0.271,p值= 0.078为血清转换,而r = -0.269,p值= 0.081用于保护水平的发展);和更好的抗体反应相关(r = 0.242,P = 0.118血清转化,和r = 0.23,P = 0.13为保护水平的发展),较高的绝对淋巴细胞计数。有接种疫苗的抗体反应和急性排斥反应发作的发展之间没有相关性。
讨论
它已被证明有肺移植患者的不良体液免疫反应接种流感疫苗。保护性抗体滴度在移植研究的参与者包括在疫苗中的抗原的19-40%发展。只有43(8.6%)五,制定保护级别给所有三种抗原。预还有疫苗接种后抗体水平在移植组低,突出这一人群的免疫抑制性质。
独立变量间的唯一的统计学显著相关性环孢素的使用与他克莫司比使用较小的抗体应答相关联。支持此进一步是趋势朝向作为环孢菌素水平增加降低抗体应答。其他趋势悉随使用霉和更大的抗体产生有较高的总IgG水平和较高的绝对淋巴细胞计数的降低抗体水平。
对体液免疫反应接种流感疫苗的几项研究已经在其他实体器官移植人群中进行。
在肾移植的文献,对流感疫苗的免疫原性研究有不同的结论。与对照组相比有三项研究表明,正常的抗体反应10,23,24而其他几个人描述受损的免疫原性3,17-20,25。在两次与正常抗体的产生,强的松和硫唑嘌呤的研究是唯一使用的免疫抑制剂。已经有至少有三个研究,包括心脏移植受者的显著数3,13,26。所有表现出比正常人小体液免疫反应。在小儿肝移植人口的两项研究显示,比较正常的抗体产生的疫苗接种10,21。一项研究,其中包括成人肝移植患者呈下降体液免疫应答3,而另一种显示抗体产生等同于对照组的27。与其他固体器官移植相比,肺移植患者倾向于接受高剂量的免疫抑制药物,因此不太可能发展到接种适当的应对措施。
目前还不清楚为什么使用环孢素会导致更小的体液反应比他克莫司作为其作用机制是相同的。肺移植受者可以使用一种或根据其临床病程其他药物(例如急性排斥反应,神经毒性,肾毒性,不耐受),或在机构偏好的情节。在肾移植文学的两项研究表明,环孢素导致抗体产生减少18,19。在这些研究中,移植受者不接受环孢素未接受任何钙调磷酸酶抑制剂。为了最好的作者的知识没有以前相比在接受环孢素那些接受他克莫司患者的免疫原性研究。目前尚不清楚本研究的结果是否代表了这些药物或在谁最终会接受一个或另一个病人本质上的差别的影响,真正的差异。
这项研究的主要限制是采用疫苗效力的替代标志的。可供研究肺移植受者的数量相对较少,使得它有足够大的样本量来检测的流感相关疾病的发展统计学和临床显著差异困难。虽然体液免疫反应的疫苗接种功效的传统标志,众所周知,某些人群具有降低抗体的产生仍然收到临床显著保护。例如,尽管分别减少已显示防止住院和死亡由72和87%的中老年人,免疫接种的体液应答,16,28。至于疫苗的体液反应并不总是对预测病情严重的临床保护,近期nontransplant人群研究调查了接种流感疫苗的细胞反应。这两种T辅助细胞和细胞毒性T淋巴细胞反应,接种流感疫苗进行了研究29。
这里报告的结果应该推广到肺移植受者的人口。这是比较难预测其相关性免疫抑制的其他人群。其他固体器官移植可能有不同程度的疫苗效力,因为肺移植受者倾向于接受医疗免疫抑制的最高水平。
在这一领域未来的研究将是非常重要的。细胞免疫反应的疫苗接种的研究将有助于阐明保护水平和机制。更多的免疫原性疫苗,分娩的方法,或使用的化学预防的发展是潜在的发展的各个领域。
最后,在肺移植患者的体液免疫反应接种流感疫苗是很差。接受环孢素肺移植受者可以具有相比于接收他克莫司一降低到流感疫苗接种的抗体应答。需要进一步的研究和替代预防战略。
致谢
笔者想感谢D. Nelson和他的团队的统计贡献。他们还感谢由J.E. McElhaney并在Glennan中心东弗吉尼亚医学院的实验室,和B颜利伯曼和实验室在克利夫兰诊所基金会提供的实验室支持。
- 收到2001年2月28日。
- 公认2001年7月10日。
- ©ERS期刊有限公司











