摘要
肺炎是世界范围内发病率和死亡率最高的主要传染病之一。影像学在肺炎患者的发现和治疗中起着至关重要的作用。
本文就不同的影像学检查方法在疑似肺部感染的诊断和治疗中的应用作一综述。影像学检查应从常规放射学检查开始。当常规放射检查结果不确定时,计算机断层扫描是必须的。模式识别与临床背景知识相结合是研究肺部感染过程的最佳方法。
参与的具体模式可以表明,在许多情况下,一个可能的诊断。在获得性免疫缺陷综合症患者,弥漫性毛玻璃和间质浸润是最通常存在于卡氏肺囊虫肺炎而在免疫抑制患者中,细菌性肺炎的节段性叶浸润暗示。回合肺炎是最常见的儿童遇到比大人最常所致链球菌引起的肺炎。实质和胸膜异常的不同组合可提示附加的诊断。
当被怀疑感染肺的过程中,改变放射学表现的知识将缩小鉴别诊断,有助于引导更多的诊断措施,并作为后续考试的理想工具。
尽管在诊断和治疗方面取得了进展,但肺部感染是成人患者发病率和死亡率的主要原因。肺炎是美国第六大最常见的死亡原因,每年有600多万例细菌性肺炎发生在免疫功能正常的人群中1。已知的引起呼吸道感染的微生物谱很广,而且随着新的病原体的发现和宿主的免疫反应被药物或其他疾病或反应改变而不断增加。在美国,据估计,每年有110万社区获得性肺炎(CAP)病例需要住院治疗,估计费用为80亿美元1。院内获得性肺炎(NP)是最重要的医院获得性感染,因为它与死亡率最高的是因果关系,以促进死亡的院内感染有关2。此外,自获得性免疫缺陷综合症(艾滋病)开始流行以来,肺部感染源不断增加。除了直接的病人护理费用之外,肺炎还导致了超过5000万天的工作受限活动,是美国第六大死亡原因,死亡率为每10万人13.4人3.,4。
在肺部感染变化趋势
肺炎呼吁的临床意识,适当的微生物测试,以及放射照相研究相结合的诊断。平原胸片是一种廉价的测试,可以迅速表现出肺异常的存在。它表示怀疑患有肺部感染的所有患者的重要初步检查。在大多数情况下,平片发现可能是诊断肺炎的和可以消除对附加的射线照相术的需求。
临床医生评估已确诊或疑似肺部感染的患者面临诊断挑战,因为大多数过程表现出相似的症状和体征,而肺炎的影像学表现不能提供具体的病因诊断。此外,特定感染过程的放射学表现可能因患者的免疫状态以及预先或同时存在的肺部疾病而不同。由于三种现象:艾滋病的流行、癌症化疗的进展和器官移植的扩大,免疫缺陷患者的数量急剧增加。在艾滋病刚开始流行的时候,在20世纪80年代早期和中期,每一次艾滋病发作有50-80%的死亡率卡氏肺囊虫肺炎(PCP)。自从1989年开始实施常规预防措施以来,PCP在艾滋病人群中的发病率有所下降5,6。除了发病率较低外,在轻度至中度病例中死亡率也有所下降(15%)7。因此,其他感染包括细菌性肺炎、真菌感染、巨细胞病毒(CMV)、鸟分枝杆菌复合物(MAC),以及结核留在这些患者中的发病率和死亡率的原因显著5- - - - - -7。放射科医生不仅要记录肺炎的位置和程度,还要评估肺炎的演变和病程,并发现疾病的任何并发症。
整合临床和影像的发现
可用于与已知或怀疑肺部感染患者的评估中的最有用的成像模态是胸片和计算机断层扫描(CT)。影像学检查应始终与症状患者如何,呼吸困难的程度,一氧化碳弥散肺容量的减损的程度(知识解释Dl,co), CD4+细胞计数,有无发热或白细胞增多,是否有咳嗽及咳嗽是否多产,以及症状的长期性8。了解患者是否患有CAP或NP,以及了解患者的免疫状态,这些都是获得可能致病微生物名单的有力工具8,9。临床信息可以大大提高x线诊断的准确性,即。急性空气传播过程中出现寒战、发热、痰中有脓的艾滋病患者可能是化脓性的,而不是PCP。在缺乏临床资料的情况下,放射科医师不能可靠地区分肺炎和其他肺部病变10。不幸的是,临床数据和x线检查结果往往不能导致肺炎的最终诊断,因为有大量的非感染性过程与发热性肺炎相关即。药物性肺疾病,急性嗜酸细胞性肺炎,闭塞性细支气管炎机化性肺炎(BOOP)和肺血管炎,模仿肺部感染11。局限性肺炎与其他肺过程的区别不能在放射学基础上确定11,12。局部大叶或节段性分布的肺部疾病不仅可由肺炎引起,还可由肺水肿和出血引起。胃酸误吸引起的局限性肺水肿可能导致与肺炎相同的图像,以及继发于血栓栓塞的肺梗死,这也可能产生类似的影像学表现。当肺炎表现为弥漫性肺部异常时,诊断也同样困难。肺水肿和成人呼吸窘迫综合征(ARDS)是与支气管肺炎最常见的区别,当x线显示为全身性肺异常时13- - - - - -15。
常规胸片
根据美国胸科协会的指导方针,当怀疑成人肺炎时,应进行后前(PA)(如果可能的话,侧位)胸片检查16。胸部X光的作用已经被描述或者作为用于检测的新浸润的筛选工具或用于监测对治疗的反应。胸部其他角色射线照相术包括评估疾病的程度的增强能力,来检测并发症(即。空化,脓肿形成,气胸,胸腔积液),并发现额外的或替代的诊断,有时指导侵入性诊断程序。
在大多数情况下,不同的异常可以被识别的胸片。更常见的放射照相发现包括节段性或大叶性肺炎合并和间质性肺病。其他较少见的放射照相发现包括纵隔淋巴结肿大,胸腔积液,气蚀和胸壁侵犯。尽管如此,放射照相发现的非特异性以及广泛的潜在原因评估疑似肺炎患者的影像学表现时往往会导致沮丧。肺部感染由PCP,典型地看作是一个漫均匀肺泡实,最近已经描述的,在箱子5-10%,有致密的合并,结节,粟粒混浊,和胸腔积液16。此外,模棱两可的或正常的胸片并不少见,在10-39%的PCP感染患者和多达10%的已证实的肺部疾病患者中有报道17。
计算机断层扫描
CT是一个有用的辅助常规射线照相术在选定的情况下10,12,18,19。大量文献表明,CT是一种敏感的肺成像方法,具有良好的空间分辨率,提供与大体病理检查相似的解剖细节。急性炎症过程引起的组织衰减和实质改变的差异在CT上很容易看到18,19。与胸片不同的是,CT提供了横断面图像,因此,肺进程的模式和分布比常规检查更容易被识别17。
随着高分辨率CT (HRCT)的出现,一个全新的词汇来描述成像的发现。对继发性肺小叶的识别对于理解薄层CT扫描的成像结果至关重要18。结果发现,空域疾病,空域(腺泡)结节,毛玻璃混浊,实变,空气支气管造影,和小叶中心或小叶周围的分布比传统的放射学更好地看到CT17,18。空气结节大小约为腺泡大小(6-10毫米),呈小叶中央型分布。它们最容易在疾病早期发现,也最容易在不完全巩固的病理过程边缘发现。毛玻璃混浊被定义为局部肺衰减的增加,使血管结构在受累区域的可视化。磨砂玻璃是一种非特异性CT发现,可能代表肺泡或间质疾病10。
间质病变的CT表现为正常间质结构因水肿、肿瘤、炎症或纤维化而增厚10,18。最常见的CT表现为间隔增厚、支气管壁增厚、镶嵌灌注、支气管血管束增厚、间质结节、蜂窝样改变。这些发现,众所周知,从普通胶片研究,更容易被CT识别。
尽管不推荐CT是肺炎患者的初始评估,这是一个有价值的辅助常规射线照相术的患者nonrevealing或不能诊断影像表现16。一些研究表明,HRCT可以在检测,有助于鉴别诊断和免疫功能低下患者的管理与肺部并发症16- - - - - -19。
特定患者组肺炎的影像学表现
社区获得性肺炎
CAP是一个主要的医疗和经济问题,因为它的高发病率和死亡率,因为它的直接和间接管理成本1,3.。即使在健康的年轻人中,肺炎也已被发现是造成工作天数减少的主要医疗原因。在美国,每年有48.5万至100万名患者因接受CAP治疗而住院。住院治疗的费用比门诊治疗高出15至20倍,占每年用于治疗肺炎患者的估计84亿美元的大部分1,3.,20.,21。
肺炎发作住院率会发生变化的CAP患者22-51%1。死亡率是在欠发达的国家要高,在年轻人和老人,并从10变化·10万-1-40·100000-1在三个欧洲国家居民20.。虽然肺炎的放射学检查结果不能提供特定的病因诊断,但在CAP中使用放射学模式识别进行鉴别诊断是可能的。尽管临床症状的出现与影像学上可见的浸润之间的时间存在差异,但众所周知,在CAP中,大多数肺浸润出现在12小时内。在这些患者中,模式识别可能有助于对潜在的微生物群进行分类,这些潜在的微生物群更倾向于一种细菌而不是一种病毒的病因学。在冠状动脉疾病中,诊断和疾病处理最常涉及胸片,通常不需要使用其他成像方式22。
冠状病毒的致病菌包括革兰氏阳性菌等链球菌引起的肺炎(该pneumoccocus),流感嗜血杆菌和金黄色葡萄球菌,以及非典型的生物,如肺炎支原体,肺炎衣原体,或嗜肺军团菌和病毒剂,如A型流感病毒和呼吸道合胞病毒。肺炎链球菌是迄今为止完成肺叶实变的最常见原因23- - - - - -25。其他导致完全大叶性固结的病原体包括肺炎克雷伯菌和其他革兰阴性杆菌,嗜肺军团菌,流感嗜血杆菌,偶尔肺炎支原体(23日)。
放射学上,大叶性肺炎出现在毗邻胸膜的周围,并向肺的核心部分扩散。回合肺炎是最常见的儿童遇到比大人最常所致肺炎链球菌(图1⇓)27。在儿童中,活动性结核和真菌感染也可出现结节状或肿块样病变27。细菌感染可以产生多个圆形的肺部结节或肿块,有或无气蚀。这可以从感染诺卡氏菌,曲霉菌,军团菌,Q热发生,结核分枝杆菌27-。
支气管肺炎,这是最常见的原因金黄色葡萄球菌和流感嗜血杆菌时,发生当传染性生物体,沉积在支气管上皮细胞,产生急性支气管发炎上皮溃疡和脓性纤维蛋白渗出物形成。因此,炎症反应迅速通过气道壁和扩散到邻接的肺小叶传播。Radiographically, these inflammatory aggregates cause a typical patchy pattern of bronchopneumonia (fig. 2⇓)或同样可能空化的均匀节段性固结(图3)。2和3⇓⇓)。
弥漫性双侧间质和/或间质-肺泡(混合)浸润最常见由病毒引起(图4)⇓),肺炎支原体30.。一般人群中多达30%的肺炎可能是由肺炎支原体10。在感染过程中,最初的损伤朝向细支气管的粘膜和以后,支气管周组织和小叶间隔成为水肿和炎性细胞浸润。
医院(医院)肺炎
的NP可以被定义为入院,这是既没有也不在入院时温育一段时间后发生的一个21。NP是导致医院获得性感染死亡的主要原因,也是一个重要的公共卫生问题。它在重症监护病房(ICU)患者中最常见,主要发生在需要机械通气的患者中(图5)⇓)31。在ICU内,NP的估计患病率为10-65%,在大多数报道的病例中病死率为20-55%[26,31,32]。在ARDS患者中,多达55%的患者有继发性肺炎,这种并发症可能会对生存期[26]产生不利影响。
NP的诊断是困难的,用于监视的标准都是基于发烧,咳嗽和脓痰的结合胸片一个新的或逐步渗透到发展的临床表现。当肺炎发生在住院病人,需氧革兰阴性杆菌,尤其是铜绿假单胞菌和肠杆菌属。和金黄色葡萄球菌,是主要的病原体33。NP的其他常见原因有h .流感、肺炎球菌、吸入性厌氧菌、军团菌和某些宿主中的病毒。呼吸道合胞体病毒、A型流感和B型流感以及副流感,是70%的院内病毒性疾病的罪魁祸首33。肺炎病因学诊断的临床和影像学线索见表1⇓。
免疫抑制宿主肺炎
患者的免疫功能受损易受感染由多种生物体的6,7。在过去的几十年里,艾滋病的流行、癌症治疗的进步、器官移植和免疫抑制疗法导致了大量的患者出现免疫系统异常34-。肺炎是免疫抑制患者的一个主要临床问题,在健康社区中引起CAP的许多细菌也是这些风险患者肺炎的原因。慢性衰弱性疾病、糖尿病、营养不良、酒精中毒、高龄、长期使用皮质类固醇和慢性阻塞性肺病等也被认为是肺部感染的诱发因素37。
获得性免疫缺陷综合征
在艾滋病患者,肺部并发症可能导致一些感染性和非感染性的原因。其中传染性肺结核的过程,主要病原体包括PCP,结核分枝杆菌此外,还有许多常见的革兰氏阳性和阴性细菌5,16,17。在过去二十年中,结核病在全世界范围内死灰复燃,包括一些几十年来结核病呈下降趋势的发展中国家。结核病病例的增加主要与艾滋病患者有关38,39。感染将取决于患者的免疫状态和机会性感染的风险也将随时间变化39。
CD4+细胞计数为>200细胞·mm的患者3.易患支气管感染和细菌性肺炎,而CD4+细胞计数<200细胞·mm的患者3.易患机会性感染,如PCP8,39。大多数患者的CD4+计数在50-75细胞·mm范围内3.在诊断第一阶段的PCP时8,17。因此,在适当的临床环境中解释放射学的发现是很重要的。通过将不同的影像学模式与症状和CD4+细胞计数相关联,放射科医生可以缩小鉴别诊断范围8。Abnormal chest radiographs have been reported in up to 90% of patients showing the typical findings of diffuse bilateral interstitial infiltrates without a pleural effusion (fig. 6⇓)。随着疾病的进展,肺泡浸润也可能发展。HRCT是评价那些有症状的病人的最佳方式,其他方面胸片正常17。
支气管侵袭性曲菌病最常见于严重中性粒细胞减少症和艾滋病患者40-。临床表现为急性气管支气管炎、细支气管炎、支气管肺炎。急性气管支气管炎患者通常有正常的放射学表现。曲霉菌性细支气管炎在HRCT上表现为小叶中心结节和线性或结节性分支,外观类似于“树芽”(图7)⇓)41。小叶中心结节具有在肺一个片状分布并类似于在许多不同的感染性疾病,包括肺结核的支气管内传播看出,鸟分枝杆菌胞内、病毒、M.肺炎。曲霉菌性支气管肺炎主要发生在支气管周围实变区(图8)⇓)41。合并很少有大叶分布。这些放射学表现与其他生物引起的支气管肺炎难以区分。
阻碍支气管肺曲菌病(OBA)是用于曲霉病,其特征在于曲霉属的大规模腔内过度生长的非侵入性形式的异常模式的描述性术语。,通常烟曲霉,在艾滋病患者中42。患者可出现咳嗽了他们的支气管和有严重的低氧血症的真菌转换。The characteristic CT findings in OBA mimic those of allergic bronchopulmonary aspergillosis (ABPA) consisting of bilateral bronchial and bronchiolar dilatations, large mucoid impactions mainly in the lower lobes and diffuse lower lobe consolidation caused by postobstructive atelectasis (fig. 9⇓)42。
实体器官移植
接受实体器官移植的患者对感染的易感性随移植后时间间隔的不同而不同35,43,44。移植后时间可以分为三个时间段:移植后30天,移植后30 - 120天,移植后>120天35,43,44。在术后早期机会性感染通常没有遇到因为免疫抑制剂治疗的发生和免疫系统功能障碍发展之间的延迟。免疫系统的抑制是在器官移植后的1-4个月期间更为严重。心脏移植后的第一个月内,革兰氏阴性细菌性肺炎是由于长期插管,肺水肿,以及手术对肺力学的影响的特别频繁35,36,43,44。
肺移植受者的感染率高达50%,是其他实体器官受者感染率的几倍35。革兰阴性菌(肠杆菌和假单胞菌)和葡萄球菌是最常见的,但它们不像病毒和真菌感染那样致命35。CMV感染是移植后最常见的病毒病原体。CMV感染通常在移植后3个月内出现。最严重的原发性感染发生在50-100%的血清阴性受者中,这些受者接受了来自血清阳性供者的移植物。多达40%的骨髓移植(BMT)患者出现侵袭性真菌病35。曲霉菌通常寄生在肺移植受者的气道上,但只有少数患者会发展成侵袭性疾病。气道侵袭性曲霉菌病的组织学特征是在气道基底膜深处存在曲霉菌43,44。
骨髓移植
目前,BMT是许多血液恶性肿瘤和严重的先天性或获得性造血或免疫系统疾病的首选治疗方法36。在移植术后,发生在达因与大气直接肺通信50%的患者肺部感染。呼吸道症状,或胸片新渗入新发病,应及时早日明确诊断。
CMV是发生在器官和BMT患者中最重要的病毒感染。它发生在50-70%的异基因BMT受体36。这些患者在肺部感染的显著较高的风险比自体移植受者36。CMV感染可能与原发感染有关,或与潜伏感染的重新激活有关,或与先前血清阳性患者的不同毒株的再次感染有关。大约三分之一的受感染患者随后发展为CMV肺炎,移植后中位发病时间为50-60天36。巨细胞病毒感染通常是移植后的发展1-4个月。这些肺炎的放射照相表现无特异性。The radiological findings of CMV infection are variable consisting of lobar consolidation, diffuse and focal parenchymal haziness, and multiple small nodules with associated areas of ground-glass attenuation (“halo”) (fig. 10⇓)45。
许多局灶性病变是由真菌感染引起的,特别是由曲霉菌引起的。条件真菌是第二常见的致病菌,在同种异体中比在自体移植受者中更容易引起感染。最常见的真菌负责急性肺部疾病的免疫缺陷患者是答:来自烟,白色念珠菌和荚膜组织胞浆菌。曲霉菌是无处不在的土壤真菌40。肺曲菌病的组织学、临床和放射学表现取决于病菌的数量和毒性以及患者的免疫反应40。
血管侵袭性曲菌病几乎只发生在免疫功能低下的严重中性粒细胞减少症患者中40-。数量有了大幅增加的病人在患侵袭性曲霉菌感染的风险,原因有很多,包括开发新的固体肿瘤,密集化疗方案的难治性淋巴瘤、骨髓瘤和耐药白血病以及增加实体器官移植的数量和增加使用其他自身免疫性疾病的免疫抑制方案。摘要血管侵袭性曲菌病以真菌菌丝侵入和阻塞中小肺动脉为特征41。这导致坏死出血性结节或胸膜基于楔形出血梗塞的形成。临床诊断困难,死亡率高40。The characteristic CT findings consist of nodules surrounded by a halo of ground-glass attenuation (Halo sign) or pleural based wedge-shaped areas of consolidation (fig. 11⇓)46。这些发现与出血性梗死相一致。在严重嗜中性粒细胞减少症患者中,晕征高度提示血管侵袭性曲菌病。类似的症状在许多其他疾病中也有描述,包括毛霉菌感染、念珠菌感染、单纯疱疹和巨细胞病毒感染、韦格纳肉芽肿病、卡波济肉瘤47和出血性转移。
轻度immunosupression
Mildy免疫功能不全的患者慢性消耗性疾病、糖尿病、营养不良、酗酒、高龄、长期类固醇管理、和慢性阻塞性肺疾病容易开发一个不同形式的曲霉菌感染称为semi-invasive或慢性坏死性曲霉病,组织学上以的存在为特征的组织坏死和肉芽肿性炎症与活化的结核病。37。这种曲霉菌感染可能与多种非特异性临床症状有关,如咳嗽、咳痰、发烧6个月。据报道,15%的半侵袭性曲菌病患者出现咯血37。
半侵袭性曲菌病的放射学表现包括单侧或双侧节段性实变区,伴或不伴空泡和/或邻近胸膜增厚,以及多发结节性混浊37。调查结果在几个月或几年的时间里进展缓慢。曲霉菌坏死性支气管炎可在CT上被视为支气管内肿块、阻塞性肺炎和/或塌陷,或肺门肿块。只有少数报告描述了曲霉菌坏死性支气管炎累及中央气道的CT表现;报告的异常包括周向支气管壁增厚和支气管阻塞。在临床实践中,曲霉菌坏死性支气管炎的诊断通常基于异常的胸片和支气管镜活检标本与组织浸润的一致性37。表2为免疫抑制宿主感染病因学诊断的临床和影像学线索⇓。
肺炎患者的介入治疗
到达特定诊断的唯一明确的方式是通过感染机体的示范,即。通过痰,胸膜液或其他生物材料的涂片染色,通过呼吸道分泌物及血培养,或通过其他介入程序的检查。可替代地,通过荧光检查或CT引导下经胸细针活组织检查获得材料的培养可以是诊断的一个可靠的成本效益的方法。
然而,在大多数大系列肺炎中,即使进行了广泛的诊断性测试,仍有33% - 45%的患者不能识别病原体。以前健康的病人是由于轻微的肺炎病是在经验管理的方式。然而,在某些情况下,由于缺乏特定的微生物,需要更积极的方法来获得肺部感染的组织病理学和文化鉴定的原因。
目前已对各种技术进行培养获得的标本诊断的准确性很多争论。材料从痰获得或鼻咽分泌物已经因为正常菌群和可变的结果用于检测厌氧菌感染的获得的存在的诊断价值有限48。
柔性纤维支气管镜与肺活检
与利用保护的刷支气管肺泡灌洗纤维支气管镜是在肺部感染的诊断良好建立的技术。虽然这种技术可能在肺部感染的诊断中具有重要作用,支气管肺泡灌洗的收益率是可变的,有时不能成立肺部感染的诊断49,50。这种方法已被证明在诊断艾滋病患者的肺囊虫肺炎方面特别有用,提供了95%的病例的病因诊断。
在the special setting of a serious pulmonary process and lack of definable cause with noninvasive methods, fibreoptic bronchoscopy in conjunction with transbronchial lung biopsy is indicated (fig. 12⇓)。
最佳成像评估策略
胸部X线检查应怀疑有肺部感染,以确认或排除肺部病变的存在,所有的患者进行。虽然放射照相异常不能确定病因的来源,他们可以在缩小的鉴别诊断和随后的诊断研究提供指导非常有帮助。
在CAP患者中,诊断和疾病处理最常依赖常规胸片,通常不需要使用进一步的诊断程序。在社区环境中,发生节段性或大叶性实变的患者中,90%为肺炎球菌性肺炎或由支原体或病毒引起的非典型性肺炎。在NP感染中,斑片状支气管肺炎是最常见的发现,最可能由革兰氏阴性菌引起,尤其是假单胞菌或克雷伯氏菌。在这种特殊情况下,吸入性肺炎通常是另一种诊断,如果双侧肺或肺后部存在肺炎,则应考虑57。在ICU患者中,有关于常规胸片的准确性和有效性研究较少。异常的医疗ICU上胸片发现整体发病率据报道高达57%的肺和不稳定的心脏病患者57。在一项对ICU病人的研究中也得到了类似的结果;43%的常规胸片显示意外发现,影响治疗58。为了评估常规胸片在ICU病人中的作用,有必要对治疗效果、治疗效果以及总费用进行进一步的研究。限制在肺部感染随访中常规胸片的需要也可以降低卫生成本。CT和有创诊断只能用于复杂的病例。
相反,免疫功能低下患者的管理,是因为致病微生物的多样性的挑战和困难。在该组患者中,薄层CT和侵入性操作更经常需要。HRCT可以是谁具有呼吸道症状,但是,胸片正常结果的患者是有用的,从而提供进一步的附加发现通过标准胸片不明确界定,描绘并发实质或胸膜疾病,和引导诊断动作。此外,HRCT是,尽管做出具体的诊断其有限的价值区分非感染性的,从急性肺实质感染性疾病有帮助19。
诊断信息也可以通过支气管肺泡灌洗和经支气管针穿刺的手段获得。在这种情况下,CT是非常有用的服务作为一个“路线图”,以向病灶直接纤维支气管镜。Algorithm for evaluation of patients suspected of having pulmonary infection is shown in figure 13⇓。
总之,放射科医生扮演患者疑似肺炎的诊断和管理的重要作用。常规胸部X线保持在成像工作了患者的第一成像过程。虽然不建议计算机断层扫描是初步评估,因为在这些情况下,正常的,模棱两可的,或非特异性放射照相发现经常合适的。高分辨率计算机断层扫描是在从非感染性急性实质性肺病的感染的鉴别诊断,但不提供发病原因。使用荧光检查和/或计算机断层摄影经皮针吸是在免疫受损的患者的肺部感染获得标本的安全且有效的诊断方法,尽管其对发病率和死亡率的遗体冲击加以证明。
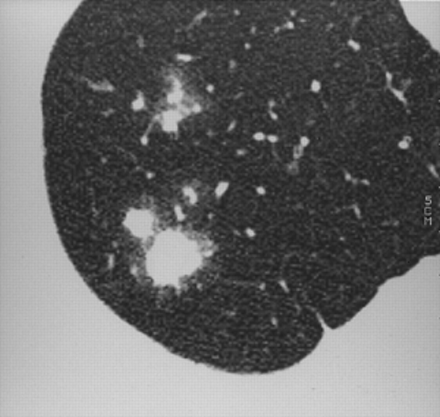
回合肺炎因链球菌引起的肺炎一位53岁的男性。计算机断层显示在左上肺叶有一个均匀实变的病灶区域。注意在实变中存在支气管充气征。痰培养产生大量的细菌肺炎链球菌。在成人中,这种类型的肺炎可能类似于支气管肺癌。
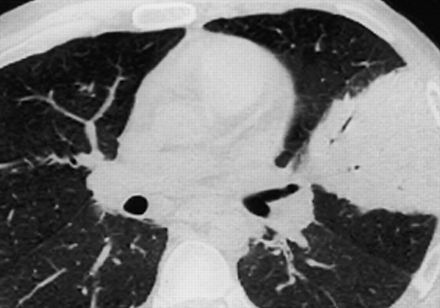
一位35岁女性的电脑断层扫描显示在中、右下肺叶有多处模糊的亚节段性混浊。小腔和中度右侧胸腔积液也是值得赞赏的。注意左下叶的感染灶。支气管镜检查标本培养物生长金黄色葡萄球菌。
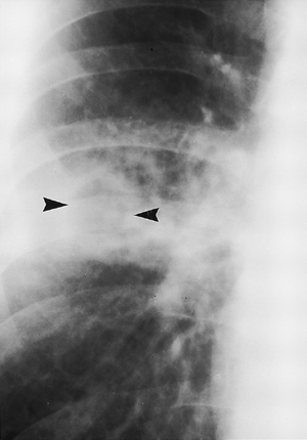
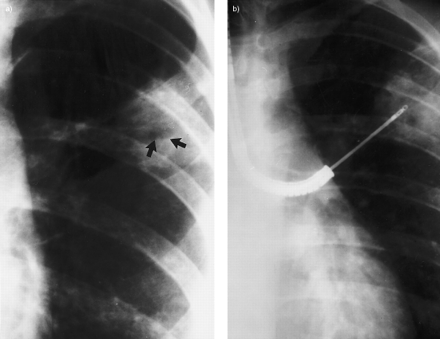
43岁男性酒精中毒并发急性空化性肺炎后胸片的特写金黄色葡萄球菌。空域固结的含有圆形射线可透性(箭头)A中定义不良的区域在右上肺中示出。
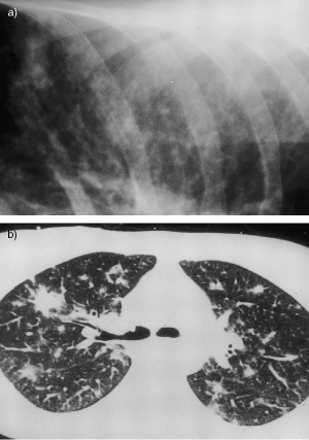
腺病毒肺炎在28年生女。一)特写后前胸片的视图演示定义不清结节混浊。b)中对应的高分辨率计算机断层扫描多个定义不清双边结节影在主要为支气管周围分布的扫描显示。
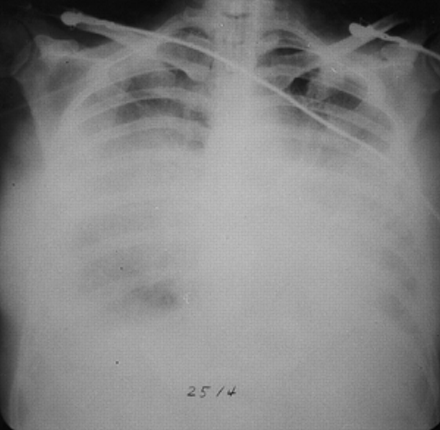
在重症监护病房患者医院获得性肺炎。便携式仰卧正位胸片显示双侧肺实变。保护支气管刷透露革兰氏阳性球菌,革兰氏阳性棒,并在涂抹革兰氏阴性杆菌。从小培养金黄色葡萄球菌以及假单胞菌和沙雷菌。
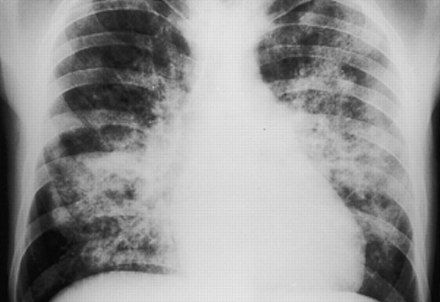
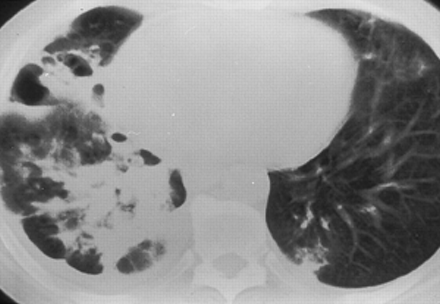
获得性免疫缺陷综合征和CD4+细胞计数为50·mm的患者的前后胸摄片3.。双侧非对称混合型(间隙性和融合性肺泡混浊)清晰可见。在这种临床环境下,x线检查结果被认为是高度诊断卡氏肺囊虫肺炎。
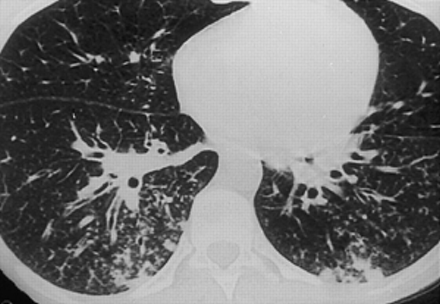
一名28岁的老病人急性白血病出现发烧和胸片正常。高分辨率CT扫描证实支气管和细支气管壁和多双边边界不清的结节影增厚与“树芽”的样子。最后诊断为黑细支气管炎。
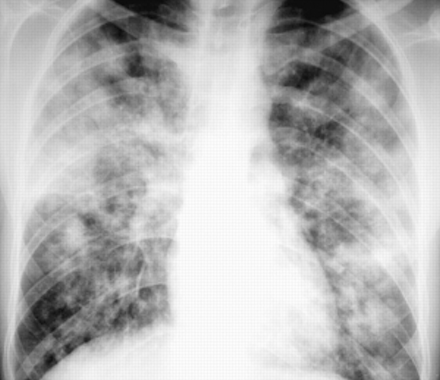
后前位胸片显示双侧非节段性强化在舌骨及右上、下叶。烟曲霉从痰中恢复。
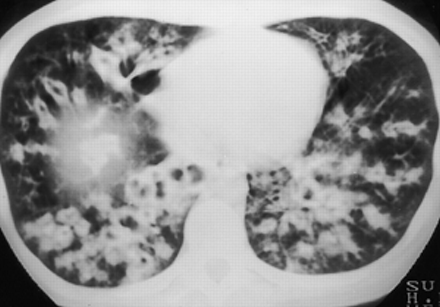
支气管阻塞性曲菌病的24岁男性获得性免疫缺陷综合征。计算机断层扫描(CT)显示双侧分叉的管状阴影是由明显扩张的支气管内的黏液物质阻塞造成的。CT表现与过敏性支气管肺曲菌病相似。
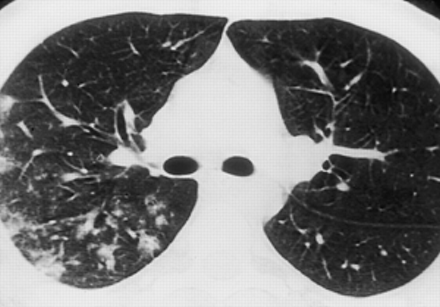
一例36岁女性骨髓移植后巨细胞病毒肺炎。高分辨率计算机断层扫描显示多个结节性混浊,边缘不规则,周围有毛玻璃衰减区。这种毛玻璃衰减晕是由于结节出血的性质。
68岁男性,严重中性粒细胞减少症,血管侵袭性曲菌病。计算机断层扫描的放大图显示左上叶有一个结节,周围有一层毛玻璃衰减晕(晕征)。
一个)的后前胸片的节目在左上叶圆形空洞合并特写视图。B)材料通过培养纤维支气管镜获得。从小培养结核分枝杆菌。
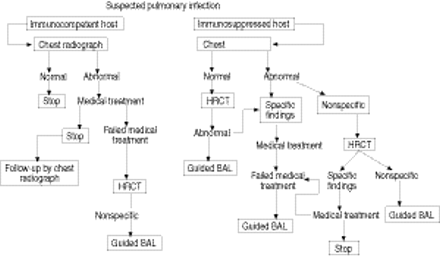
算法的怀疑有肺部感染患者的评价。HRCT:高分辨率的计算机断层扫描;BAL:支气管肺泡灌洗液。
脚注
↵本系列以前的文章:第1篇:Ghaye B,Dondelinger RF。成像制导胸干预措施。欧元和J2001;17:507 - 528。2号:Vansteenkiste JF, Stroobants SG。正电子发射层析成像的作用18呼吸肿瘤学中的f -氟-2-脱氧-d-葡萄糖。欧元和J2001;17:802-820。No. 3:胡国柱,陈小军,范贝克,许瑞柏,WG。磁共振成像肺通气:临床应用的门槛。欧元和J2001;17:1008 - 1023。No. 4:汉塞尔DM。小气道疾病:检测并用计算机断层扫描的见解。欧元和J2001;17:1294年至1313年。
- 收到2000年10月24日。
- 接受2001年2月9日。
- ©ERS杂志有限公司