摘要
PVR、DPG、PAC均与左心性肺动脉高压患者生存相关http://ow.ly/R8sF30ieHSQ
编辑器:
肺动脉高压(Pulmonary hypertension, PH)是左心疾病(left heart disease, LHD)常见的并发症,由于左心房压(left atrial pressure, LAP)“被动”增加,导致孤立的毛细血管后PH [1- - - - - -3.].有人提出了几个血液动力学参数来确定一种更严重的PH- lhd表型,其中肺动脉压力的增加不能由LAP的增加来解释,并将其描述为毛细管后PH与毛细管前成分的组合,或CpcPH [1- - - - - -3.].后一种血流动力学表型可能潜在地使患者面临更高的右心室衰竭风险和较差的预后[4,5].然而,自2013年上一届世界研讨会以来,如何定义PH-LHD中的前毛细血管成分一直是一个争论的问题,因为病理生理学的观点可能与临床和预后证据形成对比[1].
鉴于目前在这个问题上的争议和不确定性,我们试图进行荟萃分析,以确定哪个变量将与PH-LHD的死亡率相关。
我们根据PRISMA的建议进行了一项Medline文献研究[6]2013年以来发表的文章中,舒张压梯度(DPG)作为PH-LHD中毛细血管前成分的一个可能标志物被引入[2].我们使用以下搜索词的组合(“肺动脉高压”或“心衰”或“左心疾病”)和(“预后”或“结局”或“结局”或“生存”)和(“肺血管阻力”或“舒张压梯度”或“舒张压差”或“舒张压梯度”或“舒张压肺”)“血管压力梯度”或“肺动脉顺应性”或“血流动力学”)。我们只考虑了分析了DPG和/或肺血管阻力(PVR)和/或肺动脉顺应性(PAC)预测PH-LHD患者生存能力的论文。我们排除了报道综合结果的文章,那些只关注心脏移植后的结果,评估短期随访,或包括不稳定患者的文章。PRISMA流程图如图所示图1一个.
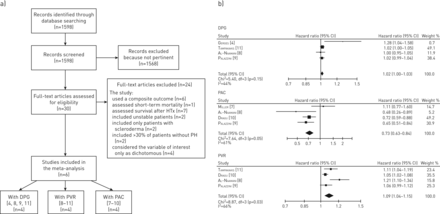
a)研究选择流程图。b)根据肺血管阻力(PVR)、舒张压梯度(DPG)和肺动脉顺应性(PAC)进行生存森林图分析。HTx:心脏移植;PH值:肺动脉高压。
在32条中,有10条对上述标准作出了答复[4,5,7- - - - - -14].这些文章将DPG、PVR和PAC视为连续或二分变量。为了一致性,并更好地区分与每个变量相关的风险,独立于任意截止值,我们只包括那些以连续方式报告变量预后能力的变量。因此,最终分析为就六条进行了讨论[4,7- - - - - -11],包括2513例LHD患者,随访9个月−15年。在四项研究中,所有患者都患有PH[4,8,9,11],而在其余两篇文章中,至少三分之二的患者有PH [7,10].在大多数研究中,进行了多变量分析,调整了与PVR、DPG和PAC相关的风险比,如年龄和性别[4,8,10,11],体重指数[10,11],种族[8,11],以及合并症[4,7]及其他血液动力学参数[8,10].
不同人群的PH-LHD在年龄、性别和病因等方面存在异质性。平均年龄为60岁,平均年龄在49岁到69岁之间。在射血分数降低(HFrEF)的心衰队列中,年轻的年龄组更有代表性,而在射血分数保留(HFpEF)或瓣膜病的心衰队列中,老年年龄组更有代表性。男性患病率在25 - 79%之间。在3项研究中,HFpEF是主要病因[4,8,10],而在三项研究中,瓣膜性心脏病是主要病因或显著的共病(高达30%的患者)[4,7,9].在这些后期研究中,有可能对一些患者进行了右心导管插入术作为治疗前评估,尽管作者尚未系统地报告。两种症状(如。纽约心脏协会功能分类),所有研究均未报道伴随的相关病理情况。
平均肺动脉压为35mmhg,平均PVR为3.0 WU,平均DPG为1.2 mmHg(后者来自五项研究[4,8- - - - - -11),平均PAC 2.5 mL·mmHg−1(来源于四项研究)[7- - - - - -10])。三项研究的平均PVR为>3 WU [7- - - - - -9,所有研究中平均DPG <7 mmHg,平均PAC <2.3 mL·mmHg−1在两个研究中[8,9].基于均值±sd在这六项研究中,至少有五项研究高度怀疑有相当比例的DPG为阴性[4,8- - - - - -11].
我们利用固定效应模型和随机效应模型合并了原始估计。研究特异性估计之间的异质性使用Q统计量和I进行检验2索引。当发现显著异质性(Q statistic p-value <0.05)时,给出随机效应模型的结果。为了评估发表偏倚,采用“修剪和填充”方法[15].这是漏斗图技术的扩展,“缺失的研究”是根据漏斗图的对称性来识别和估计的[16].
根据DPG、PVR和PAC进行生存的森林样地分析如图所示图1 b.PH-LHD患者PVR和DPG值升高与死亡风险升高相关,PAC值升高与死亡风险降低相关。仅对四项所有患者均有PH值的研究进行敏感性分析时,结果没有变化[4,8,9,11].一些存在发表偏倚的建议来自于“修剪和填充”方法的结果。即使DPG和PAC的summary估计值在统计学上没有显著性,这种方法得出的summary估计值与每个结果的summary original估计值非常相似。然而,由于纳入研究的缺乏,在解释“修剪和填充”方法获得的结果时需要谨慎[16].
因此,该荟萃分析可调和用于定义毛细血管前成分和/或预测PH-LHD预后的参数的对比理论和证据。
事实上,基于坚实的生理背景、与肺动脉重塑相关的组织学证明以及可能的预后潜力,DPG在2013年再次被引入作为疾病的标志物[2,4].然而,DPG是少数,受背景噪声影响较大,部分与舒张性肺动脉压和肺动脉楔压(PAWP)测量存在问题有关[1,17],因此发表的系列文章中超过30%的患者可能出现DPG阴性,这被认为是生理上不可能的[1].这可能是由于技术上的限制和对PAWP和/或舒张性肺动脉压力测定准确性的解释缺陷[1- - - - - -3.,17],亦可能在一定程度上影响PAC和PVR [1].值得注意的是,只有少数PH-LHD患者可能表现出较高的DPGs,这在meta分析的整个队列中被证实为较低的平均DPGs值(约1 mmHg)。然而,在与一些个别报告不同的情况下,发现DPG与结果相关,DPG单一增加的风险增加2%。
基于DPG的对比证据,PVR再次被引入,因为它可能作为右室功能的间接反映有额外的价值[3.因为,在PH-LHD患者中,当通过全身血管扩张剂或收缩剂改善心输出量时,它可能正常化。需要强调的是,PVR在临床实践中是一个巩固和长期使用的变量,尽管其血流和填充压力依赖的生理限制[1].我们的荟萃分析证实了PVR预后鉴别潜力的现有数据。PVR的单一增加与不良结局风险增加9%相关。
近年来,PAC在PH-LHD中的研究越来越多,并被提出作为预后预测因子[1,7- - - - - -10].然而PAC比DPG更小,它可能高度依赖于PAWP [18],而在临床实践中使用的计算公式可能会将真实PAC高估60 - 80% [1].尽管有这些局限性,PAC也与结果相关,较高的值与较低的风险相关。
应该强调这种分析的其他一些局限性。特别是,只有少数回顾性研究(或前瞻性注册的回顾性分析)可用于该分析,而没有对血流动力学测量进行前瞻性验证。这将鼓励我们在特别的设计的前瞻性研究。
总之,本分析证实PH-LHD人群在年龄、病因、DPGs阴性比例和血流动力学表现方面存在异质性。然而,尽管队列中存在差异,并且每个变量都有内在的局限性[1]、PVR、DPG和PAC似乎与PH-LHD患者的生存率相关。重要的是,我们可以推测这些变量应被视为互补变量,并可作为内在控制组合使用。哪种变量组合最适合用于预测结果仍存在争议。
确认
作者想感谢Irene Lang,Christian Gerges和Mario Gerges(心脏科,内科II,维也纳综合医院(AKH WIN),维也纳大学医学院,维也纳,奥地利),提供了他们自己的数据,否则不可用于这一荟萃分析。
脚注
支持声明:S. Caravita是ERS PAH短期研究培训奖学金(STRTF 2014-5264)的获得者,该奖学金由葛兰素史克提供的不限制资金支持,以及由意大利高血压协会提供的2014年“Cesare Bartorelli”国际资助。J-L。Vachiery是他所在部门的Actelion肺动脉高压研究主席。
利益冲突:J-L。Vachiéry已经收到了Actelion的资助,在提交的工作之外。
利益冲突:S. Caravita在提交的作品之外获得了Actelion的旅行补助金。
- 收到了2017年11月23日。
- 接受2018年1月23日。
- 版权©2018人队