文摘
几个病人肺感染后遗症Sars-Cov-2后经验,从自限的异常主要的肺部疾病。肺组织形态学分析可以帮助了解致病机制和提供一致的个性化管理。这项研究的目的是确定肺组织形态学和immuno-molecular的特性。Transbronchial肺cryobiopsy在持续的症状和患者进行ct提示剩余肺病从Sars-CoV-2复苏后感染。164患者被怀疑肺COVID-19后后遗症;10例肺实质疾病程度> 5%接受了肺活检。组织学模式并不均匀,在三种不同情况下的集群可以证明,这是反映在临床和放射学特征:集群(“慢性fibrosing”)一个预先存在的间质性肺炎的感染后发展为特征的;集群两个(“急性/亚急性损伤”)的特点是不同的类型和等级的肺损伤,从组织肺炎和fibrosing NSIP弥漫性肺泡损伤;集群三个(“血管变化”)的特点是弥漫性血管增加,扩张和变形(毛细血管和小静脉)在其他正常的实质。集群两个和三个被immunophenotypical特征变化所观察到的类似/年初温和covid-19肺炎(STAT3的表达异常增生性pneumocytes PD-L1,被罩和STAT3在内皮细胞)。 This is the first study correlating histological/immunohistochemical patterns with clinical and radiological pictures of patients with post-COVID lung disease. Different phenotypes with potential different underlying pathogenic mechanisms have been identified.
介绍
随着COVID-19流行的进展,一些病人正在经历长期多器官的症状和并发症(长COVID或post-COVID综合症)1- - - - - -13]。这种持续的临床表现的影响和后果是日益严重的健康问题。残留的证据器官损伤后COVID-19感染尤其适用于肺后遗症,与光谱从自限性的异常主要肺部疾病的临床资料,与变量的重要程度炎症和/或纤维异常。肺组织的组织学评估这晚阶段可能有助于揭示特殊morpho-phenotypical变化,以及未来研究模式进化,可能有助于更好地理解致病机制和提供一致的个性化治疗。在这里,我们审查的形态学和immuno-molecular特性transbronchial肺cryobiopsies (TBLC)执行持续的肺病患者康复后Sars-CoV-2感染和潜在的解释观察到肺异常。
方法
研究设计和病人的选择
我们进行了比较,前瞻性,多中心,研究者发起的观察性研究,从2021年1月1日到2021年3月31日,目的是评估组织学和免疫组织化学和分子功能患者的肺组织的持续肺HRCT上参与(高分辨率计算机断层扫描)扫描和持续的症状(呼吸和/或系统)从Sars-CoV-2复苏后感染。合格的受试者年龄在18岁和80岁,有一个历史的早期分子诊断证实的COVID-19相关肺炎、复苏前至少30天,持续肺HRCT扫描分析参与> 5%,持续的症状(呼吸和/或系统)和没有禁忌症肺活检。复苏的定义根据国家指示更新2020年12月的连续两个负面测试Sars-CoV-2 rrt - pcr在24小时与可能的改进/稳定的症状。关键的排除标准肺功能严重受损或休息时,低氧血,出血风险高,肺动脉高压的超声心动图评估和严重并发症(细节发表在在线数据补充);最后,病人无法提供同意或拒绝活检被排除在外。本研究按照规定发行的赫尔辛基宣言;机构审查委员会批准的协议是(IRB)区域Vasta大区伦理委员会(防。5285/2021)和病人提供了他们的知情同意。进行了高分辨率计算机断层扫描和Transbronchial肺Cryobiopsy前面描述和报道补充数据(14- - - - - -17]。形态学检查是基于传统hematoxylin-eosin污渍和细胞角蛋白免疫染色7。五个专门的肺部病理学家(公元,广义相对论,副总裁,m。,和C。D。) blindly and independently reviewed the slides from all biopsies and quoted several morphological features involving different compartments constituting the lung parenchyma: epithelial and vascular components, alveolar and interstitial spaces, inflammatory cells. Divergent opinions were then overtly discussed and a final consensus was reached in all cases. All immunohistochemical tests were performed in the ULTRA Benchmark automated immunostainer (Ventana Medical Systems/Roche, Tucson, AZ) using standard procedures and reagents are described in表S1。控制我们分析了15例弥漫性肺实质疾病感染控制标本:三个不明原因引起的组织肺炎(OP),三个非特异性间质性肺炎(NSIP),两个OP / NSIP,两个通常的间质性肺炎(摘要),两种纤维过敏性肺炎(当天),一个特发性急性纤维蛋白的组织肺炎(AFOP),一个结节病,一个与吸烟有关的间质纤维化(SR-IF)。
结果
临床特点
164名患者被称为我们的所有门诊疑似肺COVID-19后后遗症。在141名患者,肺实质疾病缺席或< 5%,13个病人禁忌症肺活检或没有提供同意过程;10个病人接受transbronchial肺cryobiopsy。平均年龄是61岁(范围,38 - 76年)和78%都是男性。7/10的患者被送往医院,但没有人气管插管。归纳了临床特点表S2。复苏后患者进行支气管镜检查平均3.5个月Sars-CoV-2感染。活检时所有情况下导致负面Sars-Cov-2分子拭子检测。大多数病人疲劳和报道发低烧,少数报道关节和肌肉疼痛和抑郁(表S2)。平均用力肺活量(FVC)预测值的77% (46 - 116);中位数一氧化碳扩散系数(DLCO) 51%的预测值范围(43 - 80)。最具代表性的实验室测试中所示表S3。
高分辨率计算机断层扫描
影像学检查总结表1。集群在子群(1),CT扫描显示纤维外表与间质参与的一些方面,建筑变形和牵引支气管扩张;在这些患者中,一个先前的CT扫描显示的预先存在的背景纤维化肺间质异常(马尼拉),是稳定和持久COVID-19肺炎后(图1),而在第二个病人,急性合并蒙面和覆盖的可能存在潜在的预先存在的牵引支气管扩张。
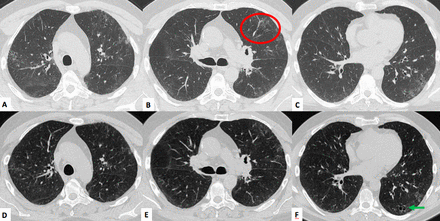
CT扫描在60 y / o男,吸烟者。CT扫描在急性感染(a - c)轻微的边缘磨砂玻璃出现在上部叶,主要在左侧半胸(红圈)。分散地区的囊性变化暗示领空扩大与纤维化相关AEF)有轻度建筑变形存在双边。CT扫描进行4个月后(d-f)显示减少磨砂玻璃衰减,残余的磨砂玻璃衰减和地区时(f,绿色箭头)。
集群在5例(2),CT扫描显示,持久性的磨砂玻璃与perilobular模式和合并中观察到组织肺炎(OP)或纤维化NSIP (无花果。2和3);一个共同特征是残留血管扩张(重力依赖perilobular模式评估后容易定位)作为peri-lobule[应该小静脉的扩张18]。最后,第三子群(集群3)的特点是只有轻微的剩余辐射变化,有轻微磨砂玻璃与外围perilobular模式2/3。在一个单一的情况下,特征表明pleuro-parenchymal fibroelastosis上部叶被观察到。
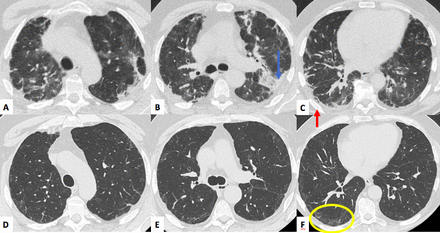
男性,62 y / o,急性Covid感染的特点是双边、外围合并(a, b,蓝色箭头)和perilobular模式(c,红色箭头)。两个月后(d-f) CT扫描显示轻微的边缘网状和最小perilobular模式,主要是在正确的下叶(f,黄色的圆圈)。
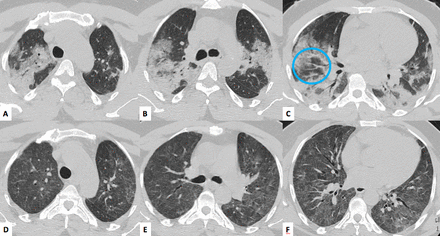
男性50 y / o, Covid-related急性肺炎(a - c)和广泛,支气管血管周围合并,两肺(a - c)和低叶小叶爱惜。温和的磨砂玻璃衰减存在于两个上部叶与血管扩张(c,蓝色圆圈)。两个月后,一个温和的,磨砂玻璃扩散衰减存在于两肺与支气管扩张中心在中部叶和叶都低。
组织模式和免疫组织化学
组织学评价)彩色幻灯片显示肺结构的重大修改所有10个调查情况下,匹配3个集群分离。所有情况下进行了测试,结果为阴性Sars-Cov-2 [原位杂交在组织(smFISH方法、HuluFISH Pixelbiotech德国)和实时逆转录酶聚合酶链反应(rt - pcr)测定在拜尔(支气管肺泡灌洗)]。
集群1(“预先存在的慢性fibrosing”)
这个集群的特征包括两例摘要(通常的间质性肺炎)所定义的建筑变形、时空异质性的疤痕修改,成纤维细胞的焦点和微蜂窝(图4),或者fibrosing与吸烟有关的间质性肺炎,定义的肺泡巨噬细胞包含与吸烟有关的浅棕色色素的积累空间和间质胶原纤维(表S4)。免疫组织化学分析在第一种情况下符合摘要,包括TUBB3 myofibroblasts和焦p16表达pneumocytes [19]。第二例吸烟(显示已存在的背景相关ILD HRCT后坚持COVID-19肺炎),显示组织学特性与吸烟相关ILD一致,也与淋巴结节(20.]。
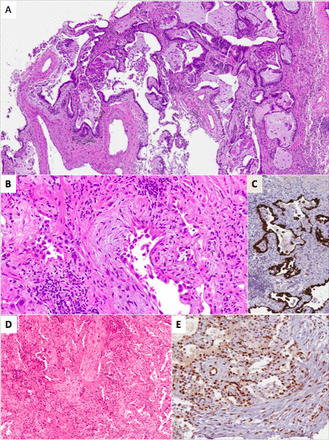
集群1。案例与摘要模式:建筑变形,疤痕的修改的时空异质性,微蜂窝。)(一个);集群2。案例与形态学的证据进行间质纤维化和扩展AECII增生中观察弥漫性肺泡损伤(爸爸),增殖的阶段。)(b)。Cytokeratin-7上皮细胞组织化学染色,低倍镜下,严重抹杀的实质结构。(c);集群2。肺炎与组织模式。)(d)。大多数上皮细胞和内皮细胞表达核pSTAT3 (e)。
集群2(急性/亚急性损伤)
集群两个特征的不同类型和等级的肺损伤,从组织肺炎或重叠OP / NSIP弥漫性肺泡损伤(爸爸——增殖阶段,2例)(图4)[21]。这些情况下共享形态学和免疫组织化学相似性与先前描述[COVID-19严重肺炎病例16]。在两种情况符合爸爸(增殖/组织没有hjaline膜),孔隙空间被密集的纤维化和弥漫性增厚myofibroblasts总量(图4)。剩余牙槽空间被片状增生性AECII集合的排列,表达pSTAT3 Ki67。四个病例的特点是发生endoalveolar马森的身体和各种大量的间质增厚(OP / NSIP) (图4)(表S4)。炎症细胞:丰富的免疫浸润,主要由淋巴细胞出现在所有集群2例,广泛地分布在孔隙空间,或形成血管周的总量;淋巴浸润T细胞和B细胞主要由;在T细胞、CD4细胞、CD8子集几乎同样表示。巨噬细胞并不代表,中性粒细胞是罕见的和没有观察到嗜酸性粒细胞。肺泡细胞:增生性AECII被高Ki67指数特征,和核pSTAT3。TUBB3染色也表示在肺泡细胞,主要在情况最严重的伤害。血管床发现:扩散被罩,PD-L1 pSTAT3疣状内皮细胞的血管间质毛细血管和小静脉,这代表最相关的发现在这个群(22]。
集群3(“血管变化”)
集群3的特点是弥漫性血管增加,扩张和变形(毛细血管和小静脉)在一个正常的实质(最小参差不齐AECII增生在一个案例中)(表S4)(图5)。这种模式相媲美,在早期阶段描述COVID-19肺炎与守恒的实质结构(16]。炎症细胞:少量巨噬细胞和间质T淋巴细胞,没有CD4和CD8明显的优势。PD-L1表示在肺泡巨噬细胞(通常可以观察到在肺泡巨噬细胞在正常情况下),但是没有PD-L1免疫反应性上皮中可观察到肺泡细胞。血管床:弥漫性PD-L1染色装饰了毛细管内壁连同被罩在内皮细胞反应性(图5)。基质/间质室:没有TUBB3反应观察。这些病例与某些情况下分享相似的早期/轻度COVID-19肺炎前所述[16),特别是PD-L1扩散和强大的表达式的持久性和吲哚胺2,3-dioxygenase (IDO)内皮细胞间质毛细血管和小静脉急性阶段情况下。这种特殊的表达谱可能表现为强烈与SARS-CoV-2肺炎更相关,因为这些标记并不是通常观察到缺席在肺组织中获得健康受试者(23,24)和/或控制例弥漫性肺实质疾病感染控制标本。这些形态学异常反映在BAL液(表S3);事实上,所有淋巴球增多在BAL患者(> 20%)的特点是组织肺炎肺组织,与丰富的免疫浸润,主要由淋巴细胞,位于血管周的间隙空间,有时形成结节聚集。
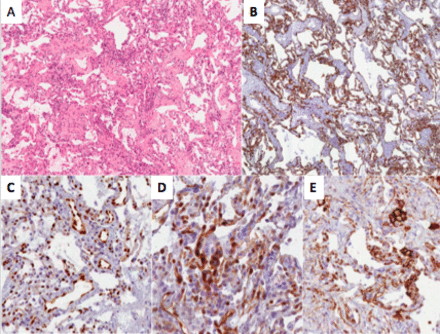
集群3。增加与弥漫性血管,扩张和变形(毛细血管和小静脉)在一个正常的实质。)(一个);Cytokeratin-7疣状(b);扩散和强劲的内皮表达pSTAT3 (c)、油(d)及PD-L1 (e)。
讨论
据我们所知,这是第一个潜在morpho-phenotypical变动分析患者持续的症状和残余肺实质疾病从COVID-19复苏后。大多数已发表的研究都很小,主要集中在临床后遗症患者住院COVID-19 [1,3- - - - - -5,6,8,10]。鲜为人知的肺部病变的范围和特点COVID-19幸存者,主要是那些温和的感染不需要住院。三例post-COVID组织学证实OP迄今已发表(两个trans-bronchial肺活检和一个外科肺活检)(25,26)和11个无症状患者曾感染COVID-19接受选择性肺切除术对其他不相关的迹象(无症状恢复幸存者被证实没有明显的组织病理学变化表明实质损害)(27]。一样与其他间质性肺疾病(ILDs),肺活检在post-COVID-ILDs可能有重要的作用,为了更好地定义组织模式管理的目的。ILDs社区一直意识到纤维化非特异性间质性肺炎肺炎和组织发展到纤维化不是经常看到爸爸的幸存者/急性肺损伤(28]。当前算法主要视图post-COVID肺部疾病作为一个单一的实体;然而,不同的COVID-induced通路的存在可能构成独立post-COVID肺实体,可能需要单独管理。在这个多学科研究中,我们已经确定了三种不同亚型或群体(表2)。
一组(集群1)是由功能特征表明间质性肺病的发生之前SARS-CoV2感染。这两种情况下包括是男性和前吸烟者。临床行为的特点是持续的呼吸道症状COVID-19肺炎后,努力和咳嗽气短,少系统性症状(表S2)。与摘要的一个案例中,模式是一致的,是由纤维的特征出现在CT扫描和肺组织,建筑变形、牵引支气管扩张、时空异质性的疤痕修改,和扩展蜂窝(图4和表1)。可以认为在这种情况下,急性合并蒙面与覆盖潜在的存在既存fibrosing ILD。第二个病人记录已存在的背景,纤维间质肺异常(马尼拉)COVID-19肺炎后的稳定和持久。前肺功能测试正常(FVC预测103%,FEV1 104%的预测,DLCO 76%预测)。肺cryobiopsy显示模式符合与吸烟有关的间质纤维化,SR-IF)。我们假设post-covid-19病例的数量,以辐射和/或纤维化的病理发现表象可能更预先存在的肺间质性疾病的一个表达式(可能是也可能不是加速了病毒感染本身)比严格与病毒感染有关。加速肺纤维化的呼吸道病毒被描述在博来霉素的肺纤维化模型(29日];有趣的是,在这些情况下,焦点相关的细胞表达细胞衰老标记观察p16在摘要/ IPF [30.- - - - - -34]。
第二个集群包含患者更“auto-inflammatory”表型,与不同的临床表现,辐射特性和immuno-morphological模式。引发的炎症通路可能是病毒本身引起2型pneumocytes扩散/激活,大量炎症细胞和血管功能障碍。CT扫描显示剩余磨砂玻璃perilobular模式,有时合并,光环和反向光环迹象迹象,没有纤维变形;这些变化可以包括在OP-like模式(表1)。所有的病人有不同的形态类型和等级的肺损伤,从组织肺炎弥漫性肺泡损伤(爸爸-增殖阶段),在共同丰富的免疫浸润,主要由淋巴细胞,血管周围和间隙空间,有时形成结节聚集。更频繁地在这个集群,患者全身症状,如发热、疲劳、和呼吸道症状(表S2)。集群两个患者用类固醇治疗后肺活检结果(报告细节补充)。组织肺炎的肺活检经历了明显改善患者症状和肺功能损害;不到随访CT扫描显示在磨砂玻璃领域的显著减少,perilobular模式在所有情况下。弥漫性肺泡损伤患者/增殖阶段功能肺活检显示温和改善,临床和功能,完全解决发热和减少呼吸短促,虽然持续的体力活动轻度至中度;不到后续扩展的CT扫描显示轻微减少实质参与。
第三组包括患者持续呼吸道和系统性症状但对CT扫描变化很小。的组织学张照片的特点是膨胀腔内的肺泡毛细血管和小静脉和毛细血管增生原本正常或轻度的实质异常(最小的片状AECII增生和异构间质增厚在一个案例中)。我们认为这种“模式”在某些方面类似于肺毛细血管hemangiomatosis(增生的间质和肺泡壁毛细血管,频繁的管腔扩张毛细血管和毛细管堵塞);然而,我们认为他们显然是两个截然不同的条件。事实上,毛细血管增生中观察到集群3例不典型围绕bronchovascular包,不创建任何结节状外观;内皮细胞增殖信号为负(即。ki - 67)和血管的变化也涉及post-capillary小静脉,显示扩张和曲折的腔,水肿的内膜增厚和不完整的血管周围淋巴细胞浸润,未观察到毛细管hemangiomatosis做的所有更改。此外,hemosiderin-laden巨噬细胞和内膜的增厚的小肌肉动脉并没有观察到。所有这些患者接受超声心动图和肺动脉高血压被排除在外。有趣的是,分子的表达参与免疫错乱和血管张力控制(STAT3、被罩、PD-L1)被改变为在早期阶段COVID-19肺炎(16]。为了评估这些发现是否与Sars-CoV-2感染,我们分析了控制例弥漫性肺实质疾病感染控制样本,我们发现这些标记的内皮表达是微弱和/或局限于罕见的细胞。
最相关的结果,我们的研究之一是持续高表达的核pSTAT3肺泡上皮细胞和内皮细胞的间质毛细血管和小静脉月SARS-CoV-2清算后的感染。核pSTAT3尤其在集群2例,特点是更加突出系统性症状(主要是发烧和疲劳)与磨砂玻璃的透明持久性有关CT扫描,perilobular模式和合并。这些情况下共享相似之处严重COVID-19肺炎先前描述的情况下(16),肺泡上皮核pSTAT3 2型细胞和内皮细胞表达。显著减少pSTAT3 Baricitinib管理后患者严重Covid-19肺炎,防止恶化,更安全、更良好的临床结果,就得以证实[35]。这些结果可能会显示一个潜在的理由使用Janus激酶JAK1和JAK2抑制剂的患者群的post-Covid持久的症状。中的所有患者研究发现负面Sars-CoV-2落下帷幕,在确认事实,肺部表现并不与持久性相关的病毒在肺,但与致病机制无论病毒清除后,持续感染。我们已经观察到血管畸形(无序血管生成与腔的扩大,扩张血管壁,血管周的t细胞浸润)从一开始就明显存在COVID-19肺炎,可以通过先进的疾病持续阶段(16),也可能持续几周/月后感染。co-regulatory配体PD-L1和耐受性酶被罩是负面反馈电路,抑制免疫反应和维护外围公差(36- - - - - -38),都与防御机制从肺损伤39- - - - - -42]。色氨酸是被罩的基质酶活性,证实了色氨酸代谢产物水平异常Covid-19,在恢复正常化(42- - - - - -44]。正如前面展示的,我参与调节血管重塑和放松24),根据这项研究其潜在作用在降低肺血管阻力也可能参与长COVID或post-COVID综合症。这些观察可以解释持久性CT扫描,在一些post-COVID情况下,毛玻璃衰减的地区,有或没有一个“疯狂的铺路”模式,与扩大静脉包含在毛玻璃地区,部分消失,改变从仰卧的卧姿(“venoplegic /充血模式”)42]。在一些post-COVID本系列的情况下,我们观察到这些功能的持久性CT扫描(表1),通过先进的疾病阶段在感染后数周/月。
这项研究有一些局限性。首先,肺功能测试的基线数据和胸部CT扫描并不可用,登记患者的数量是有限的和病人团体是异构的。第二,短时间内所有抽样和急性COVID-19感染可能进一步关注的问题,因为它可能不是代表长期异常。在未来,需要一个更大的样本和更长的纵向观察研究对阐明至关重要的健康后果归因于COVID-19。
总之,这是第一个研究表明组织学模式之间的相关性与临床和放射免疫组织化学post-COVID综合症患者的照片,确定不同亚型或表型与潜在的不同的底层致病机制(表2)。我们的研究结果证实,需要多学科评估这些患者(而不是有限的想象评价)来识别关键子组病人和他们目前的优化管理。特别是immune-histochemical评价肺组织可能有助于揭示特殊形态及morpho-phenotypical变化这个新的“Post-COVID / Long-COVID综合症”,但也有助于更好地理解致病机制和有效地进行治疗干预研究奠定基础和设计未来的后续计划如前所述17,45- - - - - -48]。尽管不同细胞类型的致病作用和机制导致不同疾病endotypes并不完全理解,这种异质性可能会反映出不同的间质性肺病COVID-induced表型,可能伤口愈合异常倾向的学科。Post-COVID肺病不是一个单一的实体,但包括不同亚型或群体(49),每个人都可能需要独立和不同的管理。
应答:
我们感谢基金会Cariverona(制定项目)的金融支持和AMMP (Associazione Morgagni Malattie Polmonari)对患者的支持。
脚注
利益的声明:我们报告没有利益冲突
作者投稿者:CR、CD, MC和VP的构思和设计研究;CR、CD和MC写论文;CR、CD, MC, SP广告,GR和副总裁导致了数据的解释;所有其他作者评论草稿纸,导致写作的最终版本的手稿
支持声明:不适用
- 收到了2021年9月4日。
- 接受2022年2月13日。
- 版权©2022年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org