摘要
背景结合抗生素阿奇霉素和羟基氯喹诱导气道免疫调节作用,后者也有在体外抗病毒性质。这可能会改善为Covid-19住院患者的患者的结果。
方法安慰剂对照双盲随机多中心试验。招募年龄≥18岁、住院≤48 h(非重症监护)且SARS-CoV-2 RT-PCR检测阳性的患者。干预方案为:每日阿奇霉素500 mg,连续3天;每日阿奇霉素250 mg,连续12天;每日羟氯喹200 mg,连续2次,连续15天。对照组给予安慰剂/安慰剂。主要转归为存活天数和14天内出院(DAOH14)。
结果在117名患者随机分组后,在第一次计划的中期分析中,数据和安全监测委员会建议基于预先指定的标准,以无效为理由停止登记。因此,审判于2021年2月1日终止。共有61例患者接受联合干预,56例患者接受安慰剂。干预组患者中位DAOH14为9.0 (IQR, 3-11)与.9.0 DAOH14 (IQR, 7-10)在安慰剂组(p=0.90)。干预组中有1例患者在第30天因所有原因死亡与.2例患者接受安慰剂(p=0.52),干预组9例患者在30天内再次入院或死亡与.6例患者接受安慰剂(p=0.57)。
结论阿奇霉素和羟氯喹联合使用并没有改善COVID-19患者的生存或住院时间。
摘要
羟氯喹与阿奇霉素联合干预对确诊2019冠状病毒病住院患者无有益或有害影响。
介绍
在2019冠状病毒病(COVID-19)大流行早期,一些证据(主要来自实验室研究)表明,氯喹及其毒性较小的衍生物羟氯喹(通常用作抗风湿药物),通过抑制数个ph依赖的复制步骤和内体病毒进入人类细胞,对冠状病毒具有抗病毒作用[1].这些发现已在感染严重急性呼吸综合征冠状病毒(SARS)-1的灵长类细胞的实验室研究中得到证实[2].羟氯喹还可与宿主细胞的唾液酸和神经节苷类高亲和力结合,从而保护细胞不与sars -冠状病毒-2结合通过它的刺突蛋白[3.].在大多数国家,羟氯喹按推荐剂量服用,每天最多可达400-500毫克,似乎是安全的,即使在使用较长时间和成本较低的情况下[4].
阿奇霉素是一种大环内酯类抗生素,已证实可有效减少气道炎症和随后需要住院治疗的慢性阻塞性肺病(COPD)加重、哮喘和支气管扩张[5- - - - - -7].最近,在急性呼吸窘迫综合征(ARDS)的危重患者中发现阿奇霉素治疗与生存率提高之间存在很强的相关性[8],并在系统性元分析中得到更有力的总结[9,10].此外,羟氯喹和阿奇霉素可能协同作用,防止冠状病毒与人类细胞上的神经节苷酸受体结合[11].
重要试验显示,瑞德西韦、抗il6和恢复期血浆等药物在病情较轻和疾病早期阶段均有积极结果[12- - - - - -14但这些干预措施对重症患者似乎效果较差[15].另一方面,在更严重的情况下,皮质类固醇等免疫抑制药物确实表现出一些影响[16].因此,在疾病的早期和较轻阶段进行抗病毒治疗似乎是这些药物的机会之窗[17].
本试验评估了氮霉素和羟基喹啉的组合,中度和批准的(用于风湿性指示)给药方案,将增加住院治疗患者的活跃和从医院排放的Covid-19。
方法
试用协议和统计分析计划可用补充信息第1及2节,并曾发表[18,19].该研究得到了所有参与站点伦理委员会(H-20022574)、丹麦药品管理局(EudraCT no 2020-001198-55)和丹麦数据保护局的批准。丹麦参与区域的GCP单位按照良好临床规范(GCP)对其进行监测。这项研究是根据《赫尔辛基宣言》进行的[20.没有向调查人员或参与者提供任何经济奖励。有一个独立的数据和安全监测委员会(DSMB),由三名临床医生和研究人员组成,他们是进行大型随机研究的专家。此外,DSMB还获得了试验统计学家Tobias Wirenfeldt Klausen先生的权限,他是一名高技能的生物统计学家,也监督了临时分析。克劳森先生随时都可以参与DSMB的工作。他也对治疗分配盲目,因为只有试验药剂师有解除盲目的关键。
该DSMB审查了试验的进展,并在试验期间进行了安全性、有效性和数据完整性评估。我们不可能(为了及时性)让患者或公众参与我们研究的设计、实施、报告或传播。本研究是一项初步分析,并根据随机试验报告综合标准(CONSORT)指南进行描述。
研究设计和地点
在住院的Covid-19(Propac-Covid)研究中与阿奇霉素和羟氯喹的主动保护是一种多期,双盲安慰剂控制,随机临床试验,调查是否加入氮霉素和羟氯喹的15天治疗到护理标准减少住院时间,减少非侵入性通风(NIV)的风险,对重症监护单位(ICU)和死亡进行入场。患者于2020年4月6日至2020年12月21日之间注册,2020年12月21日在董事会内的丹麦六名医院:Trin Collaborations(www.coptrin.dk)。选择的剂量是基于用于治疗其他疾病的良好耐受剂量(例如风湿病),同时降低心脏副作用的风险。选择持续时间是为了确保在大部分住院患者中覆盖长期住院的患者,并安全地覆盖主要结果的整个观察期间。此外,选择持续时间以防止革兰氏阳性微生物的继发感染。
参与者
符合条件的患者为:1)年龄≥18岁,2)经逆转录聚合酶链反应(RT-PCR)确诊为SARS-CoV-2感染阳性入院,3)住院时间≤48小时。每位患者都签署了参与的知情同意书。符合以下条件的患者被排除:1)接受>5 L供氧;2)已知对研究药物不耐受/过敏;3)神经性听力损失;4)牛皮癣;5)视网膜病变;6)黄斑病变;7)视野改变;8)母乳喂养/怀孕; 9) severe liver disease (international normalised ratio>1.5 spontaneously); 10) severe gastrointestinal disease (investigator-assessed liver disease, severe ulcerative colitis or Crohn's disease, peptic ulcer disease, or cancer); 11) neurological or haematological disorder; 12) estimated glomerular filtration rate (eGFR)<45 mL·min·1.73 m2;13)临床上有明显的心脏传导障碍/心律失常或校正QT间期延长(QTc;即。F>为雄性480 ms, >为雌性470 ms);14)重症肌无力;15)正在接受地高辛治疗;16)葡萄糖-6-磷酸脱氢酶缺乏;17)卟啉症;18)低血糖(血糖<3.0 mmol/L)-1);19)无法给予知情同意的;20)严重阻碍合作的语言问题;或接受麦角生物碱治疗。研究者根据这些标准评估患者的适格性。
随机和屏蔽
研究药剂师生成了随机序列,然后将其输入由参与的丹麦地区主办的在线平台REDCap电子数据捕获工具。患者按1:1随机分配阿奇霉素加羟氯喹或匹配安慰剂胶囊。在大小未知且不同的组块中进行随机分组,最终分组按年龄进行盲法和分层(> 70)与年龄≤70岁)、招募部位、患者是否有以下慢性肺病(有)与否):COPD,哮喘,支气管扩张或间质性肺病。所有患者和研究人员都对参与者治疗任务蒙蔽了蒙蔽。这包括成果评估员,调查员和学习护士,以及研究和临床工作人员。DSMB在整个盲目蒙蔽,并使所有建议都蒙蔽了治疗拨款。只有审判的首席药剂师只持有关键的遮盖。在收到并承认DSMB推荐后,2月1日在2021年2月1日发生了正式的解布式。
干预
患者随机分为两个治疗组:1)500 mg阿奇霉素1次/日+ 200 mg羟氯喹2次/日,第1 - 3天;2)用安慰剂而不是两种干预药物。药物(双臂)均标有中性标签:例如,“阿奇霉素A组”和“阿奇霉素B组”。两种研究药物的一个重要安全性考虑是QTc延长[21,22因此,试验人员在住院期间至少两次测量QTc。
主要终点和次要终点
主要终点是随机分组后14天内的存活和出院天数(DAOH)。这种结果测量方法是由试验人员开发的,既敏感又具有临床相关性,它提供了一种计算持续恢复天数的方法,没有导期偏差[23- - - - - -25].对于第一个次要终点,每个患者在第5天和第15天被置于以下8个类别中的一个,如我们之前的研究所述[12: 1)出院,活动不受限制;2)出院,但活动受限(可能/可能不在家接受长期氧疗);3)住院观察,未接受辅助氧疗或其他治疗的;4)住院且未接受补充氧治疗,但接受其他治疗(可能/可能与COVID-19无关);5)住院并接受第(2)或(3)项所述方法以外的补充氧气,如鼻导管;6)住院并接受无创通气或高流量设备输氧;7)住院并接受机械通气或体外膜氧合;或8)死了。该试验包括其他8项次要结果:1)在ICU的天数(时间框架:14天);2)住院期间需要NIV的天数(时间框架:14天); 3) mortality rates (time frames: 30, 90, and 365 days); 4) length of hospitalisation (time frame: 14 days); 5) DAOH (time frame: 30 days); 6) time to readmission for any reason (time frame: 30 days); 7) change in patient's pH, PaO2,或者PCO2分压测量(时间范围:4天);8)不需要补充氧或给予“长期氧疗”的时间(时间范围:14天)。随后报告30天>随访的结果。所有结果和分析都严格按照SAP进行。
样本大小的计算
假设双侧显著性水平为5%,功率(1 - β)为80%,计算主要结果(随机化后14天内DAOH)的样本量。采用组序研究设计,在半目标招募时进行中期分析。标准偏差设定为4天[26],检出限为1.5天(双向)。StudySize软件(版本。3.0;CreoStat HB,哥德堡,瑞典)用于计算226名参与者的样本量。
统计分析
我们比较结果使用t检验或Mann-Whitney U检验连续变量(取决于分布),χ2名义变量的Fisher精确检验,以及比较Kaplan-Meier生存曲线的log-rank检验。累积事件估计是使用Cox比例风险模型中的风险比(HRs)和95%置信区间(CIs)生成的。使用多重效应模型对连续数据进行调整。主要分析基于意向治疗(ITT),其次根据方案分析主要和次要结果。p值<0.05认为有统计学意义,所有分析均为双侧分析。我们最初计划在研究达到总样本量的50%时在两组之间进行中期分析。然而,作为对梅赫拉随后撤回的一篇文章的回应等.[27,丹麦药品管理局要求我们对招募的前75名患者进行非同寻常的急性中期分析(不暴露)。DSMB对此进行了审查,建议继续积累患者(2020年5月)。首次计划的中期分析在117名患者(50%纳入)中进行,试验因无效而停止(2021年2月)。主要结果的敏感性分析包括:1)接受部分或全部干预治疗(全天)的改良ITT患者群体;2)在所有计划天数内接受两种干预药物的方案人口;3)主要结果的多效应调整模型,其中对以下参数进行调整:我)年龄(每年递增),2)性别(男与女),3)体重指数(每单位增加),4)包括氧疗(是的与没有),v)remdesivir(是的与没有),6)任何预先存在的肺部疾病(阻塞性、间质性或支气管扩张:可以与没有),7)糖尿病(是的与没有),VIII.)跨越中位的QTC(是的与没有)。采用SAS软件进行统计分析。9.4;SAS Institute, Inc., Cary, NC, USA)和R软件。3.4.3;R开发核心团队,维也纳,奥地利)。
结果
在664例筛查患者中,117例符合纳入研究(图1)。排除原因包括:无法给予知情同意(18.8%的排除),eGFR<45 mL·min·1.73 m2(17.9%除外),并拒绝参与(16.3%除外)。在纳入的患者中,61名患者随机分配到阿奇霉素加羟氯喹组,56名患者随机分配到安慰剂组。参与者的中位年龄为65岁(四分位范围[IQR], 52-77),其中65(56%)为男性。自症状出现以来的中位时间为8天(IQR, 4-10)。随机分为干预组和安慰剂组的患者基线特征见表1,在表1和表2在补充资料第3部分.
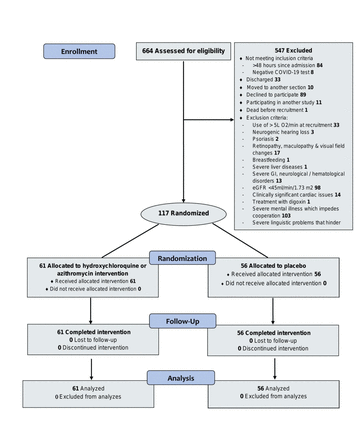
联合图。
二次结果
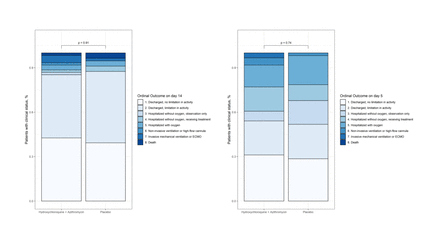
在随机化后15天,羟氯喹加二十霉素组和Covid成果规模得分中的安慰剂组无显着差异(或1.0 [95%CI,0.5-2.2]; P = 0.91;图3和补充信息第3部分的表6)。一个因果在开盲后,指导委员会要求对第5天的顺序结果进行分析,以提供及时更新的临床状态评估;该分析还表明,两组患者相似(OR, 0.9 [95% CI, 0.4-1.8];图3和ETABLE 7在补充信息教派中离子3).我们也发现两组在预先指定的辅助临床结果(表2,图2)。我们测试了试验干预和症状持续时间之间的相互作用(<8天与8天或以上),无交互作用(p=0.79)。
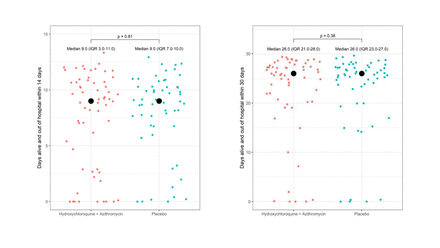
天在14天和30天内,中位数(IQR),天中的日子。
呈现不良事件数据表3和补充信息第3部分的表8.随访期间,羟氯喹联合阿奇霉素组的61例患者中有1例(1.64%),安慰剂组的56例患者中有2例(3.6%)记录的QTc大于500 ms (表2)。包括腹泻的不良事件(12与3)、恶心(11与6)和头晕(10与3)羟氯喹联合阿奇霉素组较安慰剂组发生频率高。相反,涉及QTc延长的不良事件(女性> 470 ms,男性>480 ms)在安慰剂组中更为频繁(4与7).仅报告2例严重不良事件,均发生在安慰剂组(补充信息第3部分的表8)。
讨论
在符合监测指南的情况下,在DSMB的建议下,基于预先规定的无效标准,ProPAC-COVID试验在招募一半人员时停止。与安慰剂相比,阿奇霉素和羟氯喹的联合似乎对测量结果没有任何影响。两组的主要结果(随机化后14天内DAOH)与顺序结果测量、所有原因和再入院的死亡率相似。
我们的审判是第一个报告这种羟基氯喹加氮霉素的这种组合,在正常推荐剂量中施用15天与安慰剂。其他试验报告了单药干预与安慰剂或大剂量羟氯喹加阿奇霉素与.这些药中的一种。
之前的一项试验报道了一种类似于我们的羟氯喹给药方案[29],尽管在5天内没有阿奇霉素;该试验也因无效而停止,并报告了中性结果。在我们的试验中,研究参与者普遍没有严重的疾病,这与试验的意图和理由一致:在器官衰竭明显之前减少病毒复制(羟氯喹)和高炎症(阿奇霉素)。这种药物组合未能使COVID-19患者受益的一些原因可能包括药物无法渗透到气道上皮,药效较低在活的有机体内比在体外,中和有益和有害的影响。
虽然我们知道,试验可能没有足够的力量来分析所有预先规定的结果措施,但所有分析结果的一致中立立场强烈表明,干预没有带来任何好处或伤害。的特殊利益,我们使用两种药物的推荐剂量和尊重羟氯喹的禁忌症和阿奇霉素招募参与者时,我们没有观察到变化(F),其他心脏节律和高职院校学前教育专业试验研究羟氯喹/氯喹报道这些变化,但在这些试验,使用的剂量远远高于其他适应症的推荐剂量[30.,31].
我们的结果与其他单独研究羟氯喹和阿奇霉素作用的试验结果一致。存在“中和”药物毒性危害和对抗COVID-19的潜在益处的可能性,但我们认为不太可能,因为我们没有观察到干预组严重不良反应发生率更高。赛尔夫最近的一项安慰剂对照试验等的研究结果显示,在与本试验剂量相似的情况下,羟氯喹为期5天的疗程也因无效而停止(接近目标样本量),且在所有结果衡量指标方面均为中性[29]在开放标签恢复试验中[32[,每日500 mg阿奇霉素连续10天没有产生任何益处或危害,这与COALITION II试验的结果一致,该试验将相同的阿奇霉素方案与添加到高剂量(800 mg·day)的安慰剂进行了比较-1羟氯喹。在COALITION I试验中,疑似或确诊COVID-19患者随机接受开放标签治疗我)标准治疗,2)高剂量羟氯喹7天或3)高剂量羟氯喹(800毫克/日)和阿奇霉素(500毫克/日)联合用药7天。结果是中立的所有结果,除了QTc,这是明显更长,在两个积极治疗组。所有这些测试羟氯喹的试验与标准治疗,阿奇霉素与标准治疗,或阿奇霉素加羟氯喹已产生中性结果,除了QTc,在接受高剂量羟氯喹/氯喹的患者中稍高。接受正常推荐剂量羟氯喹/氯喹的试验患者没有表现出延长的QTcs。
目前研究的一个优势是,所有入选的患者都有rt - pcr确诊的COVID-19;在探索这些药物的其他试验中,纳入了疑似但不一定确诊的COVID-19患者[30.,32,33].此外,双盲和安慰剂对照设计是一个重要的优势,特别是在比较结果时,如顺序结果和住院时间长短,这些结果严重受医生决定的影响。在完全招募前终止本研究可能被认为是一种限制。然而,我们使用了一个相对敏感的主要结果。对于目前收治的下呼吸道感染患者的研究sd是3.5 - -4.023,34].据此,将DAOH的检出限设为1.5天变化(两种方法),达到样本量,拟进行试验。1.5天的变化是否足够敏感还可以讨论,但研究组认为,如果DAOH不能改变至少1.5天,我们认为其临床价值有限。在试验终止时,跨越效力或伤害界限的机会非常低,如果结合现有证据加以考虑,似乎不太可能进一步征募会显示出任何效果。由于出现症状的中位时间为8天,如果在疾病过程中更早地进行研究干预,可能会有效果。然而,这还没有在其他试验中得到研究。我们的试验不能直接回答这个问题,然而,在症状持续时间较短的患者中,这种影响似乎不太可能,因为这对我们的结果没有影响,因为在主要结果方面,研究干预和症状持续时间之间没有相互作用。因此,我们认为我们的试验结果是中性的。阿奇霉素和羟氯喹联合使用没有增加COVID-19患者的生存或出院可能性。这一结论与欧洲呼吸学会最新的COVID-19指南一致[188bet官网地址35报告称,使用羟氯喹和/或阿奇霉素治疗住院的COVID-19患者(在无细菌感染的情况下)没有相关的临床益处。
致谢
我们要感谢丹麦所有相关部门允许我们招募患者。我们还要感谢缔约方会议:TRIN指导委员会提供的有益建议。我们也感谢DSMB和Glostrup Pharmacy的首席药剂师Kristian Østergaard Nielsen的出色工作。我们要特别感谢ProPAC COVID背后的伟大团队,特别是Mohamad Isam Saeed、Jens-Kristian Bomholt-Riis、Anna kj . Kristensen和Katja Bergenholtz。
脚注
作者贡献:概念和设计:Pradeesh Sivapalan, Charlotte Suppli Ulrik和Jens-Ulrik Jensen;数据的获取、分析和解释:Pradeesh Sivapalan, Charlotte Suppli Ulrik, Josefin Eklöf, Alexander Jordan, Therese Lapperre, Rasmus Dahlin Bojesen, Andrea Browatzki, Jon Torgny Wilcke, Vibeke Gottlieb, Kjell Erik Julius Håkansson, Casper Tidemandsen, Oliver Djurhuus Tupper, Howraman Meteran, Christina Marisa Bergsøe, Uffe Christian Steinholtz Bødtger, Daniel Bech Rasmussen,Sidse Graff Jensen, Lars Pedersen, Helene Priemé, Christian Søborg, Ida Elisabeth Steffensen, Dorthe Sandbæk Høgsberg, Martin Steen Frydland, Peter Lange, Asger Sverrild, Muzhda Ghanizada和Jens-Ulrik Jensen;起草手稿:Pradeesh Sivapalan和Jens-Ulrik Jensen;对重要知识分子内容手稿的关键性修订:所有作者;统计分析:Pradeesh Sivapalan, Jens-Ulrik Stæhr Jensen, Alexander Jordan, Tobias Wirenfeldt Klausen and Josefin Eklöf;获得资金:Jens-Ulrik Jensen;行政、技术和物资支持:Jens-Ulrik Jensen, Vibeke Gottlieb;监督:Jens- ulrik Jensen, Filip Krag Knop, Tor Biering-Sørensen和Jens D. Lundgren
通讯作者的作用:发起人和学习总监。
利益冲突/披露:PS报告勃林格殷格翰(Boehringer Ingelheim)在提交作品之外的费用。CSU报告了勃林格殷格翰、阿斯利康、葛兰素史克、TEVA、诺华、ALK-Abello、Mundipharma、Sanofi Genzyme、Orion Pharma和Actelion在提交工作之外的费用。KEJH报告来自阿斯利康、Chiesi和TEVA的个人费用,在提交的工作之外。TBS还获得了通用电气医疗保健和赛诺菲巴斯德的研究资助,以及赛诺菲巴斯德、诺华和安进的个人费用。两位作者都没有任何利益冲突。
支持声明:该研究由诺和诺德基金会资助(批准号:NNF20SA0062834)。PS的研究工资由哥本哈根大学医院Herlev and Gentofte医院赞助。资助方不参与研究的设计和实施,不参与数据的收集、管理、分析和解释,也不参与手稿的准备、审查、批准或提交手稿发表的决定.这个试验没有得到任何形式的制药工业的支持。Pradeesh Sivapalan博士和Jens-Ulrik Jensen博士可以完全访问研究中的所有数据,并对数据的完整性和数据分析的准确性负责。
数据共享声明:缔约方会议的意见:Trin指导委员会,知识分享增加了科学效果的数量和质量。审判信息请求可以提交给项目管理团队(Jens-Ulrik Jensen,Charlotte Ulrik和Pradeesh Sivapalan),他将考虑该请求。然后将与COP:TRIN指导委员会讨论任何合理的请求。
写作小组的成员(Pradeesh Sivapalan, Charlotte Suppli Ulrik, Therese Sophie Lapperre, Rasmus Dahlin Bojesen, Josefin Eklöf, Andrea Browatzki, Jon Torgny Wilcke, Vibeke Gottlieb, Kjell Erik Julius Håkansson, Casper Tidemandsen, Oliver Tupper, Howraman Meteran, Christina Bergsøe, Eva Brøndum, Uffe Bodtger, Daniel Bech Rasmussen,Sidse Graff Jensen, Lars Pedersen, Alexander Jordan, Helene Priemé, Christian Søborg, Ida E. Steffensen, Dorthe Høgsberg, Tobias Wirenfeldt Klausen, Martin Steen Frydland, Peter Lange, Asger Sverrild, Muhzda Ghanizada, Filip Krag Knop, Tor Biering-Sørensen, Jens D. Lundgren, Jens- ulrik Stæhr Jensen,[礼仪主席]哥本哈根COP:TRIN lead])和ProPAC-COVID研究小组负责本文的整体内容和完整性。写作小组成员的关系列在附录中。
这篇文章有补充资料可从www.qdcxjkg.com.
数据可用性:缔约方会议的意见:Trin指导委员会,知识分享增加了科学效果的数量和质量。审判信息请求可以提交给项目管理团队(Jens-Ulrik Jensen,Charlotte Ulrik和Pradeesh Sivapalan),他将考虑该请求。然后将与COP:TRIN指导委员会讨论任何合理的请求。
支持声明:(由诺和诺德基金会资助,批准号:NNF20SA0062834;ProPAC-COVID:多中心,NCT04322396)。
- 收到了2021年3月15日。
- 接受2021年5月22日。
- 版权所有©作者2021
这个版本是在知识共享署名许可证4.0的条款下发布的。