抽象的
由于多种可能的机制,哮喘可能有助于预防COVID-19预后不良,包括病毒进入受体表达改变、吸入皮质类固醇使用、慢性炎症、由于屏蔽和/或粘液分泌过多而减少接触https://bit.ly/3eixopp.
到编辑:
我们利息阅读了b的研究艾森尔等。[1[与普通人群相比,描述了与冠状病毒疾病(Covid-19)住院的768名患者的伴侣群(4.8%)的哮喘患病率较低与没有哮喘的对照组相比,该亚组也显着降低了死亡率。必须考虑这些发现,因为它们从相对较小的单中心的队列中产生了初步。特别是,对照组在年龄(较大的)和性别平衡(更高的男性/女性比例)中差异显着不同;这两种特征都与结果较差,这提出了结果代表统计艺术品的可能性。然而,如果证实,这些数据反映了令人惊讶的呼吸病毒性大疱,最近是2009年H1N1 /流感的爆发,观察到哮喘是需要住院治疗的主要合并症(英国委员会委员会委员会委派的─25%[2])。随后显示哮喘患者与获取H1N1 /甲型流感病毒的增加风险相关[3.]并因此加剧[4.]。引人注目的是,最初的严重急性呼吸系统综合征冠状病毒(SARS-CoV-1)大流行的特征也是慢性肺部疾病共病发病率极低[5.],进一步表明sars相关冠状病毒可能不会像其他呼吸道病毒那样加重哮喘。
这种现象的基础是未知的。作者提出了两个假设来解释他们的观察结果:血管紧张素转换酶2(ACE2)的较低表达,SARS-COV-2的推定病毒进入受体,哮喘和吸入的皮质类固醇(ICS)的保护作用,哮喘中维持治疗的主要疗效,与减少的痰Ace2表达有关[6.那7.]。我们提出了三种进一步假设的机制。首先,行为因素可能很重要。国际准则广泛提倡对高危人群(包括哮喘患者)采取保护性防护措施。因此,哮喘患者接触SARS-CoV-2的减少可能是住院队列中报告的哮喘发病率较低的原因。然而,在采取社交距离措施之前,从大流行开始开始的一系列病例中,慢性呼吸道疾病的发病率很低,这表明这不是唯一的解释。政府限制大流行传播的政策也导致空气污染的减少,这增加了病毒引起的哮喘恶化的严重程度[8.]。
其次,来自哮喘肺部的慢性炎症,由Aeroallergens,污染物和病毒反复上皮腐蚀产生可能导致一定程度的免疫耐受程度,这可能反过来可能限制开发过度炎症反应的发病,以驱动Covid-19的严重程度。因此,预先存在的哮喘与用流感住院的患者减少的系统性炎症有关[9.],降低肺炎和脓毒症相关死亡率的肺炎[10]。在呼吸道细菌感染的实验模型中,出现在哮喘患者中约50%的2型炎症也可以预防脓毒症的发展[11]。
最后,黏液分泌亢进是哮喘的一个标志,可能会阻止SARS-CoV-2到达远端肺,从而避免病理变化。分泌粘液富含Muc5ac等黏液糖蛋白,是抵御感染的第一道防线。哮喘与表达增加有关MUC5AC[12),当在转基因小鼠中过表达时,与野生型对照相比,通过减少病毒载量和减少细胞气道炎症来保护免受流感感染[13]。因此可以想到,哮喘的个体中的粘液皮肤分泌可防止SARS-COV-2穿透足够远,以获得对肺泡型2细胞的进入,这些细胞主要在肺中表达ACE2。然而,所有哮喘的患者中不存在粘液过度,因此可能只会在某些人中授予保护。值得注意的是,其他条件以高痰负荷和增加的粘蛋白(例如相比之下,COPD是与Covid-19的不良结果相关。在这些患者中,其他因素(如旧时期和可溶剂)可能抵消粘液或其他生物机制增加的任何保护作用。
总之,许多因素可能协同作用,驱动在哮喘的SARS-CoV-2感染中观察到的潜在保护性表型艾森尔等。[1],总而言之图1。包含采样的大规模纵向研究,例如由国际严重急性呼吸道感染联盟(Isaric)进行的,应阐明对SARS-COV-2的免疫反应如何在具有和没有哮喘的个体中不同。重组人ACE2的试验(nct04335136.)及信息系统(nct04416399.那nct04355637.)也在进行中,其结果是热切期待的。了解哮喘和非哮喘人群对严重COVID-19易感性差异的基础,可能最终为了解可用于减轻COVID-19整体负担的治疗靶点提供重要见解。
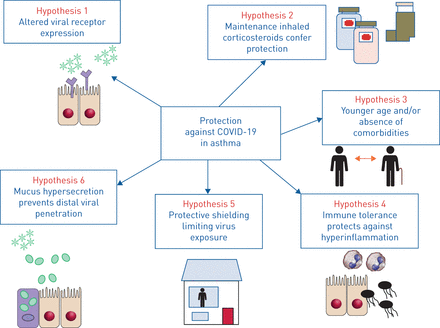
假设解释与冠状病毒疾病2019(Covid-19)住院的患者哮喘患病率低,并在这些患者中相对改善的结果。
可分享的PDF.
脚注
兴趣冲突:H. Farne没有什么可披露的。
利益冲突:A.辛格纳亚加没有什么可透露的。
- 收到了2020年8月6日。
- 公认2020年10月23日。
- 版权©2020人队
此版本在Creative Commons归因非商业许可证4.0的条款下分发。















