抽象的
使用简单的床边脉搏血氧仪来生成氧-血红蛋白去饱和曲线可能有助于对COVID-19患者进行分类。肺内分流与COVID-19预后差相关,分流程度可能预示预后。https://bit.ly/2KVv0m2
到编辑:
低氧血症是2019冠状病毒病(COVID-19)住院的关键指标[1那2].争议围绕低氧血症的病理生理学,用脑室分流,通风到灌注中的不匹配(v'一种/问的)比例,内皮损伤,微血管凝固和宿主炎症反应假设发挥作用[3.-6.].最近提出了Covid-19肺炎可能存在于依赖于保存肺部的两种表型和相对贡献v'一种/问的不匹配和脑子膜分流对低氧血症[7.].我们假设v'一种/问的在Covid-19肺炎中存在不匹配和肺旋转,旨在评估它们对结果的影响。使用数学模型构建氧气 - 血红蛋白解离曲线(ODC)[8.]确定分流程度和v'一种/问的在严重的Covid-19患者队列中不匹配。确定了有助于分流和死亡率的因素。
纳入2020年3月来我院就诊的real-time PCR诊断为COVID-19的患者[1].该研究经受当地患者安全和质量控制委员会的批准。医学研究委员会的道德决策工具表明,该研究不需要在英格兰NHS研究伦理委员会审查。随着所有患者数据都是匿名的,本研究不需要知情同意,符合本地指导。
收集流行病学、临床、实验室和放射学特征,以及所需的氧疗水平和结果。除非入院前进行抗凝,所有患者均接受静脉血栓栓塞预防治疗。NEWS2评分用于所有患者,这是一个有效的患者生理观察综合评分系统[9.].
我们回顾性收集护理人员和急诊科记录的指尖脉搏血氧仪数据。不同吸入氧含量下的两种饱和度(FIO2)用于入院和少于6次的值,用于构建ODC。在10名患者中,该模型无法导出计算的曲线v'一种/问的.这可能是因为这些患者在入场时迅速恶化,歪曲数据。然而,使用单个数据点,该模型仍然能够计算这些患者的脑室分流器。
odc的构造在其他地方有详细描述(图1) [7.那8.].该方法使用双隔室模型[10]和血红蛋白浓度校正。分流通过动静脉混合物降低了动脉氧饱和度,这不能通过增加来纠正FIO2.因此,分流可以通过ODC的下陷来计算[10].v'一种/问的减少肺泡后血氧含量降低,转化ODC向右移动[10].这是可逆的FIO2.通过与参考曲线比较来量化这些参数。
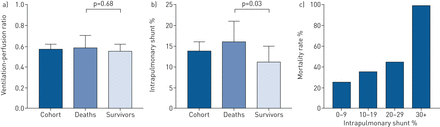
a)死亡和幸存者组中的通风到灌注比。b)死亡和幸存者群体的肺内分流。c)肺内分流水平增加的死亡率。
Spearman等级相关共同效率用于检查分流器和临床参数之间的关系。
2020年3月,108名患者被确认的Covid-19录取[1].14不需要氧气,没有足够的数据可用。剩下的87个包括在内。平均值±SD.年龄68.3±1.8岁,41% (n=36)为女性。体重指数为28.3±0.1 kg·m-2.65名患者(75%)是白人英国人;八(9%)白色其他;八(9%)黑色,亚洲或少数民族(BAME);和六(7%)未知的种族。46%的患者是非 - 或目前的吸烟者。心血管疾病(高血压(46%),中风(16%),缺血性心脏病(13%)),糖尿病(25%)和呼吸系统疾病(哮喘(15%),COPD(15%))是最常见的合并症.24%的患者有之前或目前的癌症。
基线血液检测显示炎症反应活化(中位c反应蛋白(CRP) 82,四分位范围(IQR) 49-156;乳酸脱氢酶(LDH) 62,528 - 807;铁蛋白926,357-1620)和凝血级联(中位d -二聚体1100,663-1550)。1例患者除了严重的COVID-19变化外,在ct肺血管造影中可能出现肺栓塞。31例(36%)患者死亡。
中位数分流是14%(IQR 4-21%)和v'一种/问的是0.58(IQR 0.50-0.68)(图1).Shunt在死亡患者(16%,IQR 6-23%)中比存活患者(11%,IQR 1-17%)高45% (p=0.03)。图1).中位之间没有区别(p = 0.69)v'一种/问的死亡(0.59,IQR 0.49-0.70)与存活(0.50,IQR 0.56-0.68)之比。死亡率随分流术的严重程度而增加(图1).所有五名分流患者都死于30%。
分流与入学报Need2分数有关(Spearman相关系数0.33,P = 0.0002),CRP(0.38,p = 0.001),LDH(0.45,p = 0.002)和尿素(0.29,p = 0.007),以及持续时间连续正气道压力(CPAP)治疗(0.40,P = 0.001)和住院时间长度(0.25,P = 0.02)。v'一种/问的失配与测量参数无关。
COVID-19低氧血症的病理生理机制存在争议[3.-5.].该研究鉴定了片内分流作为主要病理生理机制。分流严重程度是预测更糟糕的结果:更长的逗留时间;更长的CPAP持续时间;和更高的死亡率。此外,分流与CRP和LDH相关,但不是D-二聚体相关。v'一种/问的不匹配,虽然存在,但没有预后。
肺部建筑内的微生物和大血管血管血管血管血管血管[5.]涉及Covid-19低氧血症的发病机制。双能计算断层扫描扫描确定了血液分流与肺气交换受损的地区的深刻灌注异常[6.].我们的研究证实,肺血管分流可能在COVID-19低氧血症的发生中发挥重要作用。从病理生理学角度来看,CRP与肺内分流和预后(如CPAP的长度和死亡)的强相关性意味着更严重的炎症反应与更严重的分流相关,而更严重的分流又与更糟糕的临床预后相关。
有人假设,COVID-19肺炎可能存在于两种表型之间的一个谱[7.].较小的严重形式(“L”)可能与缺氧的保存肺部有关,提出次级肺血管炎症损害缺氧肺癌血管收缩和生理学v'一种/问的匹配。更严重的类型(“H型”)可能与更“典型”的急性呼吸窘迫综合征有关:肺顺应性降低,炎症和分流增强。这一理论模型来源于临床观察,至今尚未得到正式证实。我们的研究证实了更严重的分流与更糟糕的结果相关,从而为支持这一假设提供了证据v'一种/问的不匹配与疾病的严重程度无关。分流的病理生理学意味着低氧血症不能通过增加而完全逆转FIO2.这也许可以解释为什么这些患者的预后更差。进一步的研究还可能有助于深入了解COVID-19中描述的“隐性缺氧”的潜在机制和肺内分流的作用。
本研究还证明了两种不同的氧饱和FIO2值可用于构造odc,用于预测结果。一个简单的基于计算机的算法被使用,可以在入院时在床边执行,并可能帮助优先处理途径。这种方法的优点在于,ODC是血红蛋白的一种可预测的物理特性,即使在波动的临床情况下,也可以客观和准确地测量分流和v'一种/问的不匹配。它对更复杂的方法表现良好[11].
该研究受到小样本大小的限制。然而,在其他临床条件下使用这种技术(E. Russell-Jones和Co-Workers,未发表的结果),数量超过研究。此外,回顾性设计意味着氧饱和含量最多6小时。未来的前瞻性研究将能够在不同的情况下收集氧气饱和FIO2在较短的时间内,在间隔时间内降低患者病情恶化的风险。
本研究强调了简单的临床测量对构建ODC定量分流和v'一种/问的COVID-19患者的不匹配。我们还表明分流的程度似乎可以预测结果。此外,这些观察增加了我们对COVID-19低氧血症的病理生理机制的理解。本研究具有重要的临床适用性。我们的非侵入性方法早期计算分流,可以帮助决定分诊和风险分层。鉴于我们研究对象数量有限,且具有回顾性性质,我们研究的下一阶段将致力于在更大的前瞻性队列中验证这些结果。
可分享的PDF.
致谢
我们真诚地感谢所有医生,护士和医疗保健人员,参与在Royal Surrey NHS Foundation Trust的Covid-19患者管理。
脚注
数据共享声明:匿名研究数据可根据合理要求提供。
作者贡献:A. Kotwica, H. Knights, N. Mayor, E. Russell-Jones和D. Russell-Jones起草了手稿。A. Kotwica, T. Dassios和H. Knights进行了数据分析。所有作者都参与了研究构思和设计、手稿修订、数据收集和患者登记。D. Russell-Jones为通讯作者,有权查阅研究中的所有数据,并对提交发表的决定负有最终责任。由4名未被纳入研究队列的当前住院患者组成的患者顾问组对研究结果进行了评论,并对讨论和传播计划作出了贡献。
利益冲突:A. Kotwica没有披露。
利益冲突:H. Knights无需披露。
利益冲突:N. Mayor无意义。
利益冲突:拉塞尔-琼斯没有什么可透露的。
利益冲突:T. Dassios无意义。
利益冲突:D. Russell-Jones没有什么可以披露的。
- 收到了10月13日,2020年。
- 公认2020年11月27日。
- 版权所有©ers 2021。
此版本在Creative Commons归因非商业许可证4.0的条款下分发。















