摘要
对SARS-CoV-2的体液免疫反应表明,在冠状病毒-19患者中,IgA而不是IgM的早期反应。正如本研究所强调的,在严重冠状病毒-19中观察到的增强IgA反应可能会对严重冠状病毒-19产生损伤作用。https://bit.ly/3fA7c1I
致编辑:
与严重急性呼吸综合征冠状病毒(SARS-CoV)相比,SARS-CoV-2似乎更具传染性[1.2019年(COVID-19)患者表现出不同于SARS-CoV和中东呼吸综合征冠状病毒感染患者的临床表现[2.].临床和流行病学观察的集体结果表明,COVID-19患者中存在明显的病毒-宿主相互作用。分析SARS-CoV-2感染期间的抗体应答可能有助于我们了解病毒-宿主相互作用和疾病的免疫病理机制。
对感染的体液反应的研究主要是针对高亲和力IgG抗体的生产,这种抗体可以有效地解决感染。然而,人们已经认识到,对感染的体液免疫反应可能是一把双刃剑,它要么作为一种保护机制来解决感染,要么加重组织损伤,如。IgG反应通过扭曲sars冠状病毒的炎症分解反应而导致致命的急性肺损伤[3.].在呼吸道感染的情况下,虽然IgM和IgG亚型一直是描述免疫特性的主要重点,但可能在疾病发病机制中起关键作用的粘膜和全身IgA反应却很少受到关注。
本研究旨在更好地了解COVID-19患者队列中对SARS-CoV-2的体液免疫反应的时间和模式,并评估其与疾病病程和严重程度的关系。37例COVID-19患者,平均±sd年龄52.3±16.3岁。纳入的COVID-19患者中,男性25例(67.6%),女性12例(32.4%)。所有患者SARS-CoV-2病毒核酸检测均为阳性(Real-Time Fluorescent RT-PCR Kit;深圳华大基因研究院,中国)。根据国家卫健委发布的《新型冠状病毒感染的肺炎诊疗方案》,将入组患者分为重症20例(54.1%)和非重症17例(46.0%)两组[4.]非严重组包括有轻度和中度症状的患者,根据中国的新冠病毒-19控制政策,这些患者也需要住院治疗。重症组包括重症和危重患者。轻度患者没有表现出异常的计算机断层扫描(CT)成像。中度患者有发热和/或典型的呼吸道症状,典型的病毒性肺炎CT图像。重症患者至少满足以下一种附加条件:1)呼吸急促,呼吸频率高≥30 次·分−1.;2)脉搏氧饱和度(静息状态)≤93%;或3)动脉氧压/吸气氧压≤300mmhg。危重症患者除确诊COVID-19外,至少满足以下一项额外条件:1)呼吸衰竭,需要机械通气;2)冲击;3)多器官衰竭,需要转移到重症监护病房。所有的临床诊断都由一组训练有素的医生证实。所有血样均在入院后0-8周内采集。对37例患者住院期间采集的183份血清样本进行了SARS-CoV-2峰蛋白特异性抗体检测。化学发光免疫法检测SARS-CoV-2 S蛋白特异性IgA、IgM和IgG抗体水平。 The S-protein peptide was acquired from the University of Science and Technology of China (Hefei, China).
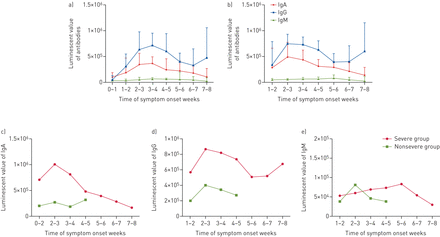
我们的研究表明,IgA血清转换的第一天是发病后2天,IgM和IgG血清转换的第一天是发病后5天。183份标本中IgA、IgM、IgG抗体阳性率分别为98.9%、93.4%和95.1%。症状出现后32天血清IgA、IgM或IgG转阴率为100%。累积血清转化曲线显示,IgA、IgM和IgG的中位转化时间分别为13、14和14天。ag特异性IgA和IgG水平在发病后2周显著升高,并持续升高2周。相反,IgM的水平和时间依赖性变化是最小的。重症患者的IgA和IgG相对水平明显高于非重症患者(图1).严重组与非严重组之间IgA (p<0.001)、IgG (p<0.001)相对水平差异有统计学意义。而重症和非重症患者发病后IgM水平无显著变化。在进一步的亚组分析中,我们发现了一个显著正关联SARS-CoV-2-specific IgA的水平和急性生理和慢性健康评估(APACHE)——分数COVID-19危重患者(r = 0.72, p = 0.01),虽然SARS-CoV-2-specific IgG、IgM的水平并没有显示出与疾病严重程度相关性。
2019冠状病毒病患者抗体的时间谱将发病后及0-1、1-2、2-3、3-4、4-5、5-6、6-7、7-8周收集的样本合并分析。a、b) a)所有患者和b)重症患者自发病以来同一时间点样本抗体检测值(发光值)的中位数。c-e)重症和非重症患者不同抗体水平的时间序列变化。c) IgA、d) IgG、e) IgM抗体检测值(荧光值)自发病以来同一时间点样品的中位数。
目前的研究表明,在严重和非严重病例中,特异性IgM抗体水平均显著低于IgA抗体水平。这种体液免疫反应模式在SARS-CoV感染中不同,其中IgM和IgA在血清转化时间和抗体滴度方面表现出相似的时序特征[5.],这与病毒血症在SARS中很常见的知识相一致。
作为一种粘膜靶向病毒,SARS-CoV-2有望产生分泌型IgA(sIgA)并诱导强烈的粘膜免疫。事实上,粘膜抗病毒免疫部分是由IgA介导的与病原微生物的相互作用导致的,以阻止病原菌粘附在细胞表面[6.].然而,最近的研究也发现sIgA能够通过正常的人肺成纤维细胞诱导白细胞介素(IL)-6、IL-8、单核细胞趋化蛋白-1和粒细胞-巨噬细胞集落刺激因子的产生[7.].也有人提出sIgA可能与IgG具有协同作用,促进抗体依赖的细胞细胞毒性(ADCC) [8.].与粘膜IgA相比,血清IgA的作用相对未被探索。先前的研究表明,IgA介导了先天免疫细胞的促炎或抗炎作用,并提出了IgA作为自身免疫性疾病的驱动因素和作为免疫过度激活的调节器的合理作用[9].血清IgA与Fcα受体(Fcα ri)的单体结合被认为介导了抑制功能通过多种髓样细胞的受体抑制信号[10]相反,IgA和病原体交联FcαRI能够传递激活信号,导致吞噬、呼吸爆发、ADCC、抗原呈递增加、脱颗粒和细胞因子释放[11].转化生长因子(TGF)-β和IL-10等细胞因子可诱导抗体同型转换[12].IgA生成上调可能是TGF-β和IL-10水平升高的结果,促进了SARS-CoV-2感染中抗体的转换。
考虑到粘膜和全身IgA在COVID-19中的作用,诱导IgA产生(使用乳铁蛋白激活典型TGF-β信号[13]或维甲酸增强乳铁蛋白诱导的IgA反应[14)已被提出作为一种新型治疗COVID-19的方法。然而,正如我们的研究所强调的,在严重COVID-19中观察到的增强IgA反应可能会在严重COVID-19中产生破坏性影响。因此,我们假设严重的COVID-19可能至少部分是IgA介导的疾病(与IgA沉积和血管炎相关),这有助于解释COVID-19常见的器官损伤,如。急性肺栓塞,肾损伤,等。[15].我们承认这项研究的局限性,包括没有测量局部IgA和有限的患者数量。未来的研究工作肯定需要探索COVID-19中黏膜和全身IgA的功能意义,以及在鼻咽/口咽黏膜水平的局部干预是否可以减少病毒载量和症状。
可共享PDF
确认
我们感谢参与这项研究的所有患者及其家属,以及为抗击新冠病毒而辛勤工作的医生、护士和平民。我们非常感谢黄绍库教授(台湾苗栗国立卫生研究院)对这篇手稿的建议和批判性阅读。
脚注
作者贡献:于海琼,孙宝清,方张福,赵金存,刘小雨,李一敏,孙希卓,刘志刚,钟南山参与研究设计。梁洪峰,钟蓓,黄志峰,郑培艳,田丽峰,瞿慧琪,刘德臣,王二仪,肖小军,李世悦,叶峰,关丽,胡东升对患者招募、数据收集、数据分析和文献检索有贡献。方张福、黄志峰、郑培炎进行了抗体检测实验。余海琼、孙宝青、方张福、田立峰、瞿慧琪、哈肯。钟南山、刘志刚等人对手稿进行了批判性的审查和修改。所有作者阅读了手稿并批准了最终版本。
利益冲突:于海琼没有什么可披露的。
利益冲突:孙宝清无需透露。
利益冲突:方张福没有什么可透露的。
利益冲突:赵金村没有什么可透露的。
利益冲突:刘小雨没什么可透露的。
利益冲突:李一敏没有什么可披露的。
利益冲突:孙锡卓无所披露。
利益冲突:梁宏峰没有什么可披露的。
利益冲突:贝忠无需披露。
利益冲突:黄志峰没有什么可透露的。
利益冲突:郑培炎没有什么可披露的。
利益冲突:田立峰没有什么可透露的。
利益冲突:惠琦区无需披露。
利益冲突:刘德臣无需披露。
利益冲突:王二宜没有什么可透露的。
利益冲突:肖小军没有什么可披露的。
利益冲突:李世跃无需透露。
利益冲突:冯烨没有什么可透露的。
利益冲突:李冠无需披露。
利益冲突:胡东生无需披露。
利益冲突:Hakon Hakonarson无需披露任何信息。
利益冲突:刘志刚没有什么可披露的。
利益冲突:钟南山没有什么可披露的。
支持声明:本项工作由深圳市科技计划研究项目(编号KQTD2017033114453160)、深圳市南山区先锋群体研究基金(编号LHTD20180007)、浙江大学新冠肺炎防控专项科研基金(编号2020xGZX0012020xGZX025)资助。该研究由作者完全独立于资金来源进行设计、实施、分析和解释。
- 收到了2020年4月29日。
- 认可的2020年5月5日。
- 版权©2020人队
本版本根据知识共享署名非商业许可4.0的条款发布。