抽象的
昼夜节律放松和睡眠不足可能会加剧COVID-19感染和严重程度https://bit.ly/2VUlIIJ
介绍
严重急性呼吸综合征冠状病毒2(SARS-COV-2),大流行冠状病毒疾病2019(Covid-19),是一种新发现的成员Coronaviridae与SARS-CoV密切相关,但有重要区别[1].它通过血管紧张素转换酶2(ACE2)的表面尖峰的结合进入人体细胞(S)糖蛋白的结合[2- - - - - -4].S蛋白的远端S1亚基负责受体结合,而跨膜S2亚基介导病毒包膜与靶细胞膜之间的融合,然后被特定的细胞酶(如跨膜丝氨酸蛋白酶2)进行蛋白裂解,从而引发S蛋白[5].因为ACE2的表达水平很可能影响病毒附着和进入的效率,以及疾病的严重程度[6],病毒S蛋白与ACE2相互作用可直接导致肺损伤[7[ACE2可以是治疗和预防性干预措施的潜在目标[8].
病毒感染的病理生理学和昼夜时钟系统的作用
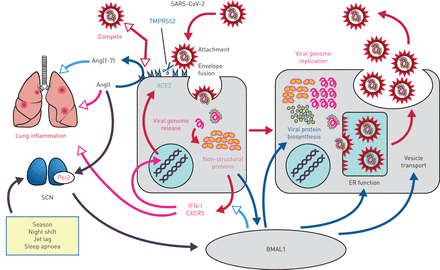
病毒感染的致病性可能受到宿主生物钟系统的影响通过两种不同的机制[9- - - - - -11) (图1): 1)直接调控靶细胞内病毒复制;2)对先天性和适应性免疫反应的间接影响。例如,昼夜节律振荡器的关键调节因子之一BMAL1,直接影响培养细胞中的小鼠疱疹病毒感染,而疱疹病毒复制在缺乏BMAL1分子的细胞中显著增强[13].相反,急性感染小鼠疱疹病毒会增加BMAL1的表达,从而扰乱或增强细胞自主节律,这取决于感染发生在昼夜节律周期的哪个点。BMAL1的缺失影响了参与蛋白质生物合成、内质网功能和囊泡运输的细胞因子的表达,这些都是冠状病毒胞内复制的重要因素[14].同样,BMAL1和rev - erba,核受体家族的细胞内转录因子,同步和维持外周时钟所需[15],影响丙型肝炎病毒生命周期中的多个步骤,包括其进入肝细胞的能力以及病毒在肝细胞内的RNA基因组复制。敲门方法BMAL1,基因过表达或使用合成激动剂增加REV-ERB活性,通过破坏脂质信号通路,不仅显著减少丙型肝炎病毒的复制,而且也显著减少其他黄病毒的复制,如登革热和寨卡病毒[16].
严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)感染与昼夜节律时钟系统之间的可能联系蓝色箭头表示细胞BMAL1表达与其他病毒复制或反应之间的已知联系。呼吸上皮细胞上血管紧张素转换酶2 (ACE2)的表达可能通过1型干扰素(IFN-I)诱导机制调控[12].由于SARS-CoV-2的表面S糖蛋白与ACE2的蛋白酶结构域结合,病毒附着可能直接与血管紧张素II (ATII)向肾素-血管紧张素系统负调控因子Ang(1-7)的过程竞争。已知ATII是促炎的,而Ang(1-7)是抗炎的。IFN-I信号在冠状病毒感染的后期诱导细胞因子的产生和更严重的肺损伤。BMAL1调控IFN-I和趋化因子CXCL5的产生。已知ATII通过影响Per2水平影响视交叉上核(SCN)的中央时钟系统。TMPRSS2:跨膜丝氨酸蛋白酶2;呃:内质网。
现在确定有季节性变化BMAL1的表情,最低的值被记录在冬天,和这些变化与呼吸道病毒性疾病的高发病率在冬天,特别的观察,低BMAL1表达增强病毒毒力(13].当老鼠在一天的不同时间点感染疱疹病毒时,显著的影响归因于昼夜节律钟[17].因此,昼夜节日时钟似乎会影响病毒的感染性以及它们在主机内复制的能力。此外,我们推测,由于昼夜钟钟机械本质上涉及血管紧张素途径的调节,特别是在ACE2的转录表达中,昼夜节奏在调节对SARS-COV-2的感染性的估算作用是非常可能的[18].
宿主生物钟现在被认为是一般免疫/炎症反应的主要调节器[19- - - - - -21.],特别是在呼吸道病毒感染之后体内.已有研究表明,肺上皮细胞内的内源性生物钟通过趋化因子配体CXCL5调节中性粒细胞募集[22.].细支气管中BMAL1的基因消融导致CXCL5表达节律的中断,导致脂多糖刺激下的炎症反应过度。由于缺乏干扰素表达的昼夜调节,BMAL1的缺失也导致小鼠发病率、死亡率和病毒复制的增加。重要的是,实验性慢性时差模型对昼夜功能的环境破坏导致BMAL1在肺部的时间表达中断,在呼吸道仙台病毒感染后体重减轻增加[23.].
感染的时间不仅改变易感性,而且预测小鼠流感病毒感染后的存活[24.].在活跃期开始时感染的老鼠比在休息期开始时感染的老鼠死亡率更高。在缺乏BMAL1表达的小鼠中,这些时间差异被消除。观察有趣的是,加剧炎症小鼠感染发病的活跃阶段,而自然杀伤(NK)细胞组显著的高于感染只是休息阶段前,表明生理调节先天免疫在这些差异中起着重要作用。事实上,NK细胞的消耗消除了白天的时间差异,这表明分子时钟控制着宿主细胞对流感病毒感染的反应通过NK细胞功能。
然而,应该注意的是,宿主免疫/炎症反应在流感病毒感染的发病机制中的作用显着不同于SARS-COV-2感染的病毒。感染后,流感病毒很快就重复,并导致巨大且有时能够失调的炎性细胞因子的产生,可能导致所谓的细胞因子风暴,而SARS-COV-2的复制较慢,肺病理变化的发展与激活一致宿主自适应免疫应答,包括T-辅助细胞17的响应[25.].
然而,应该强调的是,宿主1型干扰素(IFN-I)应答的时机决定了呼吸道冠状病毒感染的结果。在中东呼吸综合征和SARS-CoV感染中,早期IFN-I信号与病毒复制减少和轻度肺病理有关,而延迟IFN-I信号导致炎症单核细胞浸润增加,促炎细胞因子产生增加和致命肺炎[26.,27.].这些增强的炎症反应可能在BMAL1失调时进一步夸大。
ACE2在SARS-CoV-2感染中的作用
SARS-CoV-2对组织ACE2具有高亲和力。在正常情况下,ACE2负责血管紧张素II (ATII)的失活,因此在内皮和心血管稳态中发挥重要作用[28.].事实上,ACE-Ang II-AT1R途径被称为经典肾素血管紧张素系统(RAS)途径,它调节交感神经系统紧张,导致血管收缩,升高血压,促进炎症、纤维化和心肌肥厚,而ACE2-Ang 1-7-Mas原癌基因受体轴被视为反调控RAS通路,并拮抗经典通路的作用[28.],同时也是SARS-CoV-2的组织受体。ACE2存在于人体的多种细胞底物中,但在血管内皮细胞(包括肺血管)中含量尤其丰富,这可能是SARS-CoV-2倾向于肺的原因。在这种情况下,围绕ACE1或血管紧张素受体阻截剂对COVID-19感染的总体影响提出了几个假设。假定有益的结果将包括ACE2受体阻断,从而限制病毒进入器官,如肺,并通过这些药理学药物调节炎症反应。然而,不能排除可能的逆行反馈机制导致ACE2受体上调。因此,尽管先天的ACE1/血管紧张素受体阻滞剂对SARS-CoV感染的有益影响,我们不能将其推断为SARS-CoV-2导致COVID-19。此外,当出现衰老、全身性高血压和其他心血管疾病等情况时,ATII水平的增加导致ACE2活性降低和炎症增加,由于SARS-CoV-2使已经减少的ACE2失活,这些患者可能面临潜在疾病恶化的风险和更严重的不良结局[29.].
生物钟在SARS-CoV-2感染病理生理学中的假定作用
如上文所述,SARS-CoV-2细胞受体ACE2表达于气管外膜、细支气管和肺泡上皮细胞、小肠肠内细胞、血管内皮细胞和平滑肌细胞、肾小管上皮细胞及其他粘膜组织[30.].重要的是,ACE2通过在其c端切割ATII并产生血管扩张血管紧张素1-7 (Ang(1-7)),作为RAS的负调控因子发挥作用[7].ACE2的缺乏与酸吸入性肺损伤的增加有关,在基因上缺乏肺上皮血管紧张素II受体1a的小鼠中,这种有害影响显著改善[31.].此外,给药重组ACE2可以保护ACE2缺陷小鼠和野生型小鼠免受急性肺损伤。因此,ATII是促炎介质,而Ang(1-7)具有抗炎功能[6].随着ACE2在老年人中的表达减少,其作为SARS-CoV-2进入受体的双重功能以及作为将促炎ATII转化为抗炎Ang(1-7)的酶的双重功能可能会导致老年人较少的SARS-CoV-2感染,但更严重的疾病结局[6].
到目前为止,还没有关于肺中ACE2表达可能的昼夜节律变化的报道,但已知ATII影响Per2的节律表达,Per2是构成哺乳动物视交叉上核时钟回路反馈回路的关键抑制因子之一[32.].此外,心脏血管紧张素转换酶的表达水平显示出明显的日变化[33.]和ATII诱导血管细胞中昼夜节律基因表达的变化[34.],而BMA1表达的变化也会影响血管紧张素的表达,并且在血管外脂肪组织中静息血压[35.].因此,可以想象,ACE2的肺表达也会通过细胞自主调控和RAS中昼夜节律变化的间接影响而表现出昼夜节律变化。考虑到SARS-CoV-2感染较严重的表现包括急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS),这是一种以肺部血管通透性增强为特征的疾病[36.,37.],同样重要的是要考虑肺内皮细胞及其同源表达ACE2作为病毒诱导的急性呼吸窘迫综合征潜在靶点的作用[38.,39.].值得注意的是,最近在SARS-COV-2感染中提出了褪黑激素的推定佐剂作用[40].此外,COVID-19在肥胖患者和男性中表现出更高的倾向,可能也可以解释ACE2在肥胖中发挥的重要相互依赖作用[41.- - - - - -44.],以及由这种高度流行的疾病引起的下游全身炎症[45.]和这种效果的性二相[46.].
睡眠和SARS-CoV-2感染
睡眠,昼夜行为表现为主要监管性稳态机制,例如与免疫相关的机制,也显示出在分子和细胞水平的宿主防御中相互作用。实际上,广泛的文学表明稳态睡眠在先天和自适应免疫中的重要作用[47.].此外,在睡眠持续时间和质量和针对病毒,细菌和寄生病原体的免疫反应之间存在明显的互核依赖性,后者改变了睡眠模式[47.].因此,改善人群的睡眠质量和持续时间可能会减轻由SASRS-CoV-2感染引起的疾病的传播和严重程度。有趣的是,可能与SARS-CoV-2-ACE2的病理生理相互依赖有关,Carhanet al。[48.]观察到果蝇缺少ACER(一种ACE2同源基因)的成年果蝇果蝇黑胶基)或用肽酶抑制剂治疗的患者夜间睡眠中断。我们还没有任何关于睡眠对SARS-CoV-2感染影响的具体研究。尽管如此,我们应该指出,冠状病毒在患有阻塞性睡眠呼吸暂停的儿童的扁桃体组织中发现的频率越来越高[49.].
潜在的临床意义
如上所述,睡眠中断或睡眠不足如何影响SARS-CoV-2感染率及其临床表现的严重程度尚不清楚。急性肺损伤的典型症状包括呼吸困难、低氧血症和肺水肿,这些症状可能恶化为SARS。这种进展的基于细胞的病理机制包括激活免疫炎症级联反应导致肺泡-毛细血管屏障的破坏[39.].这种免疫炎症激活受到昼夜时钟的影响,因此昼夜节律的放松,如夜班工人或社会时差,可能通过改变感染易感性或修改COVID-19的临床表现,发挥特定疾病的作用。至关重要的是,要确定SARS-CoV-2在人群中的流行程度和严重程度,同时确保适当纳入有关他们的睡眠习惯和昼夜活动的充分信息。此外,由于ACE2,这可能是受时钟的活动,被证明有一个通过抑制肺内皮细胞凋亡的保护作用,可能是生物钟干预可以减轻肺损伤的进展,如果这样的干预发生在感染的早期阶段(50.].另外,根据临床研究显示ACE抑制剂治疗高血压的时间充足性的相关性[51.],在SARS-CoV-2感染的情况下给药可能需要更精确地与患者的生物钟状态校准[52.]但即使支持这种药理学治疗的证据是最令人怀疑的[53.].
基于上述考虑,阻塞性睡眠呼吸暂停(OSA)等潜在睡眠障碍的存在,可以被视为SARS-CoV-2感染的促进因素,因为在这一高度流行的疾病中,RAS已被确认发生了改变[54.- - - - - -59.].重要的是要评估OSA患者是否更容易感染,以及SARS-CoV-2患者的临床结局是否更不利。
总之,已经过审查了SARS-COV-2,昼夜节律和睡眠之间的独特潜在联系,并表明这两种稳态过程可能会显着修改对感染的易感性以及疾病的整体临床表现。因此,实施健康的睡眠措施作为免受感染的保护策略,早期检测患者风险更严重的疾病(如。夜班工人或OSA患者),可以提高支持措施的实施,并导致更好的结果,
可共享的PDF
脚注
利益冲突:宫泽明没有什么可透露的。
利益冲突:D. Gozal没有什么可披露的。
利益冲突:M. Meira E Cruz无需披露。
支持声明:D. Gozal得到了美国国家卫生研究院HL130984、AG61824和HL140548的资助。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年4月4日。
- 接受2020年4月20日。
- 版权所有©ers 2020
这个版本是在知识共享署名非商业许可4.0的条款下发布的。