抽象
FujiLAM的快速尿结核菌检测方法可以检测出住院的晚期艾滋病患者中很大比例的肺外结核和传统上难以诊断的肺外结核http://bit.ly/36Dl0Eo
致编辑:
在诊断艾滋病病毒感染者(PLHIV)人结核病(TB)仍然是部分具有挑战性,因为它的临床表现,包括肺外高利率和播散性疾病[多样性的,1]。特别地,播散TB,涉及多个器官系统,与高死亡率有关,但往往呈现非特异性,这可能妨碍迅速诊断[2,3.]。XPERT MTB / RIF(XPERT;造父变星,桑尼维尔,CA,USA),目前推荐的世界卫生组织(WHO)列为第一线分析评估的肺外结核病(EPTB)表现的一个子集[4]。为了检测特定形式的EPTB,如胸膜结核、结核性脑膜炎或结核性淋巴结炎,Xpert可能需要采集侵入性样本,这通常将其用于EPTB检测的范围限制在有适当设备和能够安全进行侵入性取样的医院。此外,即使伴有肺部疾病,病情最严重的艾滋病毒患者也很难获得痰液,难以提交Xpert检测[5,6]。因此,在PLHIV中提高结核病检测的一个紧迫的优先事项仍然是开发快速的、使用容易获得的临床标本(如尿液)、对肺和EPTB(包括弥散性疾病)具有良好诊断准确性的点对点(POC)检测方法[7]。
市售了Alere确定TB LAM(AlereLAM;雅培,芝加哥,IL,USA)测定法是一种快速,便宜,泌尿POC TB测试[8]。虽然它的使用是在病情严重,死亡率利益关联和免疫功能低下感染者[9,10],它具有仅具有中等灵敏度受限于患者CD4计数低,这导致了有限的编程摄取[11]。POC测试,类似于AlereLAM,检测脂阿拉伯甘露聚糖的尿液的存在(LAM);我们已经在富士SILVAMP TB LAM(富士,日本东京FujiLAM)此前报道12]。在CD4分层的亚群中,与AlereLAM相比,它在检测结核病(与是PTB还是EPTB无关)方面的敏感性平均提高了30%,同时保持了较高的特异性。在这里,我们报告了FujiLAM与AlereLAM的敏感性,特别是在同一组患者中检测EPTB的敏感性。
这事后分析使用了之前发表的两项对携带艾滋病毒的成年人(>18岁)的前瞻性队列研究的数据,这些成年人被收住在开普敦郊区的南非地区医院[13,14]。队列A入选患者,而没有电流TB诊断的无论呈现体征或症状,和独立的CD4计数的[13]。B组患者CD4细胞计数< 350·μL细胞−1在结核病人被认为是入院时最可能的诊断[14]。第三先前公布的队列是不包括在目前的分析,因为它排除了患者专门肺外结核病[12]。从病人谁了能力或恢复能力和所有研究相关的活动由开普敦大学的人类研究伦理委员会批准的知情同意。
对患者进行了结核病存在情况的系统评估。在可能的情况下,患者提供两份痰标本、一份血样和一份尿样进行分枝杆菌学检查;那些不能产生痰或尿液样本的人并不排除在研究登记之外。使用涂片荧光显微镜、分枝杆菌生长指示管(MGIT)液体培养(Becton Dickinson, Franklin Lakes, NJ, USA)和Xpert MTB/RIF Version G4检测痰标本。血液标本采用BACTEC Myco/F Lytic培养(Becton Dickinson, Franklin Lakes, NJ, USA)。尿液标本经30-40 mL离心后,用Xpert进行沉淀试验。常规临床组根据临床提示获得额外标本(痰液和非痰液)。FujiLAM和AlereLAM是根据制造商的说明对生物样本进行检测的,并由两名对患者状态和所有其他检测结果不知情的调查人员阅读[12]。微生物学确诊的TB被检测的定义结核分枝杆菌使用任一培养物或任何的Xpert临床标本。所有患者的微生物学确诊结核病分为三个互相排斥的群体之一:肺结核(PTB)(TB痰只检测),EPTB(TB在肺外标本(S检测)只),或PTB + EPTB(TB两者痰检测和至少一个额外的肺标本)。FujiLAM和AlereLAM的灵敏度(以及相应的95%置信区间)计算对于TB的每个形式以及用于EPTB的个别形式。
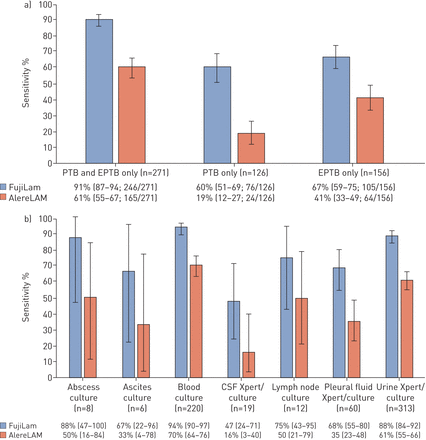
在1079名符合条件的患者中,111名患者的结核病状态无法被分类,90名患者没有尿液样本,6名患者的尿液检测结果缺失;因此,872例患者(420例来自A组,659例来自B组)获得了完整的结果,并被纳入本次分析。中位数年龄为36(差30-43)年,54%是女性,CD4细胞计数中值为84·μL (IQR 32 - 188)细胞−1,45%曾接受治疗的结核病。其中872例患者,553(138从队列A和415从队列B)上的至少一个样本已经微生物确诊的TB(患病56%),88(37从队列A和51从队列B)有可能TB和231(189从队列乙队列A和42)无TB的证据。那些有确诊的TB,126(23%)总分553的有PTB,156(28%)总分553有EPTB,和271(49%)总分553有两个PTB + EPTB。尿液LAM测定进行最好在那些与PTB + EPTB,与FujiLAM检测91%(95%CI 87-94; 246出来的271)与61%比较例(95%CI 55-67; 165出来的271)使用AlereLAM(图1一个)。患者PTB或EPTB只,FujiLAM检测60%(95%CI 51-69; 76出来的126);箱子分别,用比较和67%(105出来的156 95%CI 59-75)19%(95%CI 12-27; 24出来的126)和41%(95%CI 33-49; 64出来的156),用于分别AlereLAM(图1一个)。
(; N = 553肺,肺外或两者),在患者的疾病的参与(b)的部位与确认肺外结核病(EPTB)通过(a)型肺结核病的FujiLAM和AlereLAM的诊断灵敏度。条代表95个%置信区间。括号中的数字表示95%的置信区间。值得注意的是,同一患者可能有确定的疾病的多个站点(例如,肺,血液,尿液等)。痰液,血液和尿液中无论何时都在这个自由裁量权日常的医疗团队的获得可能的和额外的标本所有患者获得,但是有能力生产痰不进入研究的要求。该分析仅限于那些既FujiLAM间和AlereLAM结果可用。PTB:肺结核。
不同类型肺结核病对妇地兰的敏感性为47 ~ 94%,见表图1 b。值得注意的是,检测到的FujiLAM TB患者与那些与TB的TB mycobacteraemia和88%(95%CI 84-92)94%(95%CI 90-97)证实由尿的Xpert或培养物。它也显示出患者的微生物学证实胸膜TB中度敏感性;以及与TB脑膜炎(68%95%CI 55-80)(47%; 95%CI 24-71)。AlereLAM的灵敏度范围为16至70%,最好进行在那些与TB mycobacteraemia(70%; 95%CI 64-76)和TB确认由尿的Xpert或培养物(61%; 95%CI 55-67)。
总体而言,FujiLAM显示出超过市售AlereLAM基本上更高的灵敏度,用于检测HIV住院患者两个肺和肺外结核病。这表明,FujiLAM可以具有临床效用作为用于在HIV患者,独立的疾病位置的快速检测TB的第一线测试。鉴于患者大比例与HIV相关TB具有EPTB以及诊断仅可以使用可能是具有挑战性,以获得非痰样品是可能的,上前方FujiLAM测试可能基本上时间缩短至诊断。FujiLAM能够检测结核病的谁不能产生痰标本或没有肺部疾病的证据的患者67%(105出156);此类患者由研究组群的28%。
FujiLAM在结核分枝杆菌血症患者以及同时痰液阳性和非呼吸培养的患者中表现最佳,检测出90%的病例为>。结核分枝杆菌菌血症是艾滋病病毒感染者中在撒哈拉以南非洲地区最常见的血流感染的一个[3.]和这些患者具有极高的死亡率。FujiLAM在那些mycobacteraemia出色表现表明,疾病传播和泌尿LAM之间的机械关联。这一发现是由我们最近的研究显示,在尿和结核病患者的血清检测LAM之间的良好关联,独立的艾滋病病毒感染状况的支持[15]。然而,即使患者的疾病形式,如胸膜结核和结核性脑膜炎的可能区域化,FujiLAM有中度的敏感性,这可能会在这些情况下添加实实在在的好处。总之,这些发现表明,LAM antigenuria可能指示循环除了LAM(或LAM片段)肾TB的肾小球滤过的[16]。进一步的研究,其目的是检测尿超灵敏的平台LAM,以及LAM结构表征,需要更好地了解其LAM进入血液和尿液的机制。这可能有助于进一步完善血尿为主的诊断和催化血为基础的分析的发展。作为分枝杆菌的总负荷预计在HIV阳性的患者要高一些,我们的研究结果不应该被推广到与EPTB HIV阴性个体。
患者没有系统地评估EPTB存在超越分枝杆菌血培养和尿液的Xpert;额外的系统抽样(例如胸水或脑脊液)是不合理的,因为这将需要侵入性采样如果做不到这一点临床指征。再加上普遍获得临床指征样的挑战(例如痰),TB类的一些错误分类(PTB,EPTB或PTB + EPTB)可能存在。此外,由于整体队列被严重免疫缺陷(增加了疾病传播的可能性),并且因为那些低,位点特异性分枝杆菌的负担(CSF或胸水)可能没有被确诊的Xpert或培养,尿FujiLAM的真实灵敏度(和AlereLAM)本地化肺外疾病是可能的高估,可能并不普遍意义,以所有患者的这些形式的疾病。然而,由常规临床小组收集的附加试样与高负担HIV相关TB设置镜像常见的做法,遵循临床症状。最后,我们没有评估FujiLAM对于给定的缺乏系统性EPTB采样的特定疾病形式的特异性。我们以前曾报道的特定队列,特异性以及所估计的特异性三组使用贝叶斯二元随机效应模型:使用复合参考标准相比,FujiLAM的特异性为95.7%(95%CI 92.0-98.0%)用98.2%(95%CI 95.7-99.6%)为AlereLAM [12]。
总之,我们的研究结果表明,POC FujiLAM对中晚期患者HIV,其中常规诊断可能是缓慢的检测TB的两个肺和肺外形式良好的灵敏度,需要基础设施和设备或依赖于难以样本获得。虽然适当的采样仍然应该采取允许药敏试验,FujiLAM可能对所有感染者住院适当的第一微生物TB的调查,允许抗结核治疗更快速的启动。
可共享PDF
致谢
研究者感谢生的西开普省部以及谁对这些数据作出贡献的患者的临床和行政人员。作者还希望感谢已故的斯蒂芬D.草坪谁设计并带领Cohort1研究。
脚注
作者贡献:T. Broger, B. Sossen, A.D. Kerkhoff, C. Schutz, E.I. Reipold, M.P. Nicol, G. Meintjes和C.M. Denkinger设计了家长研究,并由T. Broger, B. Sossen, A. Trollip, M.P. Nicol, G. Meintjes和C.M. Denkinger监督。B. Sossen, A.D. Kerkhoff, C. Schutz, R. Burton, A. Ward和G. Meintjes协调了各个研究地点。A.D. Kerkhoff, T. Broger和C.M. Denkinger设计了统计分析,d . Kerkhoff进行了统计分析。公元后,克霍夫、布洛格和索森起草了第一份手稿。所有作者都对文章的数据解释和编辑做出了贡献,并在投稿前批准了最终版本的稿件。
利益冲突:科霍夫没有什么要披露的。
利益冲突:B. Sossen有没有透露。
利益冲突:C.舒茨没有什么要披露的。
利益冲突:E.I.Reipold有没有透露。
利益冲突:A. Trollip有没有透露。
利益冲突:E. Moreau报告GHIT和KfW在研究期间的资助情况。
利益冲突:舒马赫是FIND的员工。FIND是一个非盈利的基金会,它的使命是找到在低收入国家中克服贫困疾病的诊断解决方案。它与私营和公共部门密切合作,并从一些行业伙伴那里获得资金。它有组织的防火墙来保护它不受任何不正当的影响,在其工作或发表其调查结果。根据尽职调查、TTPs和公共部门的要求,所有的行业伙伴关系都要接受一个独立的科学咨询委员会或另一个独立的审查机构的审查。FIND催化产品开发、领导评估、担任职位并加速使用被确定为服务于其使命的工具。为业界提供间接支援(例如。获得开放的样本库、临床试验平台、技术支持、专业知识、实验室能力加强等,以促进这些领域产品的开发和使用。FIND还支持使用捐赠赠款对优先测定法和世卫组织批准的测定法(指导和PQ)的早期实施阶段进行评估。为了进行测试验证和评估,与几家私营部门公司就疾病发现达成了产品评估协议,其中严格规定了其独立性和中立性相一相对产品进行评估并描述角色和职责的公司。
利益冲突:R.伯顿没有什么要披露的。
利益冲突:A.沃德没有什么要披露的。
利益冲突:在研究进行期间,M.P. Nicol报告了FIND的资助。
利益冲突:G. Meintjes有没有透露。
利益冲突:C.M.丹金是FIND的前雇员。
利益冲突:T. Broger报告从GHIT补助金,从个人FIND费,研究进行期间;并且具有在脂阿拉伯甘露聚糖检测结核病诊断领域未决的专利。
支持声明:该作品是由全球健康创新科技(GHIT)基金的基金号G2015-201资助,英国国际发展部(DFID)的授权号300341-102,荷兰外交部授权号PDP15CH14,比尔和梅林达·盖茨基金会资助号OPP1105925,外交事务和贸易部(DFAT)授权号70957的澳大利亚国防部和教育的德国联邦与研究部(BMBF)德国复兴信贷银行通过。该Cohort1研究由韦尔科姆基金会(088590和085251)资助。B. Sossen从威康信托基金会(授权号088316)收到薪水的支持。G. Meintjes是由威康信托基金会(098316和203135 / Z / 16 / Z),南非研究椅子科技部和南非国家研究基金会(NRF)(批准号64787),NRF部的倡议支持奖励资金(UID:85858)和南非医学研究理事会通过其结核病和艾滋病防治合作中心项目,与来自美国国家卫生署(收到的资金RFA#SAMRC-RFA-CC:TB / HIV / AIDS-01-2014)。C.舒尔茨通过国家卫生奖学金项目得到资助,从南非医学研究理事会。公元Kerkhoff先生是由国家过敏和传染病研究所(批准号T32 AI060530)支持。该资助者在研究设计,数据收集,数据分析,数据解释或编写本报告没有任何作用。的观点,结论和在这个手稿表示结论反映这些单独的作者。
- 收到2019年6月24日。
- 接受2019年10月18日。
- 版权©2020人队
该版本采用知识共享署名4.0许可协议的条款分发。