文摘
针对通路引起阻塞性睡眠apnoea-associated间歇性缺氧可以显著提高生物标志物的发现和新的治疗皮肤的黑色素瘤患者的视角http://ow.ly/wF3J30nlzL4
阻塞性睡眠呼吸暂停和黑色素瘤
除了疾病代谢疾病的一个独立危险因素(1),阻塞性睡眠呼吸暂停(OSA)现在被认为是促进癌症发展。尽管实验(2,3和临床4,5)本协会的证据出现几年前(6,7),快速向前推进了知识的差距有关癌症的类型提升阻塞性睡眠呼吸暂停综合症和致癌途径参与。
最近的一项回顾性研究34 402名患者观察到总体癌症发病率增加后阻塞性睡眠呼吸暂停综合症诊断和确定一个特定的链接与黑色素瘤、肾、子宫和乳腺癌8]。阻塞性睡眠呼吸暂停综合症和皮肤黑色素瘤之间的关系已经被无数证实临床前和临床研究表明,阻塞性睡眠呼吸暂停综合症促进其发病率(9,10],进展[2,11],攻击性[11- - - - - -13)和转移潜力(3,14]。针对穷人的5年生存率的转移性皮肤黑色素瘤(15),有一种强烈的需要特征之间的关联阻塞性睡眠呼吸暂停综合症和皮肤的黑色素瘤。这可能允许识别的新皮肤的黑色素瘤进展和转移的预后因素,为创新药物和个性化的治疗开辟新的途径,针对阻塞性睡眠呼吸暂停综合症相关的一个重要条件。
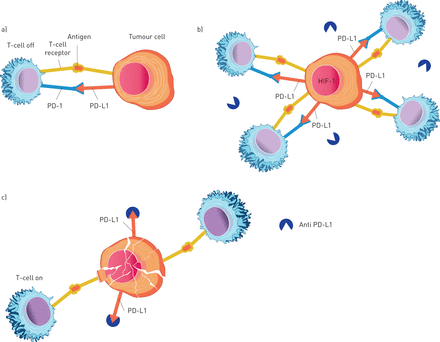
在当前的问题188bet体育备用网址欧洲呼吸杂志Cubillos -Zapataet al。(16]提出可溶性细胞程序性死亡配体1 (sPD-L1)皮肤黑色素瘤侵犯和转移的潜在生物标志物在阻塞性睡眠呼吸暂停综合症的病人。这是非常相关的程序性细胞死亡的重要作用受体1 (PD-1) / PD-L1轴在黑色素瘤的发展15,17],攻击性[18和生存19),还因为其upregulation间歇性缺氧和低氧诱导因子(HIF) 1的转录因子在皮肤黑色素瘤细胞(图1)[20.- - - - - -22]。
)免疫抑制检查站:绑定的细胞程序性死亡配体1 (PD-L1)黑色素瘤肿瘤细胞程序性细胞死亡受体1 (PD-1)抑制其细胞毒性t细胞活动。b)阻塞性睡眠呼吸暂停(OSA) -相关间歇性缺氧促进低氧诱导因子(HIF) 1激活和PD-L1表达,导致增加肿瘤细胞抵抗破坏由t细胞和免疫抑制剂(如anti-PD-L1)检查站。c)提出假设背后的有利影响持续正压通气治疗阻塞性睡眠呼吸暂停综合症诊断:肿瘤细胞死亡,由于减少了PD-L1表达增加t细胞活性和增加anti-PD-L1治疗功效。
事实上,在中介机制与阻塞性睡眠呼吸暂停综合症(即。氧化应激、交感神经过度活跃、炎症和间歇性缺氧),慢性间歇性缺氧和HIF-1激活现在被公认为主要贡献者有害代谢疾病后果(1,23]。此外,间歇性缺氧和相关HIF-1激活也被证明能够促进癌症发展在体外(11,21,24),在活的有机体内(2,3,10,11,14,24]。
PD-1 / PD-L1免疫检查点黑色素瘤侵犯
高级形式的皮肤黑素瘤,咄咄逼人,现在证实免疫调节中扮演着重要角色在背后的机制抵抗传统癌症治疗(15]。这些证据来自詹姆斯·p·埃里森和的开创性工作Tasuku Honjo,他们被授予2018年诺贝尔医学和生理学奖,显示细胞毒性T-lymphocyte-associated蛋白4 (CTLA-4)和PD-1通路功能分子“刹车”免疫系统(25]。由黑色素瘤细胞表面抗原的表达,比如PD-L1和随后的绑定在肿瘤微环境细胞毒性t细胞PD-1抑制t细胞的活动,从而抑制antitumoral免疫反应(图1)[25]。因此,“免疫检查点”复合物如PD-1 / PD-L1代表理想目标发展的预后和治疗皮肤黑色素瘤的管理工具。
先进的皮肤黑素瘤是第一个癌症免疫疗法辅助目标免疫检查点已经测试(15]。按照时间顺序,第一个辅助免疫关卡拦截器使用ipilimumab CTLA-4-blocking抗体。两种PD-1抑制剂,nivolumab pembrolizumab,迅速被介绍时,经常用于转移性黑色素瘤患者,其中包括屈光CTLA-4封锁[25]。几年后,辅助治疗策略,包括抗体针对PD-1 / PD-L1轴在先进的黑色素瘤,因此大大促进了全球生存和改善皮肤黑色素瘤患者的治疗。2018年,nivolumab定位是护理的新标准先进的黑色素瘤。
关于PD-L1的价值作为癌症的预后标记进化,最近的数据表明,增加PD-L1表达式与不利的结果在各种癌症有关,但也有冲突的报道关于其预后价值,如结肠直肠癌(26]。这种差异可以归因于技术问题的起源和形成也PD-L1调查。
例如,表达式由tumour-infiltrating PD-L1肿瘤细胞和免疫细胞对结直肠癌有相反的影响攻击性和转移(26]。此外,研究调查的角色PD-L1癌症发展应该区分肿瘤和免疫细胞上表达的膜PD-L1等离子sPD-L1和其他循环PD-L1来源27]。关于黑色素瘤,Z侯等。(28)最近证明sPD-L1可以作为预后标记转移的潜力和应对免疫治疗检查站。有趣的是,一个更近期的研究显示相同的预后价值PD-L1-containing液产生的黑色素瘤细胞(29日]。这是特别重要的,因为exosomal PD-L1, sPD-L1相比,密切反映了肿瘤和转移性细胞PD-L1表达式。
为什么要特别可靠的生物标志物sPD-L1黑色素瘤侵犯和转移在阻塞性睡眠呼吸暂停综合症?
在多中心横断面观察性研究包括360名新诊断的患者皮肤的黑色素瘤,Cubillos -Zapataet al。(16]相比血浆sPD-L1水平根据阻塞性睡眠呼吸暂停综合症的存在和严重性,与皮肤的黑色素瘤和评估关系侵略性和侵袭性16]。患者分成四组(non-OSA轻度阻塞性睡眠呼吸暂停综合症,中度阻塞性睡眠呼吸暂停综合症和重度阻塞性睡眠呼吸暂停综合症)根据他们apnoea-hypopnoea隔夜指数(AHI)评估呼吸polygraphy。完善的标记被用来评估皮肤黑色素瘤侵犯(有丝分裂指数、肿瘤溃疡和阶段)和侵袭性(‘健康指数,克拉克水平和前哨淋巴结积极性)。队列的一个全面的分析表明,sPD-L1水平更高的严重的阻塞性睡眠呼吸暂停综合症与轻度或non-apnoeic病人和他们积极、独立与你好,在整个队列和阻塞性睡眠呼吸暂停综合症的病人。然而,这是一个巨大的团体之间的重叠和相关性很弱,质疑的特异性关系。
重点分析阻塞性睡眠呼吸暂停综合症的病人显示sPD-L1最高水平被发现在患者预后差的配置文件。更具体地说,增加sPD-L1水平与黑色素瘤侵犯标记,比如高扩展阶段,深肿瘤入侵,肿瘤溃疡和前哨淋巴结的参与。这些结果中观察到non-apnoeic病人,但作者承认,这可能是由于样本量有限non-OSA组。
此外,sPD-L1作为预后的生物标志物的价值证实了阻塞性睡眠呼吸暂停患者的侵犯和转移提供的净改进传统预测模型的公司,特别是积极的前哨淋巴结的风险预测模型,导致更好的分类情况下的27.3%。
鉴于这些结果,这项研究由Cubillos -Zapataet al。(16]确实允许建议sPD-L1皮肤黑色素瘤侵犯和转移的潜在生物标志物在阻塞性睡眠呼吸暂停综合症的病人。这也强化了这一事实PD-L1表达式是调节通过间歇性缺氧,阻塞性睡眠呼吸暂停综合症的主要标志,正如前面证明了同一组(20.和别人22,30.]。事实上,PD-L1已被正式确认为一个目标基因HIF-1 [22),一个已知的转录因子参与间歇性缺氧/阻塞性睡眠呼吸暂停综合症[有害代谢疾病的结果23),但也加剧皮肤的黑色素瘤预后[21,30.]。
的主要问题之一是探索为什么有些阻塞性睡眠呼吸暂停综合症患者出现更积极比non-OSA皮肤黑色素瘤患者。独立研究已经表明,阻塞性睡眠呼吸暂停综合症是与攻击性增加皮肤黑色素瘤(12,13]。此外,间歇性缺氧严重的阻塞性睡眠呼吸暂停综合症患者的移植PD-1 / PD-L1通路没有癌症,导致CD8的免疫调节+t细胞活动(图1)[20.]。这种效果的间歇性缺氧PD-1 / PD-L1轴在黑色素瘤的生态系统可能导致有害PD-L1对皮肤黑素瘤预后的影响。的确,PD-L1表达式已经直接关系到皮肤的黑色素瘤侵犯(17- - - - - -19,29日,31日]。该领域的一个主要问题是理解为什么一些皮肤的黑色素瘤患者无免疫抑制剂检查站。大约有60%的病人新创抗免疫抑制检查站和20 - 30%的初始反应者最终会产生获得性耐药(32]。破译间歇性缺氧的混杂作用在这个特定的子群的病人可能是下一个步骤。
最后,研究Cubillos -Zapataet al。(16)当然是重要的,到目前为止最大的前瞻性多中心研究领域,和作者应该祝贺。然而,正如作者自己承认的,睡眠破碎,主要的混杂机械因素,尚未评估在当前的研究中。这种评价是需要在将来的研究中。此外,sPD-L1海拔不证明因果关系;这需要介入研究。研究议程可能预期如下:1)阻塞性睡眠呼吸暂停综合症患病率研究在无免疫抑制剂检查站;2)随机对照试验比较严重的影响几周的骗局与有效持续气道正压(CPAP) sPD-L1将高度信息;3)积极成果,CPAP应该测试作为一个联合治疗改善皮肤黑色素瘤的长期控制(图1);4)最后,鉴于其分泌肿瘤和转移性细胞,测定的exosomal PD-L1 [29日)应该在阻塞性睡眠呼吸暂停综合症患者加强分层进行测试。
由于这样一个研究项目的复杂性和成本,一个国际财团是非常可取的。跨越所有这些“研究检查点”之后,我们的希望是,真正的阻塞性睡眠呼吸暂停综合症和间歇性缺氧的影响将建立的免疫调节皮肤的黑色素瘤,将利润的黑色素瘤患者的结果。
脚注
利益冲突:m . Minoves没有披露。
利益冲突:J-L。Pepin没有披露。
利益冲突:d Godin-Ribuot没有披露。
- 收到了2018年12月23日。
- 接受2019年1月3日。
- 版权©2019人队