文摘
慢性呼吸道疾病仍是全球发病率和死亡率的主要原因。唯一的选择在终末期疾病肺移植,但没有足够的供体肺,以满足临床需求。选择选项来增加迫切需要肺移植组织的可用性缩小差距在这个未满足临床需要。越来越多的组织工程方法探索可能生成的肺部组织体外用于移植。生物衍生和制造支架与细胞和生长的种子体外一直在探索在临床前研究中,最终目标的生成功能肺组织移植。最近,已经有显著的努力扩大细胞培养方法为宏观生物工程方法生成足够的细胞数量。与此同时,有激动人心的努力在设计生物反应器,允许适当的细胞培养和发展功能肺组织。本文旨在介绍当前最先进的这些领域的进展和讨论承诺在肺部生物工程领域的新思想。
文摘
生物工程肺组织显示了承诺但主要挑战必须克服技术提前到诊所http://ow.ly/T9cU30ko0BS
介绍
背景
呼吸道疾病是全世界第三大死因,预计将继续增加在未来几年。呼吸道疾病在欧盟的总体成本相当于每年EUR380十亿以上1]。目前,终末期呼吸系统疾病的唯一选择是肺移植。每年大约2000肺移植发生在欧洲2),与相同数量或更多等待移植的患者。移植疗效仍然是一个重要的临床问题是移植排斥率高,并发症可能出现由于所需的免疫抑制药物;5年存活率仅为50% (3]。肺移植的替代选项可用来增加组织必要缩小差距在这个未满足临床需要。除了使用肺部捐赠从循环死亡(以便)捐助者,并继续发展和改善体外保存和体外肺灌注(EVLP)技术试图最大化供肺适合移植的数量(4- - - - - -9),一个令人兴奋的新领域的研究侧重于生成的肺部组织体外。
小说思想和假设
肺是一个高度复杂和动态的器官组成的许多不同的细胞类型与不同的功能(10]。生物工程肺组织体外移植是一个区域接收增加关注和解决捐献器官的短缺。目前正在研究的方法在临床前研究中利用生物提取或合成支架与自体种子细胞最终移植接受者。合成和生物衍生支架都有不同的优点和缺点。混合支架结合生物派生和合成支架可能是一个新颖的方法来限制观察到的缺点与合成或生物衍生支架。开发了各种不同的技术来帮助生成肺组织工程支架,如decellularisation生物支架,和先进的生产合成支架的制造工艺,如铸造、电纺的,cryogelation和精密加工技术。
因此,生物工程肺组织可以帮助增加可供移植的肺组织和有潜力提供福利在同种异体移植。综述,我们旨在讨论最新进展和新兴主题在肺组织工程,需要克服的主要挑战和发展这种方法更接近临床。
制造业的肺
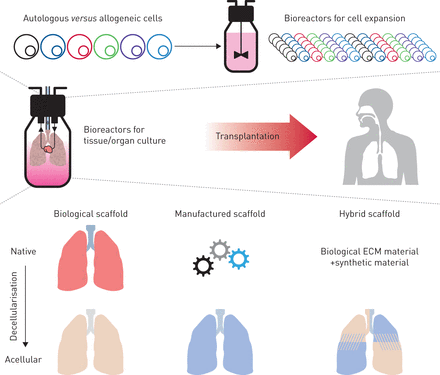
肺细胞类型(至少有40个不同的居民10),所有这些对于优化功能是必要的。驻留在这些细胞内和细胞外基质(ECM)由不同的区域组合ECM蛋白和粘多糖(如。蛋白聚糖和透明质酸)共同行动作为支架不仅提供结构,但也帮助直接修复和再生后损伤(11]。l愤怒和Vacanti(12)第一次描述了组织工程的方法,即细胞结合矩阵由天然或合成材料和种植体外,其次是移植(图1)。几个案例报告和组织工程产品的临床试验已经证明了追求这些技术的可行性在诊所(13,14]。虽然没有尝试产生肺组织体外组织工程是第一次描述时,最新的方法采用了这种模式。尽管肺组织工程方法在历史上落后于其他领域,有激动人心的最新进展与天然材料和合成材料。
肺癌生物工程方法。在大多数方法,肺脚手架播种与自体或同种异体细胞生物工程是一个肺。细胞可以扩展到适当的数字在生物反应器细胞扩张。一直在探索不同的肺,包括decellularised支架和合成支架。一个新兴的想法是使用混合结合生物材料支架,如细胞外基质(ECM)组件与合成支架以创建一个混合肺脚手架。生物反应器对机关文化可以用于成熟和评估添满肺肺移植前支架。
非细胞肺癌支架
脚手架的来源和影响处理,存储和冲销
非细胞(生物)肺支架已成为可能的支架材料体外肺组织工程近年来。在这种方法中,得到了非细胞支架的细胞从本地的肺部组织通过一个叫做decellularisation方法。最终,任何decellularisation协议的目的是去除细胞材料没有不良影响产生的宏观非细胞支架结构和ECM成分,ECM组件的机械完整性或生物活性(15- - - - - -17]。理想情况下,非细胞肺癌可以与自体的细胞或recellularised,或者,一个同种异体来源。非细胞肺癌支架的主要优势是,他们大多保留复杂的结构和宏观和微架构的原生肺组织,不能使用任何已知的制造技术生成。大多数ECM组件被发现被保留在decellularisation后的非细胞组织(18- - - - - -20.),尽管这些组件的程度保留在本国取向没有得到广泛的研究。ECM组件的保留,以及他们的组织,可能是至关重要的功能最终工程组织。
ECM是微环境的主要成分已知的直接细胞迁移等行为,增殖和分化18,21,22]。非细胞组织支架可以保持生物活性属性和一定程度的组织特异性(19,23]。最近的研究表明,年龄在支架和那些来自肺部疾病可以收购的细胞表型细胞从正常的患者(21,24- - - - - -27]。因此,人类从老年患者支架或那些存在肺部疾病很可能不是肺组织工程支架的理想来源。
有趣的是,最近的一项研究表明,支架由产后早期人类肺部支持增强re-epithelialisation与来自成人肺(28]。虽然产后肺可以用来为新生儿提供支架,主要关注使用新生儿肺成人肺组织工程是大小不匹配。一项研究调查的结果从size-mismatched肺移植捐赠者和接受者发现一丁点肺收到更高的潮汐卷因为捐赠者和接受者的重量差异(29日,30.]。此外,肺移植使用尺寸过小的肺与风险增加有关原发性移植物功能障碍(31日]。虽然还不清楚或者从新生儿肺如何被用于成人肺组织工程计划,从这些研究中获得的信息可能会导致新想法利用支架来自成人的捐助者。
当考虑来源clinical-grade脚手架材料、供体组织并不一定需要人类的起源。肺从结构上类似的物种,如猪或非人灵长类动物,可能提供一个更统一的捐赠来源,用更少的限制比人类来源(19,25,32- - - - - -35]。使用非人类灵长类动物的肺被局限于临床前模型使用灵长类生物工程和有道德问题的非细胞支架。因此,猪肺先成为一个潜在的选择由于使用其他猪异种移植的组织。然而,一些物种和组织属性在猪肺迄今已确定,可能具有挑战性的翻译异种的肺recellularised与人类细胞。胸膜气泡(囊性空腔)显示了我们和其他人decellularisation过程中出现,这可能会影响肺的通气力学,最终影响肺的功能如果移植24,33),如果破裂导致气胸(肺萎陷)。此外,猪肺的程度产生间接通风与人类相比是有限的。尽管各种细胞类型已被证明坚持猪支架(24,25,33,35],来自人体的内皮细胞附着porcine-derived支架被发现在一个更低的利率而人类——或者primate-derived支架(36),但原因仍然未知。残余,细胞相关异基因的蛋白质导致负免疫原性反应在人类已确定支架的猪肺decellularised根据当前标准(18,25),从而表明清除免疫原性蛋白通过转基因方法或post-decellularisation治疗可能是必要的。
此外,还有一些研究从人类群移植表明在供体和受体之间大小匹配的重要性(37]。的猪肺、气管和血管往往小于人类肺部。手术吻合人类受体猪肺,尤其是关于支气管,将具有挑战性和捐助者与接受者可能出现不匹配,可能导致死亡。猪肺的肺叶的形状后,猪的身体,因为它是一个四足动物。降低肺叶有一个尖的形状和肺韧带明显比人类更加明显。因此,基底下叶肺不张的肺可能发生如果肺移植到人类,因此有一个感染的风险增加。降低肺叶切除移植的时候,但是目前还不清楚如果这将是最优的。一些移植中心开展肺切除术时移植使肺更好融入胸腔。然而,一些移植中心负向这种方法因为肺部手术后的空气泄漏的风险。除了主要的解剖差异,猪内源性逆转录病毒跨物种传播的风险已经阻碍了临床应用异种的组织(38]。到目前为止,还没有正式的研究去除或保留的人畜共患病,包括猪内源性逆转录病毒,在异种的decellularised支架,因此跨物种疾病传播的危险是未知的(36]。因此,成人肺差点移植的标准和使用EVLP技术得不到提高6,7,39- - - - - -41)可能被视为最有可能的候选人来源clinical-grade肺组织工程的支架方案。
存储和冲销潜在的非细胞肺组织工程支架被发现显著影响结构和残留的蛋白质含量。此外,不同细胞类型的能力生存和增殖后接种也被证明是影响非细胞支架的存储条件和冲销42]。到目前为止,大多数的非细胞的肺已经消毒使用过乙酸;然而,这可能导致ECM降解[43,44]。最近的一份报告中描述了使用超临界二氧化碳冲销非细胞肺癌支架不诱导降解ECM (45]。优秀的技术进展,可以兼容良好生产规范(GMP) [46]。有趣的是,尽管一些基线的建立标准,商用支架的其他组织不同的企业可以有不同的反应相同的模型在活的有机体内伤害(47]。很明显,定义最优标准和端点的脚手架来源和处理非细胞支架将在未来的研究非常重要表1总结的挑战的领域内体外肺组织工程)。
Decellularisation技术
常见的decellularise肺的方法包括物理的不同组合,离子、化学和酶的方法(15]。Detergent-based灌注是最普遍地利用生成非细胞肺癌支架。常用的清洁剂包括特里同x - 100,钠脱氧胆酸盐,钠dodecylsulfate和皮套裤(3 - ((3-cholamidopropyl) dimethylammonio) 1-propanesulfonate),使用有或没有高渗氯化钠和DNase和/或核糖核酸酶解决方案。使用的洗涤剂的浓度和体积不同协议和不同物种(21,23,24,26,33,34,36,48- - - - - -51]。解决方案可能是通过血管灌注或航空公司和脉管系统。不同协议之间的差异导致了明显的组织学差异decellularised肺部和ECM和其他内容的保留蛋白(50,52,53]。目前尚不清楚差异如何肺decellularisation协议可能影响recellularisation和再生或植入支架的潜在免疫原性54,55]。大多数实验室decellularising组织利用的标准设定的Crapo等。(18),其中包括缺乏组织学检查可见细胞或核材料,< 50 ng双链DNA / 1毫克的干重的ECM支架和残余DNA < 200个基点。然而,这些都是最低标准,不考虑cytocompatibility (如。影响残余decellularising代理)、不育、写作和非细胞支架的机械性能56,57]。ECM成分和力学性能是特定于区域性的,和保留recellularisation导致这些差异可能是重要的功能性组织。
Recellularisation和临床前移植模型
各种不同的细胞类型被成功地用于recellularisation非细胞支架,包括胚胎干细胞(ESCs),诱导多能干细胞(万能)和内源性肺部祖细胞。有效的分化的多能细胞近端和远端肺上皮细胞仍然是一个挑战性的任务,但有令人兴奋的进展产生远端上皮祖细胞和多层上皮细胞则和小鼠的ESCs50,51,58- - - - - -65年]。
分化的多能干细胞到近端或远端肺上皮细胞生长因子需要已知由肺隔离ECM (66年]。因此,保留ECM组件和它们相关的生长因子在decellularised肺支架可能是最优的关键recellularisation区域特异性。的能力受移植者细胞生存,繁殖和分化是重要的评估短期和长期cytocompatibility脚手架。进一步了解其余的ECM和剩余蛋白成分可能影响种子细胞随着时间的推移,未来的研究将是一个重要的领域(表1)。
重要概念验证研究表明,非细胞肺癌支架可以recellularised与单细胞悬浮液从胎儿肺匀浆和re-endothelialised内皮细胞系中被永久地传颂或iPSC-derived内皮和上皮细胞67年用于移植。当移植到老鼠,recellularised肺被证明简单的功能在活的有机体内(48,51,68年,69年),最近,非细胞猪与人类细胞支架recellularised比例增大的猪研究[35]。然而,移植肺水肿的地区的建筑倒塌,表明长期肺再生功能尚未实现。尽管如此,这些研究鼓励这种方法的可行性。
剩余的蛋白质的金发女孩原则:“太多”,“太少”,找到“刚刚好”
大多数decellularisation过程的目的是移除支架的细胞和免疫原性物质,同时保留ECM蛋白质和结构。然而,随着质谱蛋白质组学迅速改善描述非细胞支架的组成,它已经变得越来越明显,大量non-matrisome蛋白质和细胞相关蛋白(细胞骨架元素)保留在decellularisation后的支架(21,24]。non-matrisome蛋白质的存在已被观察到在不同的组织,物种和技术用于不同的实验室(50,64年,70年]。这些残留的蛋白质和其它细胞衍生的影响组件受移植者细胞和他们潜在的免疫原性相对未知的肺组织工程。目前还不清楚如果1)decellularisation协议更积极和删除多个组件或2)协议不那么咄咄逼人,但保留更多组件将更有利于支持功能的再生。剩余的蛋白质已被证明在其他组织发挥重要作用在调节细胞的行为受移植者细胞和免疫细胞浸润一旦植入(71年]。此外,个人健康的患者之间的临床异质性观测可能使定义最低标准挑战[24]。最终,改善我们的理解decellularised支架的组成和把这些生物的结果是未来的一个重要方向。
表2以下部分,总结一些最重要的研究到目前为止,已导致仪器的进步使用非细胞肺组织工程支架(22,24,25,33,34,42,48,49,51,52,59,64年,65年,72年- - - - - -128年]。
人工肺
虽然非细胞支架显示肺部生物工程领域的承诺,人类lung-derived非细胞支架的异质性和潜在的异种的问题使这种方法具有挑战性的扩大可再生的和可控的方式(21]。替代非细胞支架可以人工(或生产)支架。合成和天然聚合物可用于这些方法,和各种材料已经探索了气管、支气管和肺实质组织工程(图2和表2)。人工支架气管更深入调查由于气管的简单,管状结构(72年- - - - - -78年]。许多材料用于生成支架临床前研究的大型航空公司POSS-PCU等合成高分子材料(多面体低聚物的silsesquioxane保利(carbonate-urea)聚氨酯)(72年),聚乙醇酸(普朗尼克f - 127 (79年)和聚丙醇-聚乳酸纤维有限公司乙醇酸(80年),所有cytocompatible聚合物力学性能在气管组织工程所需的范围。尽管这些材料可以制造具有良好的精度和加工改进的贮存稳定性,大多数缺乏必要的生物属性,如本地整合素结合位点和生物活性线索细胞依附,增殖和分化。目前未知的主题需要被添加到这些支架支持功能的再生。然而,它已经表明,细胞播种和移植覆盖可以提高通过简单地修改中使用的聚合物支架的表面,如。提供细胞附件网站通过增加表面孔隙度(72年)和/或将个人ECM组件(73年]。
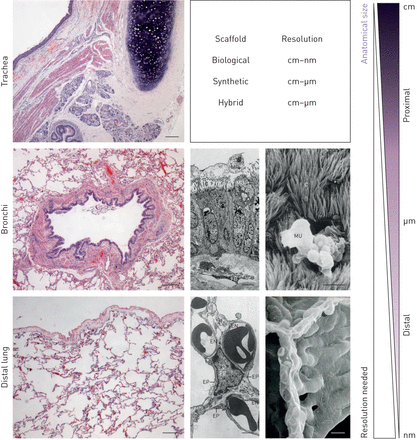
关键技术的复杂性从近端(气管)远端肺结构(支气管和肺泡):苏木精伊红(他;左栏)染色组织学、透射电子显微镜(TEM);中心柱)和扫描电子显微镜(扫描电镜;右列)近端和远端本地的肺部组织。肺内的肺结构发生巨大的变化:从近端到远端,模仿本机结构所需的分辨率高(厘米(cm)→微米(μm)→纳米(纳米))。到目前为止,生物支架是唯一的支架有一个决议,模仿的本机所有长度尺度的肺。支气管TEM显微照片的薄片的小人类支气管粘膜显示纤毛细胞(CC)和纤毛(C)和微绒毛,杯状细胞(GC)的顶端粘液栓(μ),基底细胞(BC),纤维和成纤维细胞(神奇动物)在结缔组织和巨噬细胞(MP)。支气管上皮表面的SEM显微照片显示纤毛塔夫茨(C)和粘液栓(μ)的杯状细胞在挤压的过程中。远端肺TEM和SEM显微图的结构在人体肺部肺泡隔隔纤维母细胞(神奇动物),毛细血管内皮(EN)、肺泡上皮(EP)和纤维链(F)。他组织学规模酒吧:100µm;支气管TEM比例尺:5µm; bronchi SEM scale bar: 10 µm; distal lung TEM scale bar: 2 µm; distal lung SEM scale bar: 10 µm. Electron microscopy images reproduced and modified from [129年,130年经允许)。
相反,实质肺组织结构更复杂的三维(3 d),并需要薄的边界和相互关联的毛孔,有效的气体交换(81年]。由于与生产相关的困难脚手架几何参数适用于薄壁组织的肺组织,有有限的报道。到目前为止,潜在的实质组织工程支架是捏造的通过发泡(82年,83年],porogen-solvent技术,cryogelation [84年],光降解[85年,86年)和自组装微球(87年]。尽管这些技术能够概括alveolar-like结构,他们缺乏所需的脉管系统和航空公司集成到收件人,并最终进行气体交换。然而,最近的一份报告显示,一个3 d明胶微支架植入小鼠多能干细胞促进血管生成当植入(82年]。因此,如果这些结构能被连接到一个空气供应和blood-air障碍足够薄的边界,可想而知,这些结构可以支持气体交换。尽管重要概念验证研究,这些减去或批量制造技术已成功地生成功能肺组织和整合脉管系统尚未探索。合成材料可以产生巨大价值的肺支架由于精确和可重复生产能力对于个体患者,但目前还不知道合适的制造方法。然而,有方法,用于其他器官可能对肺组织有价值的探索,将在下一节中讨论。
潜在的制造方法来生成肺组织工程多孔支架
从简单的角度来看,肺实质是一个相互联系的系统porous-like结构周围毛细血管床促进气体交换(81年]。有几个不同的制造方法,用于对其他器官组织工程多孔结构,如。冷冻干燥、发泡溶液浇铸和particulate-leaching技术(88年]。生产过程也被开发出来用于生成perfusable在组织工程血管通道结构(89年]。
电纺是一种添加剂制造技术,已成为一种有效的方法生产纳米纤维用于多个领域,包括组织工程血管的90年)、皮肤(91年和气管73年]。合成和天然聚合物可用于电纺的创建薄纳米纤维组成的多孔支架,已经被证明可以支持细胞附件、增殖和分化。通过控制纤维等参数大小、密度、成分和方向,纤维结构,类似于ECM可以生产。此外,如生长因子或药物分子可以被包括在脚手架影响和直接再生组织的空间或暂时。电纺的已经被用作在体外平台为研究纤维化肺微环境的影响在不同的细胞类型(22]。总的来说,电纺是一种很有前途的技术,但一直限于只创建一个在体外试验平台和尚未用于生物工程的肺部组织。
技术适合创建定制的、可再生的、错综复杂的3 d设计使用cytocompatible材料是组织工程的理想选择。3 d打印技术或生物打印细胞打印时,最近成为一个潜在来源为生物工程组织或支撑结构(92年- - - - - -98年]。3 d打印技术已经应用在临床上治疗tracheobronchomalacia [99年与3 d打印特定病人的气管和气管崩溃夹板(One hundred.]。然而,在这些实例中,3 d打印技术是用于支撑结构,而不是再生移植组织在人类身上。3 d打印技术已经探索了老鼠等器官组织工程气管使用scaffold-free方法(101年)、皮肤(102年),软骨(103年),主动脉瓣管道(104年和维管组织105年),但目前没有发表的报告试图3 d打印肺组织气体交换的能力。3 d生物打印将极具挑战性,远端肺的气体交换障碍是纳米的顺序和喷嘴用于打印细胞需要在微米范围内。因此,新的3 d印刷需要开发或制造方法来克服这一限制。然而,3 d打印技术足够先进的印刷结构在气管和支气管的分辨率(图2),但材料和制造方法兼容细胞尚未报道。
在3 d印制技术的生物组织的一个挑战是,目前很多技术打印高分辨率结构使用过程不符合直接打印细胞和许多生物材料。传统的3 d打印方法依赖于溶剂或加热生成聚合物解决方案,可以通过3 d打印流液体喷嘴。因此,这些限制是导致进展缓慢的3 d打印肺和其他组织。
重要的是,印刷的材料并没有降低新ECM合成之前,由种子细胞沉积和组织可以支持组织的结构和处理任何机械负荷(如。进一步的细胞育种、生物反应器参数和外科处理)(106年]。因此,降解动力学和降解产物的影响时需要考虑的重要参数选择,设计和验证新的肺组织工程生物材料的应用潜力。这些以及其他问题的成功应用需要解决制造支架产生肺或气道组织。
混合材料
尽管非细胞支架和支架生产的进步,最终也可能是最佳的支架材料。在许多其他制造业领域,优化材料是通过使用混合动力或复合材料,积极的属性可以组合两个或两个以上的材料来生成一个最终的材料最优整体属性,克服个人组成组件的局限性。使用混合或复合材料制造支架可能因此理想溶液的生物有利自然ECM-derived脚手架材料、网站等组织和分化细胞粘附和线索,可以结合合成材料和先进制造方法生产更多可再生的产品与可调或可控力学性能。
细胞类型和扩大细胞培养方法
除了识别方法可再生产地制造合适的肺组织工程支架使用非细胞或制造支架,一个额外的挑战是确定细胞来源和获得足够的细胞数量。在理想的情况下,从患者自体的细胞可用于recellularising肺为了最小化post-transplantation免疫并发症和免疫抑制药物的必要性。然而,理想GMP-grade制造方法大规模生产可能需要不同的细胞肺癌生物工程目前没有广泛建立。
完全分化主要成年细胞和/或自体肺内源性祖细胞可能是一个潜在来源。然而,当使用这种方法时,多种细胞类型可能需要从患者标本中分离出,发展到足够数量体外并引入脚手架在正确的位置,以生成功能肺组织。
虽然我们理解什么是“完全分化”或成人细胞类型的肺是不断发展的,使用终末分化细胞类型不允许后肺损伤的修复。因此,内生祖细胞,参与成人的修复过程,可能是一个更合理的方法。一个潜在的方法再生的多种细胞类型的肺可能是多个祖细胞种群种子到肺支架与导演的终极目标分化成不同类型的细胞中发现成人的肺。这将避免不必的必要性在肺中引入不同细胞类型和直接正确的解剖位置。两个激动人心的最近的报告表明,足够数量的内生上皮祖细胞可能是来自一个病人和扩展体外覆盖整个非细胞的气管移植或很大程度上人类肺叶(64年,107年]。非常重要的一点是,这些扩展方法依赖于物质容许人类临床使用(107年]。进一步发展需要使用GMP-grade生成可伸缩的方法制造方法,以确保足够的上皮细胞,内皮细胞或间充质细胞覆盖。额外的限制也可能在于确定合适的内生祖细胞的数量由现有的肺病患者。这可能是具有挑战性的,有新兴的证据表明,这些细胞异常的慢性肺部疾病(108年- - - - - -110年]。然而,这将是一个有趣的未来的研究作为先前的报道表明,脚手架影响细胞行为更强烈的细胞起源(26]。因此,一个正常的脚手架可以帮助恢复病变患者获得细胞的表型。
另一种方法内生祖细胞是万能的。这些是特别感兴趣的最近的研究表明,人类可以分化成细胞表达的细胞则远端肺上皮细胞表型和播种到非细胞(人类的肺59,61年]。此外,在肺部疾病患者由已知的基因改变引起的,如囊性纤维化(CF),则来源于这些病人可能gene-corrected后续recellularisation之前(63年,111年]。然而,则也有一些潜在的缺点:目前病人皮肤活检通常是用来制造万能,但它已经表明,这些细胞的表观遗传记忆部分保留组织起源的112年]。虽然没有详细探讨,这可能导致限制当差异化则成特定的肺血统。然而,多项研究表明,来自成纤维细胞的细胞则可以用来获得细胞含有成熟的肺上皮细胞表型和功能标记(61年- - - - - -63年,113年,114年]。其他研究也调查了ESCs的使用,发现这些可以对不同成人上皮表型分化体外(60,66年]。尽管他们承诺,ESCs携带伦理问题,为ESCs和已被证明的细胞则形成畸胎瘤(115年,116年]。因此,ESCs,则需要进一步优化和临床使用前彻底调查。
最近的报告显示承诺使用悬浮培养细胞的大规模生产和文化(搅拌)生物反应器和旋转壁式生物反应器(61年,117年),包括技术符合GMP,因此临床使用(35,117年- - - - - -119年]。这可能允许翻译干细胞研究临床和临床前应用程序建模一个潜在的GMP工作流程。然而,大规模生产的细胞为每个单元格类型需要优化。尽管取得了这些进步,很明显,新方法,需要降低成本和时间成本效益和更少的劳动密集型的大规模生产的细胞供临床使用。
生物反应器的策略肺部生物工程
虽然灌注和通风的研究更简单的使用非细胞时,完整的肺,还有报道相对较少,处理这些参数(131年- - - - - -133年),很大程度上是因为合适的肺部生物反应器的有限的可用性。近年来各种生物反应器策略已经发展为肺和气管生物工程方法或整理被拒绝的肺移植(7,134年]。Ghaediet al。(135年)开发出一种旋转生物反应器,暴露的非细胞肺癌细胞播种到薄片空气和液体交替,导致肺泡上皮细胞扩张。de - recellularisation无异的肺,Gilpinet al。(50)开发的一个细胞进行播种的压力控制装置通过引力。商用孤立肺灌注系统称为器官再生控制收购生物反应器(美国哈佛装置再生技术、Holliston MA)也被他人用于decellularisation [33,34,136年]。尽管在过去几年中所取得的进展与EVLP系统最大的时间可以保持一个健康的肺体外和移植的范围6 h (137年- - - - - -139年]。人们认为生物工程肺体外需要更长时间的成熟的生物反应器之前移植。上呼吸道的一个新兴生物工程方法,主要是水平或垂直生物反应器一直在利用之前(140年),是利用人体作为生物反应器。例如,维elaere和同事(141年,142年)生物工程异基因供者气管首先前臂的接收者,然后替换损坏的气管与同种异体移植物。尝试为新创代的器官还包括人性化的使用猪等动物生物反应器(143年,144年]。有趣的是,最近的一份报告中使用本机猪肺在交叉循环模型的报道体外36个小时,但移植不是评估作为一个结果(5]。不管体外方法,确保发展中肺或气道组织获得足够的营养和发展适当的将重要的更详细地研究未来的研究(表1)。整合实时测量如葡萄糖、乳酸、电解质、pH值和机械通风属性除了血管阻力将重要了解必要的体外文化的时间和帮助智能生物反应器设计策略。
监管和伦理对翻译的影响肺部生物工程方法
尽管最近在肺部生物工程和令人兴奋的进步,许多重要的监管,道德和现实的挑战需要解决这些技术进入诊所,规模更大。每组的挑战(如。再生医学产品的分类,批准的材料,使用干细胞,等。使用的生物工程方法)将是独一无二的。去开发新的潜在的治疗方法,非常重要的一点是,这些转化的关注点尽可能在产品开发的早期管道。建立监管框架和GMP标准对组织工程产品和这些需要优先考虑患者安全的执行(145年,146年]。此外,它仍然是完全未知的评估标准应该用于生物工程第一次作用于人体的临床试验前的肺组织可以执行,但参数的使用与用于EVLP可能是一个良好的第一指示(147年]。此外,使用一个适当的大型动物模型,研究短期和长期的结果将是必要的,然后这些方法翻译到诊所。它为学术研究者将至关重要,临床医生、行业和监管机构之间互相协作,建立这些新的框架。
迄今为止,大多数研究人类肺部用于decellularisation利用肺,不能满足临床移植或标准,另外,从正常患者尸检肺non-lung-related死亡。人体组织获得生物医学研究不同国家之间显著不同(148年- - - - - -150年]。de -因此,如果和recellularisation是意识到一个更大的规模和在诊所,监管框架需要允许对这些技术在每个国家。一个潜在的未知的来源从捐赠者DCD计划生成非细胞可能是人类的肺。捐助者DCD计划使用在许多国家,但并非所有国家允许使用由于道德问题。在大多数国家,以便决定肺移植前使用EVLP评估。然而,大部分的捐助者不用于移植,因为他们无法达成移植所需的最低标准(主要是低血气值)后评估体外(151年]。如果所有这些来源的人类肺组织可以使用和生物工程策略可以被设计成可重复生成功能肺组织移植,最大的限制因素将可能成为所有生物工程生产成本的肺的病人在候补名单上。
尽管合成材料并不限于这些相同的道德和监管限制对于确定一个合适的源,合成材料的使用的一个主要障碍是材料所需的时间和总体成本获得欧洲药品局或美国食品和药物管理局批准,其中包括彻底的描述在体外和在活的有机体内材料特性(152年,153年]。此外,干细胞和再生医学产品的监管是一个快速发展的领域,千差万别的国家。在过去的几年里,国家如日本(154年)采用了新的监管途径和传统路径非常不同的翻译,完全在大多数国家(150年]。因此,进行临床前试验的能力,最终的路径诊所将在每个国家是不同的。
讨论和展望
尽管已经取得了显著的进展在生物工程肺或气道组织体外与移植的终极目标(表2),大多数的概念验证研究肺部生物工程都集中在内皮和上皮车厢。为了生成功能肺组织能够长期功能,超过40个不同的细胞类型和可能,成千上万的不同细胞亚型可能需要又一次重复。然而,目前不清楚这些细胞类型产生肺组织可以最低限度功能是必要的在活的有机体内。在最近的一次和创新方法,提出的问题是是否所有细胞在decellularisation应该删除。Dorrello等。(155年)开发技术选择性decellularise上皮,但保留了内皮。可以采用这样的技术体外或在活的有机体内。众所周知,一个完整的血管网络是至关重要的移植以及维持血液气体屏障,允许适当的移植肾功能,还支持再生细胞(156年]。去除上皮细胞和保留血管内皮可能是一个选项来增加补种的成功,对某些病人植入。然而,在慢性肺部疾病患者血管严重受损(如。肺动脉高压(PAH)),这可能不是一个合适的方法。
一个主要的问题在非细胞肺癌支架的使用是recellularising间隙空间的挑战和平滑肌细胞神经支配的重要性。将细胞播种到decellularised构造溢出通过现有的基底膜?将受移植者成纤维细胞或平滑肌细胞仅仅“找到”到适当的解剖位置如果播种通过航空公司或脉管系统?关键是如何支配,这将如何实现在脚手架和神经系统集成到收件人?尽管制造技术,如3 d打印技术可能有助于克服对空间的一些挑战沉淀细胞,还有其他的挑战,如合并和控制多个喷嘴与每个细胞类型和生成结构长度尺度气体交换的能力。
这将是重要的更充分地理解种子细胞转变为非细胞的行为,合成或混合支架和任何后续的ECM重塑或免疫反应。目前不清楚“干净”需要肺组织工程支架的方法。从临床前研究的证据157年)和其他非细胞支架的临床使用表明,非细胞支架的处理可以影响他们的免疫原性46,158年]。一般来说,免疫细胞并没有引入任何体外生物工程方案;因此,免疫原性反应将限制在那些由于接受者的免疫系统。免疫细胞被发现能够诱导成纤维细胞的病理反应的非细胞肺癌支架,来显示他们的潜在作用,指导细胞命运的种子在非细胞支架159年]。有趣的是,免疫细胞,如巨噬细胞、最近发现指导正常的肺泡再生中发挥重要的作用在活的有机体内(160年]。因此,不同的免疫细胞的数量在导演的角色体外再生和他们潜在的调节作用在活的有机体内再生是一个有趣的领域未来的调查。一些容许大量的免疫原性蛋白可能有助于促进再生和成熟为移植在功能性组织体外成熟的阶段。肺移植受者目前放在广谱免疫抑制药物,因为各种不同的免疫细胞的数量(中性粒细胞、b细胞、t细胞、巨噬细胞等)与肺移植排斥反应,急性和慢性排斥反应(30.]。是否这将需要在相同的程度上移植生物工程的肺还不知道。
此外,关键是未来的研究在该领域更全面地描述和理解生物工程的潜在功能肺组织(表1)。在临床肺移植病人的人口统计数据,如年龄、吸烟史、没有胸部创伤和无恶性肿瘤是重要的标准选择合适的捐赠者,而功能性标准供体肺是土著的兼容性,清晰的胸片,动脉氧张力(PaO2)> 300毫米汞柱吸入氧分数(FIO2)1.0%,呼气末正压通气(偷看)5而言不啻2O (161年]。为肺二手EVLP,当前功能标准中心之间的不同(如。多伦多,隆德或“商务”(器官保健系统)协议)162年]。因此,可以预见,生物工程的最低功能标准肺PaO2> 350 - 400毫米汞柱FIO21.0%和5而言不啻偷看2啊,这是用于EVLP评估(163年]。其他标准化方法进行评估可以:血液气体从每个生物工程叶,支气管镜检查,乳酸脱氢酶值、活性氧的生产、支气管肺泡灌洗(蛋白质和炎性细胞因子)和表面活性剂分析评估。
虽然专利脉管系统和气体交换可能是最关键的初始功能评估移植能否进行,因此被先前的研究的焦点(65年),生物工程肺组织和细胞内也应该能够应对环境,这意味着很可能长期功能所必需的其他功能。在这些上皮的纤毛跳动和间隙吸入粒子和过敏原,黏膜纤毛的清除,表面活性剂的生产。内皮,构造的能力来支持事件如止血和白细胞外渗在肺损伤中探索在将来的研究中很重要。更广泛地说,任何组织工程构建应该有能力妥善应对潜在的挑战和伤害,并在本地修复。因此,接受者的免疫系统如何重新移植肺组织仍然几乎完全未知的,可能是非常重要的,尤其是新兴证据表明肺港口造血祖细胞,血小板体内生物起源的主要网站(血小板总产量的50%)(164年]。此外,它仍然不完全理解如何招募,monocyte-derived巨噬细胞不同于tissue-resident在肺巨噬细胞(165年),但他们已被证明是重要的再生的远端肺160年]。这些和其他免疫细胞是否需要或故意播种体外再生方案仍然未知。
目前,有五个主要类型的接收大部分肺移植的患者,即。慢性阻塞性肺疾病(COPD)、特发性肺纤维化(IPF)、多环芳烃、CF和α1抗胰蛋白酶缺乏症AATD患者。在所有的慢性肺部疾病(如。慢性阻塞性肺病,IPF和PAH),有已知缺陷的内生肺部祖细胞的数量。因此,在缺乏基因修正或调制与外生因素,目前还不清楚如果这些细胞类型可用于肺生物工程方案。则可能因此被视为最有前途的细胞来源的临床相关的计划。然而,在这两种CF (63年,166年和多环芳烃167年),突变也发现在iPSC-derived肺上皮细胞祖细胞和内皮细胞,分别。最近技术表明iPSC-derived肺上皮细胞祖细胞可以gene-corrected CF患者体外(63年]。由于潜在的细胞来源的差异具体患者肺部疾病,很明显,生物工程方法将不是一个“一刀切”解决方案,将需要修改为每个不同的肺移植患者的主要群体,也许对于每个病人如果个人需要gene-corrected突变。
除了方法旨在生成单引号或双肺,可能有临床影响重建单个叶或只有部分的肺部组织。虽然标准单或双肺移植,移植单叶只在一些中心执行,但可能是有益的对于某些患者团体,如慢性阻塞性肺病和AATD患者(168年]。此外,单一从成年供体移植已经完成在儿科患者与成人大小匹配是具有挑战性的捐助者(169年]。因此,生物工程单叶可以使用。临床情况只有部分的薄壁组织或气道的影响(如。创伤,当地的支气管扩张、气管崩溃和nonsmall细胞肺癌)可以从这些方法中获益。技术制造alveolar-like结构(82年,85年,86年,127年),气管支持(99年,One hundred.和替换146年)最近都被开发出来。此外,研制的生物材料可以作为人工胸膜疾病和急性条件影响肺胸膜(如。气胸和间皮瘤)(170年,171年]。因此,可能有潜在的临床影响重建或替换部分肺组织与组织工程产品的病人,只有某些地区的肺部受损。
追求肺肺组织再生的生物工程方法移植了新机会体外造型不同的肺部疾病。虽然一直不使用合成材料研究造型肺部疾病,这是一个新兴的研究领域与巨大的潜力来帮助新模型方面的肺部疾病,目前的模型不能解决。非细胞肺来自慢性肺部疾病患者更完全概括了临床异质性和忠实地模仿临床疾病。追求生物工程对移植肺组织,开发的方法也可以用来执行药物屏幕,替代动物模型,更好的理解不同的肺部疾病和再生。然而,大多数的研究已经进行简化的条件下,并不能完全概括在活的有机体内场景。未来的免疫细胞以及生理参数如通风、灌注和氧含量的控制应该检查。
(复杂的)器官的组织工程曾被认为仅限于科幻小说的范畴。然而,令人兴奋的在组织工程领域最新进展是支持这个想法,这些技术可能确实有一天导致毁灭性的和虚弱的肺疾病患者治疗。最近的肺组织工程中取得了显著的进步很大程度上是由于合作生物学家,化学家、材料科学家、医生和工程师在学术界和工业;肺组织的认识和气道工程技术在诊所将取决于持续的进化和这些领域的成功整合。
确认
作者感谢肺癌生物工程和再生实验室的所有成员(瑞典隆德大学,隆德)有用的讨论在批判阅读的手稿准备和最后的手稿。作者感谢埃瓦尔德韦贝尔(伯尔尼大学,伯尔尼,瑞士)深刻的讨论和电子显微镜图像,和斯科特Randell(教堂山北卡罗来纳大学医学院、数控、美国)的组织学图像。我们还要感谢爱丽丝Caiado(伦敦大学的交流,伦敦艺术大学,伦敦,英国)提供一些肺的图形内的手稿。
脚注
作者的贡献:所有作者都参与写作,编辑和批准最终的手稿。
利益冲突:D.E.瓦格纳报告赠款克努特和爱丽丝•瓦伦堡基金会和德国肺中心,在进行研究;除了有一个专利(WO2014169111 A1)等待。
支持声明:这项工作是由瓦伦堡分子医学奖学金(D.E.瓦格纳和美国Lindstedt)克努特和爱丽丝•瓦伦堡基金会和亥姆霍兹慕尼黑博士后奖学金(D.E.瓦格纳)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2017年12月31日。
- 接受2018年5月30日。
- 版权©2018人队