摘要
碱性重排和表皮生长因子受体/喀斯特突变是晚期非小细胞肺癌(NSCLC)患者提供靶向或非靶向治疗的主要生物标志物。我们的目标是评估非小细胞肺癌生物标志物检测的成本效益。
2013年至2014年间,在法国19家医院前瞻性招募了843名未接受治疗的患者,进行纵向观察队列研究。比较了两种测试策略,即。“至少有一个已知的生物标志物状态”和“至少喀斯特状态已知”,另外以“无生物标志物检测”作为参考策略。采用Kaplan-Meier方法评估限制平均生存时间。评估了医院在治疗、住院护理和生物标志物检测方面产生的直接医疗费用。
与“不进行生物标志物检测”相比,“已知至少一种生物标志物状态”策略的成本-效果比为每节省生命年13230欧元,而“至少”策略的成本-效果比为每节省生命年7444欧元喀斯特状态已知“测试策略”。在敏感性分析中,生物标志物检测策略在41%的迭代中成本更低且更有效。
总之,治疗开始前的分子检测在晚期NSCLC的管理中被证明是具有成本效益的,并且可以帮助决策者在全科实践中确定进一步实施这些创新的条件。
摘要
喀斯特,表皮生长因子受体而且碱性在晚期NSCLC中,开始治疗前的分子检测被证明是具有成本效益的http://ow.ly/Ld1Z30ia9qv
简介
最近在识别非小细胞肺癌(NSCLC)的致癌驱动因素方面取得的进展,导致了基于特定生物标志物检测的策略,采用适当的靶向或非靶向治疗,进一步针对个别患者进行个性化治疗[1- - - - - -3.]。这些治疗方法是指基于酪氨酸激酶抑制剂(TKIs)的抗癌治疗。表皮生长因子受体(EGFR)基因突变是TKI治疗NSCLC的第一个靶点。厄洛替尼(特罗凯)或吉非替尼(易瑞沙),特定的EGFR TKIs,以及最近的阿法替尼(Giotrif)已被证明可以改善所有NSCLC组织的无进展和总生存期,与标准的铂基化疗相比[4- - - - - -6]。然而,绝大多数患者对EGFR TKIs产生耐药性并出现复发。相反,的存在喀斯特(KRAS原癌基因)突变或表皮生长因子受体外显子20突变似乎与EGFR-TKI靶向治疗的原发性耐药有关,尽管这些突变可能在多大程度上影响治疗选择仍不清楚[7- - - - - -9]。最近,对EML4(棘皮类微管相关蛋白4)-碱性(间变性淋巴瘤激酶)融合作为信号通路驱动因素已经支持了特异性TKIs crizotinib (Xalkori)和ceritinib (Zykadia)的开发[10]。在这种重排的预处理患者中,克唑替尼的总有效率为61% [11],与标准一线培美曲塞铂双联化疗相比,在乳腺癌患者中具有优势碱性最近已证实重新排列[12]。
最近的研究比较了暴露和非暴露致癌驱动因素患者的适当治疗,证实了这种“生物标志物检测和治疗”策略在提高总生存率方面的有效性[13]。也就是说,迄今为止,很少有经济学研究发表评估这种策略与“不检测和治疗策略”相比的成本效益[14- - - - - -18]。
存在表皮生长因子受体/喀斯特突变和碱性重排在患者中是相互排斥的,在治疗开始前至少意识到这些分子改变中的一种可能有助于优化NSCLC管理护理的算法,以选择最有效的治疗药物。循序渐进的方法的利益问题在法国和所有在普通人群中有检测政策的国家仍然是相关的。下一代测序(NGS)策略,使一步一步的方法无用,正在整个法国领土和欧洲国家部署,但不是在每个地方都以相同的速度部署。此外,这种方法没有解决筛选的问题碱性重组。最后,免疫组化(IHC)诊断的准确性碱性是不完美的和一些中心执行验证荧光原位杂交(FISH)试验确认阴性结果碱性NGS检测阴性后,进行免疫组化。通过比较常规生物标记物检测策略与不检测策略的相对收益和成本,成本-效益分析可以作为向决策者提供信息和更好地确定公共卫生政策的关键因素[19]。
据我们所知,此前只有一项经济分析评估了NSCLC中生物标志物的预测性筛选,该分析使用了一种微观模拟模型,该模型具有临床结果、疾病进展概率和基于各种来源和假设评估的成本参数[18]。本研究的目的是在前瞻性患者队列中调查在开始NSCLC治疗前常规生物标志物检测的成本效益。的预测。一个mm研究enrolled all consecutive, previously untreated, advanced-stage NSCLC patients eligible for first-line therapy from 19 French regional thoracic oncology centres. We performed a cost-effectiveness analysis in terms of costs borne by the healthcare system by evaluating and comparing: 1) the potential gain in survival, and 2) the costs of testing, treatment and management care using biomarker testing strategies与没有生物标志物检测的护理标准治疗。
材料与方法
道德声明
这项研究得到了国家伦理委员会、法国卫生领域研究信息处理咨询委员会和国家信息与自由委员会的批准,符合法国法律。所有受试者均知情同意加入研究。
研究对象
2013年1月至2014年2月,连续招募了年龄≥18岁、未接受治疗且受晚期NSCLC影响的符合条件的受试者。所有患者都接受了由法国国家癌症研究所认证的28个区域分子遗传学中心之一进行的分子分析。常规分子筛查坚持国家推荐的晚期非鳞NSCLC,包括喀斯特而且表皮生长因子受体突变,碱性重排和两个新出现的生物标志物,例如BRAF(B-Raf原癌基因)和HER2(人类EGFR2)突变[3.]。出现其他肿瘤类型的病人(如。鳞状细胞和混合组织学)可以在当地多学科肿瘤委员会批准后进行筛查。
分子分析
首先,每个参与中心的病理学家完成IHC分析,以指定组织学亚型(腺癌、鳞状细胞癌、大细胞癌,未另行指定),并提供苏木精/伊红染色进行分子分析。策略来识别碱性在PREDICT中重排。Amm队列为:1)碱性首先进行免疫组化,然后对免疫组化阳性病例进行FISH试验验证[20.2)同时进行碱性IHC和FISH检测。在队列中执行的分子分析策略为:1)同时检测所有表皮生长因子受体(第18 - 21外显子),喀斯特(外显子2和13),BRAF(V600)和HER2(外显子20)外显子喀斯特首先,然后表皮生长因子受体,然后根据实验室的经验,使用靶向或非靶向技术确认突变。在后一种方法中,每一个其他的分子改变都被评估,直到发现一个突变,从最常见的(表皮生长因子受体突变),以频率最低的(HER2突变)。
每个分子遗传学中心都采用桑格测序方法或更敏感的、经过验证的等位基因特异性技术进行评估表皮生长因子受体(外显子18-21)和喀斯特(外显子2)突变[21- - - - - -23]。
分子遗传学中心将其结果以特定数据表的方式发送给每个医学调查员。数据由法国胸外科联合组织(IFCT)记录和监测。
策略相比
比较了三种策略,即。一种“无生物标志物检测”的方法,基于临床和病理参数的经验、非指导治疗,以及两种不同的检测策略,其中在并行生物标志物检测之后启动适当的治疗。在其中一个策略中,即。通过“至少一项生物标志物测试”,在一线或二线治疗开始时就知道结果,从而开始最合适的治疗,无论是铂基化疗(顺铂或卡铂+多西他赛、吉西他滨、紫杉醇、培美曲塞或长春瑞滨)、铂双化疗+贝伐单抗、非铂双化疗或TKI。对于该检测策略,患者接受基于其中一种的分子引导治疗表皮生长因子受体而且喀斯特突变或碱性重排的地位。一线和二线治疗一起考虑,以确保所有接受靶向治疗的患者,如基于克唑替尼的碱性分子引导治疗组的易位测试。在另一种策略中,即。“至少”喀斯特检测结果已知”,在一线治疗时,患者接受基于分子引导的治疗喀斯特突变测试,用任何一种表皮生长因子受体或碱性具有野生型肿瘤患者特征的检测结果喀斯特在…的基础上喀斯特外显子2表皮生长因子受体外显子18-21和碱性鱼分析)。我们关注这个特定的测试策略的原因如下:喀斯特变异是最常见的[24],突变是排他性的;因此,执行喀斯特测试可能会节省表皮生长因子受体而且碱性测试,也将允许经济的靶向治疗。“无生物标志物检测”策略包括所有在一线或二线治疗开始时由于以下原因无法获得检测结果的患者:组织不可用、技术故障、结果未恢复和结果不能及时提供治疗决定,尽管后来发现一些结果为阳性碱性,喀斯特或表皮生长因子受体突变。“无生物标记物检测”组接受上述除TKIs外的所有常规治疗。
成本及效益评估
我们根据医疗保健支付者的观点进行了成本效益分析。计算并比较两组之间的增量成本-效果比(ICERs),对应于平均成本(以欧元表示)的差异除以平均效果的差异(即。限制性平均生存时间组间差异)。icer是按照《综合卫生经济评价报告标准》的经济评价准则,以每生命年节省的费用表示的[25]。生存期计算为从开始一线治疗到患者因任何特定原因死亡的时间(以月为单位)。在最后一次随访时,对仍健在的患者进行检查。截止日期是2015年7月31日,正好是入组最后一位患者的17个月后。
经济分析考虑了与检测、治疗和管理护理有关的所有直接医疗保健成本。所有输入数据都是针对参与研究的每位患者单独和前瞻性收集的。数据包括与分子检测、TKIs、培美曲塞和贝伐珠单抗、化疗的获得和管理(包括住院和化疗疗程),以及管理不良事件、疾病进展和NSCLC疾病监测的住院护理相关的费用(表1).
单位成本来自法国国家健康保险系统,住院成本来自诊断相关群体(drg)的估值,基于2015年医院活动和相关支出(住院信息技术机构:www.atih.sante.fr).由于随访时间较短,故未采用折现。
统计和敏感性分析
由于研究设计,采用一对一倾向评分匹配方法,以尽量减少生存和成本分析方面的混杂因素[26]。采用Kruskal-Wallis、Chi-squared、Fisher精确检验或t检验分析入组时的临床特征,以确定可能影响成本和有效性结果的特征。通过年龄、性别、体重指数(BMI)、肿瘤/淋巴结/转移(TNM)分期、表现状态、转移位置、腺癌组织学和吸烟史作为样本匹配的协变量,计算每位患者的倾向评分,以平衡分子引导治疗组和“无生物标志物检测”组。测定平均限制性生存时间通过Kaplan-Meier方法,并使用log-rank检验进行比较。p<0.05为有统计学意义。在我们的观察队列设计中未观察到不朽时间偏倚,因为队列入组时间定义为一线治疗开始时间,两组之间在诊断时间长度和一线治疗步骤上无统计学差异[27]。
为了确定ICER的主要驱动参数,进行了单向确定性灵敏度分析。改变给定参数的估计值,保持其他参数不变,在95%置信区间得出的可能值范围内。龙卷风图被绘制来表示抽样变量ICER的最大变化。以雷达屏幕格式提供了具有10,000次重复的蒙特卡罗微观模拟,其中x-轴表示效果和y-轴表示不同策略的成本差异。此外,还构建了成本-效果可接受度曲线,以表示围绕成本-效果阈值的决策不确定性[28,29]。R (www.r-project.org)及TreeAge Pro 2011 (www.treeage.com)分别进行统计学分析和敏感性分析。
结果
所有研究患者和匹配人群的基线特征
843例未接受治疗的晚期NSCLC患者纳入研究。总体而言,41例患者被排除在分析之外(方案偏差,n=38;死亡,n = 1;病人的报告不可评估,n=2) (图1).最后,共有647名患者被纳入“至少一项生物标志物检测”组,与“无生物标志物检测”组的155名患者进行了比较。在第二项分析中,所有患者都来自“至少”喀斯特测试结果已知“组为谁”喀斯特在一线治疗时未探讨突变状态(n=177)被排除。然后,470名患者被纳入“至少喀斯特干预试验结果已知,并与同样的155例对照组患者进行比较。两组患者在年龄、性别比例、TNM分期等方面差异无统计学意义(补充表E1).干预组表现出明显较高的BMI和较低的性能状态,并且表现出明显较高的从不吸烟状态、脑转移和腺癌组织学的患者比例,以及较低的标准铂双重治疗的使用(补充表E2),与“无生物标志物测试”组相比。
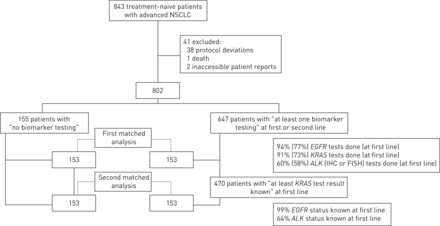
成本-效果分析患者流程图。NSCLC:非小细胞肺癌;包含IHC:免疫组织化学;鱼:荧光原位杂交。
第一次干预方案的成本-效果分析:至少已知一种生物标志物状态
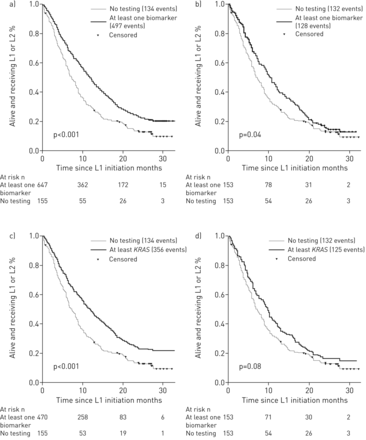
考虑到整个PREDICT。amm队列(n=802),“至少一种生物标志物状态已知”组的平均生存时间为14.9个月(95% CI 13.9-15.7),“无生物标志物检测”组的平均生存时间为10.6个月(95% CI 9.1-12.1)。图2一个).
各组总生存率(Kaplan-Meier法)。L1:一线治疗;L2:二线治疗。a)“至少一项生物标志物测试”与所有患者“无生物标志物检测”(n=802)。b)“至少进行一次生物标志物检测”与匹配人群中“无生物标志物检测”(n=306)。c)“至少喀斯特状态”与所有患者“无生物标志物检测”(n=625)。d)“至少喀斯特状态”与在匹配人群中“无生物标志物检测”(n=153)。
在倾向评分匹配后,“至少一个已知的生物标志物状态”策略在生存方面仍然比对照策略更有效,导致生存率显著更高(图2 b).与“无生物标志物检测”策略相比,“已知至少一种生物标志物状态”策略总共节省了0.20个生命年(12.94 (95% CI 11.1-14.5)。与10.58 (95% CI 9.04-12.12)个月;p < 0.05)。其ICER为每节约生命年13230欧元(表3).
第二次干预方案的成本-效果分析:至少喀斯特一线治疗决定时的状态
总体存活率在“至少”喀斯特初始人群(n=625)和匹配研究人群(每组n=153)中已知“和“无生物标志物检测”组的状态显示在图2 c和d.匹配分析的有效性和成本结果载于表3。总之,“至少”节省了1.93个月的时间喀斯特测试结果已知“策略”。“至少”的ICER喀斯特测试结果已知”策略与“无生物标志物测试”策略相比,每生命年节省7444欧元。
敏感性分析
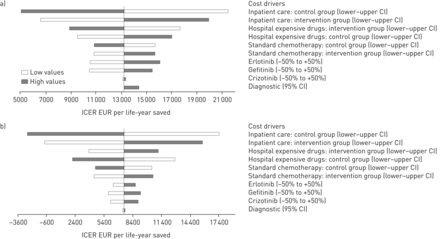
龙卷风分析(图3)表明,在比较“至少一项生物标志物检测”和“无生物标志物检测”匹配组时,住院护理和治疗管理费用是显著影响成本-效果比的因素。我们发现,当住院护理费用在95%置信区间内发生变化时,ICER在每个生命年节省的费用为5000欧元至21 500欧元。将吉非替尼或厄洛替尼的成本增加或减少50%对ICER的影响较小。生物标记物检测的不同价格对ICER的影响很小。在较小程度上,所有其他费用参数也影响ICER。
龙卷风图。CI:置信区间;ICER:增量成本-效果比。a)“至少一项生物标志物测试”与“没有生物标记物测试”。b)“至少喀斯特状态”与“没有生物标记物测试”。
基于蒙特卡罗模拟,41.0%的迭代(成本-效果对)位于东南象限,其中“至少一个已知的生物标志物状态”干预将被认为是具有较低成本和较高效果的主导(图4一).然而,散点图显示了自举估计的广泛变化。同样,成本-效果可接受度曲线表明,干预措施在60%的模拟中具有成本效益,每生命年节省5万欧元(图4 b),显示有关成本效益的决定有一些不确定性。在分析的基础上喀斯特在43%的情况下,测试策略严格主导“无生物标志物测试”策略,在58%的模拟中,成本效益为5万欧元(图4 c和d)。
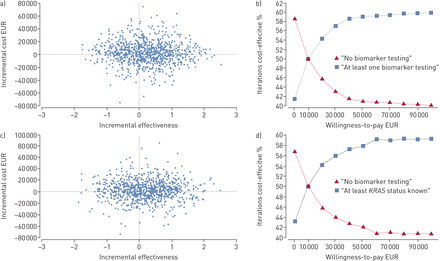
匹配人群中的增量成本-效果散点图和可接受度曲线。a)敏感性分析的增量成本-效果散点图和b)“至少一个生物标志物”的可接受性曲线与“没有生物标记物测试”。c)敏感性分析的增量成本-效果散点图;d)“至少”的可接受度曲线喀斯特状态”与“没有生物标记物测试”。
讨论
靶向治疗在特定基因肿瘤改变的患者中被证明是有效的,现在人们已经认识到需要适当的患者选择。目前的欧洲和美国指南建议晚期NSCLC患者根据临床实践中的临床、组织学和分子结果接受更多的个性化治疗[2,3.]。因此,目前在法国进行的研究结果表明,在一线或二线治疗开始前进行常规分子检测与更好的生存和有限的额外费用相关。更具体地说,我们的研究结果表明,评估三个主要基因组改变的策略(表皮生长因子受体/喀斯特突变和碱性在晚期NSCLC全患者中进行重排),然后进行适当的治疗,无论是靶向TKI治疗还是标准化疗治疗,与“无生物标志物检测”方法以及标准治疗相比,具有成本效益。在标准病例中,每个生命年节省的最大ICER低于14 000欧元,相关检测策略被证明具有成本效益,并且与迄今为止在肺癌患者生物标志物检测领域进行的大多数成本效益研究相比,其ICER更好。这类研究,要么调查单一生物标志物的测试,[14,30.]或多种生物标志物[18,31],每节省生命年或质量调整生命年的ICER从未低于30,000美元(26400欧元)。尽管如此,敏感性分析表明,这一决定存在一些不确定性。
在法国,公共当局在建议实施创新或证明向制造商报销的理由时,没有提到成本效益门槛。世界卫生组织指的是以国内生产总值为基础的门槛,这是一种创新战略,在国内生产总值总值低于人均国内生产总值三倍的发达国家具有成本效益,而在国内生产总值总值低于人均国内生产总值的国家则非常具有成本效益[32]。2015年法国人均GDP为38000欧元,远远高于我们的基本情况和最坏情况icer。
我们的分析还显示,在一个合理的人群数据范围内改变生物标志物检测的成本对ICER没有显著影响,而住院护理和TKI治疗的成本对成本-效果比的影响最大。几乎所有患者最终都出现TKI耐药,尽管已开发出第二代和第三代TKI来抵消患者的一线TKI耐药表皮生长因子受体- - -碱性借非小细胞肺癌。因此,未来的成本-效益模型应该纳入一种新的治疗后监测算法,包括重新活检或循环肿瘤DNA到检测和治疗患者的算法中。
由于分子事件通常是排他的,本研究强调了一种基于“至少一种生物标志物测试”的具有成本效益的“测试和治疗”算法。有趣的是,“测试和治疗”算法基于“至少喀斯特测试”被证明更具成本效益。虽然法国不建议采用分步生物标志物检测方法,但优先考虑喀斯特由PREDICT的一些中心进行测试。一个mm队列。法国生物标记研究表明存在喀斯特法国NSCLC患者的基因突变约为29% [1]。首先喀斯特突变测试似乎是一个相关的策略,以优化相互排斥的关系喀斯特,表皮生长因子受体而且碱性改变。事实上,这种方法通过避免在患者一生中进行不必要的测试,可以节省更多的成本。这一结果在逐步检测方法为参考干预和生物标记物成本主要由患者承担的国家尤其重要。
也就是说,这种相对划算的方法固有的风险是,由于获得第二组分子分析的周转时间过长,在开始一线治疗之前显示未知致癌驱动因素的患者比例会增加(表皮生长因子受体而且碱性) [1,33]。另一个风险是无法识别在~ 1%的患者中观察到的多个分子改变喀斯特67%的人都有突变。在这些突变体中喀斯特案例中,与表皮生长因子受体突变或碱性可能会观察到重排,这可能受益于靶向治疗,尽管在这种情况下效果较差[34]。
因此,生物标记物检测替代方案的最新成本-效果分析产生了有关未来检测方法相对兴趣的有用信息。例如,ROS1(ROS原癌基因1)/克唑替尼和BRAFV600/达拉非尼+曲美替尼成为有前景的生物标志物/治疗组合[35,36],强调了靶向多基因面板在诊断中的潜在作用,并增加了需要搜索的潜在分子事件的数量。最后,针对固定福尔马林、石蜡包埋和小尺寸样品优化的NGS策略的开发可能有助于在常规设置中验证多基因检测策略[37,38]。这种复杂的基因组研究的进化,可以对数百个基因进行多个并发分析,可能会产生不可忽视的经济影响,即。NGS有可能降低成本与循环DNA监测成本的增加。最近的研究评估了基因组测序检测的成本效益,主要使用决策模型方法[39- - - - - -41]。尽管这些研究的患者群体不同,但总体结果表明,与“无生物标志物检测”或“单一生物标志物检测”相比,NGS产生了较高的成本-效果比,每节省的质量调整生命年超过10万美元(8.8万欧元)。这相当于法国人均GDP的三倍多的ICER。我们的研究以及大多数关于NSCLC患者诊断和治疗的成本效益研究表明,治疗成本对检测和治疗策略的全球成本有重大影响。通过确定更多的靶向靶点,NGS可以增加靶向治疗的使用,从而导致更高的治疗成本。因此,很难估计NGS技术未来的成本影响,这将取决于靶向疗法的可用性以及单个NGS成本和治疗价格的降低。虽然NGS似乎非常适合于晚期癌症中越来越多的生物标志物的分子特征,但在未来几年,临床医生很可能会使用分步和NGS策略的结合。
我们的研究显示出的一个局限性是非随机设计。然而,我们提出了一种队列设计,其中“无生物标志物检测”组嵌套在前瞻性队列中,以进行医学-经济分析。事实上,所有新诊断的晚期NSCLC患者在研究期间首次接受了抗癌治疗,并在参与PREDICT的临床部门进行了随访。Amm项目被通知给研究协调员,因此被纳入研究队列。从方法论的角度来看,这一点是至关重要的,因为它避免了与“之前”相关的偏见。与“之后”的方法或与历史队列。此外,我们的设计在医疗实践中没有引起任何变化。最后,使用倾向评分匹配减少了缺乏随机化的潜在持续偏差。另一个限制是随访时间短。一般来说,为了弥补有限研究时间的限制,疾病进展的概率和费用是根据文献数据和推导的假设在患者一生中推断的。也就是说,这种模型方法可能会产生潜在的偏倚来源(源于假设),最终结果可能与观察到的临床实践不同(不是基于前瞻性的、观察性的人群数据)。事实上,几项研究已经证明,2年的随访期足够长,足以捕捉转移性癌症带来的主要健康和经济后果[18,42]。值得注意的是,我们研究中80%的患者在2年随访期结束前死亡。
补充材料
确认
作者对所有参与研究的研究者表示感谢。我们感谢Cécile Fortanier (APHM,马赛,法国)对研究设计和拨款提案的贡献,以及Quân Tran、Antoine Deroy和Sandy Dos Santos(均为IFCT,法国巴黎)对数据收集、监测和计算的参与。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:D. Moro-Sibilot在提交的工作之外,从礼来、罗氏、辉瑞、阿里亚德、勃林格、阿斯利康、诺华、MSD和BMS收取了个人费用。在提交的工作之外,S. Friard还获得了罗氏、阿斯利康、BMS、勃林格、礼来、诺华和辉瑞的非经济支持。M. Wislez获得了BMS基金会的资助,罗氏公司的非经济支持,礼来和勃林格殷格翰公司的个人费用和非经济支持,以及阿斯利康、MSD和BMS在提交工作之外的个人费用。V. Westeel在提交的工作之外,从礼来公司收取了个人费用(发言人局、顾问角色、会议费用、研究经费),从罗氏公司收取了个人费用(发言人局、顾问角色、会议费用、研究经费),从阿斯利康公司收取了个人费用(发言人局、顾问角色),从勃林格殷格翰公司收取了个人费用(发言人局、会议费用、研究经费)。H. Léna获得了来自罗氏的资助和非经济支持,阿斯利康、默克、皮埃尔法布肿瘤学、百时美施贵宝和勃林格殷格翰的个人费用,以及辉瑞和礼来在提交工作之外的个人费用和非经济支持。G. Zalcman曾获得资助、个人费用,并担任罗氏(Roche)和辉瑞(Pfizer)的临床试验研究员,并在研究进行期间担任阿斯利康(AstraZeneca)、勃林格(Boehringer)和GSK的临床试验研究员;并在提交的工作之外,在BMS和罗氏的临床试验中获得了资助并担任研究员。M. Antoine在提交的工作之外,还从罗氏和默沙东收取了个人费用(参与董事会)。F. Barlesi在提交的工作之外收到了来自阿斯利康、百时美施贵宝、勃林格殷格翰、克洛维斯肿瘤学、礼来肿瘤学、F. Hoffmann-La Roche有限公司、诺华、默克、MSD、皮埃尔法布尔和辉瑞的个人费用。J. Cadranel在提交的工作之外,还获得了辉瑞公司的资助(用于ALK免疫反应研究)和个人费用(用于参加临床试验委员会),诺华公司和阿斯利康公司的资助(用于研究NGS)和个人费用(用于参加临床试验委员会),以及罗氏公司、勃林格殷格翰公司、BMS和礼来公司的个人费用(用于参加临床试验委员会)。
支持声明:这项工作得到了法国国家倩碧医院研究项目(PRME 2009)——法国卫生部、法国国家癌症研究所(INCa)、法国抗癌联盟、罗氏、葛兰素史克、勃林格殷格翰和礼来-阿斯利康的机构资助。这些资金来源在本研究的设计中没有任何作用,在其执行、分析、数据解释或提交结果的决定中也不会有任何作用。赞助机构代表为法国巴黎的公共援助组织Hôpitaux;它的作用是控制道德和法律考虑的适当性。本文的资助信息已存入交叉参考基金注册。
- 收到了2017年7月19日。
- 接受2018年1月31日。
- 版权所有©ERS 2018