文摘
热休克蛋白在特发性肺纤维化的潜在生物标志物和治疗目标http://ow.ly/fHVP30hJUOl
热休克蛋白(休克),也被称为应激蛋白,构成一个复杂的蛋白质网络高度交谈跨物种被分为不同的家庭根据其分子量:HSP110,一半,HSP70、HSP60, HSP40和小热休克(1]。尽管他们主要是伴侣和cytoprotective性能著称,休克蛋白还参与许多细胞信号过程的监管2]。这些蛋白参与了各种生理和病理条件下,包括呼吸系统疾病如哮喘、慢性阻塞性肺病、结节病或肺动脉高压发病机制。休克蛋白在肿瘤领域都进行了广泛的研究由于其监管几个蛋白质参与致癌作用。应激蛋白质通常是在癌症细胞,促进癌症表型特征如细胞重新编程,维持增殖信号,支持复制的不朽,逃避生长抑制或抵抗细胞死亡。因此,一些研究集中在潜在使用HSP抑制剂与化疗的癌症患者(3,4]。特别是,一半已成为癌症的一个重要目标,除了17 -N-allylamino-17-demethoxygeldanamycin (17-AAG),第一个抑制剂针对一半寿命测试1999年在临床试验中,几个抑制剂针对一半人类已经开发和正在测试(5]。
特发性肺纤维化(IPF)和癌症有许多功能,如细胞重新编程和抵抗细胞死亡(6,7]。几项研究从我们组和其他描述HSP超表达在实验和人类肺纤维化(8- - - - - -17]。越来越多的证据表明,热休克可能代表有趣的在肺纤维化的治疗目标,主要通过转化生长因子(TGF) -β信号调节18]。在肺纤维化的背景下,小HSP的潜在抑制肺纤维化的研究在不同的动物模型。小的老鼠缺乏HSPαB-crystallin保护从实验性肝纤维化引起的几个代理14,15]。以同样的方式,当地注入ogx - 427,一个针对HSP27表达反义寡核苷酸,干扰TGF-β-induced胸膜下纤维化在啮齿动物模型(16]。尽管一些研究表明热休克的作用在纤维发生机制在体外的影响,调查HSP实验性肺纤维化的抑制作用仍然不佳。
在这个问题的欧洲呼吸杂志Bellaye等。(19)很好地揭示了一个复杂的细胞外HSP90α调节myofibroblast激活机制,强调在肺纤维化的关键作用,尤其是在IPF。此外,他们表明,抑制细胞外一半,这是提高IPF患者的血清与控制相比,妨碍myofibroblast profibrotic活动和TGF-β1诱导肺纤维化在啮齿动物,从而确定了潜在的新治疗IPF的目标。
IPF是一个逐步从未知起源和致命的慢性肺部疾病20.]。两种药物在肺移植,pirfenidone [21]和nintedanib [22慢下来,但不能阻碍疾病进展,已获批准IPF管理经过几十年的临床试验(23]。IPF患者的治疗选择是非常有限,因此,需要开发新的治疗方法。IPF patho-biology是复杂的和最近的模型提出,反复刺激上皮损伤导致异常上皮,相声受损后,促进成纤维细胞增殖和活化导致myofibroblast积累和随后的胶原蛋白生产过剩(20.]。TGF-β纤维化的过程中是一个关键的细胞因子,参与了成纤维细胞的分化和激活导致胶原蛋白的积累和其他细胞外基质组件生产。
Bellaye等。(19)提出一个新颖的机制影响myofibroblast分化和表明,一半在肺纤维化可能是一个有趣的目标。与HSP70,一半是主要的伴护蛋白质折叠系统。两种亚型的描述了一半:HSP90αHSP90β,和在细胞内,一半伴侣蛋白二聚体。尽管每个同种型的角色仍然知之甚少,最近的两项研究凸显了全球一半的有益作用中使用geldanamycin-derived化合物抑制肺纤维化。此前在今年欧洲呼吸杂志17-dimethylaminoethylamino-17-demethoxygeldanamycin的治疗潜力(17-DMAG 17-AAG模拟)测试在肺纤维化小鼠模型13]。这种方法干扰bleomycin-induced肺纤维化。机械化,HSP90β稳定TGF-βII受体,从而有助于增强TGF-βprofibrotic活动。这些发现后来被证实使用17-AAG TGF-αoverexpressing转基因小鼠模型(17]。在这项研究中,作者展示了使用核方法HSP90β(但不是HSP90α)被要求驱动迁徙特性和成纤维细胞的增殖。Bellaye等。(19)已经证实HSP90β的重要性myofibroblast LRP1恰巧表面受体的激活通过稳定。进一步说,这项研究很好地证明了一个关键的角色,其他一半对碘氧基苯甲醚HSP90αmyofibroblast生物学和提供证据表明HSP90αmyofibroblasts(但不是HSP90β)分泌的机械应力体外。作者观察到细胞外HSP90α激活myofibroblast分化LRP1-dependent的方式。
重要的是,从B的工作ellaye等。(19还表明,循环水平的HSP90αIPF患者比对照组增加。此外,严重的IPF患者有显著更高层次的循环HSP90α相比与温和的IPF血清HSP90α水平之间的负相关,在这些患者肺功能。,示范,HSP90α水平增加血液和支气管肺泡灌洗液的IPF患者,这种细胞外一半在IPF发展一个重要的角色,打开的可能性同时使用作为生物标志物可用于诊断和治疗的目标。然而,需要进一步的研究表明细胞外的潜在使用HSP90α作为IPF进展的生物标志物。Theranostic医学已经提出了在不同的病理情况下其他热休克。这样,循环血浆HSP70水平转移的标志和抑制细胞外物质本身,通过阻断其功能激活myeloid-derived抑制细胞,诱发的发展一种有效的抗癌免疫反应(24,25]。同样,循环HSP27在骨髓纤维化发展及其抑制血清水平提高块骨髓纤维化(26]。
许多不同抑制剂的一半是可用的和一些先进的癌症临床试验(5]。大多数这些分子geldanamycin衍生品(如17-AAG或17-DMAG)块两种亚型的一半。考虑到一半有一个广泛的活动影响一些信号和生理过程,一半的警告将抑制最有可能出现不必要的副作用。此外,组织学染色清楚地表明,一半寿命表达式不仅是局部成纤维细胞增生的上皮细胞也在IPF肺。这些问题的答案可能来自研究从Bellaye等。(19]。与其他研究表明一半的潜在效应抑制使用geldanamycin衍生品,Bellaye等。(19)使用一半的non-permeable抑制剂HS30 HSP90α目标细胞外的形式。他们表明,特定的抑制细胞外HSP90αantifibrotic效果的体外展示肺片TGF-β1-induced肺纤维化模型。尽管一半细胞外活动并不完全理解目前采取的方法Bellaye等。(19可能有几个优势与一半抑制剂的长期治疗,这将是最可能出现的情况在IPF等慢性病。此外,这些研究结果最近被证实在小鼠1 g6-d7 HSP90α引起的细胞的抗体,这阻碍了bleomycin-induced肺纤维化(27]。然而,作者注入1 g6-d7开始第二天post-bleomycin因此肺纤维化发生之前。因此,细胞外HSP90α抑制的潜在的治疗作用还有待充分证明在活的有机体内。
尽管关键需要更完整的研究在动物模型来证实最近的发现,我们目睹的出现越来越多的证据表明热休克,特别是一半,作为未来潜在的有趣的目标治疗肺纤维化(图1)。如B所示ellaye等。(19),HSP90α可以衡量在血液和支气管肺泡灌洗液的病人和与临床参数。这个开创性的研究扩大景观的热休克肺纤维化和打开的方式作为生物标志物,这将是有用的选择病人的人口可能会受益于此靶向治疗在现代个性化医学的时代。
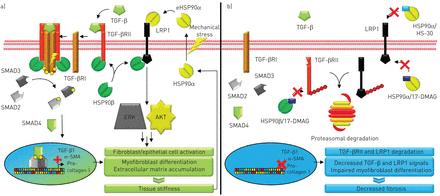
热休克蛋白(HSP) 90抑制阻碍profibrotic信号在不同的水平。一)HSP90β企稳II型TGF-β受体(TGF-βRII)促进转化生长因子(TGF) -βprofibrotic信号。一半也干扰LRP1恰巧蛋白酶体降解。组织刚度HSP90α诱导分泌的细胞外环境。细胞外HSP90α进一步信号通过LRP1恰巧加强myofibroblast分化和profibrotic属性。b)一半抑制geldanamycin衍生品(如17-DMAG)干扰TGF-βRII而LRP1恰巧稳定细胞内一半,引发他们的蛋白酶体降解和减少TGF-β和LRP1恰巧纤维化信号。此外,特定的抑制细胞外HSP90α一半寿命使用non-permeable抑制剂HS-30块与LRP1恰巧HSP90α交互。
脚注
利益冲突:p . Bonniaud已收到个人费用按照顾问委员会从罗氏,勃林格,诺华公司和阿斯利康TEVA)和国会报销旅行的人从基耶西,在提交工作。
- 收到了2017年12月15日。
- 接受2017年12月21日。
- 版权©2018人队