摘要
IL1R修改疾病严重性CF患者,强调IL-1信号传导的用于CF的发病机制的重要性http://ow.ly/pIN730gL10G
给编辑:
最近在囊性纤维化(CF)样肺疾病小鼠的研究发现,白细胞介素(IL)-1受体(IL- 1r)信号作为触发中性粒细胞性气道炎症的重要途径,这是CF患者肺部疾病发病和进展的关键危险因素[1- - - - - -4].这些研究表明,cf样气道黏液阻塞导致上皮细胞缺氧和坏死,进而导致死亡细胞释放IL-1α,激活IL-1R信号,触发中性粒细胞炎症和结构性肺损伤在活的有机体内[1,5].此外,在CF患者的肺切片中,在黏膜阻塞的气道中检测到坏死的上皮细胞[1].缺氧细胞死亡是许多其他器官中无菌中性粒细胞炎症的一个确定的触发器,以前的研究已经确定IL-1R信号是触发这种对死亡细胞的炎症反应的关键途径[6].此外,由细菌感染引起的编码IL-1R配体IL-1β的基因已被确定为独立的北美和欧洲CF改良剂的研究CF的遗传修饰[7,8].总的来说,这些研究表明,IL-1R信号可能在是在CF患者气道不约而同地检测到的中性粒细胞炎症的发病机制中起重要作用,在细菌感染的缺乏和存在[2,3.].然而,IL-1R在CF患者中的作用及其与疾病严重程度的关系尚不清楚。
因此,这项研究的目的是评估潜在的作用IL1R基因,编码IL-1R信号通路的中心分子,作为CF患者疾病严重程度的调节剂。为了实现这一目标,我们对位于内含子1内的信息丰富的微卫星标记IL1RSat进行了基因分型IL1R在几个独立的CF患者队列和来自PopGen生物样本库的一个人口对照(图1)。我们扩增的(AAT)n重复基序IL1RSat特征在于高多态性信息含量,这是一个标记,以在链接站点捕获功能遗传变异(一个先决条件图1一个)。我们认为IL1RSat是一个中性的遗传标记,并用它作为在其附近是共同继承与IL1RSat因为连锁不平衡再加上其他变种的替代指标。我们基因型在IL1RSat三个独立的CF患者群:谁是负担1957和1990年(出生1979年平均年)之间,并招募了1996年,其中只对两兄妹够老来执行欧洲双人和兄弟研究(EUCFTSib)的CF患者肺功能测量被接受[8],和谁是1970年以前出生并存活至少要等到1990年。EUCFTSib人口包含总共使用318对被选择的39患者对慕尼黑(<1970M)和汉诺威(<1970H)从CF中心患者以下策略:人体测量学和肺功能数据是根据其疾病的严重程度来排序的所有个体[8].这些被选择的配对代表了轻度和重度CF疾病,其中个体的表型由生长和肺功能的临床参数描述,所有来自EUCFTSib排名的被选择患者的两项参数均低于25厘位(严重)或高于75厘位(轻微)[8].如果是F508del纯合子的基因,则对cf修饰基因进行分析,以最大限度地减少F508del的影响CFTR.基因型对表型变异性的影响,强调非cftr基因的影响;2)如果对的表型极其一致(一致轻微影响,13对;和谐的,严重影响的12对)或不和谐的(14对)[8].因为在研究极端表现型时,可以预期遗传因素对表现型表现有更高的影响[11.,12.,这一策略导致了EUCFTSib中cf修饰基因的功能变异的富集。来自其他两个CF队列的患者为F508del-CFTR纯合子,但没有选择任何疾病表现来覆盖幸存者的整个疾病严重程度谱。对于不相关的患者,CF出生队列的流行病学数据提供了关于死亡率如何影响可以纳入我们研究的患者比例的估计。一项对1977年至1985年期间英国CF患者存活率的分析报告称,19岁患者存活率为50% [13.].这些英国幸存者的出生年份范围与我们的两个德国无血缘关系患者队列相似,表明如果我们在1977-1985年招募这些幸存者,我们将只纳入CF人群的约50%,而在1990年或更晚的时候纳入的更少。目前还没有相应的流行病学数据来描述CF兄弟姐妹对的生存情况,但从具有显著死亡率的出生队列中同时招募两个生命兄弟姐妹的机会[13.,14.,甚至比从同一出生队列中招募不相关患者的概率更低(因此幸存者效应更高)。因此,我们期望纳入标准“两个幸存的兄弟姐妹”有助于进一步富集EUCFTSib人群中的良性等位基因。
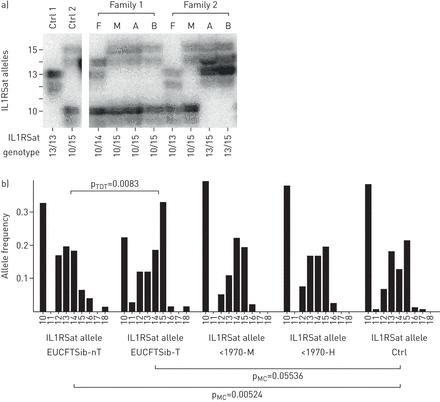
在囊性纤维化患者中,白细胞介素1受体(IL1R)基因内含子1内的一个信息丰富的微卫星标记与生存有关。从8个位于IL1R内含子1内的微卫星基序中选择了这个微卫星IL1Rsat进行基因分型,这些微卫星基序在5个不相关的对照样本上进行了检测。IL1RSat位于IL1R的内含子1内,起始位点为2号染色体参考序列GRCh37的核苷酸102725407。p13,引物(5 ' - tcacttgactcccagctca -3 '和5 ' -gcggtacctaaaaccaggtc-3 ')围绕一个(AAT)n重复基序。我们观察到三个核苷酸大小不同的信号,描述了总共9个IL1RSat等位基因,表明AAT重复基序的数量在群体中个体之间是不同的,这至少部分地反映了IL1R基因的遗传背景。a) IL1RSat基因分型初步资料。所有的分析都使用了两个对照样本来根据大小确定等位基因。欧洲CF双胞胎和兄弟姐妹(EUCFTSib)研究中的两个家庭将IL1RSat基因型分配给观察到的信号。例如,在家族2中,从父母遗传给后代的等位基因有13个(父系)和15个(母系),而非遗传的等位基因有10个(父系)和10个(母系)。b) IL1RSat等位基因在囊性纤维化(CF)家族和患者中的分布。通过对来自EUCFTSib的f508hel - cftr纯合子患者(39个家庭,78例患者)的IL1R内含子1中的信息性微卫星标记IL1RSat的基因分型,研究了il - 1受体(IL1R)基因作为CF的遗传修饰因子。 18 unrelated patients) and from the CF centre in Hannover (<1970-H, 39 unrelated patients). Patients of these independent cohorts had survived at least until school age (affected patient pairs of EUCFTSib; mean age at day of recruitment 17 years, range 6–39 years) or adulthood (unrelated patients born prior to 1970 who have survived until recruitment for DNA analysis in 1990 or later; <1970-M and <1970-H; mean age in 1990, 24 years, range 21–32 years) and a population control from Schleswig-Holstein in Germany (Ctrl, 94 individuals). Distributions of IL1RSat allele frequencies are shown for transmitted (EUCFTSib-T) and non-transmitted (EUCFTSib-nT) alleles in families of the European CF Twin and Sibling Study and for independent patient cohorts followed at the CF centres in Munich (<1970-M) and Hannover (<1970-H). Genetic data of CF patients and their parents in the EUCFTSib were analysed with the software package FAMHAP, which corrects for sibpair dependency in association and linkage studies (p负2)[9]。使用蒙特卡罗模拟与丛(对直接比较无关患者和对照的队列之间等位基因分布马克)[10]。
我们首先使用传输不平衡测试(TDT),最初由Spielman等.[15.,比较传递给CF患者的遗传基因信息(传递等位基因)中IL1RSat等位基因频率的分布。与保留在EUCFTSib CF家族亲代(非遗传等位基因)中的信息。我们发现,在招募的CF兄弟姐妹中,IL1RSat等位基因15的传播不平衡比例过高(p负2=0.0083),将IL1RSat等位基因15标记为良性变异,与CF患者的生存相关,直到纳入研究(平均年龄17岁,范围6-39岁)。对照群体的等位基因分布与遗传等位基因上的IL1R1Sat等位基因分布(即.幸存的CF患者)(P马克=0.055),以及非遗传等位基因(p马克=0.00524)来自EUCFTSib (图1)。在被1970年之前出生并存活至少1990直到CF患者的独立队列中,除了无处不等位基因10占三分之一在所有群体中的染色体,IL1RSat等位基因14(<1970M)和15(<1970H)是最常观察到的等位基因(图1),尽管在IL1RSat等位基因15富集的类似模式的趋势没有达到统计学意义(p最好的事物=0.08)。
在TDT建立在核心家庭内发送和非发送的等位基因的比较与内部控制使得能够引起疾病的基因的鉴定[关联研究15.].单基因疾病CF是由CFTR.基因,我们之前表明,TDT也可以用于检测附加基因修饰物的影响,这些基因修饰物在纳入横断面研究之前对患者生存有影响[8].在CF患者人群中,由于横断面招募策略导致等位基因频率的扭曲,因此,在过去几十年里,疾病管理和患者生存的改善可能会实现,已经通过富集轻度胰腺充分相关CFTR突变被注意到,这些突变占1966年或更早出生的患者CFTR等位基因的18%,这些患者在1990年或更晚被招募进行CFTR突变分析[16.].此外,还通过富集检测到了幸存者效应TGFB1- leu10在F508delCFTR.纯合子CF患者群体(p=0.066) [16.]和由之间EUCFTSib TDT在TNFα受体基因D12S889TNFR1(p值= 0.0067),在基因编码阿米洛利敏感钠通道的γ亚基SCNN1G(p=0.0034),默认情况下,在CFTR.轨迹(p = 10−6)作为CF致病基因本身[的指示8].
综上所述,我们已经评估了内含子1是否具有高度多态性的微卫星IL1R基因显示,在参与研究的CF患者中,一种特定的等位基因富集。我们发现内含子1内的信息微卫星标记IL1R发现CF患者的生存优势,通过患者队列中的传播失衡揭示(图1),存在存活者依赖的招募偏倚[13.,14.,支持IL-1R参与CF发病。这一概念与IL-1R信号通路在中性粒细胞炎症发病机制中的重要作用相一致,也与之前的研究发现相一致IL1B在CF中编码IL-1R配体IL-1β作为修饰基因[7,8].早些时候,我evy等.[7]描述了一个与肺部疾病相关的信号IL1R其中女性F508del-CFTR纯合子患者来自北卡罗莱纳州和凯斯西储大学(UNC /凯斯西储大学)队列。总之,这些研究引起人们对IL-1R信号通路中的作用,无论是在粘液阻塞气道或由细菌感染引起的IL-1β从缺氧细胞释放IL-1α激活[1,5,6,17.],在慢性中性粒细胞炎症导致CF患者进行性肺损伤的发病机制中[1- - - - - -4].从遗传和功能研究这些结果还表明,IL-1R信号传导的抑制可以是CF有希望的抗炎策略和与慢性气道粘液阻塞和中性粒细胞炎症相关联的潜在的其他肺部疾病。
披露的信息
确认
我们感谢“PopGen生物库”(https://www.epidemiologie.uni-kiel.de/biobanking/biobank-popgen)提供对照人群的DNA样本。
作者贡献:本研究的概念与设计:F. Stanke, B. Tümmler, M.A. Mall;数据的获取、分析和解释:F. Stanke, A. Hector, S. Hedtfeld, D. Hartl, M. Griese, B. Tümmler, M.A. Mall;为重要的知识内容起草或批判性地修改文章:F. Stanke, M.A. Mall
脚注
支持声明:本研究由德国联邦教育和研究部资助(82DZL00401, 82DZL004A1, 82DZL00201和82DZL002A1)。本文的资金信息已存入Crossref资助者注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 已收到2017年2月27日。
- 接受2017年10月7日。
- 版权所有©ERS 2017年