抽象的
宿主响应生物标志物可以准确区分流感和细菌感染。然而,公布的生物标志物需要测量许多基因,从而难以在临床实践中实现它们。该研究旨在鉴定单基因生物标志物,其具有相当于多基因生物标志物的高诊断精度。
在这项研究中,我们组合了1071个个体的综合基因组分析体外使用良好的感染模型进行实验。
我们鉴定了单一基因生物标志物,IFI27.,其具有相当于通过多基因生物标志物获得的高预测准确度(91%)。体外研究表明IFI27.TLR7在浆细胞样树突状细胞中上调,这些细胞是对流感病毒而不是细菌作出反应的抗原提呈细胞。体内研究证实了这一点IFI27.在流感患者中表达但不在细菌感染中,如多重患者队列中所示(n = 521)。在患有未分化呼吸疾病的患者的大型前瞻性研究(n = 439)中(疾病包括病毒,细菌和非传染病),IFI27.在歧视流感和细菌感染之间显示88%的诊断准确度(AUC)和90%的特异性。
IFI27.代表了在临床应用基因组分析中克服翻译障碍的重要一步;其实施可提高呼吸道感染的诊断和管理水平。
抽象的
IFI27.可以区分疑似呼吸道感染病例的流感和细菌感染http:///wly/veay30bmls3.
介绍
急性呼吸道感染是世界上传染病发病和死亡的最常见原因(世卫组织- 2014年)。病毒和细菌是呼吸道感染的主要原因。在所有病毒中,流感病毒造成的发病率和死亡率最高。准确区分流感病毒和细菌是处理呼吸道感染的第一个关键步骤,因为初始治疗(抗病毒药物)相对抗生素主要由疾病引导。然而,在临床地上的流感和细菌感染之间的区分往往难以困难,因为感染均有相似的临床特征(例如咳嗽,呼吸困难和发烧)。
病原体测试(例如病毒PCR检测)是明确诊断的重要一步。虽然病毒检测很重要,但仅凭病毒检测不足以指导患者管理。像大多数呼吸道病毒一样,流感病毒产生广泛的临床谱。在一些病人中,病毒充当旁观者,它的存在与目前的疾病无关[1].在其他人中,病毒直接负责患者的症状。临床决策需要考虑病毒是否是旁观者或提出症状的原因,因为抗病毒治疗(例如Oseltamivir)应该仅用于症状严重且直接引起病毒的个体施用[2- - - - - -4].目前,不存在实验室测试,可以区分病毒检测和“活性感染”。
宿主响应生物标志物代表替代方法来规避这个问题。宿主基因表达生物标志物可以准确识别不纯化流感感染的免疫应答,从而帮助临床医生区分流感和细菌感染[5- - - - - -8].这些生物标志物代表了一种很有前途的策略,以补充当前的诊断方法。然而,已发表的生物标志物面板包含大量的基因,使其难以应用于临床实践。为了克服这一翻译障碍,我们对1071个个体进行了整合基因组分析,以寻找一种具有与多基因生物标志物相同的诊断准确性的单基因生物标志物,以区分流感和细菌感染。
材料和方法
参与者
参与者在发现队列和前瞻性验证队列中被招募。发现队列包括三个病例对照研究。每项研究包括表型明确的患者(流感感染、细菌感染和非传染性疾病)和健康对照组。在第二阶段的验证中,我们对急诊科出现“流感样”疾病的患者进行了一项大型、多中心的研究(“前瞻性验证研究”)。研究方案由各参与机构的机构审查委员会批准,所有研究参与者均知情同意。所有研究参与者的人口学和临床特征总结在表格1.辅助材料中提出了有关所有群组(纳入标准,招聘流程,样品收集和随访)的详细信息。
统计分析
为了评价该生物标志物的诊断性能,使用已建立的方法计算受者工作特征曲线的敏感性、特异性、诊断阈值和曲线下面积(AUC)(详细信息见补充资料)。两组之间的比较采用非配对双尾进行计算t- 在适当的情况下,最低或非参数曼 - 惠特尼U-Test。在适当的情况下,使用单向ANOVA或Kruskal-Wallis测试计算多个组之间的比较。使用NCSS(LLC,Kaysville,UT,USA)和棱镜(GraphPad Software,La Jolla,CA,USA)软件包进行统计分析。
结果
发现队列
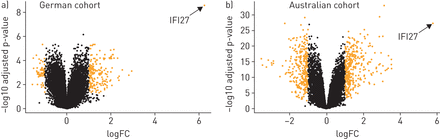
为了筛选流感生物标志物,我们分析了三个发现队列的流感患者的全血(表格1和补充表S1)。流感患者指的是病毒核酸检测结果呈阳性,并伴有与流感相适应的重症,需要住院或重症监护的患者。我们首先进行了微阵列分析,以确定(在流感患者和健康对照者之间)差异表达基因(图1).该分析显示,在差异表达基因中,干扰素α诱导蛋白27(IFI27.)显着比所有其他基因更好(图2).这一发现在两个独立的发现队列(图2)和不同的微阵列平台(补充图S1)。我们随后在所有三个队列中进行了PCR验证,证实了这一点IFI27.在流感阳性患者中上调(补充表S1)。总的来说,所有发现队列的发现彼此一致,并共同表明IFI27.是流感感染的潜在生物标志物。
IFI27.作为流感感染的生物标志物,比其他基因表现更好。微阵列数据以火山图的形式呈现,按照生物学意义(横轴)和统计学意义(纵轴)的维度排列基因。横轴表示两组(流感)之间的log2刻度的基因表达水平(折叠变化)相对健康控制)。垂直轴在组之间的负日志2比例上表示调整后的p值。具有较高表达水平(> 2倍变化)和调节的P值(<0.05)的基因以黄色突出。
主机响应
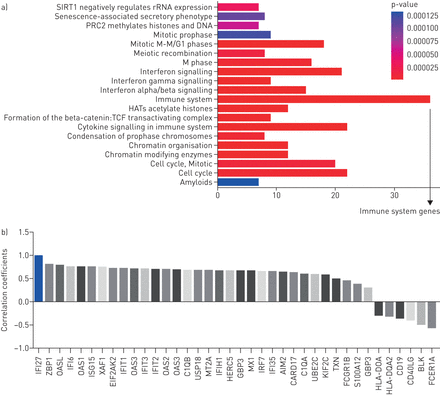
确认IFI27.反映了患者的“活性感染”,我们检查了IFI27.与免疫应答基因的相关性。该分析表明IFI27.与许多抗病毒免疫反应基因共同表达。它还表明了IFI27.温度相关(相关系数> 0.6),在免疫系统途径中,69%的差异表达基因(35/35),干扰素信号通路中的90%的差异表达基因(19例为21)(图3.).其中很多IFI27.- 胶合基因具有抗病毒功能,例如MX1.(抗流感),ISG15(抑制流感病毒复制),OAS1,OAS2.和OAS3.(降解病毒RNA),EIF2AK2(抑制病毒复制),HERC5.(抗病毒反应的阳性调节剂)和IFIT2.(抑制病毒mRNA的表达)。这些调查结果证实了IFI27.是对呼吸病毒的宿主反应的一部分。
a)免疫系统途径是最常见的途径。利用流感阳性患者的差异表达基因进行通路富集分析。y轴表示通路项,x轴表示各通路类别中差异表达基因的数量。观察到的表达式分布偶然发生的概率的p值用不同颜色的棒子表示。b)IFI27.与免疫系统途径相关。在免疫系统途径中的IFI27和单个基因之间进行相关分析。这里呈现代表性基因以及它们的相关系数表示y设在。仅显示了具有统计学意义的基因(Pearson相关分析p<0.05)。IFI27.这里提供作为参考基因(相关系数= 1)。
外部验证
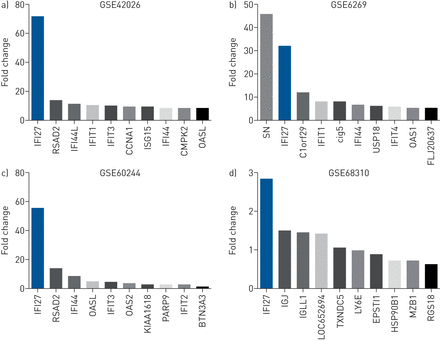
在第1阶段验证中,我们在鼠标和人类数据集中验证了我们的研究结果。鼠标数据建议IFI27.在不同严重程度的流感感染中上调(补充图S2)。在人类数据集中,我们分析了4个独立的外部队列(GSE6269, GSE42026, GSE68310和GSE60244)的微阵列数据集(表格1).两位队列由儿科患者组成:GSE6269(n = 131)和GSE42026(n = 92)[9,10.].另外两个队列由成年患者组成:GSE60244(n = 158)和GSE68310(n = 133)[11.,12.].我们发现了IFI27.是所有四个队列中流感感染的签名基因。在三个队列中(GSE42026,GSE60244和GSE68310),IFI27.是受感染患者中最高度上调的基因(图4.).在一个队列中(GSE6269),IFI27.是受感染患者的第二个最高度上调的基因。这些发现与那些发现的那些结果一致,确认这一点IFI27.是流感感染的重要签名基因。
体外模型
确认是否是IFI27.基因表达由流感病毒直接激活,我们共同培养从健康志愿者与活流感病毒获得的外周血样品。这些实验揭示了一种剂量 - 反应关系IFI27.基因表达响应病毒载荷(图5A),确认这一点IFI27.被流感病毒激活。使用不同流感病毒株(H3N2和H1N1)和流感B病毒菌株的附加实验显示出类似的发现(数据未示出)。
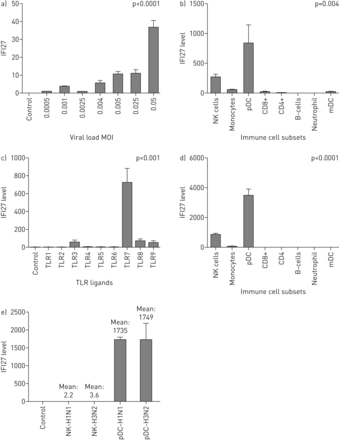
体外学习。实验在外周血样品中进行,并从健康的志愿者获得纯化的免疫细胞。使用来自至少三种不同受试者的独立样品进行所有实验。IFI27.通过定量实时PCR在所有实验中测量基因表达。IFI27.水平(在y轴上)表达为fold change(相对于甘油醛3-磷酸(GAPDH))。列高表示平均折叠变化±SD..除非另有说明,否则使用Kruskal-Wallis测试计算p值以进行多个组比较。一种)IFI27.对流感病毒的反应。X轴表示病毒载荷(H1N1)的范围,其通过多种感染(MOI)=病毒与细胞总数的比率表示。使用线性回归模型计算p值IFI27.表达式作为依赖变量和病毒载荷作为预测变量。b)IFI27.免疫细胞亚群的基因表达。流感病毒抗原血凝素(0.135µg·mL−1)用不同的免疫细胞亚组共培养。c)含量的受体(TLR)激活IFI27..外周血样品用TLR1-9配体共培养。d)免疫细胞亚集中的TLR7活化。加里尼德(TLR7配体)(1μg·ml−1)用于刺激免疫细胞的不同子集。e)IFI27.在天然杀伤(NK)细胞和血浆骨质特性细胞(PDC)中。流感病毒(H1N1和H3N2)与NK细胞和PDC共培养。IFI27.在NK细胞中,基因表达可忽略不计,但它在PDC中高度上调。MDC:骨髓树突细胞。
IFI27.由识别流感病毒的血浆骨质树突细胞产生
鉴定表达的免疫细胞IFI27.在外周血中,我们研究了IFI27.在八个免疫细胞亚群中的基因表达,包括中性粒细胞,B细胞,CD4,CD8,单核细胞,天然杀伤(NK)细胞,骨髓树突细胞和血浆性树突细胞(PDC)。我们发现,响应流感抗原的刺激,PDC显示出最高水平IFI27.相对于其他细胞亚群的基因表达(图5B.).值得注意的是,中性粒细胞没有上调IFI27.尽管他们对干扰素途径有所了解(图5B.和d)。我们也发现了IFI27.外周血的反应主要由TLR7激活驱动(图5C.),而这个tlr7驱动IFI27.在PDC和NK细胞中主要观察到响应(图5D).我们指出了IFI27.响应在PDC中特别强烈(其表达水平在PDC中显着高于NK细胞)(图5E.).基于这些发现,我们得出结论,PDC(以及较小程度,NK细胞)最有可能是主要的来源IFI27.在外周血中。因为PDC-TLR7途径专门识别呼吸病毒(例如流感病毒)但不识别细菌,这些研究结果表明IFI27.可能是一个有用的生物标志物,以区分流感和细菌感染。
IFI27.细菌和流感感染之间的歧视
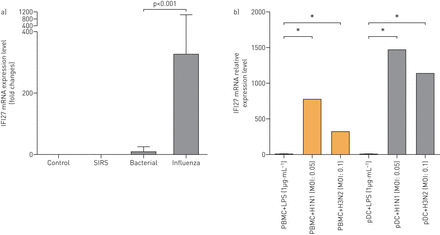
与上述调查结果一致,我们发现了IFI27.外周血中的表达可以在发现队列中从细菌肺炎中区分流感肺炎(图6A).我们进一步证实了这一点体外实验(图6B.).在这些实验中,流感病毒(H1N1和H3N2)和细菌抗原(脂多糖)与外周血或纯化的PDC共同培养。响应脂多糖刺激,IFI27.上调可忽略不计(在外周血和PDC中)。相比之下,IFI27.响应流感病毒的上调(H1N1和H3N2)非常高(外周血倍数为777倍,PDC中的1475倍)(图6B.).⇓
一种)IFI27.水平区分细菌从患者中的流感感染。IFI27.流感病毒肺炎患者外周血样品中的基因表达(n = 8),细菌肺炎(n = 16),全身炎症反应综合征(SIRS)(n = 12)和健康对照(n = 18)。患有SIRS的患者具有非传染性表型,包括手术,创伤,胰腺炎,心脏和肺部条件。IFI27.通过定量实时PCR测量水平。b)体外IFI27对细菌抗原和流感病毒的反应。外周血单核细胞(PBMC)和血浆胸泡树突细胞(PDC)与脂多糖(LPS)或活流感病毒(H3N2和H1N1)共培养。多种感染(MOI)是病毒与细胞总数的比率。*:使用非参数曼 - 惠特尼U-Test,两组之间的统计学显着差异(P <0.05)。
前瞻性验证组
在第2阶段验证中,我们从2012年到2016年从澳大利亚的五个教学医院促进了402名疑似呼吸道感染和37名健康志愿者的患者(表格1,补充表S2-S3)。在这一潜在的队列中,诊断阈值IFI27.在实时PCR平台上进行了测试。我们将群组划分为训练集(n = 200)和测试集(n = 202)。首先在训练集中优化诊断阈值,随后在测试集中确认。在火车和测试集中,接收器操作特征曲线,特异性和灵敏度的特异性和灵敏度的计算的AUC几乎相同。从此,我们将两个数据集结合使用的摘要结果。
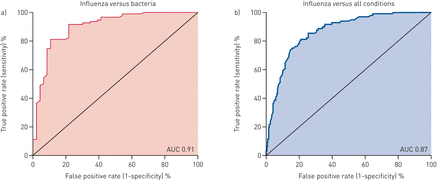
我们发现,74倍变化的阈值(基于PCR)提供了最佳的水平IFI27.为了区分流感和细菌感染(有关如何确定该阈值的完整细节,请参阅补充材料)。在这种截止值,IFI27.敏感性为0.80,特异性为0.90。此外,IFI27.有91%的AUC(图7.),其在多基因生物标志物的相同范围内(87%-95%)(表3).此外,IFI27.在将流感病毒与其他呼吸道病毒中的流感病毒中有83%(敏感性0.80和特异性0.75)的AUC。与其区分流感与细菌感染的能力相比,这种表现是适度的。但是,我们指出,之前出版的多基因生物标志物都没有区分流感来自其他呼吸道病毒(表3).
诊断性能IFI27.在实时PCR平台上。a)流感感染(n = 96)相对细菌感染(n = 48)。曲线下面积(AUC)为0.91(95%CI 0.83-0.95,P <0.001)。b)流感感染(n = 96)相对所有条件(细菌感染,病毒感染和非传染性“流感状”疾病)(n = 293)。AUC为0.87(95%CI 0.82-0.90,P <0.001)。使用全部范围计算AUCIFI27.截止值(fold change 10-6000)。
进一步评估临床效用IFI27.,我们试图确定它是否可以在队列中的所有患者中识别流感感染(图7.).这种额外的评估代表了对其性能的更具剧烈评估,因为IFI27.需要鉴定对多种替代性的流感感染(细菌感染,其他病毒感染和所有非传染性条件),而不是仅仅是两种疾病(流感相对细菌)。以前唯一的多基因生物标志物研究以这种方式评估生物标志物(GSE63990,见表3)[13.].在我们的评估中,IFI27.展示了鉴定患流感感染的高AUC(88%)(敏感性0.80和特异性0.80)(图7.).这种性能类似于先前的多基因生物标志物研究(87%)(GSE63990)[13.].集体,这些调查结果表明IFI27.具有较高的诊断准确性,相当于以前发表的多基因生物标志物。
讨论
这项研究解决了将基因组科学转化为临床实践的主要挑战。在过去的十年中,在发现呼吸道病毒感染的基因表达特征方面取得了相当大的进展。这些基因表达标记识别与感染相关的免疫反应,从而显著提高临床医生作出准确诊断的能力。然而,所有发表的基因表达签名都包含多基因列表,从一些研究中的几十个基因到其他研究中的数百个基因。在临床实践中测量大量基因的表达水平是有问题的。目前的实时PCR技术只能检测少量的基因。此外,为许多基因确定诊断阈值在计算上具有挑战性。大多数研究使用非常复杂的机器学习算法来确定这个阈值。这在临床实践中是不切实际的,因为大多数机构没有获得专业的生物信息学专业知识。在这篇论文中,我们证明了一个精心选择的单基因生物标志物可能提供一种替代方法。 Using evidence from体外实验,小鼠模型和多名患者队列,我们证明作为单一基因生物标志物,IFI27.可以始终如一地鉴定不同患者种群的流感感染,在具有不同疾病严重程度和多种可用性患者的患者中的个体中。此外,我们的研究结果表明,该生物标志物可以在区分流感和细菌感染方面实现高预测准确性,相当于多基因生物标志物获得的细菌感染。
我们的研究是迄今为止在流感病毒感染中进行的最大的生物标志物研究。它包括八个队列(n = 1071),患者从不同地理位置,环境(门诊,急诊部门和重症监护病房)和不同程度的感染严重程度(轻度,中度至严重)中汲取的患者。这种广泛的临床案例混合使我们的发现可能是其他患者群体的发现。我们的研究结果也与最近公布的呼吸道病毒感染的荟萃分析一致。荟萃分析包括五个流感队列(n = 292)(起源于本研究的两群)[14.].它鉴定了与流感感染相关的127种多基因签名。其中127个基因,IFI27.是上调率最高的基因。
我们的体外数据很重要,因为它提供了对能力的生物合理的解释IFI27.从细菌感染中区分流感。我们的调查结果显示IFI27.由血浆骨质树突细胞(PDC)产生,众所周知的枢轴免疫细胞子集,识别流感病毒,但不是细菌[15.,16.].我们的数据还透露了TLR7路径调解IFI27.上调。这与已建立的文献一致,表明PDC使用TLR7识别单链RNA病毒,例如流感病毒[17.,18.].我们还发现细菌识别TLR(TLR1,TLR2,TLR4,TLR5和TLR6)没有诱导IFI27.而TLR7配体则上调。这些发现加上以前的研究[17.- - - - - -20.[共同支持TLR7-PDC途径代表病毒特异性检测系统(用于单链RNA病毒)的观念。这种机械洞察力有助于解释该能力IFI27.区分流感和细菌感染的生物标记。
本研究中的前瞻性验证队列有两种设计特征(大型样品大小和前瞻性患者招募),这使得可以解决以前公布的生物标志物研究中的一个重要限制。在以前的研究中,验证队列通常使用患者表型,这些表型清楚地是“感染性”或显然“非传染性”(例如健康的志愿者)。最近的一个研究Salik.等等。[13.[证明,使用这种明确定义的表型导致过度估计生物标志物性能。一种方法论上更具活力的方法应包括较少的独特表型,例如患有非传染性“流感的”疾病的患者[13.].与之前的研究相比,我们的前瞻性验证队列中非传染性患者的数量显著增加(表格1).本研究的另一个实力是患者前瞻性招募。患者以无差异化的方式呈现,由此可能是传染性和非传染性的疾病,从而模拟临床医生通常面临的现实临床情景。此外,我们的许多患者患有呼吸道组织(哮喘17%和慢性肺病22%),这也可以模仿呼吸道感染(例如具有类似的咳嗽症状和呼吸急促)。因此,我们的队列因此重新承诺了许多真实世界的挑战,体现了最严格的条件IFI27.可以测试。
单基因生物标志物,如IFI27.避免多基因生物标志物面临的几种方法论问题。多基因生物标志物容易受到过度拟合(使用太多基因来发展疾病签名)。这导致外部患者群体的可重复性差。在本研究中,我们通过专注于少量生物标志物最小化过度拟合,从中鉴定了在多个患者队列中高度可重复的单一生物标志物。多基因生物标志物的另一个常见问题是公布研究中存在许多非重叠基因。这产生了巨大的翻译问题,因为临床医生无法确定与患者一起使用的基因列表。使用单一基因生物标志物的简单性如IFI27.代表着在克服这一转化障碍方面向前迈进了一大步。多基因列表的第三个问题是,大多数研究都来自于微阵列研究。在这里,我们进行验证IFI27.在大多数医院的实时PCR平台上。这为其他临床医生开辟了大门,以进行独立验证,这是一个必不一的下一步,迈向临床实践。
值得注意的是,现有的多基因生物标志物确实在单个生物标志物上具有优势。通过从免疫信号通路的不同部分捕获基因组信号的星座,多基因生物标志物广泛反射宿主响应。与多基因生物标志物相比,单一生物标志物可能低估了宿主响应的范围和深度。但是,我们的研究结果表明IFI27.水平确实提供了对免疫信号通路的合理评估。这是通过与之间的高水平相关性证明IFI27.干扰素途径(90%)和免疫系统途径中的许多基因(69%)。总的来说,这些研究结果表明IFI27.作为单基因生物标志物,反映免疫应答与类似程度的反映为多基因生物标志物。
IFI27.与先前建立的流感生物标志物不同(例如OAS.和PKR.)在三个重要方面。第一的,IFI27.如我们的微阵列分析所示,比其他生物标志物显着更好。第二,IFI27.主要由血浆曲线细胞(PDC),识别呼吸病毒的免疫细胞产生。相比之下,大多数生物标志物由免疫细胞产生(例如可通过细菌激活的中性粒细胞和巨噬细胞。第三,IFI27.在分化流感和细菌感染之间具有相当大的歧视力。我们的数据显示,作为一个单一基因生物标志物,IFI27.单独提供与多基因生物标志物相当的等效诊断能力。以前的生物标志物没有可比性能力。
然而,目前的研究有局限性。首先,特异性IFI27.在差异化流感病毒和其他呼吸道病毒之间是中等的(AUC 83%)。其次,我们对DNA病毒感染患者的数据不足(例如巨细胞病毒)或病毒-细菌合并感染;我们的队列中只有13例这样的病例,这个数字太小,不足以进行深入分析。在我们之前发表的研究中,我们发现需要一项纵向研究设计来调查合并感染的患者(为了捕捉从流感感染到合并感染的转变)[21.].不幸的是,目前的研究受到仅在一次点收集的患者样品的限制。第三,我们的研究没有评估可能影响临床决策的重要因素,例如先前的概率或错过诊断的成本及其对患者/经济结果的影响。这些因素在未来的成本效益研究或临床试验中最好地解决。
总之,我们的研究结果表明IFI27.是一个有前途的免疫生物标志物;然而,需要进一步研究来评估其在病毒/细菌联合感染患者中的临床效用。
补充材料
补充材料
请注意:编辑部没有编辑补充材料,并随着作者提供的,上传。
补充方法ERJ-02098-2016_SUPPLEMENTARY_METHODS.
图S1。基因表达分析使用不同的微阵列平台ERJ-02098-2016_FIGURE_S1
图S2。IFI27基因在小鼠流感感染模型中的表达ERJ-02098-2016_FIGURE_S2
表S1。探索队列 - 流感阳性患者ERJ-02098-2016_TABLE_S1
表S2。前瞻性验证队列 - 患者特征ERJ-02098-2016_TABLE_S2
表S3。预期验证队列 - 鉴定病原体ERJ-02098-2016_TABLE_S3
披露
补充材料
A.麦克莱恩ERJ-02098-2016_MCLEAN.
格兰特P. Parnell.ERJ-02098-2016_PARNELL.
M. Shojaei.ERJ-02098-2016_Shojaei.
B.M.唐ERJ-02098-2016_TANG.
致谢
我们要感谢Kenneth McPhie和Ian Barr(世卫组织(Who Barr(Who Comperenta,Melbourne,澳大利亚)合作和研究中心),供我们的流感病毒股体外雅王(重症监护医学部,Nepean医院,Kingswood,澳大利亚)和尼科夫(免疫学和过敏研究中心,西比医学研究所,Westmead,澳大利亚)的援助分析流式细胞术数据和IAN Bart有用的审查我们的稿件早期版本。我们还要感谢若干组织,以协助我们的学习,包括:Nepean关键护理教育和研究所(澳大利亚Kingswood,澳大利亚),为提供资金,以支持我们在澳大利亚,捷克共和国和香港的学习;加拿大公共卫生机构(PHAC)(加拿大渥太华)提供资金支持我们研究的加拿大手臂;Roche Pharmaceuticals(加拿大渥太华)用于加拿大的H1N1样品收集;和加拿大严重流感研究组(见下文),用于促进患者样品在研究中。
加拿大严重流感研究组的合作成员如下:Anand Kumar(关键护理医学和传染病,医学部,医学微生物学和药理学,Manitoba大学,Winnipeg);戈登伍德(维多利亚皇家禧医院和维多利亚综合医院);史蒂夫雷诺兹(温哥华综合医院,不列颠哥伦比亚省,温哥华);布伦特温斯顿(山麓医疗中心和Peter Lougheed医院,卡尔加里大学);Sean Bagshaw(艾伯塔大学艾伯塔大学,埃德蒙顿);Jim Kutsogiannis(埃尔伯塔大学亚历山德拉医院(埃德蒙顿大学);Michael Silverman(Rouge Valley Hospital,Ajax,加拿大和Lakeidge医院,Oshawa);玛格丽特赫里奇(多伦多综合医院和多伦多大学多伦多西医院);Rob Fowler(桑尼布鲁克医院,多伦多大学,多伦多);艾莉森麦杰尔(多伦多大学西奈山医院); Mary-Anne Aarts (St Michael's Hospital, University of Toronto, Toronto); Deborah Cook (St Joseph's Healthcare, McMaster University, Hamilton); Lauralyn McIntyre (Ottawa Hospital General Campus and Civic Campus, University of Ottawa, Ottawa); Kosar Khwaja (Montreal General Hospital and Royal Victoria Hospital, McGill University, Montreal); Natalie Bandrauk (Health Sciences Centre and St Claire's Mercy Hospital, Memorial University, St. John's); Richard Hall (Queen Elizabeth Health Sciences Centre – Halifax Infirmary and Victoria General Site, Dalhousie University, Halifax).
作者以下列方式促进了研究。本杰明M.唐构思了这项研究。Maryam Shojaei进行了体外学习。Klaus Schughart进行了鼠标研究。Klaus Schughart和Grant P. Parnell进行了微阵列分析。Maryam Shojaei.,格兰特P. Parnell.,Anand Kumar.,Aseem Kumar.,约翰何,yoav keynan.,一个drienne F.A. Meyers, Terry Ball, Amarnath Pisipati, Amy L. Phu, Stephen Huang, Marek Nalos, Kate O'Connor, Stephen Schibeci, Kevin Lai, Hao Luo, Fahad Gul, Mark Gillett, David Booth, Elizabeth Moore, Robert Geffers, Jens Schreiber, Damon Eisen and Benjamin M. Tang participated in the study and critical review of the manuscript; B. Tang drafted the manuscript.
脚注
本文提供了补充材料www.qdcxjkg.com
支持声明:这项工作得到了Nepean关键护理教育和研究所(Kingswood,澳大利亚)的支持。鼠标研究由亥姆霍兹协会(Program Creation和Immunity)的历史媒体授权资助,以及来自德国教育和研究的德国教育和研究部的研究许可证·普鲁斯探查网络。Benjamin M. Tang,Grant P. Parnell,Maryam Shojaei和Anthony McLean提出了专利申请(PCT)IFI27..Nepean关键护理教育和研究所和加拿大的公共卫生机构在:研究的设计和行为中没有作用;数据的收集,管理,分析和解释;或准备,审查或批准稿件。相应的作者可以完全访问所有数据以及提交出版物的最终责任。本文的资金信息已存入Crossref资助者注册表.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 已收到2015年6月21日。
- 接受2017年3月15日。
- 版权所有©2017